Что значит фиброз створок аортального и митрального клапанов
Что такое приобретённый порок сердца? Причины возникновения, диагностику и методы лечения разберем в статье доктора Петрова А. А., терапевта со стажем в 6 лет.
Определение болезни. Причины заболевания
Порок сердца — это органическое поражение клапанов сердца, его перегородок, больших сосудов и миокарда (мышечной ткани сердца). Заболевание приводит к нарушению функции сердца, застою крови в венах, тканях и органах.
Пороки могут быть как врождёнными, так и приобретёнными. Врождённые пороки выявляют в первый год жизни во время диспансеризации с помощью УЗИ сердца.
Изменение клапанов возникает под влиянием следующих причин:
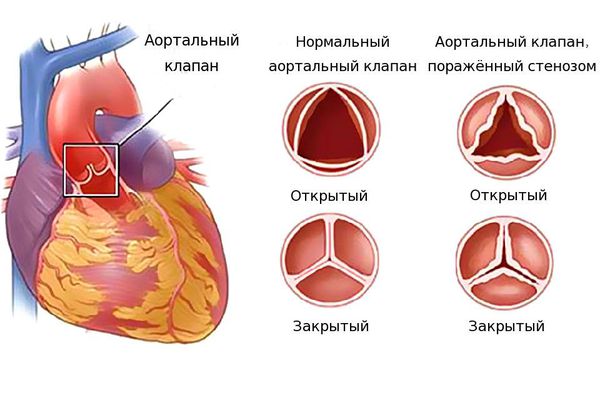
Изменение клапанов проявляется фиброзом (разрастанием соединительной ткани), утолщением створок и кальцинозом (отложением кальция в мягких тканях).
Пороки сердца могут возникнуть в любом возрасте, например после травмы грудной клетки. Но чаще всего заболевание формируется в пожилом возрасте. Это связано с тем, что для воздействия на организм большинства факторов требуется продолжительное время.
Симптомы приобретённых пороков сердца
В большинстве случаев заболевание проходит без симптомов, пока не приведёт к значимому изменению тока крови внутри сердца — ускорению потока или его обратному движению. Это становится причиной нарушения функции сердца и проявляется следующими симптомами:
Другим признаком приобретённых пороков сердца может быть цианоз — синюшное окрашивание кожи и слизистых оболочек разной интенсивности: от лёгкой светло-синей до выраженной синевато-чёрной. Цианоз на губах, кончике носа и кончиках пальцев называют акроцианозом. Он особенно выражен при митральном пороке сердца и получил название «митральный румянец». При аортальных пороках кожные покровы обычно бледные. Это связано с недостаточным наполнением капилляров кровью.
Если застой жидкости происходит в печени и сопровождается разрушением её клеток, то кожные покровы могут приобрести желтушный цвет. Особенно это заметно на белках глаз.
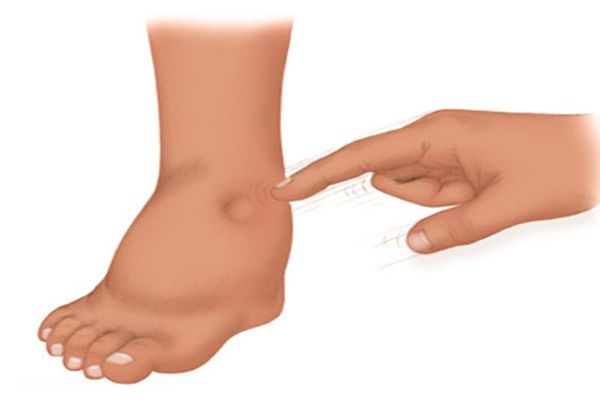
При приобретённых пороках сердца могут появиться отёки. Они выявляются при надавливании большим пальцем в области лодыжек, стопы, крестца и других частей тела.
При выслушивании сердца (аускультации) можно выявить различные шумы. При аускультации лёгких выслушиваются симметричные мелкопузырчатые, напоминающие лопанье пузырьков в газированном напитке влажные хрипы и ослабленное дыхание в нижних отделах.
Патогенез приобретённых пороков сердца
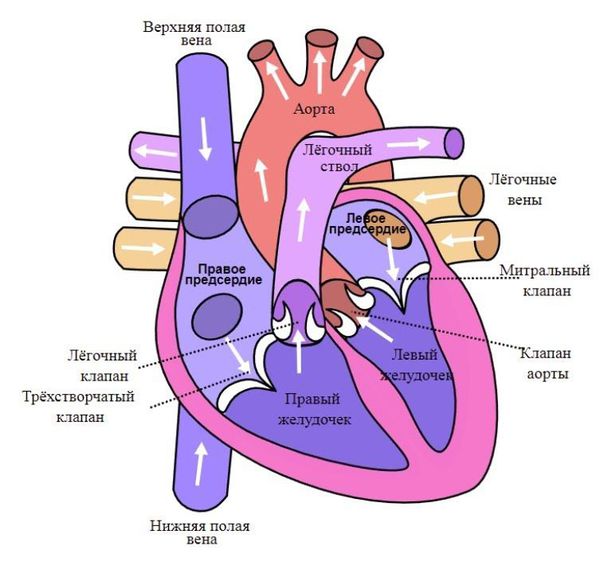
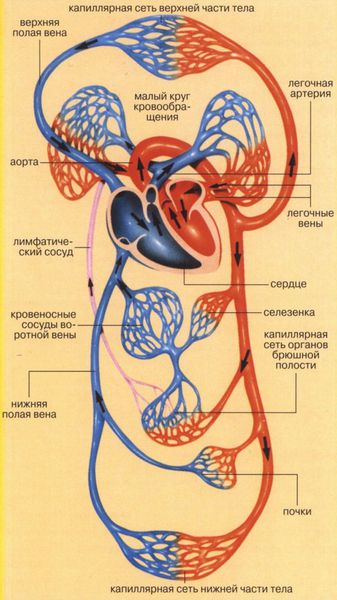
Сердце состоит из двух отделов: левого — артериального и правого — венозного. Артериальная кровь, обогащённая кислородом, течёт в левых отделах сердца, а венозная, обеднённая кислородом кровь, — в правых.
«Левое» сердце состоит из левого предсердия и лёгочных вен, левого желудочка и аорты. «Правое» сердце включает правое предсердие, верхнюю и нижнюю полые вены, правый желудочек и лёгочную артерию. Между предсердиями и желудочками находятся клапаны сердца:
Клапаны, словно двери, пропускают поток крови в одну сторону и не допускают прохода обратно. Если же клапан изменён и при закрытии его образуется щель, то происходит обратный поток крови — регургитация. Щель возникает из-за следующих патологических изменений:
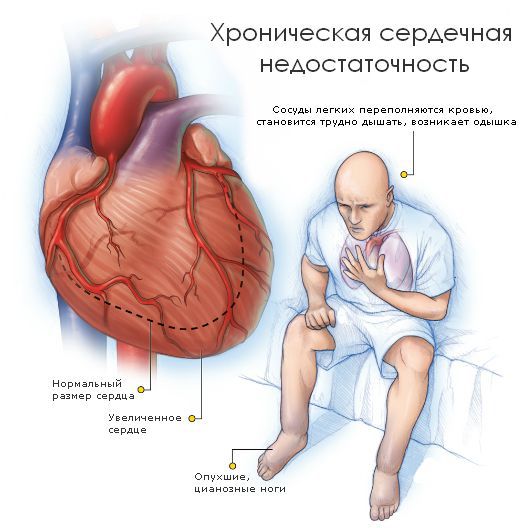
Если же клапан сужен, то это препятствует току крови. Такое состояние называется стенозом. Чаще всего стеноз или недостаточность возникают изолированно в отдельных клапанах, однако возможны ситуации, когда поражены несколько клапанов. Разрушение клапанов приводит к нарушению циркуляции крови, возникновению застойных явлений в малом и большом круге кровообращений. Из-за этого появляются признаки сердечной недостаточности: одышка, отёки, кашель и другие симптомы.
Классификация и стадии развития приобретённых пороков сердца
Существующие классификации приобретённых пороков сердца имеют некоторые различия. Это связано с тем, для каких специалистов они предназначены — кардиологов или кардиохирургов. В общей клинической практике целесообразно использовать классификацию по признакам заболевания в той последовательности, которая принята для постановки диагноза. Наиболее распространено разделение на следующие виды:
Осложнения приобретённых пороков сердца
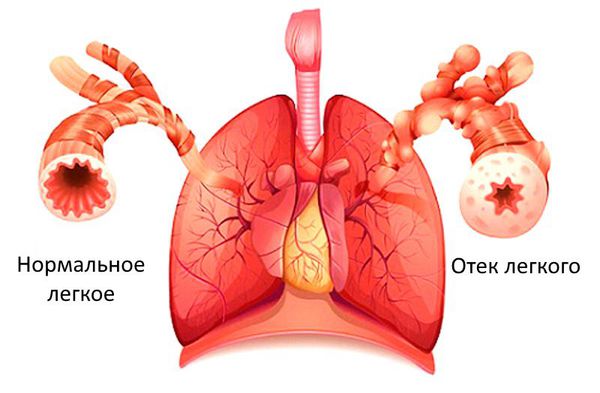
Если застойные явления происходят в малом круге кровообращения, то возникает дыхательная недостаточность и возможен отёк лёгких. Признаком дыхательной недостаточности является одышка при физической нагрузке. Если одышка возникает при нагрузке, которую пациент раньше выполнял без особых усилий, то она является патологической и следует обратиться к врачу.
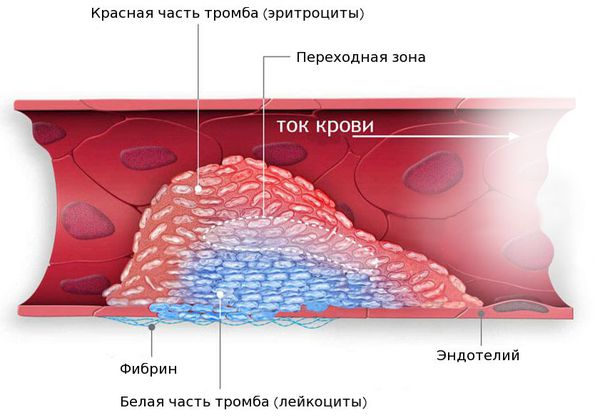
При структурных изменениях в сердце могут происходить нарушения ритма: частые экстрасистолии (сильные сердечные толчки с «провалом» или «замиранием» после них), мерцательная аритмия (неравномерное учащённое сердцебиение), приступы тахикардии (увеличение частоты сердечных сокращений). Мерцательная аритмия часто возникает при расширении левого предсердия. Это может привести к тромбозу (закупорке сосуда, питающему головной мозг) и в результате — ишемическому инсульту (нарушению мозгового кровообращения), ослаблению мышц или параличу.
Диагностика приобретённых пороков сердца
После тщательного опроса, изучения истории болезни и осмотра переходят к инструментальным и лабораторным методам исследований:
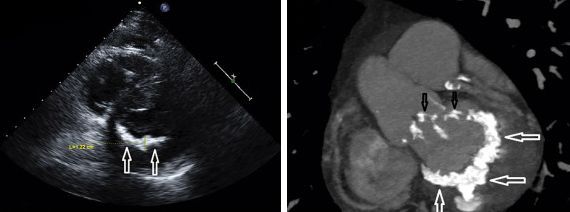
Эхокардиография.
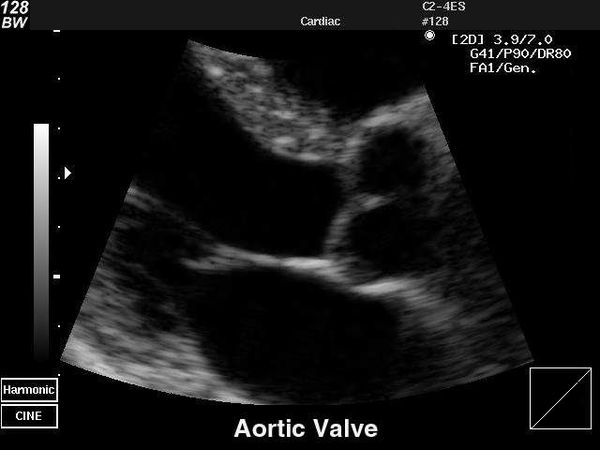
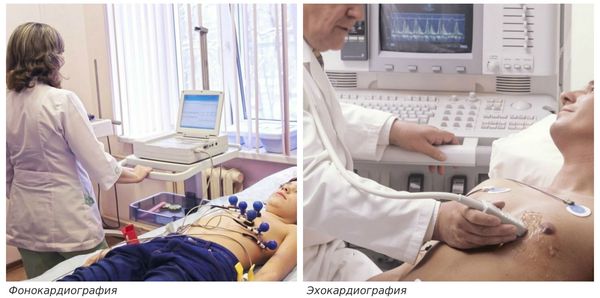
Эхокардиография (ЭхоКГ) — ключевой метод подтверждения диагноза клапанной болезни сердца, а также оценки её тяжести и прогноза. В ходе исследования визуализируют структуру клапанного аппарата, измеряют объёмы и размеры камер сердца, определяют стеноз и наличие обратного тока крови.
Существует трансторакальная и чреспищеводная эхокардиографическая диагностика. Трансторакальный метод — более доступный и неинвазивный. Ультразвуковой датчик располагается на грудной клетке спереди. При чреспищеводном ЭхоКГ датчик вводится в пищевод, исследование проводят на уровне сердца. Так как датчик находится ближе к сердцу, то структуры на экране визуализируются более чётко.
На первом этапе обследования достаточно проведения трансторакального ЭхоКГ.
Другие неинвазивные методы исследования.
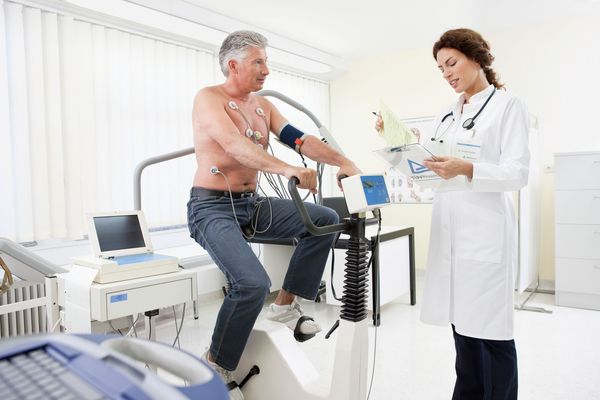
2.1 Нагрузочные тесты (стресс-эхокардиография, тредмил-тест, велоэргометрия)
Нагрузочные тесты применяют для выявления объективных признаков заболевания при неспецифических симптомах или их полном отсутствии. Эти тесты особенно полезны для оценки риска сердечно-сосудистых осложнений при аортальном стенозе. Пробы с физической нагрузкой также помогают определить уровень рекомендуемой активности, в том числе оптимальную интенсивность спортивных тренировок. Например при велоэргометрии на пациента прикрепляют электроды, просят сесть на велотренажер и крутить педали. Постепенно нагрузку увеличивают, одновременно следя за состоянием больного.
2.2 Магнитно-резонансная томография сердца. Для обследования пациентов с неодназначными результатами ЭхоКГ применяют магнитно-резонансную томографию сердца (МРТ). С помощью МРТ оценивают тяжесть поражения клапанов, выраженность обратного тока крови, определяют объём желудочков, систолическую функцию, аномалии восходящей аорты и фиброз миокарда. МРТ сердца — эталонный метод для определения объёма и функции правого желудочка. Исследование полезно для оценки последствий обратного тока крови при закрытии трикуспидального клапана.
2.3 Компьютерная томография. Мультиспиральную компьютерную томографию (МСКТ) используют для оценки тяжести поражения клапанов, особенно при аортальном стенозе. МСКТ играет важную роль при планировании транскатетерных вмешательств. Компьютерная томография может быть полезна для исключения ишемической болезни сердца.
2.4 Видеофлюороскопия — это съёмка работы сердца при помощи рентгеновских лучей. Предварительно в организм пациента вводят рентгеноконтрастное вещество, что даёт возможность наблюдать за током крови. Видеофлюороскопия важна для оценки механической дисфункции искусственного клапана.
3. Инвазивные методы исследования.
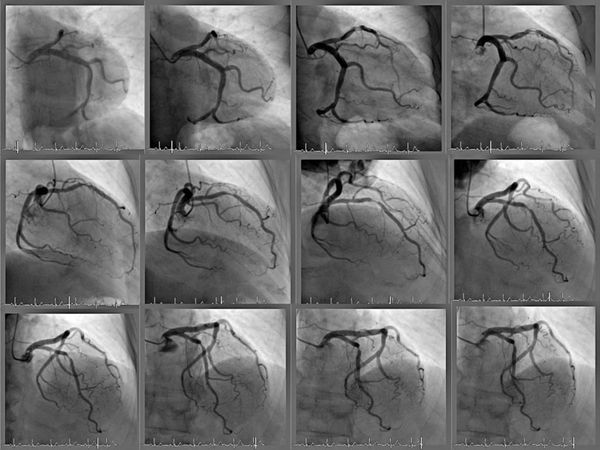
3.1 Коронарная ангиография (КАГ) показана для оценки ишемической болезни сердца (ИБС) при планировании открытого или эндоваскулярного вмешательства — операции на кровеносных сосудах, осуществляемой без разрезов через небольшие проколы на коже.
3.2 Катетеризация сердца — процедура, при которой гибкий катетер (полая трубка) через периферическую артерию или вену на руке или ноге вводится внутрь сосуда. Под контролем рентгеновского аппарата проверяют движение катетера до нужной полости сердца. Процедура даёт представление о давлении внутри камер сердца, составе крови в каждом отделе, работе клапанов, строении стенок и перегородок и используется для оценки кровотока.
Данные ЭхоКГ требуется подтверждать результатами инвазивного исследования, если единственным показанием к хирургическому лечению является высокое давление в лёгочной артерии. В большинстве же случаев эхокардиография — самый доступный метод обследования, с помощью которого с высокой достоверностью можно определить наличие или отсутствие порока сердца.
Лечение приобретённых пороков сердца
Лекарства, способного запустить обратный процесс и восстановить клапан до первоначального состояния, не существует. С помощью медикаментозного метода лечения возможно лишь повлиять на сердечно-сосудистую систему и снизить риск развития осложнений. В тяжёлых случаях применяют хирургические методы лечения.
Медикаментозное лечение
Цель терапии — устранить причины недостаточности кровообращения, улучшить функциональное состояние миокарда, восстановить нормальную циркуляцию крови, микроциркуляцию (транспорт клеток крови и веществ к тканям и от тканей) и предотвратить повторные расстройства кровообращения. Лечение при хронической недостаточности кровообращения включает полноценное сбалансированное питание и лекарственную терапию.
Основные группы препаратов, применяемых при нарушении в работе клапанов:
1. Ингибиторы АПФ (ангиотензинпревращающего фермента) — эналаприл, лизиноприл, рамиприл, периндоприл, фозиноприл. Препараты блокируют превращение гормона ангиотензина I в ангиотензин II. Ангиотензин II оказывает сосудосуживающее действие и вызывает быстрое повышение артериального давления. Ингибиторы АПФ применяют для лечения артериальной гипертензии, терапии или профилактики сердечной недостаточности.
2. Бета-блокаторы — карведилол, бисопролол, метопролол. Эти препараты снижают артериальное давление и нормализуют ритм сердечных сокращений. Действие вызвано блокированием бета-адренорецепторов, отвечающих за реакцию организма на стресс.
3. Антагонисты минералокортикоидных рецепторов — спиронолактон, эплеренон. Препараты понижают артериальное давление и обладают мочегонным воздействием, уменьшая содержание жидкости в тканях.
Существуют различные варианты пороков сердца, для лечения каждого из них применяют различные комбинации препаратов. Также учитывают сопутствующие патологии и индивидуальные особенности пациента.
Например при преобладании застойных явлений дополнительно назначают мочегонные препараты (фуросемид, торасемид), которые снижают объём циркулирующей крови, уменьшая застойные явления в малом и большом круге кровообращений. При наличии тромбов или при высоком риске их появления применяют антикоагулянты — препараты, снижающие свёртываемость крови (варфарин, ривароксабан, дабигатран, апиксабан).
Относительно недавно был разработан новый класс препаратов — ингибиторы рецепторов ангиотензина-неприлизина (сакубитрил). Основное их действие — это повышение количества пептидов, расщепляемых неприлизином. Препараты увеличивают диурез (объём мочи), натрийурез (выведения натрия с мочой), вызывают расслабление миокарда и препятствуют процессам нарушения структуры и функции сердца.
Хирургическое лечение
При наличии показаний, недостаточной эффективности медикаментозного лечения и отсутствии противопоказаний применяют хирургические методы. Многих пациентов пугает необходимость проведения операции на сердце. В некоторых случаях хирургические методы действительно несут определённый риск, но существуют достаточно безопасные операции не на открытом сердце и без больших разрезов. К таким операциям относится баллонная комиссуротомия при стенозе митрального клапана. Метод состоит в расширении клапана с помощью катетера, проведённого через артерию.
Перед оперативным вмешательством проводят необходимые лабораторные, инструментальные исследования и стабилизируют состояние пациента лекарственными препаратами. При подготовке к операции важно уменьшить одышку, отёки, нормализовать пульс и артериальное давление.
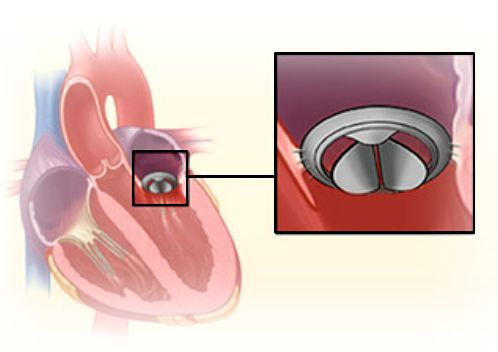
Распространённым хирургическим методом является протезирование искусственным или биологическим клапаном. Существуют и клапан-сохраняющие операции, которые заключаются в пластике повреждённого клапана.
Прогноз. Профилактика
При своевременном обращении пациента к врачу и соблюдении рекомендаций прогноз благоприятный. К каждому случаю врач подходит индивидуально, начиная с подбора медикаментозного лечения и до выбора оперативных методов.
Первичная профилактика приобретённых пороков сердца состоит в предупреждении болезней, приводящих к поражению клапанного аппарата сердца: ревматизма, инфекционных эндокардитов, атеросклероза, сифилиса и более редких патологий, например карциноидной болезни.
Профилактика предполагает ведение здорового образа жизни, который включает:
Что такое недостаточность митрального клапана? Причины возникновения, диагностику и методы лечения разберем в статье доктора Верещагиной Н. В., врача общей практики со стажем в 28 лет.
Определение болезни. Причины заболевания
Патология проявляется слабостью, головокружением, ощущением нехватки кислорода и утомлением, так как при заболевании нарушается кровоснабжение головного мозга. Без лечения тяжёлая регургитация митрального клапана может стать причиной сердечной недостаточности и нарушений сердечного ритма (аритмии).
Причины митральной недостаточности:
Симптомы недостаточности митрального клапана
Симптомы заболевания:
Патогенез недостаточности митрального клапана
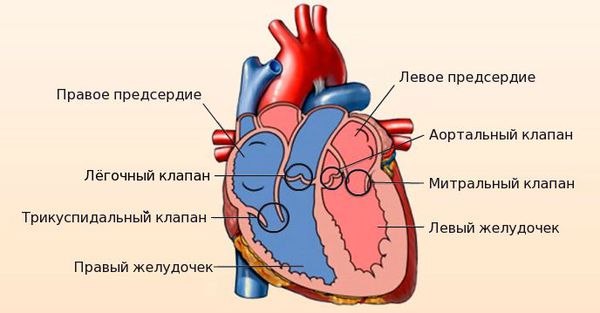
Сердце человека состоит из четырёх камер: правое и левое предсердия, правый и левый желудочки. Между предсердиями и желудочками расположены входные клапаны — трикуспидальный и митральный. На выходе из желудочков находятся похожие по строению выходные клапаны — лёгочный и аортальный.
Клапаны имеют створки, которые открываются и закрываются во время сердечных сокращений. Иногда клапаны не открываются или не закрываются должным образом, при этом нарушается ток крови.
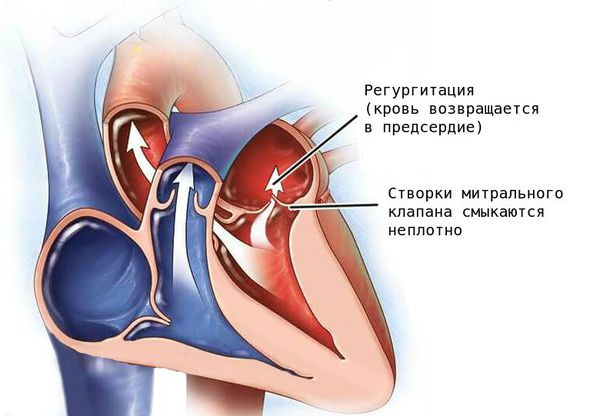
Митральный клапан состоит из двух створок и открывается, позволяя крови течь в левый желудочек. Затем клапан закрывается, чтобы кровь не текла обратно в левое предсердие. При митральной недостаточности этот клапан закрывается неплотно, в результате чего кровь попадает обратно в левое предсердие.
Классификация и стадии развития недостаточности митрального клапана
В течении заболевания выделяют три периода:
С учётом выраженности обратного тока крови выделяют четыре степени митральной недостаточности: с незначительной митральной регургитацией, с умеренной, выраженной и тяжёлой.
Стадии митральной недостаточности:
Осложнения недостаточности митрального клапана
Осложнения порока:
Диагностика недостаточности митрального клапана
При сборе анамнеза кардиолог уточняет:
Лечение недостаточности митрального клапана
При обострении заболевания необходим постельный режим. Также следует принимать препараты, содержащие магний и B6 по две таблетки три раза в день (например, «Магнелис»).
Если беспокоит частый пульс (более 80 ударов в минуту), то назначаются бета-адреноблокаторы, диуретики, антикоагулянты, нитроглицерин.
Если пациент страдает от приступов тревоги, то в качестве симптоматической терапии можно рекомендовать короткий курс феназепама на ночь.
Если развивается сердечная недостаточность и нарушается сердечный ритм, то проводят лечение бета-адреноблокаторами, диуретиками, ингибиторами ангиотензинпревращающего фермента, антикоагулянтами, блокаторами кальциевых каналов.
При значительной недостаточности митрального клапана показано оперативное лечение.
Основные хирургические методы коррекции митральной недостаточности:
Своевременное хирургическое вмешательство позволяет достичь хороших результатов и не допустить развитие осложнений.
Прогноз. Профилактика
При соблюдении рекомендаций врача прогноз благоприятный.
Для профилактики осложнений следует:
При ревматизме и после перенесённой ангины для профилактики недостаточности митрального клапана назначают антибиотик «Бициллин-3». Препарат подавляет развитие стрептококковой и стафилококковой инфекций.
После 40 лет всем пациентам, страдающим недостаточностью митрального клапана, необходимо контролировать уровни фибриногена, РФМК (растворимых фибринмономерных комплексов), D-димера (продукта распада фибрина). Эти анализы нужны для предотвращения тромбоэмболии лёгочной артерии и артерий внутренних органов. При повышении вышеуказанных показателей назначают антикоагулянты.
Если недостаточность митрального клапана обнаружена у ребёнка и его беспокоит слабость, головокружение, расстройство внимания, то рекомендуется временно перейти на домашнее обучение. Таким детям следует избегать чрезмерных физических нагрузок, им разрешена только лечебная физкультура.
Если при проведении Эхо-КГ обнаружено сильное прогибание створок клапана, то необходима консультация у кардиохирурга. Восстановление клапана или его замена могут потребоваться при эндокардите, сердечной недостаточности, нарушениях ритма, сильных болях в грудной клетке, признаках застоя в лёгочной системе (одышке, уменьшении объёма вдоха и ощущении нехватки воздуха).
«Старческий» порок сердца: истина и мифы
Что скрывается за диагнозом «атеросклеротический стеноз устья аорты»? Каков механизм развития аортального стеноза? Есть ли разница в лечебной тактике в России и за рубежом? Рисунок 1 Многим терапевтам и кардиологам
Что скрывается за диагнозом «атеросклеротический стеноз устья аорты»?
Каков механизм развития аортального стеноза?
Есть ли разница в лечебной тактике в России и за рубежом?
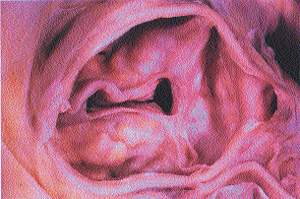 |
| Рисунок 1 |
Многим терапевтам и кардиологам хорошо известен такой нередко встречающийся клинический феномен: у пожилого человека без ревматического анамнеза при выслушивании сердца определяется грубый систолический шум над аортальными точками. Зачастую его практически никак не трактуют и в диагнозе не отражают. Но иногда в попытке объяснить подобную аускультативную картину врач все же выносит примерно такой вердикт: «атеросклеротический стеноз устья аорты». Но нельзя забывать, что диагноз — это формула для лечения, и от того, насколько правильно он будет сформулирован, во многом зависит дальнейшая тактика. Это касается любого диагноза, и данного — в частности. Именно поэтому следует серьезно разобраться не только и не столько в правомочности термина «атеросклеротический стеноз», сколько в том, что же в действительности скрывает за собой «неревматический» систолический шум на основании сердца.
В СССР традиционно рассматривались три основные причины приобретенного аортального стеноза: 1) ревматизм, 2) инфекционный эндокардит и 3) атеросклероз. Именно эта триада, и, как правило, именно в таком порядке перекочевывала из руководства в руководство, из одного учебника в другой до середины настоящего десятилетия, тогда как другим предпосылкам отводилось место в графе «и прочие». Большинство авторов после описания ревматического и «септического» эндокардитов в той или иной форме упоминают атеросклероз, который обычно в преклонном возрасте может привести к формированию кальцинированного стеноза аортального клапана [1].
Между тем за рубежом уже более 30 лет придерживаются иной точки зрения. Она последовательно рассматривается в англоязычных источниках, вышедших в свет в 60-е, 70-е и 80-е годы, и последнее десятилетие исключением не является. Согласно мнению западных исследователей, аортальный стеноз у взрослых может быть результатом: 1) кальцификации и дистрофических изменений нормального клапана, 2) кальцификации и фиброза врожденного двустворчатого аортального клапана или 3) ревматического поражения клапана, причем первая ситуация является наиболее частой причиной аортального стеноза [2].
Итак, налицо очевидная разница в подходах к этой проблеме в России и за рубежом. «Точкой пересечения» был и остается лишь ревматизм, тогда как отечественная и зарубежная школы «дополняют» его каждая двумя разными этиологическими формами: первая — инфекционным эндокардитом и атеросклерозом, вторая — идиопатическим кальцинозом и кальцификацией врожденного порока (чаще двустворчатого клапана). Но следует учитывать, что существуют две оговорки. Во-первых, изолированный кальциноз как трикуспидального, так и бикуспидального аортального клапана — по сути есть один и тот же процесс, наблюдающийся лишь в разных временных диапазонах. Во-вторых, инфекционный эндокардит работами современных авторов фактически исключен из списка существенных причин аортального стеноза. Таким образом, по большому счету остаются два состояния, определяющие диагностические, лечебные и методологические разночтения: атеросклероз и идиопатический кальциноз. Принципиальная разница между этими двумя патологическими состояниями станет понятна после более детального рассмотрения сенильного кальциноза устья аорты как самостоятельной нозологической формы.
В 1904 году в журнале «Архив патологической анатомии» 28-летний немецкий врач Иоганн Георг Менкеберг описал два случая стеноза устья аорты со значительным обызвествлением клапанов [3]. Он предложил рассматривать изменения в створках как дегенеративные, как результат изнашивания тканей с последующим их «склерозом» и обызвествлением. Обнаружив, по-видимому, что-то подобное тому, что изображено на рис. 1, он изобразил в своей статье деформированный клапан, в котором на фоне жировой дегенерации расположено множество известковых депозитов (рис. 2). Его правота будет подтверждена спустя много лет, что найдет отражение в самом термине «дегенеративный кальцинированный аортальный стеноз». Но в начале века статья И. Г. Менкеберга существенного резонанса не вызвала. И лишь через полтора десятка лет она станет объектом внимания и ляжет в основу жарких дискуссий, ведущихся на протяжении долгого времени. Морфогенез порока также вызвал много споров.
 |
| Рисунок 2 |
С менкеберговской гипотезой конкурировали в основном две теории: атеросклеротического поражения и поствоспалительного кальцинирования.
В нашей стране основное значение приобрела атеросклеротическая гипотеза. Считается, что детальное изучение «атеросклероза аортального клапана» в динамике развития «атеросклеротического порока» было выполнено профессором А. В. Вальтером в конце 40-х годов. Он описывал интенсивную липоидную инфильтрацию фиброзного пласта клапана на уровне замыкательной линии и на дне синусов Вальсальвы, причем отложение липоидов он наблюдал также на синусовой поверхности створок в небольших утолщениях субэндотелиального слоя. Далее имела место петрификация липоматозных очагов. Известковые массы раскалываются, что исследователь объяснял подвижностью створок, а образовавшиеся трещины заполняются плазменными белками и новыми порциями липоидов, в которых снова откладывается кальций. Раскалывание петрификатов продолжается, а вслед за этим продолжается и кальцинирование клапана. Фиброзное кольцо становится ригидным, створки твердыми и малоподвижными. Развивается аортальный стеноз [4].
Думается, в 1948 году опубликования этих данных было достаточно для обоснования атеросклеротической гипотезы, хотя критического осмысления требует даже сама идея «раскалывания» петрифицированных масс: если бы оно имело место, вероятно, в значительной степени возросла бы частота микроэмболических осложнений. Сегодня же, когда знания об атерогенезе куда более обширны, представляется возможным выдвинуть минимум два контраргумента теории А. В. Вальтера.
Черту под этими рассуждениями можно подвести выдержкой из статьи об атеросклерозе профессора Вашингтонского университета Э. Бирмана: «С атеросклерозом не следует путать локальное кальцифицирующее поражение клапана аорты, когда с возрастом происходит постепенное накопление кальция на аортальной поверхности клапана» [8].
Поствоспалительная гипотеза, распространенная в основном на Западе, предлагала искать связь кальцинирования с перенесенным когда-то инфекционным эндокардитом, или, что еще более вероятно, латентным ревмокардитом. Так, одни исследователи указывают на наличие в кальциевых конгломератах микробных агентов [9]. Другие публикуют сообщение о результатах гистологического исследования 200 обызвествленных аортальных клапанов, в 196 из которых обнаружены признаки ревматического поражения [10]. Сейчас сложно дать объективную оценку таким данным, но, вероятно, это были секционные находки у людей не столь пожилых и без выраженных известковых отложений. Именно к таким выводам приходишь, изучая мнение современных патологов, утверждающих, что у старых пациентов массивность петрификации всегда маскирует признаки, быть может, когда-то перенесенного ревматического эндокардита.
Однако наметившийся в первой половине века подход привел к формированию двух бытующих теперь за рубежом взглядов. Один из них предполагает, что ревматический вальвулит, даже не оставив стойких гранулематозных повреждений, делает клапан более ранимым в будущем, в значительной степени повышая риск структурной дегенерации [11] и позволяя рассматривать сенильный аортальный стеноз действительно как «дегенеративный», тогда как имеет место поствоспалительная дистрофия, постревматическая дегенерация; при этом перенесенное воспаление как бы детерминирует соединительнотканную деструктуризацию створок в пожилом и старческом возрасте, оказываясь своего рода предиктором кальцинирования клапанного аппарата аорты. Согласно другому взгляду, старческий кальцинированный стеноз является не столько результатом инфекционного эндокардита, сколько сам по себе может вызываться персистирующим в аортальных створках инфекционным возбудителем [12], то есть речь вообще идет о совершенно самостоятельной нозологической форме.
О своеобразности разбираемой патологии свидетельствует также и то, что все чаще появляются публикации об обнаружении в обызвествленных створках аортального клапана различных клеток костной ткани и даже элементов красного костного мозга [13].
Напоминание хорошо известных признаков аортального стеноза врачебной аудитории в данном случае не случайно. Дело в том, что у пожилых и старых пациентов доктора зачастую склонны объяснять наличие тех или иных жалоб скорее ишемической болезнью или общими инволютивными процессами в организме, нежели сформировавшимся «старческим» пороком сердца. Поэтому — коротко об основных особенностях этого заболевания.
 |
| Рисунок 3 |
Аортальный стеноз — один из самых длительно компенсируемых пороков из-за гипертрофии миокарда, столь сильно выраженной, как можно встретить при других заболеваниях сердца (рис. 3). В связи с этим значительно возрастает конечное диастолическое давление в левом желудочке, его наполнение (особенно при физической нагрузке и в условиях тахикардии) затрудняется, что постепенно приводит к повышению давления заклинивания легочной артерии. Развивающаяся при этом одышка, таким образом, на первых порах оказывается следствием первичной диастолической дисфункции левого желудочка, а в период декомпенсации — и систолической дисфункции. С повышенным тонусом миокарда в диастолу связано и нарушение его оксигенации. В то время как увеличение массы левого желудочка усиливает потребность миокарда в кислороде, сдавленные коронарные артерии удовлетворить ее не могут. Отсюда столь типичные для этой категории больных стенокардические боли. При этом, хотя стенокардия возникает у 70% больных с аортальным стенозом, лишь у половины из них имеется коронарный атеросклероз [2]. Третья частая жалоба — обмороки — является следствием снижения сердечного выброса, развивающегося в результате, с одной стороны, уменьшения диастолического наполнения желудочка, с другой — возрастающего градиента давления на уровне аортального клапана [14]. Эквивалентами синкопального состояния могут служить головокружения.
Среди осложнений сенильного стеноза следует отметить эмболии крошащимися известковыми массами (чаще всего коронарных, почечных и церебральных артерий), плохо переносимые и прогностически неблагоприятные аритмии (связанные как с ишемической миокардиопатией, так и с увеличением и дисфункцией левого предсердия) и изредка развивающиеся желудочно-кишечные кровотечения, связанные с ангиодисплазией правых отделов толстой кишки. При этом риск инфекционного эндокардита кальцинированных клапанов снижается в сравнении с изолированными аортальными стенозами ревматической этиологии.
При осмотре редко можно обнаружить что-то специфическое для дегенеративного стеноза у пожилых больных. В отличие от молодых пациентов, имеющих нередко «медленный и малый» пульс, у них даже при тяжелом стенозе в силу снижения эластичности артерий пульс может оставаться нормальным. Пальпаторно длительный приподнимающийся верхушечный толчок определяется в V межреберье несколько кнаружи от среднеключичной линии; нередко может пальпироваться систолическое дрожание. При аускультации первый тон может не изменяться, но в силу функционально-гемодинамических изменений нередко наблюдается его
 |
| Рисунок 4 |
ослабление. При этом второй тон, как правило, меняется, что особенно отчетливо фиксируется при длительном наблюдении за пациентом: пока кальциноз клапана не привел к стенозу, второй тон усилен (при этом в точке Боткина вслед за первым тоном иногда выслушивается систолический тон изгнания), затем из-за уменьшения подвижности створок ослаблен. Для аортального стеноза характерен грубый веретенообразный систолический шум, максимально выслушивающийся у левого края грудины и проводящийся на сонные артерии. При сенильном поражении этот шум имеет некоторые патогенетические особенности (рис. 4). Как видно из схемы, ревматический кальцинированный порок создает при систолическом изгнании гемодинамический эффект «струи», рождающий одни аускультативные феномены, а изолированный кальцинированный стеноз — эффект «спрея» с несколько другими гемодинамикой и нюансами выслушиваемой картины [15]. Так, при выраженной петрификации возникает симптом Галлавардена: высокочастотные компоненты шума проводятся в подмышечную область, имитируя шум митральной регургитации.
В диагностике клиницисту помогут рутинные инструментальные методики: ЭКГ (признаки гипертрофии и нарушения кровоснабжения миокарда левого желудочка, аритмии), рентгенография (кальциноз аортального клапана, изменение конфигурации сердца, признаки застоя в легких) и, конечно, ЭхоКГ (характер изменений в створках клапана, точная оценка степени стеноза и гипертрофии миокарда, измерение показаний внутрисердечной гемодинамики, нарушение локальной сократимости, фракция выброса, градиент давления между аортой и левым желудочком).
Лабораторные показатели, как правило, малоспецифичны и отражают экстракардиальную патологию.
Прогноз при изолированном дегенеративном аортальном стенозе определяется степенью сужения отверстия аортального клапана (см. табл.), но в целом, как правило, благоприятен. Это определяется длительной компенсацией с бессимптомным течением и медленной прогрессией из-за отсутствия комиссуральных сращений, как при ревматическом пороке. При этом следует помнить, что при появлении симптомов летальность и риск осложнений резко возрастает, а 15-20% больных умирают внезапно.
В России изучения этой нозологии как таковой не проводилось, а значит, практикующий врач не ориентирован на соответствующий диагностический поиск. При этом довольно редкое установление диагноза «атеросклеротический стеноз устья аорты» из-за непонимания истинной природы порока приводит к тому, что больному чаще назначают диету и холестеролснижающие средства, нежели направляют на консультацию к кардиохирургу. Но подобное «патогенетическое лечение» приводит лишь к прогрессированию петрифицированного стеноза. Консервативная же симптоматическая тактика вообще у больных аортальным стенозом малоэффективна, а кальцинированным — тем более. Вазодилатирующая и инотропная терапия требует большой осторожности, а назначения нитратов и диуретиков следует избегать.
Скорость прогрессирования стеноза устья аорты
Другими словами, отказ от трактовки сенильного кальцинированного стеноза устья аорты как «атеросклеротического» подведет российских кардиологов и терапевтов к формированию совершенно определенного взгляда на лечебные перспективы у таких пациентов. Единственно эффективным во всем мире признано хирургическое лечение либо путем протезирования аортального клапана (метод с наилучшими показателями отдаленной выживаемости), либо путем баллонной вальвулопластики. Второй метод имеет целый ряд существенных недостатков: большой риск осложнений и вероятность повторной обструкции, высокая интраоперационная летальность (>6%) и смертность в течение года (25%). Между тем именно этот вариант вмешательства остается основным у пожилых пациентов за рубежом; и вообще дегенеративный кальциноз стал основной причиной хирургического лечения при изолированном аортальном стенозе (51% случаев чрескожной баллонной вальвулопластики, тогда как кальциноз бикуспидального клапана и постревматическое поражение — соответственно 40 и 8% случаев). Причем возраст прооперированных больных нередко превышает 80 лет [16].
При написании последнего параграфа автор, разумеется, отдавал себе отчет в том, что проецировать зарубежную ситуацию на российскую действительность невозможно. Нередкая соматическая «запущенность» наших пациентов и стоимость кардиохирургической операции в ближайшее время не позволяют надеяться на какие-то кардинальные изменения в этом вопросе. Настоящая статья лишь подняла геронтологическую проблему, к обсуждению которой в нашей стране не обращались уже многие годы. И дело не столько в том, что 1999 год объявлен «годом пожилого человека» — отечественные медики должны располагать современной информацией и отказаться от устаревших формулировок и несуществующих диагнозов.