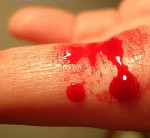
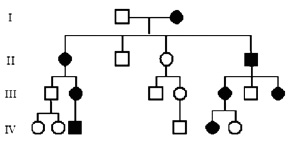
гемофилия сцепленное с полом или нет
Гемофилия
Заболевание из группы наследственных коагулопатий, обусловленное дефицитом факторов свертывания плазмы крови и характеризующееся повышенной склонностью к геморрагиям – кровотечениям и кровоизлияниям, связанным с нарушением целостности или проницаемости стенок сосудов.
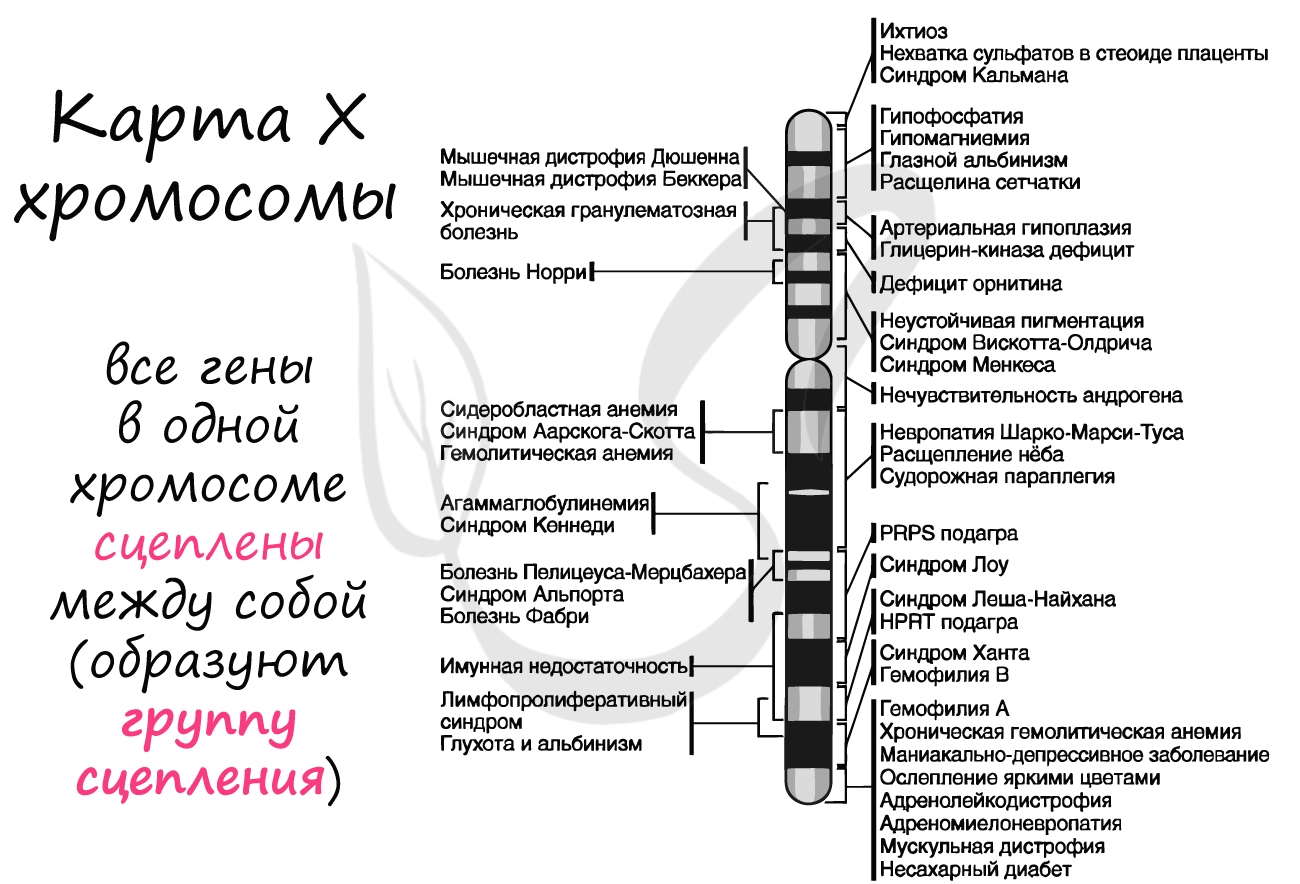
Причины возникновения. Гены, обусловливающие развитие гемофилии, сцеплены с половой Х-хромосомой, поэтому заболевание наследуется по рецессивному признаку по женской линии. Наследственной гемофилией болеют практически исключительно лица мужского пола. Женщины являются проводниками (кондукторами, носителями) гена гемофилии, передающими заболевание части своих сыновей.
Врожденная гемофилия встречается почти у 70 % пациентов. В этом случае наследуется форма и тяжесть гемофилии. Около 30% наблюдений приходится на спорадические, спонтанные формы гемофилии, которые впоследствии становятся наследственными.
Риск передачи заболевания. У здорового мужчины и женщины-кондуктора с одинаковой вероятностью могут родиться как больные, так и здоровые сыновья. От брака мужчины, больного гемофилией, со здоровой женщиной рождаются здоровые сыновья или дочери-кондукторы. Описаны единичные случаи гемофилии у девочек, рожденных от матери-носителя и больного гемофилией отца.
Типы. В зависимости от дефицита того или иного фактора свертываемости крови, различают гемофилию А (классическую), В (болезнь Кристмаса), С и др.
Классическая гемофилия составляет подавляющее большинство (около 85%) случаев синдрома и связана с дефицитом VIII фактора свертывания (антигемофильного глобулина), приводящим к нарушению образования активной тромбокиназы.
При гемофилии В, составляющей 13% случаев заболевания, имеет место недостаток IX фактора (плазменного компонента тромбопластина, фактора Кристмаса), также участвующего в образовании активной тромбокиназы в I фазе свертывания крови.
Гемофилия С встречается с частотой 1-2% и обусловлена недостаточностью XI фактора свертывания крови (предшественника тромбопластина). На остальные разновидности гемофилии приходится менее 0,5% случаев; при этом может отмечаться дефицит различных плазменных факторов.
Симптомы. У новорожденных детей – длительное кровотечение из культи пуповины, подкожные гематомы, кефалогематомы.
У детей первого года жизни – длительные кровотечения в ходе прорезывания зубов, при оперативных вмешательствах. Острые края молочных зубов могут стать причиной прикусывания языка, губ, щек и кровотечений из слизистых оболочек полости рта. Однако в грудном возрасте гемофилия дебютирует редко в связи с тем, что материнском молоке содержится достаточное количество активной тромбокиназы.
Вероятность посттравматических кровотечений значительно возрастает, когда ребенок с гемофилией начинает вставать и ходить. Для детей после года характерны носовые кровотечения, подкожные и межмышечные гематомы, кровоизлияния в крупные суставы. Обострения геморрагического диатеза случаются после перенесенных инфекций (ОРВИ, ветрянки, краснухи, кори, гриппа и др.) вследствие нарушения проницаемости сосудов. Ввиду постоянных и длительных кровотечений у детей с гемофилией имеется анемия различной степени выраженности.
По степени убывания частоты кровоизлияния при гемофилии распределяются следующим образом:
гемартрозы (70—80%) – кровоизлияния в суставы;
гематомы (10-20%) – ограниченнное скопление крови при повреждении органов и тканей;
гематурия (14-20%) – наличие крови в моче;
желудочно-кишечные кровотечения (8%),
кровоизлияния в ЦНС (5%).
Лечение. В лечении гемофилии выделяют два направления – профилактические и «по требованию», в период проявлений геморрагического синдрома.
Профилактическое введение концентратов факторов свертывания крови показано пациентам с тяжелой формой гемофилии и проводится 2-3 раза в неделю для предупреждения развития гемофилической артропатии и прочих кровотечений. При развитии геморрагического синдрома требуются повторные трансфузии препарата. Дополнительно используются свежезамороженная плазма, эритромасса, гемостатики. Все инвазивные вмешательства у больных с гемофилией (наложение швов, удаление зубов, любые операции) проводятся под прикрытием гемостатической терапии.
При незначительных наружных кровотечениях (порезах, кровотечениях из полости носа и рта) используется гемостатическая губка, на рану накладывается давящая повязка, раны обрабатываются тромбином. При неосложненном кровоизлиянии ребенку необходим полный покой, холод, иммобилизация больного сустава гипсовой лонгетой, в дальнейшем – УВЧ, электрофорез, ЛФК, легкий массаж. Больным с гемофилией рекомендуется диета, обогащенная витаминами А, В, С, D, солями кальция и фосфора.
Наблюдение. Пациентам показан охранительный режим, профилактика травм; диспансерное наблюдение педиатра, гематолога, детского стоматолога, детского ортопеда и др. специалистов; наблюдение в условиях специализированного гемофильного центра.
Хромосомная теория
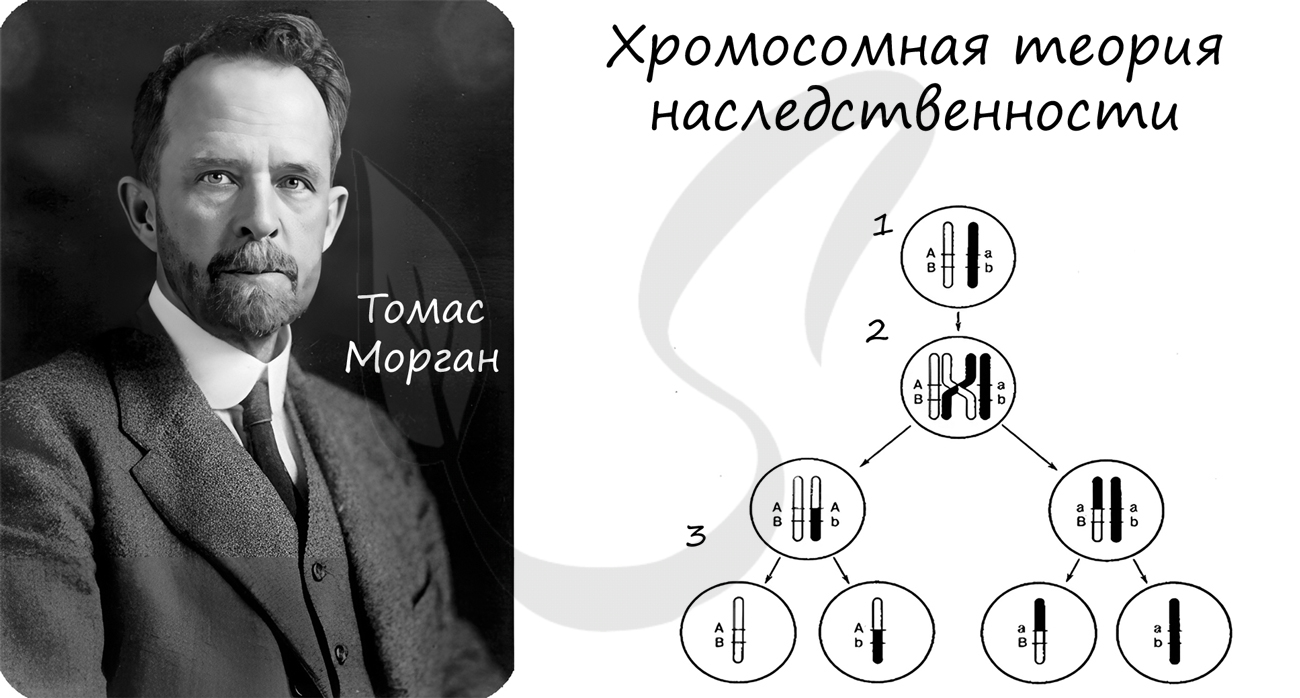
Хромосомная теория наследственности
Концепция данной теории заключается в том, что передача наследственной информации в ряду поколений осуществляется путем передачи хромосом, в которых в определенной линейной последовательности расположены гены.
Данная теория была сформулирована в начале XX века. Значительный вклад в ее развитие внес американский генетик Томас Морган.
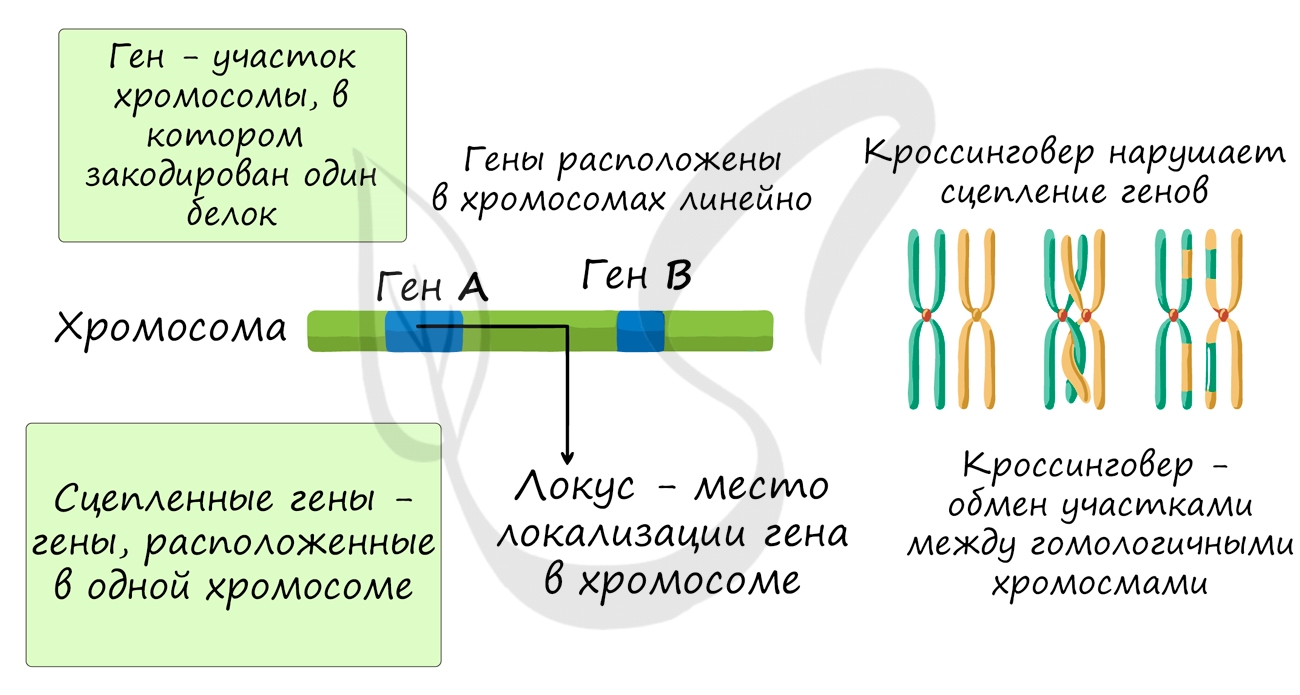
Группы сцепления
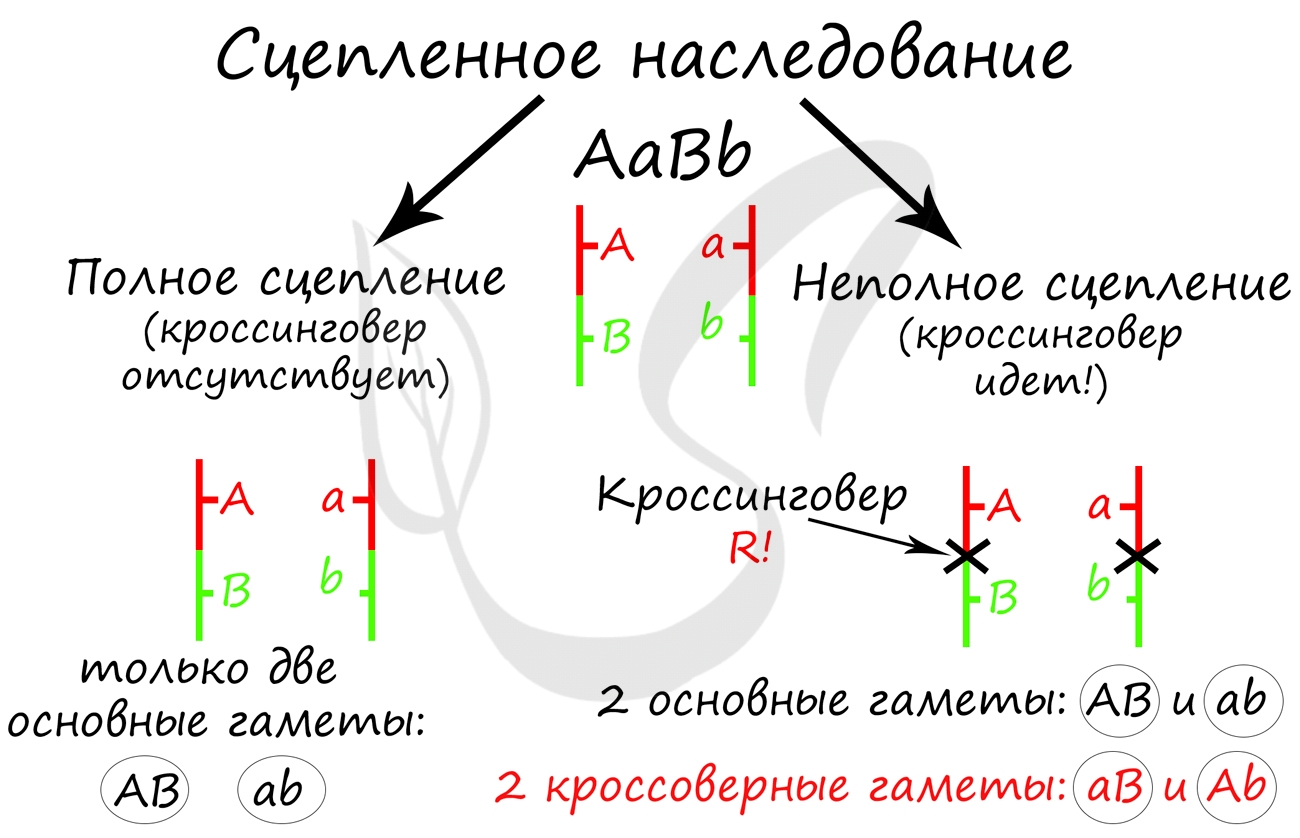
В предыдущей статье были раскрыты суть и применение в задачах III закона Менделя, закона независимого наследования, в основе которого лежат гены, расположенные в разных хромосомах. Но что если гены лежат в одной хромосоме? Такие гены образуют группу сцепления, в этом случае говорят о сцепленном наследовании.
Сцепление генов
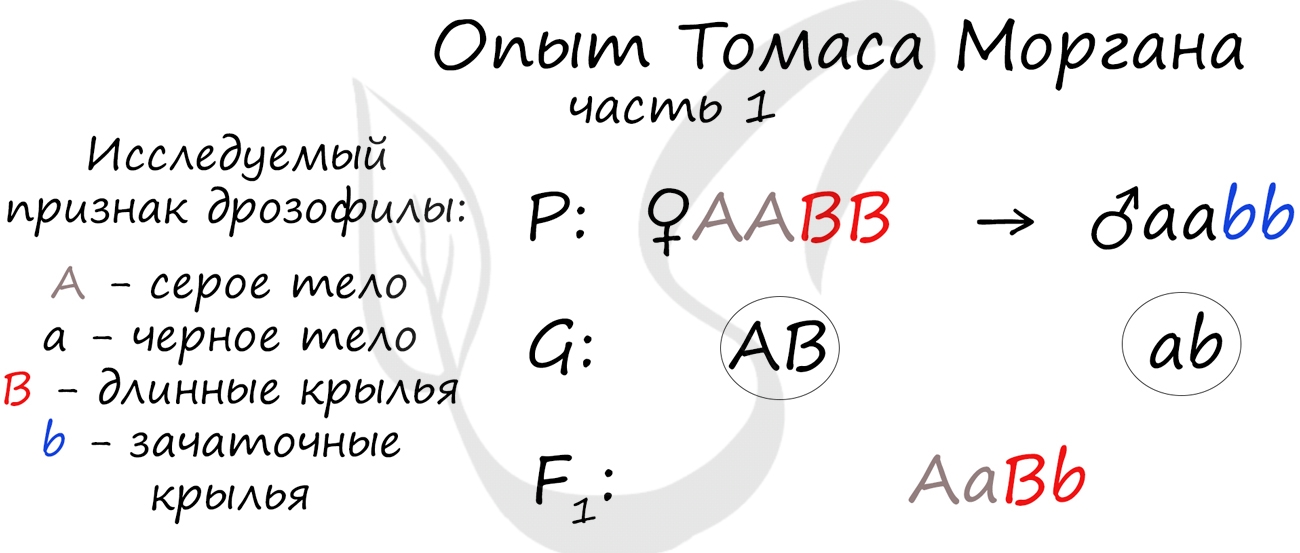
Далее Морган применил анализирующее скрещивание. Полученную в первом поколении дигетерозиготу (AaBb) он скрестил с черной особью с зачаточными крыльями (aabb). Результат весьма удивил Моргана и его коллег: помимо потомства с ожидаемыми фенотипами (серое тело + длинные крылья, черное тело + зачаточные крылья) были получены особи со смешанными признаками.
Потомство со смешанными признаками подразумевает под собой особи Aabb (серое тело + зачаточные крылья) и aaBb (черные тело + длинные крылья). Но откуда они могли взяться, если гены A и B находятся в одной хромосоме? Значит, образовались еще какие-то дополнительные гаметы, помимо AB и ab?
Пример решения генетической задачи №1
«Катаракта и полидактилия у человека обусловлены доминантными аутосомными генами, расположенными в одной хромосоме. Гены полностью сцеплены. Какова вероятность родить здорового ребенка в семье, где муж нормален, жена гетерозиготна по обоим признакам, мать жены также страдала обеими аномалиями, а отец был нормален».
Пример решения генетической задачи №2
«Гены доминантных признаков катаракты и эллиптоцитоза локализованы в 1-й аутосоме. Гены неполностью сцеплены. Женщина, болеющая катарактой и эллиптоцитозом, отец которой был здоров, выходит замуж за здорового мужчину. Определите возможные фенотипы потомства и вероятность рождения больного обеими аномалиями ребенка в этой семье».
Ключевые слова в тексте этой задачи, на которые следует обратить внимание: «гены неполностью сцеплены». Это означает, что между ними происходит кроссинговер.
Наследование, сцепленное с полом
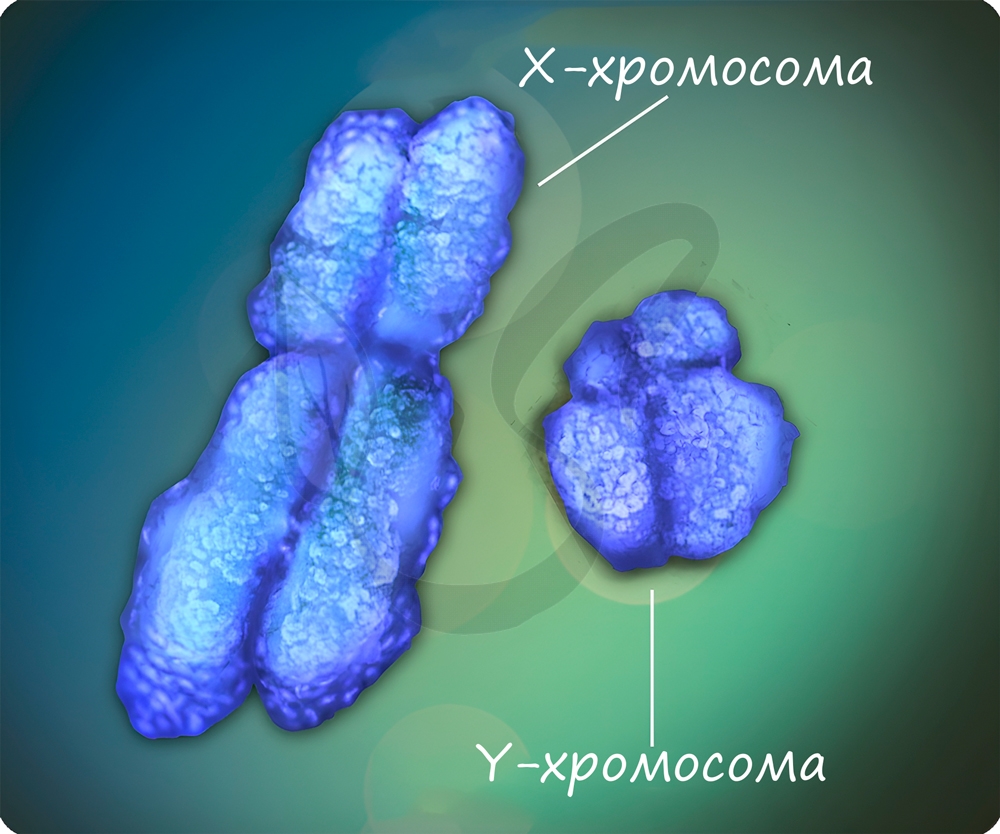
Природа, несомненно, бережет женских особей. Женщины имеют две гомологичные хромосомы XX, и если ген наследственного заболевания попал в одну из X-хромосом, то чаще всего в другой X-хромосоме окажется «здоровый» ген, доминантный, которой подавит действие рецессивного гена. С генетической точки зрения, женщина будет носительницей заболевания, может его передать по поколению, но сама болеть не будет.
У мужчин если ген заболевания оказался в X-хромосоме, то не проявиться он не может. Именно по этой причине мужчины чаще страдают дальтонизмом, гемофилией и т.д.
Пример решения генетической задачи №3
«Рецессивный ген дальтонизма располагается в X-хромосоме. Женщина с нормальным зрением (отец был дальтоник) выходит замуж за мужчину с нормальным зрением, отец которого был дальтоником. Определите возможные фенотипы потомства».
Пример решения генетической задачи №4
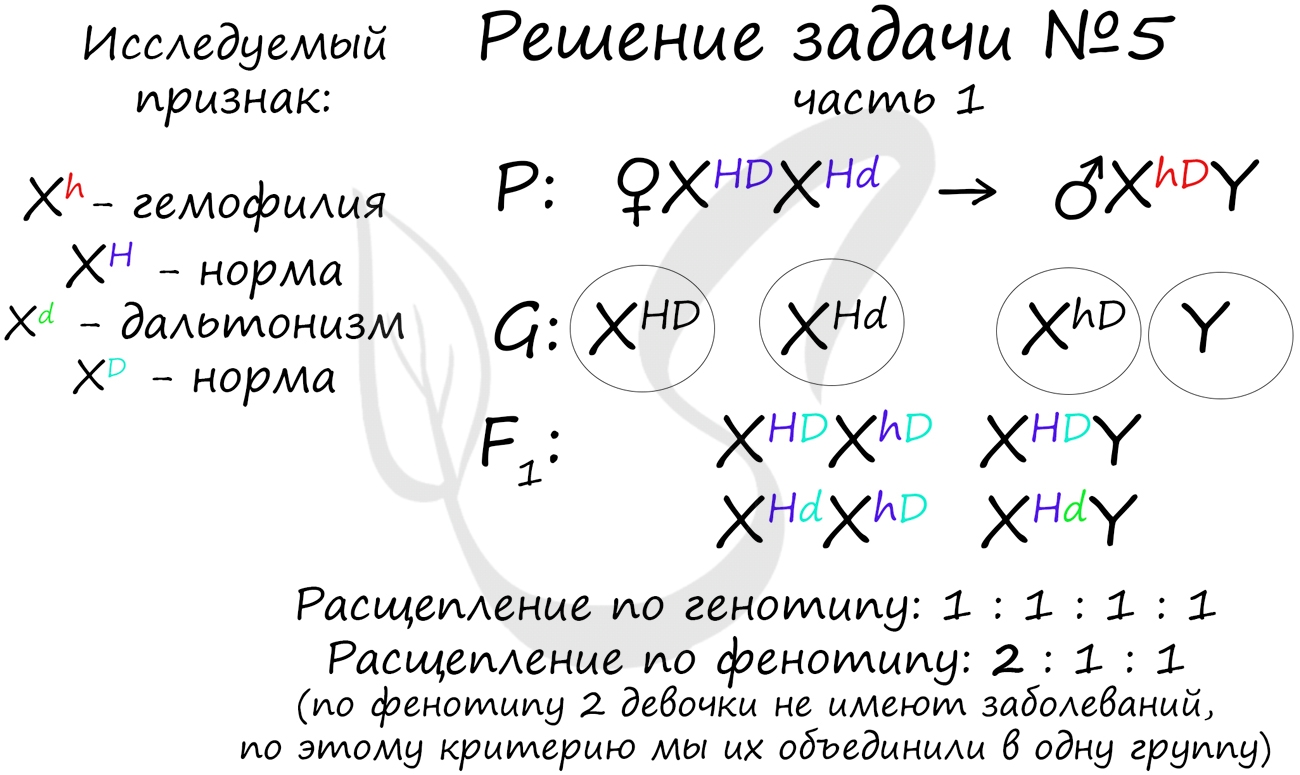
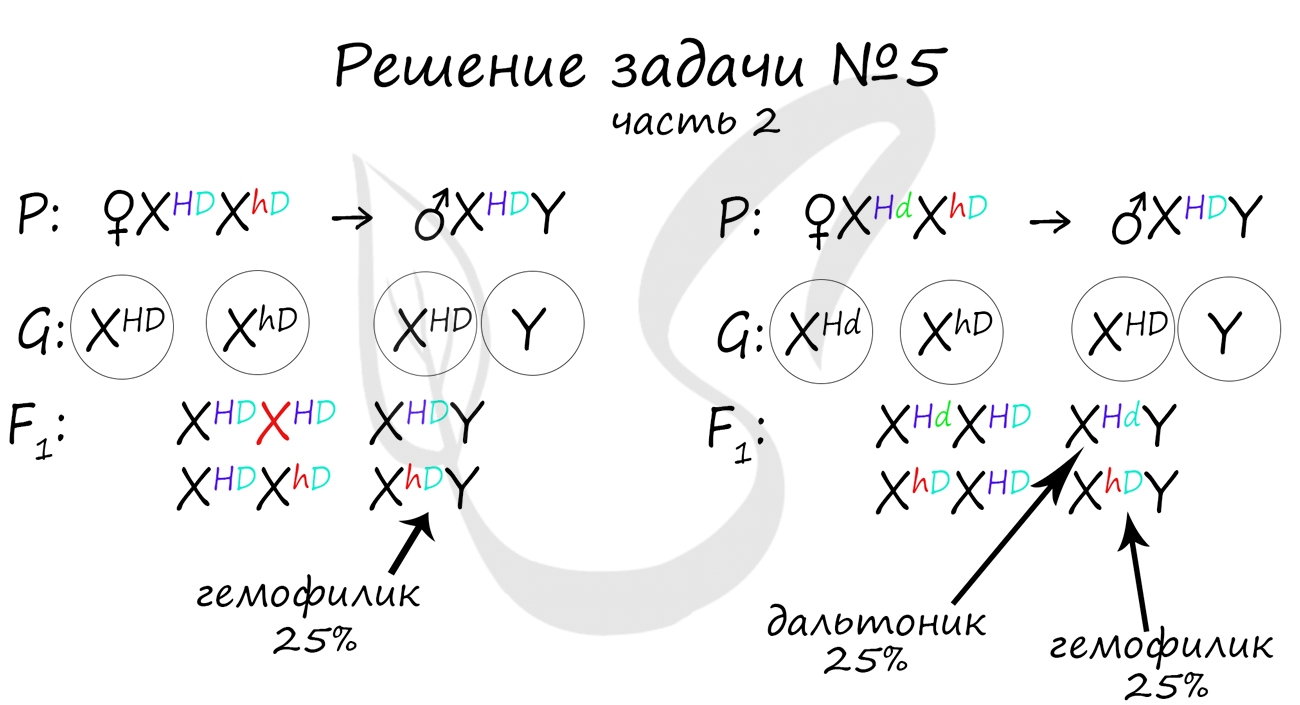
Пример решения генетической задачи №5
«Рецессивные гены, кодирующие признаки дальтонизма и гемофилии, сцеплены с X-хромосомой. Мужчина с нормальным цветовым зрением и гемофилией женится на здоровой женщине, отец которой был дальтоником, но не гемофиликом. Известно, что мать женщины была гомозиготна по исследуемым признакам. Какое потомство получится от брака их дочери со здоровым мужчиной?»
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Гемофилия
Гемофилия – наследственная патология системы гемостаза, в основе которой лежит снижение или нарушение синтеза VIII, IX или XI факторов свертывания крови. Специфическим проявлением гемофилии служит склонность больного к различным кровотечениям: гемартрозам, внутримышечным и забрюшинным гематомам, гематурии, желудочно-кишечным кровотечениям, длительным кровотечениям при операциях и травмах и др. В диагностике гемофилии первостепенное значение имеет генетическое консультирование, определение уровня активности факторов свертываемости, ДНК-исследование, анализ коагулограммы. Лечение гемофилии предполагает проведение заместительной терапии: трансфузии гемоконцентратов с факторами свертывания VIII или IX, свежезамороженной плазмы, антигемофильного глобулина и др.
Общие сведения
Гемофилия – заболевание из группы наследственных коагулопатий, обусловленное дефицитом факторов свертывания плазмы крови и характеризующееся повышенной склонностью к геморрагиям. Распространенность гемофилии А и В составляет 1 случай на 10000-50000 представителей мужского пола. Чаще всего дебют заболевания приходится на ранний детский возраст, поэтому гемофилия у ребенка является актуальной проблемой педиатрии и детской гематологии. Кроме гемофилии, у детей встречаются и другие наследственные геморрагические диатезы: геморрагическая телеангиэктазия, тромбоцитопатия, болезнь Гланцмана т. п.
Причины гемофилии
Гены, обусловливающие развитие гемофилии, сцеплены с половой Х-хромосомой, поэтому заболевание наследуется по рецессивному признаку по женской линии. Наследственной гемофилией болеют практически исключительно лица мужского пола. Женщины являются проводниками (кондукторами, носителями) гена гемофилии, передающими заболевание части своих сыновей.
У здорового мужчины и женщины-кондуктора с одинаковой вероятностью могут родиться как больные, так и здоровые сыновья. От брака мужчины, больного гемофилией со здоровой женщиной рождаются здоровые сыновья или дочери-кондукторы. Описаны единичные случаи гемофилии у девочек, рожденных от матери-носителя и больного гемофилией отца.
Врожденная гемофилия встречается почти у 70 % пациентов. В этом случае наследуется форма и тяжесть гемофилии. Около 30% наблюдений приходится на спорадические формы гемофилии, связанные с мутацией в локусе, кодирующем синтез плазменных факторов свертывания крови на Х-хромосоме. В дальнейшем такая спонтанная форма гемофилии становится наследственной.
Классификация гемофилии
В зависимости от дефицита того или иного фактора свертываемости крови, различают гемофилию А (классическую), В (болезнь Кристмаса), С и др.
Тяжесть клинического течения гемофилии зависит от степени недостаточности коагуляционной активности плазменных факторов свертывания крови.
Симптомы гемофилии
У новорожденных детей признаками гемофилии могут служить длительное кровотечение из культи пуповины, подкожные гематомы, кефалогематомы. Кровотечения у детей первого года жизни могут быть связаны с прорезыванием зубов, оперативными вмешательствами (инцизией уздечки языка, циркумцизио). Острые края молочных зубов могут стать причиной прикусывания языка, губ, щек и кровотечений из слизистых оболочек полости рта. Однако в грудном возрасте гемофилия дебютирует редко в связи с тем, что материнском молоке содержится достаточное количество активной тромбокиназы.
Вероятность посттравматических кровотечений значительно возрастает, когда ребенок с гемофилией начинает вставать и ходить. Для детей после года характерны носовые кровотечения, подкожные и межмышечные гематомы, кровоизлияния в крупные суставы. Обострения геморрагического диатеза случаются после перенесенных инфекций (ОРВИ, ветрянки, краснухи, кори, гриппа и др.) вследствие нарушения проницаемости сосудов. В этом случае нередко возникают самопроизвольные диапедезные геморрагии. Ввиду постоянных и длительных кровотечений у детей с гемофилией имеется анемия различной степени выраженности.
По степени убывания частоты кровоизлияния при гемофилии распределяются следующим образом: гемартрозы (70—80%), гематомы (10-20%), гематурия (14-20%), желудочно-кишечные кровотечения (8%), кровоизлияния в ЦНС (5%).
Гемартрозы являются наиболее частым и специфическим проявлением гемофилии. Первые внутрисуставные кровоизлияния у детей с гемофилией случаются в возрасте 1-8 лет после ушибов, травм или спонтанно. При гемартрозе выражен болевой синдром, отмечается увеличение сустава в объеме, гиперемия и гипертермия кожи над ним. Рецидивирующие гемартрозы приводят к развитию хронического синовита, деформирующего остеоартроза и контрактур. Деформирующий остеоартроз приводит к нарушению динамики опорно-двигательного аппарата в целом (искривлению позвоночника и таза, гипотрофии мышц, остеопорозу, вальгусной деформации стопы и др.) и к наступлению инвалидности уже в детском возрасте.
При гемофилии часто возникают кровоизлияния в мягкие ткани – подкожную клетчатку и мышцы. У детей обнаруживаются непроходящие синяки на туловище и конечностях, часто возникают глубокие межмышечные гематомы. Такие гематомы склонны к распространению, поскольку излившаяся кровь не сворачивается и, проникая вдоль фасций, инфильтрирует ткани. Обширные и напряженные гематомы могут сдавливать крупные артерии и периферические нервные стволы, вызывая интенсивные боли, паралич, атрофию мышц или гангрену.
Довольно часто при гемофилии возникают кровотечения из десен, носа, почек, органов ЖКТ. Кровотечение может быть инициировано любыми медицинскими манипуляциями (внутримышечной инъекцией, экстракцией зуба, тонзиллэктомией и др.). Крайне опасными для ребенка с гемофилией являются кровотечения из зева и носоглотки, поскольку могут привести к обструкции дыхательных путей и потребовать экстренной трахеостомии. Кровоизлияния в мозговые оболочки и головной мозг приводят к тяжелым поражениям ЦНС или летальному исходу.
Желудочно-кишечные кровотечения у пациентов с гемофилией могут быть связаны с приемом НПВС и др. лекарств, с обострением латентного течения язвенной болезни желудка и двенадцатиперстной кишки, эрозивным гастритом, геморроем. При кровоизлияниях в брыжейку и сальник развивается картина острого живота, требующая дифференциальной диагностики с острым аппендицитом, кишечной непроходимостью и др.
Характерным признаком гемофилии является отсроченный характер кровотечения, которое обычно развивается не сразу после травмы, а через некоторое время, иногда спустя 6-12 и более часов.
Диагностика гемофилии
Диагностика гемофилии проводится при участии ряда специалистов: неонатолога, педиатра, генетика, гематолога. При наличии у ребенка сопутствующей патологии или осложнений основного заболевания проводятся консультации детского гастроэнтеролога, детского травматолога-ортопеда, детского отоларинголога, детского невролога и др.
Супружеские пары, находящиеся в группе риска по рождению ребенка с гемофилией, должны пройти медико-генетическое консультирование еще на этапе планирования беременности. Выявить носительство дефектного гена позволяет анализ генеалогических данных и молекулярно-генетическое исследование. Возможно проведение пренатальной диагностики гемофилии с помощью биопсии хориона или амниоцентеза и исследования ДНК клеточного материала.
После рождения ребенка диагноз гемофилии подтверждается с помощью лабораторных исследований гемостаза. Основные изменения показателей коагулограммы при гемофилии представлены увеличением времени свертывания крови, АЧТВ, тромбинового времени, МНО, времени рекальцификации; уменьшением ПТИ и др. Решающее значение при диагностике формы гемофилии принадлежит определению снижения прокоагулянтной активности одного из факторов свертывания ниже 50%.
При гемартрозах ребенку с гемофилией проводится рентгенография суставов; при внутренних кровотечениях и забрюшинных гематомах – УЗИ брюшной полости и забрюшинного пространства; при гематурии – общий анализ мочи и УЗИ почек и т. д.
Лечение гемофилии
При гемофилии полное избавление от заболевания невозможно, поэтому основу лечения составляет заместительная гемостатическая терапия концентратами VIII и IX факторов свертывания крови. Необходимая доза концентрата определяется степенью выраженности гемофилии, тяжестью и видом кровотечения.
В лечении гемофилии выделяют два направления – профилактические и «по требованию», в период проявлений геморрагического синдрома. Профилактическое введение концентратов факторов свертывания крови показано пациентам с тяжелой формой гемофилии и проводится 2-3 раза в неделю для предупреждения развития гемофилической артропатии и прочих кровотечений. При развитии геморрагического синдрома требуются повторные трансфузии препарата. Дополнительно используются свежезамороженная плазма, эритромасса, гемостатики. Все инвазивные вмешательства у больных с гемофилией (наложение швов, удаление зубов, любые операции) проводятся под прикрытием гемостатической терапии.
При незначительных наружных кровотечениях (порезах, кровотечениях из полости носа и рта) может использоваться гемостатическая губка, наложение давящей повязки, обработка раны тромбином. При неосложненном кровоизлиянии ребенку необходим полный покой, холод, иммобилизация больного сустава гипсовой лонгетой, в дальнейшем – УВЧ, электрофорез, ЛФК, легкий массаж. Больным с гемофилией рекомендуется диета, обогащенная витаминами А, В, С, D, солями кальция и фосфора.
Прогноз и профилактика гемофилии
Длительная заместительная терапия приводит к изоиммунизации, образованию антител, блокирующих прокоагулянтную активность вводимых факторов, и неэффективности гемостатической терапии в обычных дозах. В таких случаях больному с гемофилией проводится плазмаферез, назначаются иммунодепрессанты. Поскольку больным с гемофилией проводится частое переливание компонентов крови, не исключается риск инфицирования ВИЧ-инфекцией, гепатитами В, С и D, герпесом, цитомегалией.
Легкая степень гемофилии не влияет на продолжительность жизни; при тяжелой гемофилии прогноз ухудшается при массивных кровотечениях, обусловленных операциями, травмами.
Научная электронная библиотека
Юров И. Ю., Воинова В. Ю., Ворсанова С. Г., Юров Ю. Б.,
4.3. Наследование, сцепленное с полом
Х-сцепленное наследование принято делить на Х-сцепленное рецессивное и Х-сцепленное доминантное.
Х-сцепленное рецессивное наследование
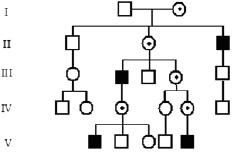
Поскольку мужчины имеют только одну хромосому Х, они являются гемизиготными по Х-сцепленным генам. Х-сцепленные рецессивные болезни проявляются у мальчиков, которые имеют только один мутантный аллель, а передаются здоровыми гетерозиготными женщинами-носительницами их сыновьям. Пораженные мужчины, в свою очередь, передают мутантный ген своим дочерям – облигатным носительницам, но не сыновьям. Этот тип передачи в родословной иногда называют «диагональным» (рис. 12).
Рис. 12. Родословная при Х-сцепленном рецессивном типе наследовании
Генетический риск. Если облигатная носительница Х-сцепленной рецессивной мутации вступает в брак со здоровым мужчиной, то каждый их сын будет иметь 50 %-й риск заболевания, а каждая дочь – 50 %-й риск быть носительницей. Поскольку мужчина передает хромосому Х только своим дочерям, а хромосому Y – сыновьям, то все дочери пораженных мужчин от браков со здоровыми женщинами являются облигатными носительницами, а все их сыновья здоровы. Таким образом, мужчина не может передать Х-сцепленное заболевание своему сыну за очень редким исключением при унипарентальной гетеродисомии.
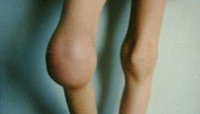
В качестве примера Х-сцепленного рецессивного заболевания можно привести мышечную дистрофию Дюшена. Это самая частая мышечная дистрофия, первыми признаками которой являются переваливающаяся походка, трудности при подъеме по лестнице без болевых ощущений и тенденция к падениям ребёнка при ходьбе. Мышечная слабость
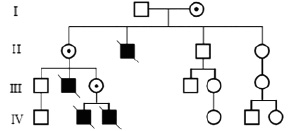
прогрессирует и пораженные мальчики умирают в конце второго – начале третьего десятилетия жизни. Таким образом, пораженные мужчины не имеют детей и не передают соответствующие мутации потомкам (рис. 13).
Рис. 13. Родословная семьи с мышечной дистрофией Дюшена
Вариабельная экспрессивность у женщин-гетерозигот. При многих Х-сцепленных болезнях женщины-гетерозиготы имеют мозаичный фенотип. Например, при Х-сцепленном альбинизме радужная оболочка и глазное дно больных мужчин не имеют пигмента, а у гетерозиготных женщин выявляется мозаичная (пятнистая) пигментация. Это объясняется феноменом Х-инактивации.
Х-сцепленное доминантное наследование
Х-сцепленные доминантные болезни являются редкими и выявляются у женщин-гетерозигот, а также у мужчин-гемизигот, имеющих мутантный аллель на единственной хромосоме Х. Х-сцепленное доминантное наследование напоминает аутосомно-доминантное. Но есть значимое отличие: пораженные мужчины передают заболевание только своим дочерям, а передача от отца к сыну невозможна (рис. 14). Примером этого типа наследования является витамин Д-резистентный рахит, при котором женщины обычно имеют более легкие формы заболевания, чем мужчины.
При многих Х-сцепленных доминантных болезнях у женщин может наблюдаться мозаицизм проявления болезни. Например, при синдроме Блоха – Сульцбергера (синдром недержания пигмента, тип II) наблюдается мозаичная пигментация кожи. Кроме того, это заболевание, также как синдром Ретта, является примером болезни, летальной для плодов мужского пола.
Рис. 14. Родословная при Х-сцепленном доминантном типе наследования
Наследование, сцепленное с хромосомой Y
Наследование, сцепленное с хромосомой Y, предполагает, что болеют только мальчики. Заболевание передается только от отца к сыну. В случае мутаций в генах хромосомы Y, вовлеченных в сперматогенез, возникает бесплодие вследствие азооспермии у мужчин. Технологии искусственного оплодотворения позволяют им иметь детей, но если при этом рождается сын, он также страдает азооспермией.
Влияние пола. Некоторые аутосомные признаки значительно чаще выявляются у одного из полов. Этот феномен получил название влияние пола. Лысина у мужчин является примером аутосомно-доминантного признака, ограниченного полом, что, по-видимому, является результатом влияния мужских половых гормонов. Другой пример – подагра, которая является очень редким состоянием у женщин до менопаузы, но после нее частота этого заболевания возрастает. При гемохроматозе
(аутосомно-рецессивном заболевании) у женщин-гомозигот намного реже возникает перегрузка железом и связанные с ней симптомы, чем у мужчин-гомозигот. Объяснением является физиологическая потеря железа женщинами во время менструаций.
Ограничение полом – это проявление определенных признаков у индивидуумов только одного пола. Пример: вирилизация девочек с аутосомно-рецессивным эндокринным заболеванием – врожденной гиперплазией коры надпочечников.
В табл. 4 кратко представлены основные признаки менделевских типов наследования.
Признаки менделевских типов наследования
Особенности заболевания у лиц разного пола
Особенности передачи
в родословной
Мужчины и женщины болеют в равной пропорции
«Вертикальный» тип передачи – больные во многих поколениях родословной. Передача от лица любого пола лицу любого пола.
Мужчины и женщины болеют в равной пропорции
«Горизонтальный» тип передачи – больные в одном поколении. Родители больного (больных) нередко могут быть родственниками.
Как правило, больны мужчины
«Диагональный» тип передачи: мужчины не могут передавать заболевание своим сыновьям. Возможна передача только внуку от деда через его дочь, которая является непораженой облигатной носительницей.
Болеют мужчины и женщины с преобладанием женщин. Женщины поражены в меньшей степени, чем мужчины. В случае летальных для мальчиков болезней поражены только девочки, наблюдаются спонтанные аборты в семье.
Пораженные мужчины могут передавать заболевание своим дочерям, но не сыновьям. Передача от мужчины к мужчине исключает Х-сцепленный тип наследования.
Сцепленный с хромосомой Y
Болеют только мужчины.
Пораженные мужчины могут передавать заболевание только своим сыновьям.
Множественные аллели и комплексные признаки
Выше рассмотрены признаки, с которыми связаны только два аллеля – нормальный и мутантный. Некоторые гены имеют более двух аллельных форм, т.е. множественные аллели. Некоторые из них могут быть доминантными, другие – рецессивными по отношению к нормальному аллелю. Пример множественных аллелей – наследование групп крови человека.
Развитие генетики сделало возможным исследование комплексных признаков, которые формируются при взаимодействии нескольких генов. На этой основе возникла концепция олигогенного (дигенного и триаллельного) наследования.
При дигенном наследовании наблюдается аддитивный эффект гетерозиготных мутаций в двух различных локусах. Например, одна из форм пигментного ретинита, приводящая к потере зрения, вызвана гетерозиготностью по мутациям двух генов (ROM1 и periferin). Оба эти гена кодируют белки, присутствующие в фоторецепторах сетчатки глаза. Индивидуумы, гетерозиготные по мутации только одного из этих двух генов, не имеют клинических проявлений.
Триаллельное наследование можно рассмотреть на примере синдрома Барде-Бидля – редкого заболевания, характеризующегося ожирением, полидактилией, аномалиями почек, пигментным ретинитом и когнитивными нарушениями. Семь различных генных локусов, мутации в которых ведут к синдрому Барде–Бидля, были идентифицированы. До недавнего времени считалось, что заболевание наследуется аутосомно-рецессивно. Однако, сейчас известно, что есть одна форма синдрома, когда индивидуум, гомозиготный по мутациям одного локуса, является также гетерозиготным по мутации другого локуса. Таким образом, для того, чтобы заболевание проявлялось, необходимо три мутантных аллеля.
Антиципация. При некоторых аутосомно-доминантных болезнях манифестация симптомов более ранняя и течение болезни более тяжелое у потомков по сравнению с их родителями, также страдающими этим заболеванием. Феномен увеличения тяжести болезни из поколения в поколение называют антиципацией. Одним из объяснений антиципации является экспансия нестабильных триплетных повторов. В качестве примеров можно привести такие болезни экспансии триплетных повторов как миотоническая дистрофия, хорея Гентингтона, болезнь Кеннеди.