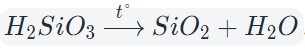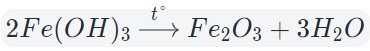Что значит солеобразующие и несолеобразующие оксиды
СОЛЕОБРАЗУЮЩИЕ НЕСОЛЕОБРАЗУЮЩИЕ
 |  |
Основные Амфотерные Кислотные
Несолеобразующие оксиды – это оксиды, которые не взаимодействуют ни с основаниями, ни с кислотами и поэтому не образуют солей. К ним относятся: N2O, NO, SiO, CO (CO с расплавами щелочей образует соли муравьиной кислоты – формиаты). Такие оксиды не имеют гидратов (водных соединений).
Солеобразующие оксиды – это оксиды, которые при взаимодействии с кислотами или основаниями (или с теми и другими) образуют соли. Таким оксидам в качестве гидратов соответствуют основания, кислоты или амфотерные гидроксиды.
ОСНОВНЫЕ ОКСИДЫ
Основные оксиды – это оксиды, которым в качестве гидратов (водных соединений) соответствуют основания, а при взаимодействии с кислотами они образуют соли. К ним относятся только оксиды металлов: Li2O, Na2O, K2O, Rb2O, Cs2O, Fr2O, MgO, CaO, SrO, BaO, RaO, Cu2O, Ag2O, In2O, PoO, Sc2O3, La2O3, TiO, HfO, CrO, MnO, FeO, CoO, NiO и др.
Физические свойства.Основные оксиды при обычных условияхтвердые кристаллические вещества преимущественно с ионной кристаллической решеткой.Имеют разную окраску. Оксиды щелочных и щелочноземельных металлов растворимы в воде.
Химические свойства.
1. Оксиды щелочных и щелочноземельных металлов взаимодействуют с водой с образованием щелочей:
2. Взаимодействуют с кислотами с образованием соли и воды:
3. Взаимодействуют с кислотными оксидами, образуя соль:
4. Взаимодейстуют с амфотерными оксидами, образуя соль:
ZnO + CaO = CaZnO2 (в расплаве).
КИСЛОТНЫЕ ОКСИДЫ
Кислотные оксиды – это оксиды, которым в качестве гидратов соответствуют кислоты, а при взаимодействии с основаниями они образуют соли. Кислотные оксиды делят на оксиды неметаллов и оксиды металлов.
Кислотные оксиды неметаллов и соответствующие им кислоты:
Классификация неорганических веществ
Среди простых веществ выделяют металлы и неметаллы. Среди сложных: оксиды, основания, кислоты и соли. Классификация неорганических веществ построена следующим образом:
Большинство химических свойств мы изучим по мере продвижения по периодической таблице Д.И. Менделеева. В этой статье мне хотелось бы подчеркнуть ряд принципиальных деталей, которые помогут в дальнейшем при изучении химии.
Оксиды
Все оксиды подразделяются на солеобразующие и несолеобразующие. Солеобразующие имеют соответствующие им основания и кислоты (в той же степени окисления (СО)!) и охотно вступают в реакции солеобразования. К ним относятся, например:
Солеобразующие оксиды, в свою очередь, делятся на основные, амфотерные и кислотные.
Основным оксидам соответствуют основания в той же СО. В химических реакциях основные оксиды проявляют основные свойства, образуются исключительно металлами. Примеры: Li2O, Na2O, K2O, Rb2O CaO, FeO, CrO, MnO.
Основные оксиды взаимодействуют с водой с образованием соответствующего основания (реакцию идет, если основание растворимо) и с кислотными оксидами и кислотами с образованием солей. Между собой основные оксиды не взаимодействуют.
Li2O + H2O → LiOH (основный оксид + вода → основание)
Здесь не происходит окисления/восстановления, поэтому сохраняйте исходные степени окисления атомов.
Эти оксиды действительно имеют двойственный характер: они проявляют как кислотные, так и основные свойства. Примеры: BeO, ZnO, Al2O3, Fe2O3, Cr2O3, MnO2, PbO, PbO2, Ga2O3.
С водой они не взаимодействуют, так как продукт реакции, основание, получается нерастворимым. Амфотерные оксиды реагируют как с кислотами и кислотными оксидами, так и с основаниями и основными оксидами.
ZnO + KOH + H2O → K2[Zn(OH)4] (амф. оксид + основание = комплексная соль)
ZnO + N2O5 → Zn(NO3)2 (амф. оксид + кисл. оксид = соль; СО азота сохраняется в ходе реакции)
Fe2O3 + HCl → FeCl3 + H2O (амф. оксид + кислота = соль + вода; обратите внимание на то, что СО Fe = +3 не меняется в ходе реакции)
Проявляют в ходе химических реакций кислотные свойства. Образованы металлами и неметаллами, чаще всего в высокой СО. Примеры: SO2, SO3, P2O5, N2O3, NO2, N2O5, SiO2, MnO3, Mn2O7.
Кислотные оксиды вступают в реакцию с основными и амфотерными, реагируют с основаниями. Реакции между кислотными оксидами не характерны.
SO2 + Na2O → Na2SO3 (кисл. оксид + осн. оксид = соль; сохраняем СО S = +4)
SO3 + Li2O → Li2SO4 (кисл. оксид + осн. оксид = соль; сохраняем СО S = +6)
P2O5 + NaOH → Na3PO4 + H2O (кисл. оксид + основание = соль + вода)
Реакции несолеобразующих оксидов с основаниями, кислотами и солеобразующими оксидов редки и не приводят к образованию солей. Некоторые из несолеобразующих оксидов используют в качестве восстановителей:
FeO + CO → Fe + CO2 (восстановление железа из его оксида)
Основания
Основания классифицируются по количеству гидроксид-ионов в молекуле на одно-, двух- и трехкислотные.
Так же, как и оксиды, основания различаются по свойствам. Все основания хорошо реагируют с кислотами, даже нерастворимые основания способны растворяться в кислотах. Также нерастворимые основания при нагревании легко разлагаются на воду и соответствующий оксид.
Mg(OH)2 → (t) MgO + H2O (при нагревании нерастворимые основания легко разлагаются)
Если в ходе реакции основания с солью выделяется газ, выпадает осадок или образуется слабый электролит (вода), то такая реакция идет. Нерастворимые основания с солями почти не реагируют.
Ba(OH)2 + NH4Cl → BaCl2 + NH3 + H2O (в ходе реакции образуется нестойкое основание NH4OH, которое распадается на NH3 и H2O)
KOH + BaCl2 ↛ реакция не идет, так как в продуктах нет газа/осадка/слабого электролита (воды)
В растворах щелочей pH > 7, поэтому лакмус окрашивает их в синий цвет.
Al(OH)3 + HCl → AlCl3 + H2O (амф. гидроксид + кислота = соль + вода)
Al(OH)3 + KOH → K[Al(OH)4] (амф. гидроксид + основание = комплексная соль)
При нагревании до высоких температур комплексные соли не образуются.
Кислоты
Кислоты отлично реагируют с основными оксидами, основаниями, растворяя даже те, которые выпали в осадок (реакция нейтрализации). Также кислоты способны вступать в реакцию с теми металлами, которые стоят в ряду напряжений до водорода (то есть способны вытеснить его из кислоты).
Zn + HCl → ZnCl2 + H2↑ (реакция идет, так как цинк стоил в ряду активности левее водорода и способен вытеснить его из кислоты)
Cu + HCl ↛ (реакция не идет, так как медь расположена в ряду активности правее водорода, менее активна и не способна вытеснить его из кислоты)
Все кислоты подразделяются на сильные и слабые. Напомню, что мы составили подробную таблицу сильных и слабых кислот (и оснований!) в теме гидролиз. В реакции из сильной кислоты (соляной) можно получить более слабую, например, сероводородную или угольную кислоту.
В завершении подтемы кислот предлагаю вам вспомнить названия основных кислот и их кислотных остатков.
Блиц-опрос по теме Классификация неорганических веществ
Они бывают солеобразующими и несолеобразующие



Солеобразующие оксиды– это такие оксиды, которые в результате химических реакций образуют соли. Это оксиды металлов и неметаллов, которые при взаимодействии с водой образуют соответствующие кислоты, а при взаимодействии с основаниями – соответствующие кислые и нормальные соли. Например, оксид меди (CuO) является оксидом солеобразующим, потому что, например, при взаимодействии её с соляной кислотой (HCl) образуется соль:
В результате химических реакций можно получать и другие соли:
Несолеобразующими оксидами называются такие оксиды, которые не образуют солей. Примером могут служить СО, N2O, NO.
Солеобразующие оксиды в свою очередь бывают 3-х типов: основными (от слова«основание»), кислотными и амфотерными.
Основными оксидаминазываются такие оксиды металлов, которым соответствуют гидроксиды, относящиеся к классу оснований. К основным оксидам относятся, например, Na2O, K2O, MgO, CaO и т.д.
Химические свойства основных оксидов
1. Растворимые в воде основные оксиды вступают в реакцию с водой, образуя основания:
2. Взаимодействуют с кислотными оксидами, образуя соответствующие соли
3. Реагируют с кислотами, образуя соль и воду:
4. Реагируют с амфотерными оксидами:
Если в составе оксидов в качестве второго элемента будет неметалл или металл, проявляющий высшую валентность (обычно проявляют от IV до VII), то такие оксиды будут кислотными. Кислотными оксидами (ангидридами кислот) называются такие оксиды, которым соответствуют гидроксиды, относящие к классу кислот. Это, например, CO2, SO3, P2O5, N2O3, Cl2O5, Mn2O7 и т.д. Кислотные оксиды растворяются в воде и щелочах, образуя при этом соль и воду.
Химические свойства кислотных оксидов
1. Взаимодействуют с водой, образуя кислоту:
Но не все кислотные оксиды непосредственно реагируют с водой (SiO2 и др.).
2. Реагируют с основанными оксидами с образованием соли:
3. Взаимодействуют со щелочами, образуя соль и воду:
В состав амфотерного оксидавходит элемент, который обладает амфотерными свойствами. Под амфотерностью понимают способность соединений проявлять в зависимости от условий кислотные и основные свойства. Например, оксид цинка ZnO может быть как основанием, так и кислотой (Zn(OH)2 и H2ZnO2). Амфотерность выражается в том, что в зависимости от условий амфотерные оксиды проявляют либо осно́вные, либо кислотные свойства.
Солеобразующие и несолеобразующие оксиды.
Оксиды подразделяются на солеобразующие и несолеобразующие.
Солеобразующими называют такие оксиды, которые в результате химических реакций способны образовывать соли.
— Дайте определение понятию «Соли».
Несолеобразующие оксиды такой способностью не обладают. Примером несолеобразующих оксидов могут служить следующие вещества: CO, N2O, NO.
Солеобразующие оксиды, в свою очередь подразделяются на основные, кислотные и амфотерные.
Основные, амфотерные и кислотные оксиды. Зависимость характера оксида от степени окисления образующего его металла.
Основными оксидами называются такие оксиды, которым в качестве гидратов (продуктов присоединения воды) соответствуют основания.
Основные оксиды Соответствующая гидратная форма(основание)
Кислотными оксидами называются такие оксиды, которым в качестве гидратов соответствуют кислоты. Кислотные оксиды называют также ангидридами кислот. Например: кислотные оксиды и соответствующая гидратная форма (кислота)
Большинство кислотных оксидов могут взаимодействовать с водой непосредственно и при этом образовывать кислоты.
Некоторые оксиды непосредственно с водой не взаимодействуют. Такого типа оксиды сами могут быть получены из кислот. Например:
Амфотерные оксиды представляют собой оксиды, которые в зависимости от условий проявляют свойства как основных (в кислой среде), так и кислотных (в щелочной среде) оксидов.
К амфотерным оксидам относятся только оксиды некоторых металлов.
а) В кислой среде PbO (оксид свинца (II)) проявляет свойства основного оксида
б) в щелочной среде PbO проявляет свойства кислотного оксида.
Химические свойства оксидов.
| Схема реакций | Примеры | |
| 1. Оксид основный | + кислота = соль (раств.)+ вода | CaO + 2HCl = CaCl2 + H2O 3Na2O + 2H3PO4 = 2Na3PO4 + 3H2O |
| + вода = гидроксид (раств.) | ВaO + H2O = Вa(OH)2 Na2O + H2O = 2NaOH | |
| + вода ≠ гидроксид (нераств.) | FeO + H2O ≠ MgO + H2O ≠ | |
| + кислотный оксид = соль(раств.) | CaO + СO2 = CaCO3 FeO + SO3 = FeSO4 | |
| разлагаются HgO, Ag2O | 2HgO 2Hg + O2 2 Ag2O 4Ag + O2 | |
| 2. Оксид амфотерный | + кислота = соль (раств.)+ вода | Al2O3 +3H2SО4 = Al2(SO4)3 + 3H2O |
| + щелочь = соль + вода | Al2O3 + 2NaOHH2O + 2NaAlO2 ZnO + 2NaOHH2O + Na2ZnO2 | |
| + вода ≠ | Al2O3 + H2O ≠ | |
| 3. Оксид кислотный | + щелочь = соль + вода | SO2 + 2KOH = K2SO3 + H2O P2O5 + 6NaOH = 2Na3PO4 + 3H2O |
| + вода = кислота, растворимая в воде | SO2 + H2O = H2SO3 P2O5 + 3H2O = 2H3PO4 | |
| + вода ≠ кислота, нераств. в воде | SiO2 + H2O ≠ | |
| + основной оксид = соль | 3CaO + P2O5 = Ca3(PO4)2 | |
| + соль = соль(раств.) + кислотный оксид | SiO2 + CaCO3 = CaSiO3 + CO2 |
Получение оксидов.
1) окисление металлов: 2Cu + O2 = 2CuO оксид меди (II) черный налет
2) окисление неметаллов: C + O2 = CO2 оксид углерода (IV)
3) разложение кислот: Н2SО4 = SО2 + Н2О оксид серы (IV)
4) разложение солей: CaCО3 = CaО + CО2
5) разложение оснований: Fe(ОН)2 = FeО + Н2О оксид железа (II)
Вопросы для самоконтроля
1) Вещества подразделяют на простые и сложные, укажите их отличия?
2) Перечислите классы неорганических соединений.
3) Дайте определение понятию «Оксиды».
4) Перечислите виды оксидов.
5) Дайте определения понятий основных, кислотных, амфотерных оксидов.
6) Дайте определение понятию «Основания».
7) Какие элементы образуют основные оксиды?
8) Какие оксиды относят к кислотным?
9) Дайте определение понятию «Кислоты»
10) Какие элементы образуют кислотные оксиды?
11) Назовите особенности амфотерных оксидов.
12) Как изменяют цвета индикаторы в кислой среде?
13) Как изменяют цвета индикаторы в щелочной среде?
14) Напишите уравнения диссоциации: воды, гидроксида натрия, соляной кислоты, хлорида натрия.
15) Какие элементы образуют амфотерные оксиды?
16) Закончите уравнения химических реакций, дайте название веществам:
а) P + O2 →
б) Al + O2 →
в) H2SO4 + Fe2O3 →
г) BaO + HCl →
д) C2H4 + O2 →
С какими из следующих веществ будет реагировать ВаО:
| ВаО + SO3 → |
| ВаО + P2O5 → |
| ВаО + NaOH→ |
| ВаО + Na2SO4 → |
| ВаО + HNO3→ |
| AI2О3+ SO3 → |
| AI2О3 + P2O5 → |
| AI2О3 + NaOH→ |
| AI2О3 + Na2SO4 → |
| AI2О3 + HNO3→ |
| N2О5 + SO3 → |
| N2О5 + P2O5 → |
| N2О5 + NaOH→ |
| N2О5 + Na2SO4 → |
| N2О5 + HNO3→ |
17.Из приведенных формул оксидов выписать оксиды:
А) Солеобразующие : основные, кислотные, амфотерные Б) Несолеобразующие.
| Солеобразующие | Несолеобразующие | |
| Основные | Кислотные | Амфотерные |
ПЛАН ЗАНЯТИЯ №17
Дисциплина: Химия.
Тема: Классификация химических реакций.
Цель занятия: систематизировать, обобщить и углубить знания учащихся о химических реакциях и их классификации, развить навыки самостоятельной работы, умения записывать уравнения реакций и расставлять коэффициенты, указывать типы реакций, делать выводы и обобщения.
Предметные: сформированность умения давать количественные оценки и производить расчеты по химическим формулам и уравнениям;
Метапредметные: использование различных видов познавательной деятельности и основных интеллектуальных операций (постановки задачи, формулирования гипотез, анализа и синтеза, сравнения, обобщения, систематизации, выявления причинно-следственных связей, поиска аналогов, формулирования выводов) для решения поставленной задачи;
Личностные: готовность к продолжению образования и повышения квалификации в избранной профессиональной деятельности и объективное осознание роли химических компетенций в этом;
Норма времени:2 часа
Вид занятия:Лекция.
План занятия:
1) Реакции соединения, разложения, замещения, обмена.
Оснащение:Учебник.
Литература:
Преподаватель:Тубальцева Ю.Н.
Оксиды
Определение оксидов
Оксиды — это сложные вещества, состоящие из двух химических элементов (т. е. бинарные соединения), один из которых — кислород в степени окисления −2.
Общая формула оксидов: ЭxOy, где Э – химический элемент, а x и y — индексы, определяемые степенью окисления химических элементов.
Виды оксидов
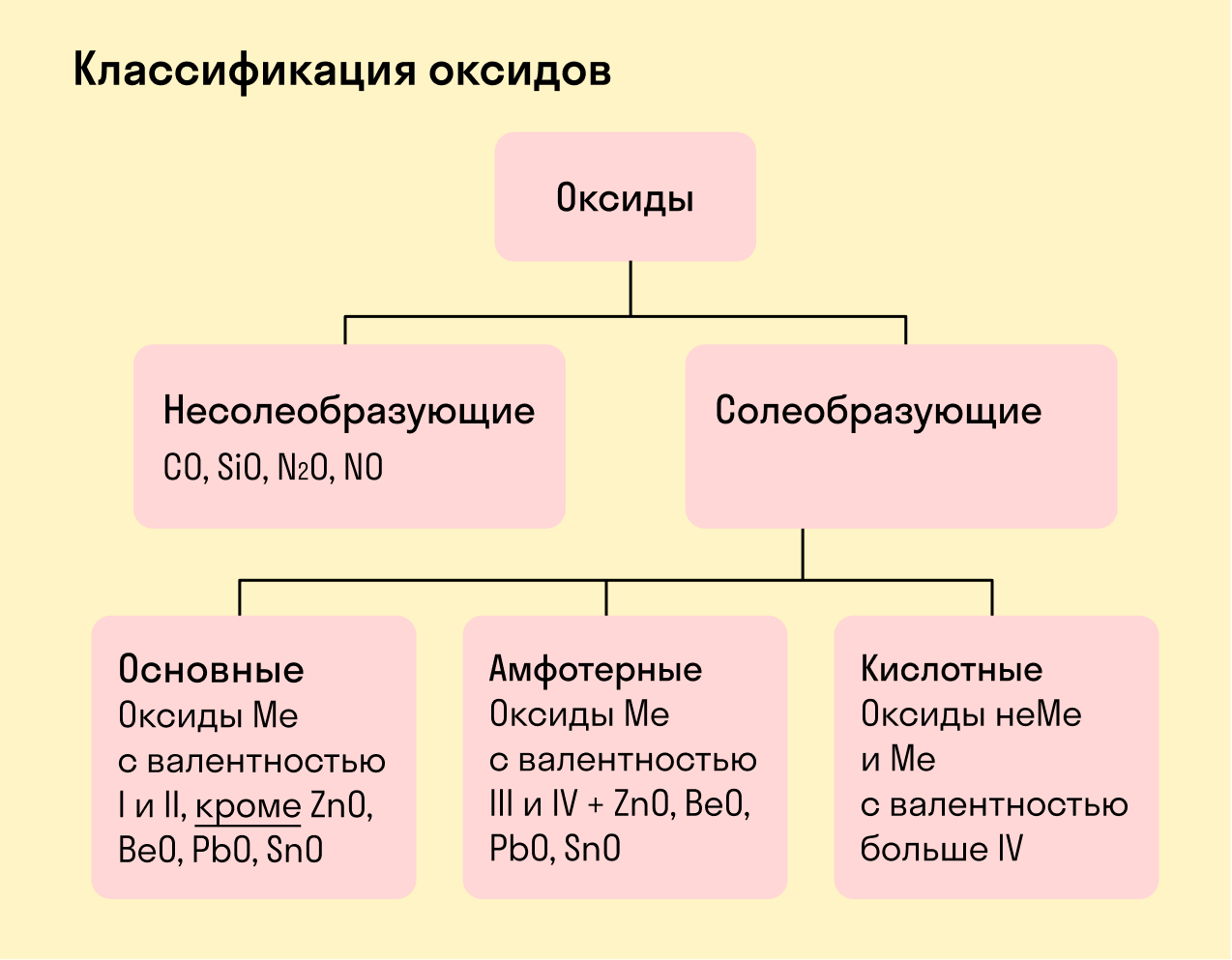
Все оксиды делятся на солеобразующие и несолеобразующие.
Несолеобразующие оксиды — это оксиды, которые не взаимодействуют с кислотами и щелочами, то есть не способны образовать соли.
К несолеобразующим оксидам относят: CO, SiO, N2O, NO.
Солеобразующие оксиды — это оксиды, которые взаимодействуют с кислотами и щелочами с образованием солей.
Солеобразующие оксиды делятся на три группы:
Основные оксиды — это оксиды, образованные металлами со степенью окисления +1 или +2.
Примеры основных оксидов: Na +1 2O, Ca +2 O, Ba +2 O.
Амфотерные оксиды — оксиды, образованные металлами со степенью окисления +3 или +4.
К амфотерным оксидам относят также: ZnO, BeO, PbO, SnO.
Несмотря на то, что эти металлы проявляют степень окисления +2 в данных соединениях, их оксиды проявляют амфотерные свойства.
Примеры амфотерных оксидов: Al +3 2O3, Fe2 +3 O3.
Кислотные оксиды — оксиды, образованные металлами с валентностью V и более или неметаллами с любой валентностью (за исключением несолеобразующих оксидов, то есть CO, SiO, N2O, NO).
Примеры кислотных оксидов: S +6 O3, N2 +5 O5, Mn2 +7 O7.
Если один и тот же химический элемент образовывает несколько оксидов, то с увеличением степени окисления основные свойства оксидов ослабевают и усиливаются кислотные.
CrO (оксид хрома (II)) — проявляет основные свойства;
Cr2O3 (оксид хрома (III)) — проявляет амфотерные свойства;
CrO3 (оксид хрома (VI)) — проявляет кислотные свойства.
Закрепим знания о типах оксидов, изучив схему:
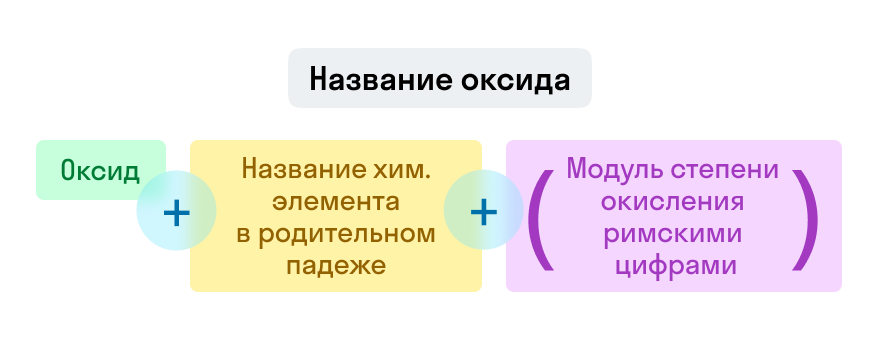
Номенклатура оксидов
Названия оксидов строятся по систематической номенклатуре следующим образом:
Указываем название второго химического элемента в родительном падеже.
Если этот элемент имеет переменную валентность, то указываем валентность элемента в этом соединении в скобках римской цифрой.
Примеры названий оксидов:
Fe2O3 — оксид железа (III). Читается: феррум два о три.
Na2O — оксид натрия. Читается: натрия два о.
SO3 — оксид серы (VI). Читается: эс о три.
До появления систематической номенклатуры вещества называли по присущим им специфическим свойства (цвету, запаху и т. д.). Такой способ названия веществ — тривиальная номенклатура. Некоторые названия используются и сейчас.
Названия некоторых оксидов: таблица
Химическая формула оксида
Бытовое (тривиальное название)
Возможное научное название
Химические свойства основных оксидов
1. Взаимодействие с водой
С водой способны реагировать оксиды тех металлов, которым соответствуют растворимые гидроксиды. То есть с водой реагируют только оксиды щелочных и щелочноземельных металлов.
Основный оксид + вода = основание
Оксид магния взаимодействует с водой только при нагревании.
2. Взаимодействие с кислотными оксидами и кислотами
Основные оксиды, соответствующие щелочам, взаимодействуют со всеми кислотными оксидами и кислотами. Оксиды неактивных металлов взаимодействуют только с кислотными оксидами, соответствующими сильным кислотам, или с сильными кислотами.
Основный оксид + кислотный оксид = соль
Основный оксид + кислота = соль + вода
3. Взаимодействие с амфотерными оксидами
В эту реакцию могут вступать только основные оксиды щелочных или щелочноземельных металлов. При сплавлении двух оксидов образуется соль.
Основный оксид + амфотерный оксид = соль
Как составлять такие соли: металл в этой соли берем из основного оксида, а кислотный остаток из амфотерного оксида (они проявляют более кислотные свойства).
Химические свойства кислотных оксидов
1. Взаимодействие с водой
Кислотные оксиды взаимодействуют с водой с образованием соответствующих кислот. За исключением SiO2, которому соответствует нерастворимая кремниевая кислота.
Кислотный оксид + вода = кислота
2. Взаимодействие с основными оксидами и щелочами
Кислотные оксиды сильных кислот способны взаимодействовать с любыми основными оксидами или основаниями.
Кислотный оксид + основный оксид = соль
Кислотный оксид + основание = соль + вода
Кислотные оксиды, соответствующие слабым кислотам (такие как CO2, SO2), способны взаимодействовать с основными оксидами, соответствующим щелочам, а также с щелочами.
3. Взаимодействие с амфотерными оксидами и гидроксидами
С амфотерными оксидами в реакцию вступают кислотные оксиды — как правило, сильных кислот.
Кислотный оксид + амфотерный оксид = соль
Кислотный оксид + амфотерный оксид = соль + вода
Химические свойства амфотерных оксидов
1. Взаимодействие с водой
Амфотерные оксиды не взаимодействуют с водой — даже при нагревании!
Амфотерный оксид + вода ≠
2. Взаимодействие с кислотными оксидами и кислотой
Амфотерные оксиды взаимодействуют только с сильными и средними кислотами и их оксидами.
Амфотерный оксид + кислотный оксид = соль
Амфотерный оксид + кислота = соль + вода
3. Взаимодействие с основными оксидами
Амфотерные оксиды взаимодействуют только с теми оксидами, которые соответствуют щелочам. Реакция протекает только в расплаве, так как в растворе такие оксиды взаимодействуют преимущественно с водой с образованием щелочей.
Амфотерный оксид + основный оксид (расплав) = соль
4. Взаимодействие со щелочами
Продукты взаимодействия амфотерных оксидов со щелочами зависят от условий проведения реакции. В растворе образуются комплексные соли, а при сплавлении – средние соли.
Амфотерный оксид + щелочь (раствор) + вода = комплексная соль
Амфотерный оксид + щелочь (расплав) = средняя соль + вода
Получение оксидов
1. Окисление металлов
Почти все металлы окисляются кислородом до устойчивых степеней окисления.
Металлы с переменной степенью окисления, как правило, образуют соединения в степени окисления +3:
При взаимодействии щелочных металлов (элемента IA группы) образуются пероксиды Me2O2 или надпероксиды MeO2, где Ме — щелочной металл.
2. Окисление простых веществ — неметаллов
При окислении неметаллов в избытке кислорода, как правило, образуются высшие оксиды (это оксиды, в которых неметалл проявляют высшую степень окисления):
При недостаточном количестве кислорода образуются оксиды неметаллов в промежуточной степени окисления:
Существуют и исключения. Например, сера окисляется лишь до оксида серы (IV) даже в избытке кислорода:
Или азот, который взаимодействует с кислородом только при температуре 2 000̊С или под действием электрического разряда с образованием оксида азота (II):
3. Разложение гидроксидов
Некоторые кислоты и гидроксиды неустойчивы и самопроизвольно разлагаются по схеме:
Гидроксид (кислота) = оксид + вода
Оксиды тяжелых металлов (нерастворимые гидроксиды) и кремниевая кислота разлагаются при нагревании по той же самой схеме.
4. Окисление сложных веществ
Сложные бинарные (состоящие из двух химических элементов) соединения окисляются с образованием двух оксидов этих элементов в устойчивых степенях окисления.
Также оксиды получают разложением солей, например, карбонатов, нитратов сульфатов и т. д.
Мы узнали, какие вещества в химии называют оксидами, какие бывают оксиды, а также разобрали свойства каждого вида. Осталось подкрепить теорию практикой — а сделать это можно на курсах по химии в онлайн-школе Skysmart!