Что значит серозометра в матке
Серозометра
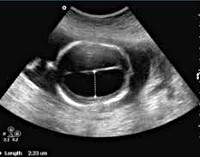
Серозометра — накопление серозной жидкости в полости матки из-за наличия механических препятствий на пути ее оттока во влагалище или повышенной секреции. На начальных этапах клинически не проявляется и выявляется случайно во время гинекологического обследования. При накоплении больших объемов жидкости пациентку беспокоит тупая боль в надлобковой области, учащенное мочеиспускание, запоры и другие нарушения функции тазовых органов. Для диагностики используют бимануальное обследование, УЗИ, эндоскопические, томографические, цитологические и микробиологические методы. Лечение направлено на устранение заболевания, вызвавшего серозометру.
Общие сведения
Накопление серозной жидкости в матке является неспецифическим проявлением ряда заболеваний, сопровождающихся повышенной секрецией или нарушением оттока экссудата во влагалище. Серозометра чаще возникает во время постменопаузы на фоне инволютивных процессов в женских половых органах и в ходе гинекологического УЗИ диагностируется у 40% пациенток этой группы. При этом наиболее часто подобное нарушение выявляют у женщин с длительностью постменопаузы от 15 до 25 лет. Появление внутриматочной жидкости у пациенток репродуктивного возраста, как правило, имеет другие причины, чем серозометра в постменопаузе, и требует быстрой тщательной дифференциальной диагностики.
Причины серозометры
Скопление серозной жидкости в полости матки может быть обусловлено механическим нарушением проходимости путей оттока во влагалище или повышенной секрецией на фоне неадекватной резорбции и выведения. Основными причинами органической несостоятельности служат:
К возникновению серозометры также приводит избыточная секреция экссудата эндометрием или его поступление из фаллопиевых труб. Гиперпродукция серозной жидкости наблюдается при таких патологических состояниях, как:
Важную роль в формировании серозометры играют факторы, которые снижают местный или общий иммунитет, вызывают гормональные сбои и преждевременное старение репродуктивной системы. Ключевыми из них являются:
Дополнительными факторами риска возникновения серозометры служат малоподвижный образ жизни, нерациональное питание с употреблением жирных и других продуктов, усугубляющих обменные нарушения.
Патогенез
Симптомы серозометры
На начальных этапах присутствие серозной жидкости в полости матки не проявляется клинически и в подавляющем большинстве случаев становится случайной находкой при плановом гинекологическом УЗИ. Если серозометра сочетается с увеличением матки, пациентку беспокоят тупые или ноющие боли в надлобковой области, иногда возникает учащенное мочеиспускание, ощущение давления на мочевой пузырь или прямую кишку, появляются запоры или, наоборот, более частые позывы к дефекации. Боли могут усиливаться во время полового акта или при значительных физических нагрузках.
При сохранении проходимости цервикального канала женщина обычно отмечает увеличение количества влагалищных выделений. Зачастую они имеют водянистую консистенцию, выглядят прозрачными или светло-серыми. Когда к серозометре присоединяются гнойно-воспалительные процессы, характер выделений изменяется: они становятся более густыми, желто-зелеными с неприятным запахом. При этом усиливаются боли, может повышаться температура, беспокоить общее недомогание, слабость, разбитость, усталость, головокружение.
Осложнения
Наиболее грозным осложнением серозометры является присоединение воспалительного процесса с нагноением, выраженными местными и общими проявлениями интоксикации, инфекционным поражением других органов женской половой сферы. Давление увеличенной матки приводит к нарушению функций органов малого таза, а также нарушению оттока крови из нижних конечностей с формированием отеков. Кроме того, поскольку серозометра — не заболевание, а состояние, спровоцированное другой патологией, при несвоевременной диагностике основных причин накопления жидкости в матке могут быть пропущены опухоли и воспалительные заболевания.
Диагностика
Основная задача диагностики при обнаружении серозометры — выявление причин, вызвавших накопление жидкости. С этой целью пациентке рекомендовано комплексное гинекологическое обследование, в которое входят:
В репродуктивном возрасте особенно важна дифференциальная диагностика серозометры от других состояний, при которых в полости матки выявляется жидкость, — лохиометры, гематометры, пиометры. В сомнительных случаях к постановке диагноза привлекают онкогинекологов и хирургов.
Лечение серозометры
Схема лечения зависит от объема серозной жидкости, выявленной в полости матки, динамики ее накопления и причин, приведших к возникновению патологического состояния. При небольшом объеме жидкости (до 5 мл) и отсутствии признаков инфекционных процессов рекомендовано динамическое наблюдение с проведением УЗ-контроля и назначение препаратов, которые стимулируют маточное кровообращение, улучшают тонус сосудов и регенерацию эпителия. В таких случаях эффективно дополнительное назначение физиотерапевтических процедур.
Если объем серозной жидкости превышает 5 мл, ее количество увеличивается в динамике, отсутствуют механические препятствия на пути оттока во влагалище, выявлены воспалительные изменения, рекомендована комплексная терапия серозометры. Как правило, пациентке назначают:
При наличии органической патологии, препятствующей оттоку серозной жидкости, показаны специальные методы лечения основной патологии — бужирование цервикального канала, удаление полипа, миомэктомия, терапевтическое и хирургическое лечение объемных новообразований и т. п.
Прогноз и профилактика
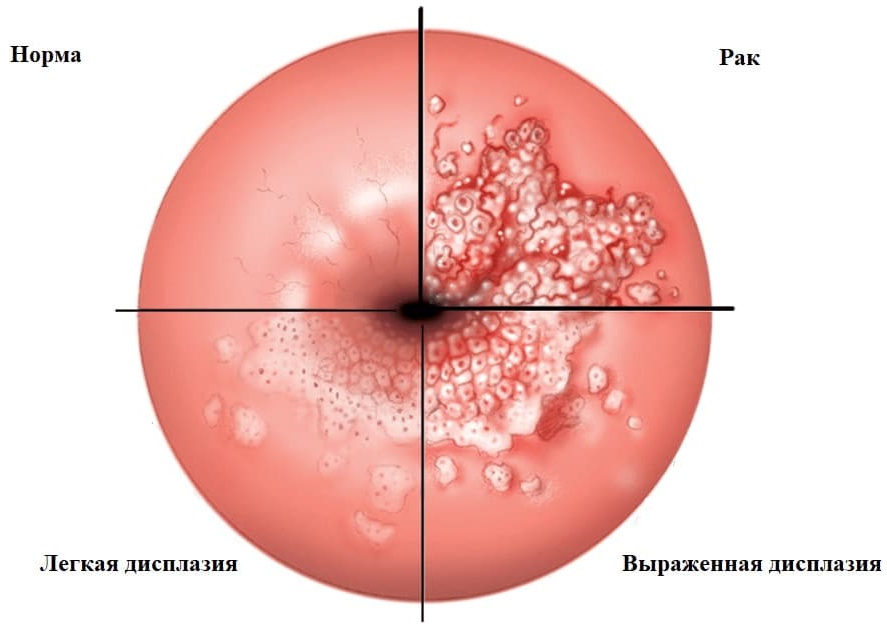
Симптомы доброкачественных и предраковых заболеваний шейки матки
Существует множество заболеваний шейки матки, часть из которых представляют угрозу с точки зрения малигнизации. Другие же не вызывают никакой онкологической настороженности. Важно знать основные типы патологий шейки матки и их симптомы, чтобы вовремя принять меры.
К основным доброкачественным и предраковым заболеваниям шейки матки относят:
Симптомы доброкачественных болезней шейки матки
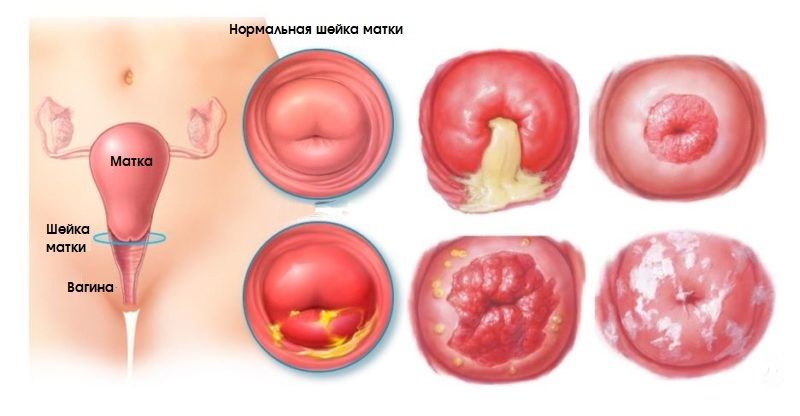
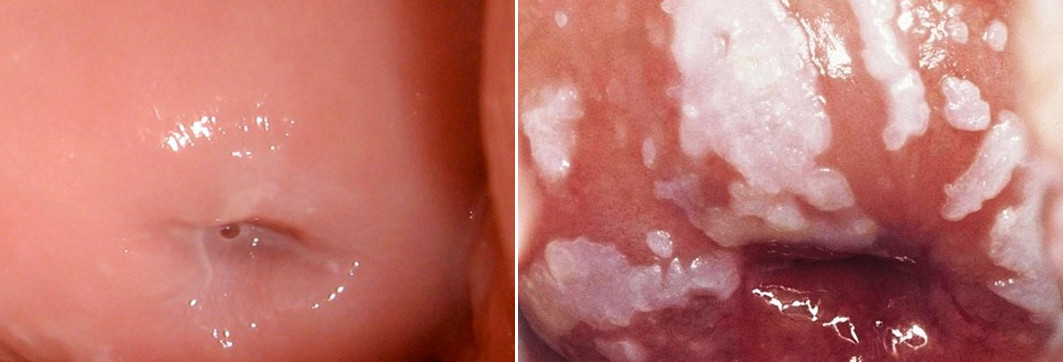
К доброкачественным состояниям, как мы писали выше, относят эктопию, эктропион, лейкоплакию, эрозию. Для них характерны следующие симптомы:
Доброкачественные заболевания шейки матки никогда не вызывают тяжелых симптомов. Женщина себя чувствует хорошо и не предъявляет никаких особенных жалоб. Как правило, ее могут беспокоить только обильные выделения и кровомазание после полового акта, но и это встречается не часто.
Признаки предраковых патологий шейки матки
Дисплазия шейки матки, аденоматоз, эритроплакия обычно проявляются стерто. Это еще одна причина, по которой необходимы регулярные посещения врача, ведь сама женщина не может увидеть, что у нее внутри и вовремя определить опасную болезнь. Распространенные симптомы предраковых заболеваний шейки матки такие:
Лечение доброкачественных и предраковых заболеваний шейки матки не представляет никакого труда, но их важно вовремя выявить, чтобы нивелировать угрозу. Если у вас появились непривычные симптомы, связанные с гинекологией, обратитесь в клинику Dr.AkNer, здесь вам обязательно окажут нужную помощь.
Задать вопрос или записаться на прием
Лицензии
Существует множество заболеваний шейки матки, часть из которых представляют угрозу с точки зрения малигнизации. Другие же не вызывают никакой онкологической настороженности. Важно знать основные типы патологий шейки матки и их симптомы, чтобы вовремя принять меры.
К основным доброкачественным и предраковым заболеваниям шейки матки относят:
Симптомы доброкачественных болезней шейки матки
К доброкачественным состояниям, как мы писали выше, относят эктопию, эктропион, лейкоплакию, эрозию. Для них характерны следующие симптомы:
Доброкачественные заболевания шейки матки никогда не вызывают тяжелых симптомов. Женщина себя чувствует хорошо и не предъявляет никаких особенных жалоб. Как правило, ее могут беспокоить только обильные выделения и кровомазание после полового акта, но и это встречается не часто.
Признаки предраковых патологий шейки матки
Дисплазия шейки матки, аденоматоз, эритроплакия обычно проявляются стерто. Это еще одна причина, по которой необходимы регулярные посещения врача, ведь сама женщина не может увидеть, что у нее внутри и вовремя определить опасную болезнь. Распространенные симптомы предраковых заболеваний шейки матки такие:
Патологии эндометрия, полости матки и цервикального канала
1. Паталогии эндометрия
Полость матки выстлана эндометрием – пронизанной кровеносными сосудами слизистой оболочкой (мукозный слой), ткань которой постоянно меняется и обновляется в зависимости от фазы менструального цикла.
Природное предназначение эндометрия – обеспечить надежное прикрепление и кровоснабжение (питание) оплодотворенной яйцеклетки. В эндометрии, как и в любом другом структурно сложном образовании живого организма, обнаруживаются многочисленные заболевания, функциональные расстройства и аномалии развития. К наиболее распространенным относятся следующие.
2. Гиперплазия и полипы
Гиперплазия
Увеличение, разрастание эндометрия, зачастую неравномерное, очаговое, полипообразное, железисто-кистовое и т.д. Согласно статистическим данным, гиперплазия эндометрия наблюдается примерно у 40% всех гинекологических пациенток, причем частота встречаемости не зависит от возраста. Основными этиопатогенетическими факторами считаются эндокринные нарушения, инфекционные заболевания, генетические сбои; однако, пусковые механизмы остаются неясными. Как правило, больные жалуются на патологически обильные менструации, выделения или маточные кровотечения, не связанные с циклом. Основными диагностическими методами являются УЗИ (трансвагинальный вариант наиболее информативен), гистероскопия (при необходимости отбирается материал для гистологического исследования). Терапия гиперплазии эндометрия включает гормональные препараты и/или малоинвазивное вмешательство: хирургическую гистероскопию, аблацию, гистерорезектоскопию.
Полипы
Очаговая доброкачественная пролиферация (разрастание) клеток эндометрия матки и/или цервикального канала (участка между маткой и влагалищем). Обнаруживаются более чем у половины пациенток после менопаузы; проявляются, в основном, кровянистыми выделениями. К главным причинам образования полипов относят неоднократные и неполные выскабливания. Различают несколько видов полипов (аденоматозные, железистые и пр.). Диагностика и лечение (удаление) полипов осуществляется, как правило, гистероскопическим методом.
3. Перегородка полости матки
4. Синехии и серозометра
Синехии
Внутриматочные синехии (спайки, сращения – синдром Ашермана) могут быть обусловлены рядом причин: травмы (в т.ч. хирургические), инфекции, нарушения нейровисцеральной регуляции. По охвату внутриматочного пространства выделяют три степени синехий. Основным клиническим симптомом является неспособность забеременеть либо выносить беременность. Диагностируется аппаратными методами. Единственным лечением является хирургическая коррекция (в настоящее время подавляющее большинство вмешательств производится малоинвазивными методами).
Серозометра
Скопление серозной жидкости (т.е. секрета слизистой оболочки) в полости матки. Серозометра не является самостоятельным диагнозом – это всегда симптом иного заболевания или состояния (в частности, послеродовое скопление носит название лохиометра, наличие жидкой крови – гематометра). Часто встречается в раннем климактерическом периоде на фоне гормональной перестройки. Провоцирующими факторами считают также вредные привычки и гиподинамический образ жизни. Проявляется ноющей болью, при большом объеме жидкости – видимым увеличением живота, водянистыми выделениями, при инфицировании – симптоматикой острого воспаления. Терапией выбора обычно является расширение цервикального канала с отводом жидкости; обязательно проводится гистологическое исследование, при необходимости – бактериальный посев и лечение инфекции.
Заболевания 
Жалобы и симптомы 
Диагностика 
Наши цены 
Мы стараемся оперативно обновлять данные по ценам, но, во избежание недоразумений, просьба уточнять цены в клинике.
Данный прайс-лист не является офертой. Медицинские услуги предоставляются на основании договора.
Диагностика патологии эндометрия в постменопаузе: применение 2D и 3D технологий
УЗИ сканер RS80
Эталон новых стандартов! Беспрецедентная четкость, разрешение, сверхбыстрая обработка данных, а также исчерпывающий набор современных ультразвуковых технологий для решения самых сложных задач диагностики.
Введение
Трехмерное УЗИ в последние годы чаще используется в работе как врачей ультразвуковой диагностики, так и врачей акушеров-гинекологов, несмотря на то, что остается ряд дискуссионных вопросов, роль которых в диагностике гинекологической патологии еще предстоит определить 1.
В большей мере освещены вопросы патологии эндометрия в постменопаузальном возрасте. Так, S. Kupesic и соавт. определили, что трехмерная энергетическая допплерография может использоваться для раннего выявления рака эндометрия, особенно у женщин в постменопаузальном возрасте без клинической симптоматики заболевания, а также для уточнения инвазии опухоли в миометрий [4].
При обследовании пациенток постменопаузального возраста с аденокарциномой, гиперплазией, атрофией эндометрия и субмукозной миомой матки, J.L. Alcazar и R. Galv n установили, что 3D энергетическая допплерография может быть полезна в диагностике рака эндометрия, так как у этих пациенток статистически значимо повышены индекс васкуляризации (ИВ) и васкуляризационно-потоковый индекс (ВПИ) эндометрия в сравнении с пациентками других групп [5].
В свою очередь R. Galv n и соавт. при изучении стадийности эндометриального рака у пациенток в постменопаузе определили, что ИВ в малигнизированном эндометрии коррелирует с некоторыми гистологическими характеристиками опухоли [6].
G. Opolskiene и соавт. определили, что у женщин с кровотечением в постменопаузальном возрасте ИВ и ВПИ не отличались как при доброкачественных, так и при злокачественных изменениях в эндометрии [7]. К противоположным выводам пришли A.K. Makled и соавт., которые в своих исследованиях доказали, что значение ИВ является достоверным диагностическим критерием рака эндометрия в постменопаузе [8].
Как видно из изложенного выше, в последние годы увеличивается интерес к проблемам постменопаузы, что связано в первую очередь с тенденцией населения развитых стран к старению. Поэтому так актуальны вопросы патологии эндометрия в постменопаузальном периоде [9].
Кроме того, заболеваемость раком эндометрия увеличилась во всех экономически развитых странах [10, 11].
В постменопаузальном возрасте у ряда пациенток происходит полная облитерация цервикального канала, и показанием для проведения раздельного диагностического выскабливания становится расширение полости матки за счет жидкости, выявленное при УЗИ в 2D режиме. Между тем у врачей ультразвуковой диагностики нет четких критериев, позволяющих исключить злокачественную трансформацию эндометрия у таких пациенток. Следовательно, поиск путей улучшения диагностики патологических состояний эндометрия у пациенток в постменопаузальном возрасте с использованием трехмерной эхографии с опцией энергетического допплера побудил нас к исследованиям в этой области.
Целью настоящего исследования стало проведение анализа совпадений результатов рутинного двухмерного трансвагинального УЗИ у пациенток постменопаузального возраста с окончательным патоморфологическим заключением исследования биоптата эндометрия, определение возможности использования трехмерной энергетической допплерографии у пациенток с облитерацией цервикального канала в постменопаузе.
Материал и методы
Для достижения поставленной цели нами ретроспективно оценено 50 историй болезни женщин постменопаузального возраста, госпитализированных в гинекологическое отделение для проведения раздельного диагностического выскабливания и гистероскопии в плановом порядке. Показанием для госпитализации явились данные рутинного трансвагинального УЗИ (ультразвуковое заключение: патология эндометрия). Данные ультразвуковых заключений, послужившие поводом для госпитализации в стационар, были оценены ретроспективно и сопоставлены с данными гистологических заключений после раздельного диагностического выскабливания.
Пациентке с атрезией цервикального канала и скоплением жидкости в полости матки проведено трансвагинальное сканирование с использованием объемного ректовагинального датчика 4-9 МГц на стационарном ультразвуковом сканере Accuvix-V10 компании Samsung Medison в режиме 3D реконструкции с опцией энергетического допплера по методике И.А. Озерской [12], с последующим автоматическим получением ИВ, индекса потока (кровотока) (ИП), ВПИ реконструированной матки в программе Virtual Organ Computeraided AnaLysis (VOCAL).
Статистическая обработка данных осуществлялась с применением прикладного программного пакета «Statistica 6.0», адаптированного для медико-биологических исследований. Производилось вычисление относительных частот признака (%) в группе.
Результаты и обсуждение
Анализ приведенных результатов побуждает к поиску дополнительных ультразвуковых методик, которые можно применить в постменопаузальном возрасте, особенно в ситуации с атрезией цервикального канала и последующим скоплением жидкости в полости матки. Именно это состояние занимает высокий удельный вес в постменопаузальном возрасте и, не представляя трудностей в диагностике при рутинном трансвагинальном УЗИ, ведет к проведению раздельного диагностического выскабливания.
Мы попытались применить у такой категории пациенток 3D энергетическую допплерографию и приводим клинический пример.
Пациентка К., 60 лет, поступила в гинекологическое отделение для проведения раздельного диагностического выскабливания под контролем гистероскопии с диагнозом: подозрение на рак тела матки. Данные трансвагинального УЗИ, проведенного амбулаторно: тело матки нормальных размеров, контур матки ровный, миометрий однородный, полость матки расширена до 6 мм, заполнена анэхогенным содержимым. Яичники обычных размеров и эхоструктуры, свободная жидкость в позадиматочном пространстве не визуализируется. Ультразвуковое заключение: серозометра.
Анамнестические данные: постменопауз 5 лет, из гинекологических заболеваний в анамнезе пациентка отмечает эктопию шейки матки, по поводу чего была произведена диатермоэлектрокоагуляция шейки матки. В анамнезе 2 родов, в срок, без осложнений и один медицинский аборт в срок 8-9 нед, без осложнений.
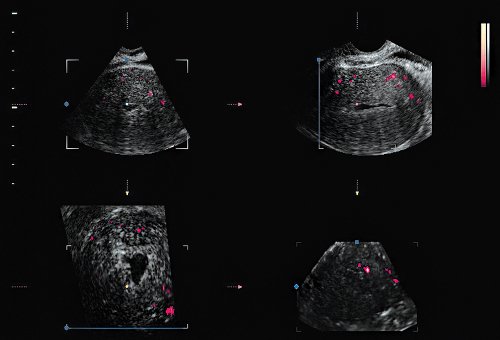
До проведения раздельного диагностического выскабливания, на стационарном ультразвуковом сканере Accuvix-V10 компании Samsung Medison после опорожнения мочевого пузыря мы провели трансвагинальное сканирование с использованием объемного ректовагинального датчика 4-9 МГц в режиме 3D реконструкции с опцией энергетического допплера и получили объемное изображение (рис. 1).
Рис. 1. Объемное изображение в режиме энергетического допплера.
Урогенитальные расстройства в постменопаузе и заместительная гормонотерапия
Изменение демографической структуры общества во второй половине XX в. привело к увеличению в популяции доли женщин старшей возрастной группы. С каждым годом возрастает число женщин, вступающих в период менопаузы. Если
Изменение демографической структуры общества во второй половине XX в. привело к увеличению в популяции доли женщин старшей возрастной группы. С каждым годом возрастает число женщин, вступающих в период менопаузы. Если 75 лет принять за 100%, то продолжительность препубертатного периода составляет 16%, репродуктивного — 44%, пременопаузального — 7%, а постменопаузального — 33% (H. Нaney, 1986). То есть более трети своей жизни женщина проводит в состоянии дефицита женских половых гормонов. Менопауза, не являясь собственно заболеванием, приводит к нарушению эндокринного равновесия в организме женщины, вызывая приливы, раздражительность, бессонницу, урогенитальные расстройства, а также повышая риск развития остеопороза и сердечно-сосудистых заболеваний. Все эти данные свидетельствуют о необходимости разработки целого ряда медицинских и социальных мер по защите здоровья, сохранению работоспособности и достойного качества жизни женщин пери- и постменопаузального периода.
В последние годы в симптоматологии климактерических нарушений стала лидировать проблема урогенитальных расстройств, что связано с их выраженным отрицательным влиянием на качество жизни женщины в постменопаузе. Частота развития возрастных урогенитальных расстройств достигает 30%. В перименопаузальном периоде урогенитальные нарушения встречаются у 10% женщин, тогда как в возрастной группе 55—60 лет — у 50%. К 75 годам уже 2/3 женщин испытывают урогенитальный дискомфорт, а после 75 лет трудно встретить женщину, у которой не наблюдалось отдельных симптомов урогенитальных расстройств.
Урогенитальные расстройства в климактерии — это симптомокомплекс вторичных изменений, связанных с развитием атрофических и дистрофических процессов в эстроген-зависимых тканях и структурах нижней трети мочеполового тракта, мочевом пузыре, уретре, влагалище, связочном аппарате малого таза и мышцах тазового дна.
Прогрессирующее увеличение с возрастом частоты развития урогенитальной атрофии связывают с развивающимися на фоне эстрогенного дефицита необратимыми возрастными метаболическими изменениями. Влагалище, уретра, мочевой пузырь и нижняя треть мочеточников имеют единое эмбриональное происхождение и развиваются из урогенитального синуса. Это объясняет наличие рецепторов к эстрогенам, прогестерону и андрогенам в мышцах, слизистой оболочке, сосудистых сплетениях влагалища, мочевого пузыря и уретры, а также в мышцах и связочном аппарате малого таза.
Процессы старения урогенитального тракта развиваются в двух направлениях:
Атрофический вагинит возникает в результате эстрогенного дефицита и характеризуется резким истончением слизистой оболочки влагалища, прекращением пролиферативных процессов во влагалищном эпителии, уменьшением продукции гликогена эпителиальными клетками, снижением или полным исчезновением лактобацилл, повышением влагалищного рН (см. таблицу 1).
Основные клинические проявлениями атрофического вагинита — это сухость и зуд во влагалище, рецидивирующие выделения, диспареуния, контактные кровянистые выделения.
Диагностика атрофического вагинита включает:
К проявлениям атрофического цистоуретрита относятся «сенсорные» или раздражающие симптомы:
Обследование женщин с расстройствами мочеиспускания:
Вычленение симптомов атрофического вагинита и цистоуретрита условно, так как в большинстве случаев они сочетаются. Различные сочетания симптомов атрофического вагинита и цистоуретрита позволили выделить три степени тяжести урогенитальных расстройств (В. Е. Балан, 1997).
К легким урогенитальным расстройствам (16% женщин) относится сочетание симптомов атрофического вагинита и «сенсорных симптомов» атрофического цистоуретрита без нарушения акта мочеиспускания.
К среднетяжелым урогенитальным расстройствам (80% женщин) относится сочетание симптомов атрофического вагинита, цистоуретрита и истинного недержания мочи при напряжении.
К тяжелым урогенитальным расстройствам (4% женщин) относится сочетание симптомов атрофического вагинита, цистоуретрита, истинного недержания мочи при напряжении и неудержание мочи.
Итак, установлено, что эстрогенный дефицит является причиной развития урогенитальных нарушений у женщин в климактерии. Проблема лечения урогенитальных расстройств неоднозначна. Акцент ставится на том, какой вид заместительной гормонотерапии (ЗГТ) считать оптимальным. ЗГТ урогенитальных нарушений может осуществляться препаратами, обладающими как системным, так и местным действием. К системной ЗГТ относятся все препараты, содержащие эстрадиол, эстрадиол валерат и конъюгированные эстрогены.
К местной ЗГТ — препараты, содержащие эстриол. Выбор типа ЗГТ для лечения урогенитальных расстройств является индивидуальным и зависит от возраста пациентки, длительности постменопаузы, ведущих жалоб, необходимости лечения климактерического синдрома либо профилактики поздних метаболических нарушений.
Назначение системной ЗГТ должно соответствовать общепринятым правилам с учетом абсолютных и относительных противопоказаний. При назначении ЗГТ пациенткам с урогенитальными нарушениями преследуется цель восстановления нормального состояния местных гормонозависимых структур нижних отделов мочеполовой системы и стимуляции механизмов биологической тканевой защиты.
При решении вопроса о выборе типа препарата для ЗГТ крайне важно определить:
При интактной матке применяется комбинированная терапия препаратами, содержащими эстрогены и гестагены:
У женщин после гистерэктомии системное воздействие обеспечивает монотерапия натуральными эстрогенами в циклическом или непрерывном режиме (эстрофем, прогинова, климара, дивигель, эстрадерм).
Приоритетная роль в выборе ЗГТ расстройств урогенитального тракта, обусловленных снижением функции гонад, принадлежит эстриол-содержащим препаратам, обладающим избирательной активностью в отношении мочеполовой системы. Специфичность действия эстриола определяется особенностями его метаболизма и сродством с соответствующими рецепторными системами. Местный эффект стероидных гормонов реализуется путем пассивной диффузии их в клетки организма. Задерживаясь лишь в клетках чувствительных тканей, они образуют комплексы с цитозольными рецепторами с последующей транслокацией в ядро клетки. Таким путем реализуется действие на уровне генетических структур клетки. Это и определяет специфичность эффекта, свойственного данной ткани.
Ответ тканей на воздействие эстрогенов определяется концентрацией рецепторов, их структурой и свойствами эстрогенов. Эстриол является конечным метаболитом в обмене эстрогенов. Он выводится из организма в конъюгированной форме с мочой и лишь в незначительном количестве экскретируется с калом, в основном в неконъюгированной форме.
При пероральном введении эстриола его максимальная концентрация в плазме крови достигается через 1-2 ч. Попавший в плазму крови эстриол не связывается с глобулином, связывающим половые стероиды, и довольно быстро элиминируется. Эстриол является наименее активным эстрогеном с кратковременным действием.
Установлено, что ткани, чувствительные к эстриолу, широко представлены в нижних отделах урогенитального тракта. Терапия эстриолом способствует развитию и восстановлению влагалищного эпителия, а также приводит к восстановлению основных элементов соединительной ткани — коллагена и эластина. При этом главным в назначении эстриол-содержащих препаратов является минимальное системное действие. Известно, что для стимуляции развития эндометрия связь его рецепторов с эстрогеном должна быть длительной, не менее 8—10 ч. Эстриол же связывается с чувствительными к нему структурами не более чем на 2—4 ч. Такого непродолжительного действия недостаточно для пролиферативной реакции эндометрия, но достаточно для эффективного воздействия на структуры нижних отделов урогенитального тракта. Таким образом, при однократном введении эстриол связывается с ядерным рецептором на непродолжительное время и не вызывает пролиферацию эндометрия, поэтому при его назначении не требуется добавления прогестагенов.
При урогенитальных расстройствах традиционно отдается предпочтение местному введению эстрогенов и именно эстриола (овестин) в мазях и свечах (см. таблицу 2).
В любой форме эстриол-содержащие препараты принимаются один раз в сутки. Не рекомендуется сочетание системных и местных форм препарата.
Выбор терапии зависит также от степени тяжести урогенитальных расстройств.
При легкой степени тяжести урогенитальных расстройств применяются препараты эстриола (свечи, крем) ежедневно или три раза в неделю, в зависимости от степени выраженности клинических симптомов. При сочетании явлений атрофического вагинита или атрофического цистоуретрита с климактерическим синдромом назначаются препараты для системной ЗГТ.
При средней степени тяжести урогенитальных расстройств проводится сочетанная терапия (системная и местная) не менее шести месяцев для нормализации уродинамических показателей.
При тяжелой степени урогенитальных расстройств в случае имеющихся показаний к системной ЗГТ проводится комбинированная терапия препаратами для системной ЗГТ в сочетании с местным введением препаратов эстриола и одного из препаратов аддитивного воздействия, обладающих избирательным действием на холинергические (парасимпатические) и адренергические (симпатические) или мускариновые рецепторы, расположенные в мышечной стенке мочевого пузыря и различных структурах урогенитального тракта: гладкомышечной мускулатуре уретры и мышцах тазового дна, участвующих в создании уретральной поддержки. Комбинированную терапию необходимо проводить в течение шести месяцев и более, после чего вопрос о типе терапии решается индивидуально в отношении каждой пациентки (см. таблицу 3).
 |
| Таблица 3. Схема лечения урогенитальных расстройств. |
Такая система дифференцированной ЗГТ позволяет повысить качество жизни больных с урогенитальными расстройствами на 60—70%.
Таким образом, представленные данные позволяют говорить о ЗГТ как об основной терапии урогенитальных нарушений в постменопаузе.
В связи с прогрессирующим характером урогенитальных расстройств преимущество отдается профилактическому назначению ЗГТ и ее долговременному применению. ЗГТ урогенитальных расстройств должна назначаться длительно, практически пожизненно, и в этой ситуации на помощь приходит именно местная терапия эстриолом.
На сегодняшний день современная медицина располагает достаточно широким выбором хороших препаратов для ЗГТ и опытом их применения, свидетельствующим о том, что преимущества назначения ЗГТ заметно преобладают над риском развития побочных эффектов. Все это дает основание рекомендовать широкое применение ЗГТ для профилактики и лечения урогенитальных нарушений в пери- и постменопаузе с целью улучшения качества жизни и сохранения работоспособности женщин, вступающих в этот «осенний» период.
А. Л. Тихомиров, доктор медицинских наук, профессор
Ч. Г. Олейник, кандидат медицинских наук
МГМСУ, Москва