Что означает число в таблице менделеева
Крупная, многогранная и неоднозначная группировка химических элементов порождает немало вопросов на тему того, как пользоваться таблицей Менделеева. Между тем, это самый полный и завершенный вариант сортировки атомов всех веществ этой планеты.
Область применения данной классификации – не только химия или иные точные и естественные науки. Полезна она будет и простому обывателю для тренировки памяти или приспособлению к большим и сложным формулировкам и документам. С должным усердием и прилежанием в изучении таблицы, она станет легко понимаемым справочным материалом.
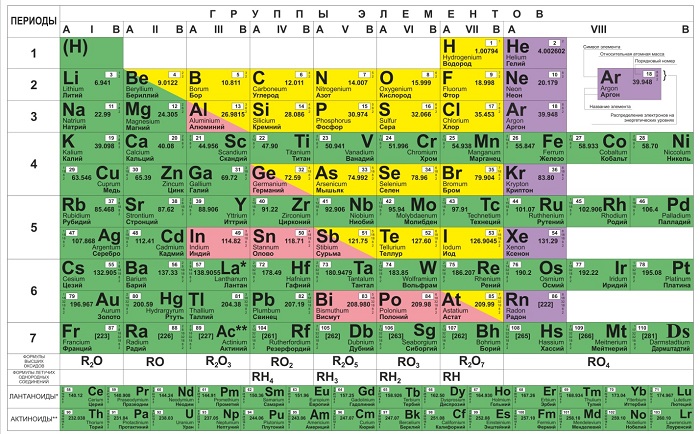
Периодическая таблица Менделеева
До Дмитрия Ивановича собрать элементы в один список пытались многие умы Европы. С начала XIX века они предприняли множество попыток сопоставления веществ.
В 1869 г. свой первый план представляет и Менделеев, через 2 года – завершает доработку и издает последний вариант таблицы.
Основная идея группировки – периодичность. Расположив элементы в порядке увеличения атомной массы, он заметил, что время от времени их свойства повторяются.
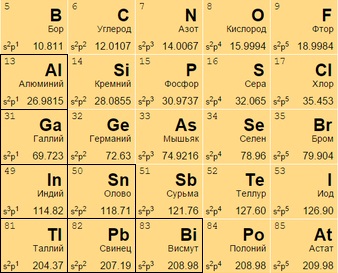
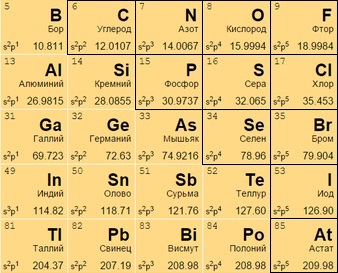
Ко 2-й половине XIX века миру было известно намного меньше веществ, чем сегодня, так что химик оставил пустые места в своей таблице, предполагая открытие новых элементов, и даже сумел заранее определить свойства открытых впоследствии галлия Ga 31 и германия Ge 32.
С каждым последующим номером элемента возрастает его атомная масса, заряд ядра, уровень электронов (количество элементов и их связей), показатели активности повторяются в зависимости от периода.
Формулировка периодического закона химических элементов
Русский ученый составлял наброски таблицы около 20 лет, пытаясь подобрать верную закономерность в их размещении. Отметив концепцию цикличности, он превратил её в периодический закон, изложив свое понимание правила:
«Свойства элементов, как и формируемых ими простых и сложных веществ, предполагают периодическую зависимость от их атомного веса».
Как читать таблицу Дмитрия Ивановича Менделеева
Ячейки химической базы данных разбиты в группы последовательностей по горизонтали и вертикали. Элементы имеют краткое обозначение из 1-3 букв (для формул и вычислений).
Группы
Представлены в виде столбцов таблицы. В системе старого образца их 8.
В настоящий же момент выделено 18.
Распределяют элементы в группы по однотипности: по строению атома они подобны друг другу. Также у представителей одного столбца схожая формула высшего оксида.
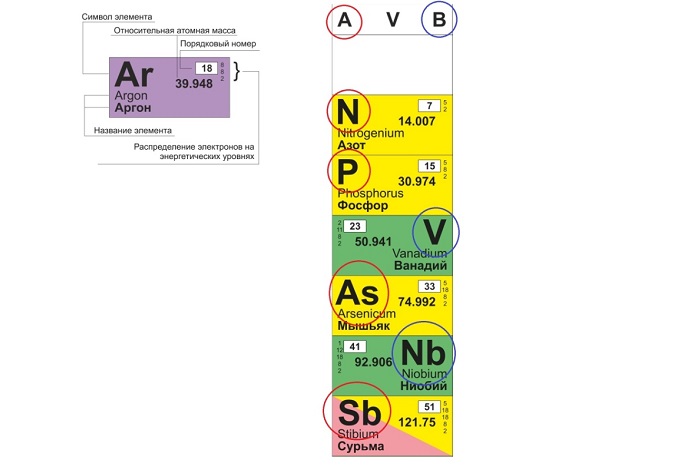
Традиционные типы столбцов делятся на подкатегории: А (с яркими признаками группы) и В (переходные металлы). Принадлежность зависит от положения символа (слева для A или справа для B):
Периоды
Горизонтальные цепочки в таблице, в которых элементы расположены по росту порядкового номера. В линии слева направо увеличиваются заряды ядра атомов.
1-й период содержит лишь гелий He 2 и водород H 1 ;
2 и 3 содержат по 8 компонентов;
4-й и 5-й содержат 18 единиц каждый;
6-й период вмещает 32 элемента;
7-й хранит 31 единицу и продолжает дополняться.
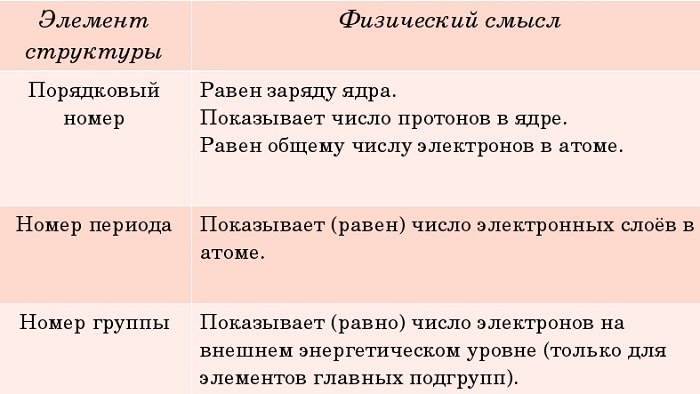
Физический смысл порядкового номера
Порядковый номер химического элемента также показывает, сколько в составе ядра атома протонов и сколько электронов вращается вокруг него.
Свойства таблицы Менделеева
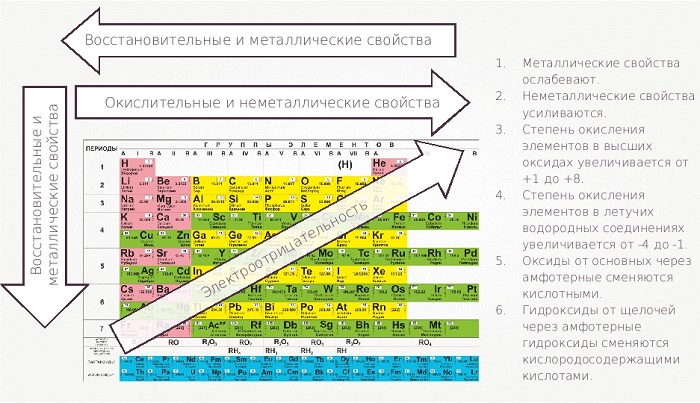
Химические элементы оцениваются по множеству параметров. Один из основных – окислительно-восстановительные свойства.
С убыванием в периоде и возрастанием в группе (стремление к левому нижнему углу) проявляются металлические характеристики, обратное направление в правый верхний угол увеличивает окислительные неметаллические качества.
Элементы таблицы Менделеева
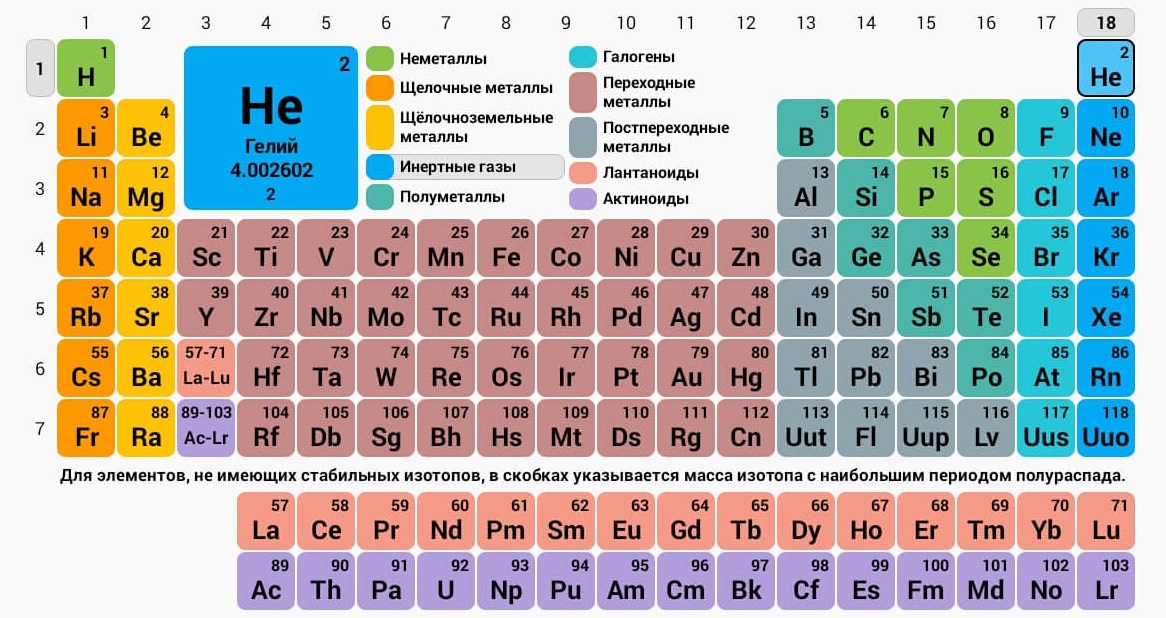
Также есть класс «металлоподобных» полупроводников с неопределенным статусом. Отдельно располагаются благородные газы, не подверженные реакциям.
Часть элементов с номером более 100 открыта сравнительно недавно, их принадлежность к каким-либо группам только предположительна.
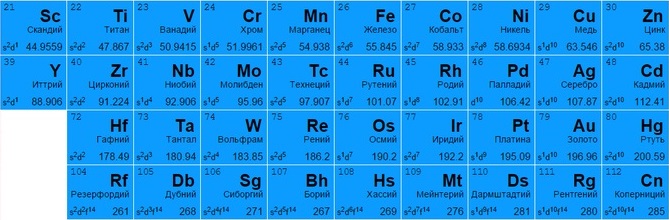
Щелочные и щелочноземельные элементы
Щелочные металлы имеют серебристый отблеск, хорошо разламываются и режутся. Из всех размещенных в таблице металлов активнее других вступают в реакцию с молекулами других веществ, отдавая единственный свободный электрон. При контакте с водой создают гидроксиды – щелочи:
Щелочноземельные металлы более твердые и тугоплавкие, с бледно-серым оттенком. В их список входят:
Большая часть из них способна создавать щелочь, но не так легко расстается с двумя незанятыми электронами. Другие металлы они замещают, но перед щелочными бессильны и вытесняются ими из молекул.
Лантаноиды и актиноиды
Прежде получили название редкоземельных металлов из-за малого количества месторождений и трудностей в выводе чистого металла из соединений. Им соответствует 3 (III B) группа, хотя это иногда оспаривается.
В рамках семейства лантаноиды («скрытые») имеют схожую форму атома и внешние признаки, но различаются свойствами. Поодиночке почти не встречаются.
Актиноиды, помимо общих черт, радиоактивны. В природе, кроме, урана U 92, почти не встречаются, создаются искусственно.
Для удобства обе группы элементов выведены в 2 строки под общей таблицей.
Галогены и благородные газы
17 (VII A) группа состоит из галогенов:
В противоположность щелочам, эти неметаллы – самые сильные окислители, активно принимающие 8-й электрон к имеющимся семи для заполнения внешней оболочки.
Самый реактивный – фтор F 9 (способен разрушать молекулы воды):
С ростом периода свойства элементов слабеют.
Все галогены токсичны, опасны для жизни, поражают дыхательные пути.
В последней, VIII A или 18 группе, находятся инертные газы:
Их внешний уровень электронов равен 8 (полностью заполнен), отчего они не способны вступать в реакцию с другими атомами. Крайне редко создают непрочные молекулы, распадающиеся при нагревании.
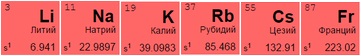
Переходные металлы
Представлены всеми подгруппами в традиционной системе или занимают с 3 по 12 столбцы в современных таблицах. Большинство обладает металлическим блеском, по цвету и состоянию различаются (большинство – твердые, но есть исключения, например, жидкая ртуть).
Могут отдавать разное количество электронов с нескольких оболочек для создания вещества (например, титан Ti 22 и железо Fe 26 способны отдавать от 2 до 4, медь Cu 29 – от 1 до 2, цинк Zn 30 – только 2, золото Au 79 и серебро Ag 47 практически не вступают в реакцию).
Металлоиды
Располагаются на стыке посреди легких металлов и неметаллов, в диагонали с 13 по 17 группах. В своем большинстве – полупроводники (хуже металлов проводят электрический ток).
Часть из них – металлы внешне, неметаллы по активности, часть – наоборот. Бор B 5, к примеру, является неметаллом с полупроводниковыми качествами.
Постпереходные металлы
Они же «легкие». От переходных аналогов отличаются меньшей твердостью и весом. Имеют иные температуры плавления и кипения. Для соединений отдают электроны только с внешней оболочки. Превосходят полуметаллы по восстановительности. Легкий металл выглядит как вещество с матовым оттенком вместо блеска.
Размещаются после переходных металлов под полупроводниками (в 13-17 столбцах или IIIA – VIIA). Алюминий Al 13 носит неопределенный статус (иногда причисляется к металлоидам).
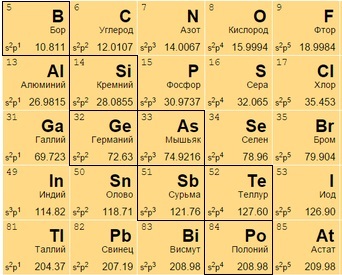
Неметаллы
Располагаются в правом верхнем углу между полуметаллами и инертными газами (начала 13-17 групп). Имеют больше электронов на внешней оболочке, стремятся присоединить к себе еще больше (в противоположность металлам), чтобы набрать полный уровень электронов.
в виде газа (кислород O 8, азот N 7);
жидкости (бром Br 35);
в твердом (углерод C 6, кремний Si 14) состоянии.
Интересное положение занимает водород H 1. Его причисляют то к 1, то к 17 группе: он, будучи неметаллом, может проявлять и окислительные, и восстановительные свойства.
Заключение
При детальном рассмотрении таблица Менделеева уже не кажется столь огромной. Главные моменты в пользовании – отследить группу и период элемента, после чего будет несложно определить его свойства и показатели.
Различные картинки в 8 или 18 столбцов не будут поводом для замешательства: семейства и категории выделяются разными цветами (полуметаллы – двухцветные). Ученики найдут решение задач, а любители головоломок получат новый способ тренировки мышления. Ячейка с нужными обозначениями найдется без особых препятствий.
Периодический закон Д. И. Менделеева и периодическая система химических элементов
Периодический Закон Д.И. Менделеева
Периодический закон Д.И. Менделеева и периодическая система химических элементов имеет большое значение в развитии химии. Окунемся в 1871 год, когда профессор химии Д.И. Менделеев, методом многочисленных проб и ошибок, пришел к выводу, что
«… свойства элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса».
Периодичность изменения свойств элементов возникает вследствие периодического повторения электронной конфигурации внешнего электронного слоя с увеличением заряда ядра.
Современная формулировка периодического закона
звучит следующим образом
«свойства химических элементов (т.е. свойства и форма образуемых ими соединений) находятся в периодической зависимости от заряда ядра атомов химических элементов».
Преподавая химию, Менделеев понимал, что запоминание индивидуальных свойств каждого элемента, вызывает у студентов трудности. Он стал искать пути создания системного метода, чтобы облегчить запоминание свойств элементов. В результате появилась естественная таблица, позже она стала называться периодической.
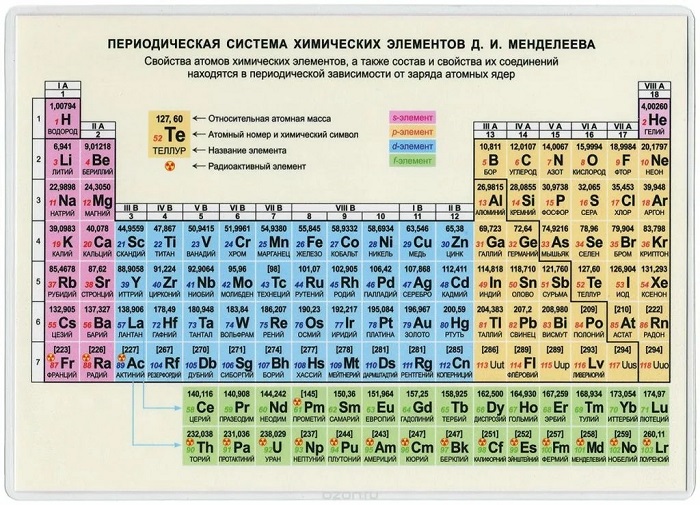
Наша современная таблица очень похожа на менделеевскую. Рассмотрим ее подробнее.
Таблица Менделеева
Периодическая таблица Менделеева состоит из 8 групп и 7 периодов. Рассмотрим подробнее что такое период и что такое группа в периодической таблице Менделеева.
Группы в таблице Менделеева
Вертикальные столбцы таблицы называют группами.
Элементы, внутри каждой группы, обладают сходными химическими и физическими свойствами. Это объясняется тем, что элементы одной группы имеют сходные электронные конфигурации внешнего слоя, число электронов на котором равно номеру группы. При этом группа разделяется на главные и побочные подгруппы.
В Главные подгруппы входят элементы, у которых валентные электроны располагаются на внешних ns- и np- подуровнях.
В Побочные подгруппы входят элементы, у которых валентные электроны располагаются на внешнем ns- подуровне и внутреннем (n — 1) d- подуровне (или (n — 2) f- подуровне).
Все элементы в периодической таблице, в зависимости от того, на каком подуровне (s-, p-, d- или f-) находятся валентные электроны классифицируются на:
Высшая и низшая степени окисления элементов
Высшая валентность элемента и высшая степень окисления (за исключением O, F, элементов подгруппы меди и восьмой группы) равна номеру группы, в которой он находится.
Низшая степень окисления элемента равна
Номер группы — 8
Для элементов главных и побочных подгрупп одинаковыми являются формулы высших оксидов (и их гидратов).
В главных подгруппах состав водородных соединений являются одинаковыми, для элементов, находящихся в этой группе.
Твердые гидриды образуют элементы главных подгрупп I — III групп, а IV — VII групп образуют а газообразные водородные соединения. Водородные соединения типа ЭН4 – нейтральнее соединения, ЭН3 – основания, Н2Э и НЭ — кислоты.
Периоды в таблице Менделеева
Горизонтальные ряды таблицы называют периодами. Элементы в периодах отличаются между собой. Общим является то, что последние электроны находятся на одном энергетическом уровне (главное квантовое число n — одинаково).
Как определить металл или неметалл?
Если посмотреть на периодическую таблицу Менделеева и провести воображаемую черту, начинающуюся у бора и заканчивающуюся между полонием и астатом, то все металлы будут находиться слева от черты, а неметаллы главных подгрупп – справа.
Элементы, непосредственно прилегающие к этой линии будут обладать свойствами как металлов, так и неметаллов. Их называют металлоидами или полуметаллами. Это бор, кремний, германий, мышьяк, сурьма, теллур и полоний.
Как изменяются свойства элементов в Периодической таблице?
Правило октета
Правило октета утверждает, что все элементы стремятся приобрести или потерять электрон, чтобы иметь восьмиэлектронную конфигурацию ближайшего благородного газа. Т.к. внешние s- и p-орбитали благородных газов полностью заполнены, то они являются самыми стабильными элементами.
Согласно правилу октета, при движении по периодической таблице слева направо для отрыва электрона требуется больше энергии. Поэтому элементы с левой стороны таблицы стремятся потерять электрон, а с правой стороны – его приобрести.
Изменение энергии ионизации
Энергия ионизации – это количество энергии, необходимое для отрыва электрона от атома.
Изменение сродства к электрону
Сродство к электрону – изменение энергии при приобретении дополнительного электрона атомом вещества в газообразном состоянии.
Изменение электроотрицательности
Электроотрицательность — мера того, насколько сильно атом стремится притягивать к себе электроны связанного с ним другого атома.
Электроотрицательность увеличивается при движении в периодической таблице слева направо и снизу вверх. При этом надо помнить, что благородные газы не имеют электроотрицательности. Таким образом, самый электроотрицательный элемент – фтор.
Итак, в периодической зависимости находятся такие свойства атома, которые связанны с его электронной конфигурацией: атомный радиус, энергия ионизации, электроотрицательность.
Изменение металлических и неметаллических свойств атомов
Неметалличность атома увеличивается при движении в периодической таблице слева направо и снизу вверх.
Изменение основных и кислотных свойств оксидов и гидроксидов
О сновные свойства оксидов уменьшаются, а кислотные свойства увеличиваются при движении слева направо и снизу вверх. При этом кислотные свойства оксидов тем сильнее, чем больше степень окисления образующего его элемента
По периоду слева направо основные свойства гидроксидов ослабевают.
По главным подгруппам сверху вниз сила оснований увеличивается. При этом, если металл может образовать несколько гидроксидов, то с увеличением степени окисления металла, основные свойства гидроксидов ослабевают.
По периоду слева направо увеличивается сила кислородосодержащих кислот. При движении сверху вниз в пределах одной группы сила кислородосодержащих кислот уменьшается. При этом сила кислоты увеличивается с увеличением степени окисления образующего кислоту элемента.
По периоду слева направо увеличивается сила бескислородных кислот. При движении сверху вниз в пределах одной группы сила бескислородных кислот увеличивается.
На рисунке ниже схематично показано изменение свойств атомов химических элементов в периодах и группах периодической таблицы Менделеева
Задания и примеры по строению таблицы Менделеева, положению атомов химического элемента в ней и закономерностям изменения свойств атомов элементов в периодах и группах периодической таблицы Менделеева представлены с разделе Задачи к разделу Периодический закон Д.И. Менделеева и периодическая система химических элементов
Таблица Менделеева — периодическая система элементов
Сложно ли было Менделееву создать собственную таблицу? Почему именно она прошла испытание временем и располагается на данный момент у людей? Сложно ли читать по ней что-либо об элементе?
Каждому школьнику, перешедшему порог восьмого класса понятие «Периодическая система химических элементов» («Таблица Менделеева») становится понятным даже при упоминании первого слова. Созданная величайшим Дмитрием Ивановичем Менделеевым, она очень хорошо помогает людям, работающим в химической сфере. Даже нет, не так. Это основное, чем они пользуются при проведении собственных опытов.
Периодическая система элементов
Каждому, наверное, известно, как она появилась. Однажды Дмитрий Иванович засыпал в собственной кровати, думая над тем, как же можно классифицировать все известные на тот момент химические элементы. По отдельным группам? Нет, тогда их будет слишком много. Может, по каким-то свойствам? А что тогда делать с теми, у кого их несколько и они входят сразу в несколько сфер? Может, тогда по каким-то признакам, которые они проявляют при соединении с чем-нибудь? Нет, тоже не то. Может же встретиться что-то такое, что обязательно не будет ни с чем контактировать. И что тогда? Выкидывать?

Но долго мучиться мужчине не пришлось. Во сне к нему пришла полная периодическая таблица химических элементов, которая на данный момент украшает стены очень многих кабинетов химии в школах. Конечно, всё было не так уж и просто, да и сам Менделеев высказался по этому поводу таким образом, что никакое глобальное изобретение не приходит по щелчку пальцев. Можно ли тогда считать его систему одним из самых великих изобретений? Но почему именно она, да и вообще, по какому принципу, в каком порядке там поставлены все элементы?
Менделеев Дмитрий Иванович — был 17 ребёнком в семье
Как пользоваться Таблицей Менделеева
Честно говоря, в первый раз смотря на таблицу, невозможно её прочитать. Почему где-то есть пропуски, а где-то целые десятки элементов входят в одну ячейку? По какому принципу летучие вещества были расположены в конце группы, в то время как те, у которых более выражены металлические свойства, располагаются ближе к началу? На большую часть этих вопросов отвечают уроки химии, на которых учитель тратит огромное время на обучение детей прочтению таблицы Менделеева. Но, если в памяти это не отложилось, или что-то осталось непонятным — не беда, всё не так уж и сложно.

Наверное, многие успели заметить то, что все элементы расположены по порядку, а у каждого есть свой собственный номер. Именно он характеризует количество протонов в ядре, а также количество электронов, движущихся вокруг него. Чем оно больше – тем больше уровней, так называемых, «орбиталей», по которым они в состоянии передвигаться.
Следующее, на что обращается внимание – иногда даже огромное число внизу. Это относительная атомная масса элемента, характеризующая, сколько будет весить один его моль. Как правило, она измеряется в граммах на моль, поэтому нетрудно предположить, насколько же легка. Как правило, кстати, это усреднённое значение, поэтому записывается с числами после запятой. Исключения составляют лишь элементы, стоящие в седьмом периоде, то есть, радиоактивные.
Иногда также сбоку подписываются несколько чисел, которые в сумме дают порядковый номер. Это не случайно. Это расположение электронов по тем самым орбиталям, о которых ранее шла речь. Это довольно-таки удобно для использования в будущем, но, к сожалению, не всегда присутствует.
Самое главное же, что осталось на конец, – это группы и периоды в данной таблице. Столбики и строчки, простыми словами. Это один из самых важных моментов, характеризующий элементы в таблице Менделеева. Чтобы проще запомнить, стоит понять, что в группе, как правило, расположены элементы со сходными химическими свойствами, в то время, как в периоде они изменяются.
Период, как правило, совпадает с валентной оболочкой элемента. Как правило, чем правее вещество расположено, тем более выражены его металлические (восстановительные) свойства, в то время как в левой части больший акцент делается на окислительных.
Группа же, в свою очередь, это валентность элемента. Это число электронов, которые могут вступать в сложные химические связи. Но не стоит сразу же бежать писать и уравнивать соединения, в которых «неправильно» поставлены индексы. На самом же деле, валентность не всегда совпадает с номером группы. Но не стоит сомневаться в первых трёх – там всё более, чем нормально.
2018 в Дании был введен запрет на изучение таблицы Менделеева. В министерстве иностранных дел посчитали, что «русские используют Периодическую систему в качестве пиара интеллектуальных достижений России». А также она опасна для детей.
Таким образом, несложно понять, что таблица Менделеева – очень полезная вещь в химии, без которой невозможно было бы выполнять огромного количества действий. А сама её история создания просто завораживает дух!