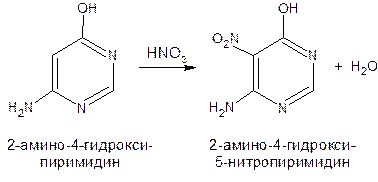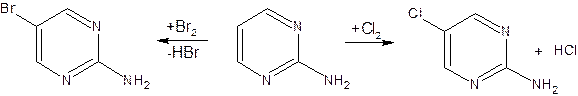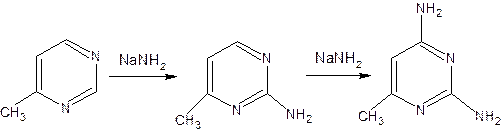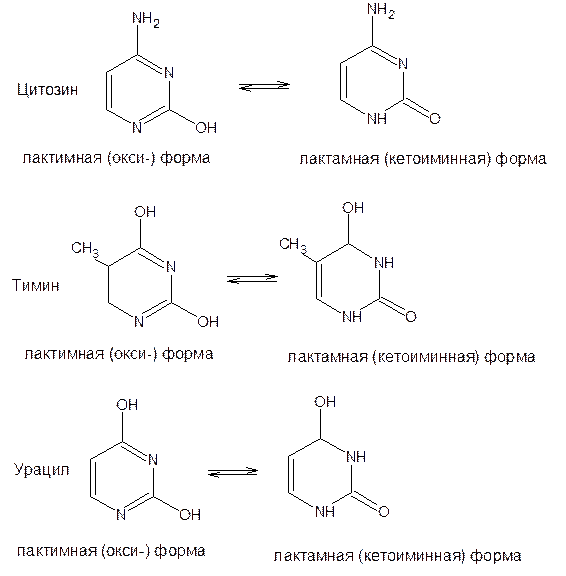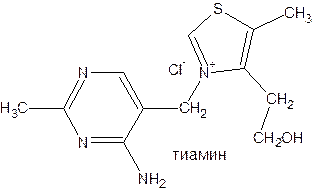Что относится к минорным пиримидиновым основаниям
МИНОРНЫЕ КОМПОНЕНТЫ НУКЛЕИНОВЫХ АЗОТИСТЫХ ОСНОВАНИЙ В ДНК И РНК.
Нуклеиновые кислоты ВМС – биологические полимерные молекулы, хранящие всю информацию об отдельном живом организме, определяющие его рост и развитие, а также наследственные признаки, передаваемые следующему поколению. С уверенностью можно сказать, что они по праву являются основной жизни на Земле, именно поэтому так важно изучать их строение и свойства. Данные знания помогут более плодотворно использовать их во всех сферах жизни человека, а самое главное в медицине и фармации. Даже такие незначительные структуры нуклеиновых кислот, как минорные – редкие нуклеиновые азотистые основания, активно используются человеком. Они, безусловно, привлекают внимание ученых и исследователей. Строение и свойства их не до конца изучены, но существующие знания о роли минорных нуклеиновых азотистых оснований, уже позволяют сделать вывод о том, на сколько широким может быть спектр их применения. Исходя из этого, задачей данной работы было рассмотреть строение, свойства, методы выделения и функции минорных нуклеиновых азотистых оснований.
Существуют различные методы выделения минорных компонентов, для последующего их использования. Наиболее общим методом выделения редких компонентов РНК является, по-видимому, метод, предложенный Холлом. Он состоит в ферментативном расщеплении РНК до нуклеотидов под действием смеси фосфодиэстеразы змеиного яда и щелочной фосфомоноэстеразы из Escherichia coli. Смесь нуклеотидов разделяют далее с помощью распределительной хроматографии на целите. Мягкость условий расщепления полимера сочетается здесь с высокой эффективностью разделения мономеров, что и позволило обнаружить целый ряд неизвестных ранее редких компонентов РНК.
5-метилцитозин — метилированная форма цитозина, в котором метильная группа добавлена к 5-му углероду, изменяя его структуру без изменения его свойств образования пар оснований в нуклеиновых кислотах. После семи десятилетий, было выяснено, что он часто присутствует в различных молекулах РНК, хотя его функция точно неизвестна. Обнаружен в составе ДНК высших растений и некоторых бактерий.
5-оксиметилцитозин — пиримидиновое основание, замещающее цитозин в ДНК Т-четных фагов. Обнаружен в некоторых штаммах фагов кишечной палочки.
Уникальное строение и способ образования минорных компонентов, наделяет их особенными свойствами. Именно это и будет характеризовать их роль в жизнидеятельности человека.
Так же обнаружено, что 3–метиладенин–ДНК–гликозилаза ингибировала способность топоизомеразы I вызывать релаксацию сверхскрученной молекулы ДНК. Напротив, топоизомераза I стимулировала гликозилазную активность 3–метиладенин–ДНК–гликозилазы по отношению к поврежденному ДНК–олигонуклеотидному субстрату, содержащему гипоксантин. Предположено, что существуют устойчивые взаимосвязи между этими ферментами в клетках микобактерий двух исследованных видов. Также охарактеризованы некоторые мутантные формы 3–метиладенин–ДНК–гликозилазы, не способные взаимодействовать с топоизомеразой I и активировать ее. Представленные данные проливают свет на регуляцию активности гликозилазы в клетках микобактерий M. smegmatis и M. tuberculosis.
Минорные компоненты могут принимать участие в биосинтезе белка, так, например, при сканирующем механизме нахождения стартового AUG рибосома (точнее, её малая субъединица) садится на 5′-конец мРНК в области кэпа и двигается вдоль молекулы мРНК, «сканируя» один кодон за другим, пока не наткнётся на инициаторный AUG. Для привлечения рибосомы к 5′-концу мРНК требуется специальная структура, кэп — 7-метилгуанин, прикреплённый к 5′-концевому нуклеотиду мРНК.
Важно отметить, что минорные компоненты активно используются в изготовление различных препаратов для лечения онкологических заболеваний. На данный момент количество, таких медицинских средств довольно велико.
Фторурацил
Синтетический аналог естественного пиримидинового основания урацила. В процессе распада фторурацила несколько его метаболитов оказывают повреждающее воздействие на синтез и функционирование ДИК и рибонуклеиновых кислот опухолевых клеток. Рандомизированные исследования по применению фторурацила в комбинации с доксорубицином (адриамицином), митомицином и этопозидом по сравнению с симптоматической терапией показали достоверное увеличение выживаемости в группе больных, которым проводили химиотерапию. Используется для лечения рака поджелудочной железы в виде химиотерапии.
Зидовудин
Обладает высокой активностью в отношении ретровирусов (в т.ч. ВИЧ)В клетке при участии клеточных тимидинкиназы, тимидилаткиназы и неспецифической киназы фосфорилируется с образованием моно-, ди- и трифосфатного соединения. Зидовудин-трифосфат встраивается в провирус и блокирует дальнейшее наращивание цепи вирусной ДНК и делает невозможным синтез вирусной ДНК. Способствует увеличению количества T4 клеток.
Ацикловир
Обладает высокой специфичностью в отношении вируса Herpes simplexАцикловир проникает непосредственно в инфицированные вирусом клетки. Клетки, инфицированные вирусом, продуцируют вирусную тимидинкиназу, которая фосфорилирует ацикловир до ацикловира монофосфата. Кроме того, активность вирусной тимидинкиназы по отношению к ацикловиру намного выше, чем действие на него клеточных ферментов (в инфицированных клетках концентрация ацикловира монофосфата выше в 40–100 раз). Дальнейшее фосфорилирование клеточными ферментами приводит к образованию ацикловир-трифосфата, являющегося чрезвычайно активным и селективным ингибитором ДНК-полимеразы вирусов. Вероятно механизм ингибирования ацикловир-трифосфатом синтеза ДНК состоит в том, что она является для этого фермента субстратом, позволяющим осуществить связь 3’–5′, необходимую для продления цепочки ДНК. Таким образом осуществляется преждевременный обрыв цепи ДНК.
Вывод
Благодарим за руководство работой доцентов Е.И.Шостак и М.М.Павлову.
МИНОРНЫЕ ОСНОВАНИЯ
Смотреть что такое «МИНОРНЫЕ ОСНОВАНИЯ» в других словарях:
МИНОРНЫЕ ОСНОВАНИЯ — необычные, гл. обр. метилированные формы обычных азотистых оснований (аденина, гуанина, цитозина, тимина, урацила), редко встречающиеся в нуклеиновых к тах наряду с обычными. Минорные пиримидиновые основания 5 метилцитозин, 5 оксиметилцитозин и… … Биологический энциклопедический словарь
Минорные основания — * мінорныя асновы * minor bases необычные, гл. обр. метилированные, редко встречающиеся в нуклеиновых кислотах наряду с обычными азотистыми основаниями (аденина, гуанина, тмина, цитозина, урацила). Компоненты тРНК (до 10% общего содержания… … Генетика. Энциклопедический словарь
минорные основания — пиримидиновые и пуриновые основания, которые (в отличие от обычных оснований аденина, гуанина, тимина и цитозина) сравнительно редко встречаются в составе нуклеиновых кислот. Минорные основания в ДНК 5 метилцитозин, 6 метиламинопурин, урацил, 5 … Энциклопедический словарь
МИНОРНЫЕ ОСНОВАНИЯ — пиримидиновые и пуриновые основания, к рые (в отличие от обычных оснований аденина, гуанина, тимина и цитозина) сравнительно редко встречаются в составе нуклеиновых к т. М. о. в ДНК 5 метилцитозин, 6 метиламинопурин, урацил, 5 оксиметилурацил и… … Естествознание. Энциклопедический словарь
редкие (минорные) основания — Пуриновые и пиримидиновые основания, входящие в состав молекул тРНК помимо аденина, урацила, гуанина и цитозина: инозин, метилинозин, диметилгуанозин, метилгуанозин, риботимидин, псевдоуридин, 5,6 дигидроуридин и др.; все Р.о. являются… … Справочник технического переводчика
МИНОРНЫЕ НУКЛЕОЗИДЫ — пуриновые и пиримидино выс нуклеозиды, входящие в молекулы прир. нуклеиновых к т в относительно небольших кол вах. В отличие от наиб. распространенных нуклеозидов (аденозина, гуанозина, ури дина, тимидина и цитидина) содержат модифицир. гетеро… … Химическая энциклопедия
Пиримидиновые основания — пиримидины, группа природных соединений, производных гетероциклического азотистого основания Пиримидина. Играют важнейшую роль в жизнедеятельности организмов, входя в состав нуклеиновых кислот. В последних найдены П. о.: Цитозин (2 окси б … Большая советская энциклопедия
редкие основания — редкие основания. См. минорные основания. (Источник: «Англо русский толковый словарь генетических терминов». Арефьев В.А., Лисовенко Л.А., Москва: Изд во ВНИРО, 1995 г.) … Молекулярная биология и генетика. Толковый словарь.
ПУРИНОВЫЕ ОСНОВАНИЯ — прир. производные пурина. Входят в качестве агликонов (неуглеводного компонента) в нуклеиновые к ты, нуклеозиды, нуклеотиды; фрагменты коферментов, витаминов и др. Канонические П. о. нуклеиновых к т аденин (6 аминопурин, сокращенно А) и гуанин (2 … Химическая энциклопедия
Пиримидин, пиримидиновые основания



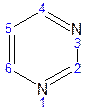
В положениях 2,4 и 6, где влияние отрицательного индуктивного эффекта (–I-эффект) атомов азота проявляется особенно сильно, будет наибольший положительный d-электронный заряд, т.е. наименьшая электронная плотность, в то же время положение 5 испытывает наименьшую потерю электронов, где и будет наибольшая электронная плотность. Нуклеофильные реагенты атакуют положения 2, 4, 6, а электрофильные – положение 5 в соответствии с поляризацией этих положений.
Взаимодействие неподеленных электронных пар атомов азота с
p-электронами в ароматической системе приводит к уменьшению основности атомов азота пиримидина и поэтому она значительно ниже, чем у пиридина. Вследствие этого протонирование по атомам азота пиримидина протекает лишь в очень сильных кислотах и приводит к образованию соли только по одному атому азота.
Сам пиримидин инертен к электрофильной атаке. И только введение электронодонорных заместителей (–NH2, –OH, –SH) в положения 2, 4, 6 делает возможным электрофильную атаку положения 5 кольца пиримидина. Пиримидин с двумя электронодонорными заместителями вступает в электрофильное замещение как бензол, а с тремя электронодонорными заместителями в кольце реагирует легко, подобно фенолу. Например, нитрование требует двух электронодонорных групп:
Для галогенирования достаточно одной электронодонорной группы. Так,
2-аминопиримидин хлорируется и бромируется в положение 5:
Значительно больше распространены в ряду пиримидина реакции нуклеофильного замещения. При этом речь идет о нуклеофильном замещении различных групп, находящихся в положениях 2, 4, 6. Так, при действии амида натрия на 6-метилпиридин образуются 2-амино- и 2,4-диамино-6-метилпиримидин:
Следует отметить, что алкильные группы в положениях 2, 4 и 6 пиримидина обладают повышенной активностью: легко вступают в конденсацию с альдегидами и в реакцию азосочетания.
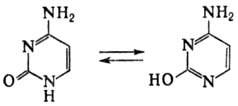
При гидролизе нуклеиновых кислот получаются три важных производных пиримидина: цитозин (4-амино-2-гидроксипиримидин), тимин (2,4-дигидрокси-5-метилпиримидин) и урацил (2,4-дигидроксипиримидин), которые относятся к группе пиримидиновых оснований. Одним из важных свойств пиримидиновых азотистых оснований является возможность их существования в двух таутомерных формах – лактим-лактамной формах, в зависимости от значения рН среды, при рН 7,0 они находятся в лактамной форме, которая и является главной таутомерной формой:
Лактимная форма присутствует только в растворах в кислой среде в весьма незначительном количестве. Помимо главных пиримидиновых оснований в составе нуклеиновых кислот открыты минорные пиримидиновые основания: 5-метил и 5-оксиметилцитозин, дигидроурацил, псевдоурацил, 1-метилурацил, 4-тиоурацил и др. На долю минорных оснований приходится до 10% всех нуклеотидов транспортных рибонуклеиновых кислот (тРНК), что имеет важный физиологический смысл – защита молекулы РНК от действия гидролитических ферментов.
Витамин В1(тиамин) тоже содержит пиримидиновый цикл, соединенный метиленовой связью с кольцом тиазола
Отсутствие витамина В1 в пище, например, при питании ободранным рисом (он содержится в рисовых отрубях), вызывает известное на востоке нервное заболевание бери-бери. Суточная потребность в витамине В1 для человека – 4 мг. Необходимость в нем связана с тем, что витамин В1 (в виде дифосфата – ТДФ – тиаминдифосфат) входит в структуру двух сложных ферментных систем: пируват- и a-кетоглутаратдегидрогеназных комплексов, катализирующих окислительное декарбоксилирование пировиноградной и a-кетоглутаровой кислот и других оксокислот, образующихся при распаде аминокислот с разветвленной боковой цепью. Основное количество витамина В1 человек получает с растительной пищей, а также им богаты печень, почки, мозг.
ПИРИМИДИНОВЫЕ ОСНОВАНИЯ
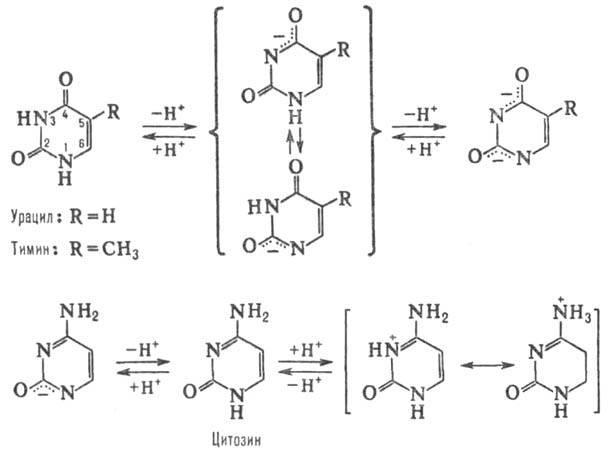
производные пиримидина, входящие в состав нуклеиновых к-т, нуклео-тидов, коферментов и др. Канонич. П. о.-цитозин (4-амино-2-пиримидон, сокращенно С), тимин (3-метил-пиримидин-2,4-дион, T) и урацил (пиримидин-2,4-дион, U); разл. формы молекул. П. о. (они существуют при разных значениях рН) показаны на схеме.
Специфич. наборы водородных связей между пирими-диновыми и пуриновыми основаниями в комплементарных участках цепей (см. Комплементарностъ), а также межплоскостные взаимод. между соседними основаниями в цепи определяют формирование и стабилизацию вторичной и третичной структуры нуклеиновых к-т. Последовательность пуриновых и пиримидиновых оснований в полинуклеотидной цепи определяет генетич. информацию ДНК и матричных РНК. Модификация П. о. в полинуклеотидах под воздействием мутагенов может приводить к изменению информац. смысла (точковой мутации).
П. о. представляют собой высокоплавкие (т. пл. 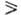
При радиолизе водных р-ров П. о. образуются 5,6-дигид-рокси-, 5-гидрокси-6-гидроперокси- и 5-гидроперокси-6-гидрокси-5,6-дигидропиримидины и продукты их дальнейших превращений. Действие УФ излучения (l > 200 нм) на водные р-ры П. о. приводит к образованию 5,6-дигидро-6-гидроксипиримидинов (фотогидратов), циклобутановых димеров (через триплетное состояние) с раскрытием связей C=C, нециклобутановых димеров П. о. (через нижнее синглетное возбужденное состояние). Фотогидраты спонтанно превращ. в исходные соед., а циклобутановые димеры дедимеризуются фотохимически.
Различие реакц. способности П. о. позволяет избирательно модифицировать их в составе полинуклеотидов. Такие р-ции лежат в основе определения нуклеотидной последовательности (первичной структуры) нуклеиновых к-т. Взаимод. с соседними основаниями, зависящие от локальной высшей структуры полинуклеотидов, оказывают влияние на скорость модификации П. о. при действии разл. агентов. В связи с этим сопоставление относит. скоростей модификации П. о. используется для изучения вторичной и третичной структуры нуклеиновых к-т.
Как канонические, так и минорные П. о. обычно получают препаративно из нуклеиновых к-т путем кислотного гидролиза и послед. разделения.
Лит.: Кочетков H. К. [и др.], Органическая химия нуклеиновых кислот, M., 1970; Бородавкин А. В. [и др.], Электронная структура, УФ-спектры поглощения и реакционная способность компонентов нуклеиновых кислот, в сб.: Итоги науки и техники, сер. Молекулярная биология, т. 14, M., 1977; Шаба-ров а 3. А., Богданов А. А., Химия нуклеиновых кислот и их компонентов, M., 1978; Photochemistry and photobiology of nucleic acids, v. 1 (Chemistry), ed. by Shi Yi Wang. N. Y., 1976. Э. И. Будовский.
Полезное
Смотреть что такое «ПИРИМИДИНОВЫЕ ОСНОВАНИЯ» в других словарях:
Пиримидиновые основания — Пиримидиновые основания группа природных веществ, производные пиримидина. Различаются характером и положением заместителей в пиримидиновом ядре. Представляют собой бесцветные, кристаллические вещества, с температурой плавления выше… … Википедия
пиримидиновые основания — Пиримидиновые основания. Формула. Пиримидиновые основания. Формула. пиримидиновые основания, органические соединения, производные пиримидина, различающиеся заместителями в пиримидиновом кольце. К ним относятся урацил (I>>), тимин (II), цитозин… … Ветеринарный энциклопедический словарь
ПИРИМИДИНОВЫЕ ОСНОВАНИЯ — группа природных соединений (цитозин, урацил, тимин, а также минорные П. о.), производных гетероциклич. Азотистого основания пиримидина. Входят в состав нуклеиновых к т; благодаря способности специфически (по принципу комплементарности)… … Биологический энциклопедический словарь
ПИРИМИДИНОВЫЕ ОСНОВАНИЯ — природные органические соединения, производные пиримидина. Биологическая роль в жизнедеятельности всех организмов обусловлена участием пиримидиновых оснований в построении нуклеиновых кислот, коферментов и других биологически активных соединений … Большой Энциклопедический словарь
пиримидиновые основания — природные органические соединения, производные пиримидина. Биологическая роль в жизнедеятельности всех организмов обусловлена участием пиримидиновых оснований (в том числе цитозин, урацил, тимин) в построении нуклеиновых кислот, коферментов и др … Энциклопедический словарь
пиримидиновые основания — pirimidino bazės statusas T sritis chemija apibrėžtis Bendras citozino, timino ir uracilo pavadinimas. atitikmenys: angl. pyrimidine bases rus. пиримидиновые основания … Chemijos terminų aiškinamasis žodynas
Пиримидиновые основания — пиримидины, группа природных соединений, производных гетероциклического азотистого основания Пиримидина. Играют важнейшую роль в жизнедеятельности организмов, входя в состав нуклеиновых кислот. В последних найдены П. о.: Цитозин (2 окси б … Большая советская энциклопедия
пиримидиновые основания — общее название производных пиримидина (напр., цитозин, урацил, тимин); входят в состав нуклеиновых кислот, коферментов и других биологически активных веществ … Большой медицинский словарь
ПИРИМИДИНОВЫЕ ОСНОВАНИЯ — природные органич. соединения, производные пиримидина. Биол. роль в жизнедеятельности всех организмов обусловлена участием П. о. (в т. ч. цитозин, урацил, тимин) в построении нуклеиновых к т, коферментов и др. биологически активных соединений … Естествознание. Энциклопедический словарь
Пиримидиновые основания — группа соединений (цитозин, тимин, урацил), входящих в состав нуклеиновых кислот (ДНК, РНК); комплементарно взаимодействуя с пуринами (пуриновыми основаниями) (аде нин, гуанин), они участвуют в кодировании и передаче наследственной (генетической) … Начала современного естествознания
Пуриновые и пиримидиновые основания. нуклеозиды. нуклеотиды
ПУРИНОВЫЕ И ПИРИМИДИНОВЫЕ ОСНОВАНИЯ. НУКЛЕОЗИДЫ. НУКЛЕОТИДЫ
Цель : сформировать знания строения и свойств нуклеотидов, их роли в метаболизме; первичной и вторичной структуры нуклеиновых кислот.
[1] С. 420–444, [2] С. 109–115.
Нуклеиновые кислоты обеспечивают хранение и передачу наследственной информации, непосредственно участвуют в механизмах реализации этой информации путем программированного синтеза всех клеточных белков. Нуклеиновые кислоты представляют собой высокомолекулярные соединения, молекулярная масса которых колеблется в пределах от 25 тыс. до 1 млн дальтон и более. Полимерные цепи нуклеиновых кислот построены из мономерных единиц — нуклеотидов, в связи с чем нуклеиновые кислоты называют полинуклеотидами. Существуют два типа нуклеиновых кислот — ДНК и РНК, различающиеся по молекулярной массе, составу азотистых оснований, сахаров, устойчивости и функциям.
Нуклеиновые кислоты обладают выраженными кислотными свойствами (обусловленными наличием остатков ортофосфорной кислоты в их составе) и при физиологических значениях рН несут отрицательный заряд. Этим объясняется одно из важных свойств нуклеиновых кислот — взаимодействовать с основными белками (гистонами). Нуклеиновые кислоты также образуют ионные связи с катионами металлов, преимущественно с Мg2+.
При полном гидролизе нуклеиновых кислот (нагревании в присутствии хлорной кислоты) в гидролизате обнаруживаются пуриновые и пиримидиновые основания, углеводы (рибоза и дезоксирибоза) и фосфорная кислота:
Дезоксирибоза
Тимин
Рибоза
Урацил
НУКЛЕИНОВЫЕ ОСНОВАНИЯ, ИХ ТАУТОМЕРНЫЕ ФОРМЫ
К пуриновым основаниям относятся аденин и гуанин. Для аденина характерна амино-иминная таутомерия. А для гуанина — лактам-лактимная и амино-иминная.
При физиологических условиях нуклеиновые основания существуют только в лактамной и аминной формах.
Нуклеиновые основания растворимы в воде, их растворы имеют слабощелочную
реакцию среды (рН 8–9).
Цитозин + Рибоза ® Цитидин
Цитозин + Дезоксирибоза ® Дезоксицитидин
Аденин + Рибоза ® Аденозин
Аденин + Дезоксирибоза ® Дезоксиаденозин
Нуклеотиды — это фосфорные эфиры нуклеозидов, являющиеся структурными единицами нуклеиновых кислот. Они образуются в реакции фосфорилирования, протекающей по типу нуклеофильного замещения, приводящей к формированию сложноэфирной связи.
Нуклеотиды способны гидролизоваться в кислой и щелочной среде.
Гидролизу могут подвергаться как N-гликозидная, так и сложноэфирная связи, и в зависимости от рН среды могут образовываться или нуклеозиды или компоненты нуклеотида.
Обнаружить в продуктах гидролиза нуклеотидов пуриновые основания можно при помощи «серебряной пробы».
В ходе реакции образуется светло-коричневый осадок серебряных солей пуриновых оснований.
Пентозы обнаруживают с помощью реакции Биаля.
Фурфурол далее конденсируется с орцином, о чем свидетельствует появление сине-зеленой окраски.
Фосфорную кислоту можно обнаружить при помощи молибденового реактива.
H3PO4 + 12(NH4)2MoO4 + 21HNO3 → (NH4)3PO4 · 12MoO3 + 21NH4 NO3 + 12H2O
Образующийся фосфорномолиденовокислый аммоний — осадок желтого цвета.
Нуклеотиды входят в состав нуклеиновых кислот; но, кроме того, они встречаются
в клетке в свободном состоянии, выполняя энергетическую и регуляторную функции. К наиболее важным из них относятся циклические нуклеотиды, аденозинтрифосфат и гуанозинтрифосфат.

Они содержат две ангидридные связи, называемые макроэргическими. При расщеплении макроэргической связи Р
О (обозначаемой волнистой линией) выделяется
32 кДж/моль. С этим связана важнейшая роль АТФ как «поставщика» энергии во всех живых клетках. Нуклеозидная часть молекулы важна для узнавания и связывания с различными ферментами, использующими АТФ или ГТФ.
При физиологических значениях рН АТФ находится в ионизированном состоянии и в клетке связывается с ионами двухвалентных металлов (Мg2+, Са2+). Такое связывание частично нейтрализует общий отрицательный заряд и облегчает гидролиз АТФ под действием нуклеофилов (ОН-, Н2О). АТФ способен переносить потенциальную энергию на множество важных биологических соединений. Так, с участием АТФ осуществляется активный транспорт ионов через биологические мембраны, активирование аминокислот перед их связыванием с т-РНК, синтез полинуклеотидных цепей, образование пептидных связей в белках и т. д.
Наиболее важными представителями этой группы соединений являются никотинамидадениндинуклеотид (НАД) и его фосфат (НАДФ). Эти соединения выполняют роль коферментов большого числа ферментов дегидрогеназ и, следовательно, являются участниками окислительно-восстановительных реакций. В соответствии с этим они могут существовать как в окисленной (НАД+, НАДФ+), так и восстановленной (НАДН, НАДФН) формах.
Структурным фрагментом НАД+, НАДФ+ является никотинамидный остаток в виде пиридиниевого катиона. В организме человека с участием НАД+ происходит окисление гидроксилсодержащих соединений, например, этанола в ацетальдегид.
Ароматический пиридиниевый цикл в НАД+ в результате окисления гидроксилсодержащего субстрата восстанавливается и переходит в менее стабильное неароматическое
состояние в восстановленной форме НАДН, т. е. энергия НАДН будет выше, чем у НАД+. Повышение энергии в молекуле НАДН происходит за счет части энергии, выделяющейся
в результате окисления молочной кислоты. Таким образом НАДН запасает энергию, которая затем расходуется в других биохимических процессах, требующих энергетических затрат.
ПЕРВИЧНАЯ СТРУКТУРА НУКЛЕИНОВЫХ КИСЛОТ
Нуклеиновые кислоты представляют собой макромолекулы, построенные из нуклеотидов, соединенных в линейную последовательность фосфодиэфирными связями. Рибонуклеотиды образуют РНК, дезоксирибонуклеотиды — ДНК.
Мононуклеотиды в структуре нуклеиновых кислот связываются друг с другом через остатки фосфорной кислоты, которые образуют две сложноэфирные (фосфодиэфирные)
связи: с С3′ предыдущего нуклеотидного звена и с С5′ последующего нуклеотидного звена. Полимерная цепь нуклеиновых кислот состоит из чередующихся пентозных и фосфатных остатков, а гетероциклические основания являются «боковыми» группами, присоединенными к пентозным остаткам. Концы линейной полинуклеотидной цепи обозначают: 5′-конец (слева) и 3′ — конец (справа). Написание цепи обычно начинают с 5′-конца. В этом случае общее направление образования фосфодиэфирных связей в цепи обозначается 5’→3′. На
5′-конце находится фосфатная группа, и такой конец цепи сокращенно обозначают буквой «Р». На другом конце цепи в пентозном остатке сохраняется свободной гидроксильная группа у С-3′, и поэтому этот конец цепи обозначают как ОН-конец. На рисунке приведено строение участка цепи ДНК, включающего четыре нуклеотида.
Принцип построения цепи РНК такой же, как и у ДНК, с двумя исключениями: пентозным остатком в РНК является D-рибоза, и в наборе гетероциклических оснований используется не тимин, а урацил. Таким образом, первичная структура нуклеиновых кислот — это линейная последовательность нуклеотидных звеньев, связанных ковалентными фосфодиэфирными связями в непрерывную цепь полинуклеотида.
ПОНЯТИЕ О ДВОЙНОЙ СПИРАЛИ ДНК
Вторичная структура ДНК — это пространственная организация полинуклеотидных цепей в ее молекуле. Согласно модели Дж. Уотсона и Ф. Крика, молекула ДНК состоит из двух полинуклеотидных цепей, правозакрученных вокруг общей оси с образованием двойной спирали, имеющей диаметр 1,8–2,0 нм. Эти две полинуклеотидные цепи антипараллельны друг другу, т. е. направления образования фосфодиэфирных связей в них противоположны: в одной цепи 5’–3′, в другой 3’–5′.
Стэкинг-взаимодействия между основаниями стабилизируют спиральную структуру, преодолевая силы электростатического отталкивания между отрицательно заряженными фосфатными группами. Эта энергия стабилизации может быть равна или превышать энергию связывания цепей водородными связями. Построение молекулярных моделей показывает, что именно в правой спирали взаимодействие между нуклеотидами оптимально.
Водородные связи между комплементарными основаниями — это один из видов взаимодействия, стабилизирующих двойную спираль. Данный вид взаимодействия называют «поперечным» в отличие от «вертикального» (стэкинг-взаимодействия). Две цепи ДНК, образующие двойную спираль, не идентичны, но комплементарны друг другу. Это означает, что первичная структура, т. е. нуклеотидная последовательность, одной цепи предопределяет первичную структуру второй цепи.
Пуриновые и пиримидиновые основания нуклеотидных звеньев направлены внутрь двойной спирали. Между пуриновым основанием со стороны одной цепи и пиримидиновым основанием со стороны другой цепи образуются водородные связи. Эти основания, связанные водородными связями составляют комплементарные пары.

с ДНК родительских клеток. Аналогичным образом на деспирализованном участке цепи ДНК в ядре происходит синтез молекулы матричной (информационной) РНК
(и-РНК), которая затем сама служит матрицей для биосинтеза белка в цитоплазме. Возникающая цепь и-РНК комплементарна той цепи ДНК, на которой она синтезируется. При этом адениновому основанию в ДНК будет соответствовать урациловое основание в РНК, а в качестве углеводного остатка в цепи РНК будет использоваться рибоза. Синтез и-РНК является по существу переписыванием, транскрипцией генетической информации с ДНК на и-РНК. Генетическая информация, т. е. информация о синтезе определенных белков, закодирована в нуклеотидной последовательности ДНК. Одну аминокислоту кодирует трехнуклеотидная последовательность, поэтому код
называют триплетным. Три нуклеотида, контролирующие включение данной аминокислоты в определенный белок в процессе его биосинтеза, называются кодоном.
Третичная структура ДНК. Выделить и изучить нативную молекулу ДНК из ядер эукариотических организмов чрезвычайно трудно, так как молекулы ДНК разрушаются нуклеазами тканей и подвергаются деструкции в условиях выделения.
К настоящему времени удалось выделить в неповрежденном виде ДНК вирусов, митохондрий, некоторых бактерий. Оказалось, что двойная спираль ДНК на некоторых участках может подвергаться дальнейшей спирализации с образованием суперспирали или открытой кольцевой формы.
 |
Суперспирализованная структура обеспечивает экономичную упаковку огромной молекулы ДНК в хромосоме. У человека ДНК клетки организовано в 23 пары хромосом. Средняя протяженность ДНК хромосомы, включающая 130 млн пар оснований, имеет среднюю длину 5 см. Понятно, что уместить такой длины ДНК в ядре можно лишь путем ее определенной упаковки. Многократная спирализация ДНК, сопровождающаяся образованием комплексов с белками, и представляет собой ее третичную структуру. В результате образования такой структуры происходит уменьшение размеров ДНК в 100 тысяч раз. Основным компонентом клеточного ядра является хроматин. Фибриллы хроматина представляют собой структуры, напоминающие бусы на нитке: небольшие, около 10 нм глобулы, связанные друг с другом отрезками ДНК длиной около 20 нм. Эти глобулы получили название нуклеосом. Нуклеосомы состоят из ядра, представленного 8 молекулами гистонов и навитой на него по поверхности молекулы ДНК, делающей 1,75 оборота. Структура нуклеосомы поддерживается гистоном Н1. Количество таких частиц в гаплоидном наборе ДНК человека может составлять величину равную 1,5×107. Одновременно были обнаружены и фибриллы хроматина
с диаметром 25–30 нм, которые могут обратимо превращаться в фибриллы диаметром 10 нм. Полагают, что нить плотно упакованных нуклеосом диаметром 10 нм, образует в свою очередь спиральные витки с шагом спирали около 10 нм. На один виток такой суперспирали приходится 6–7 нуклеосом.
Такие 25–30-нанометровые глобулы получили название нуклеомеров. Нуклеомерный уровень укладки хроматина обеспечивает 40-кратное уплотнение ДНК.
Как нуклеосомный, так и нуклеомерный уровни компактизации ДНК хроматина осуществляются за счет гистоновых белков, которые соединяются неспецифически с ДНК в бороздках. В ДНК встречаются положительные и отрицательные супервитки, образованные
за счет скручивания по часовой или против часовой стрелки двойной спирали. Дальнейшие более высокие уровни организации хроматина, приводящие к еще большей компактизации, связаны со специфическим взаимодействием особых участков ДНК с белками негистоновой природы. Это специфическое связывание приводит к дальнейшему формированию в этих участках больших петель или доменов, на электронных микрофотографиях они выглядят
в виде розеткообразных образований. Эти образования, состоящие из многих петель
30-нанометровых фибрилл, соединяющихся в общем плотном центре, получили название хромомер. Размер отдельной петли совпадает с размером средних репликонов (единиц репликации ДНК) и может соответствовать одному или нескольким генам. На хромосому
в среднем приходится более 2000 таких петельных доменов ДНК. В своих основаниях петли ДНК связаны негистоновыми белками ядерного матрикса. В их состав могут входить как ферменты репликации ДНК, так и транскрипции.
Такая петельно-доменная структура хроматина обеспечивает не только компактизацию хроматина, но и организует функциональные единицы хромосом — репликоны и транскрибируемые гены.
ВИДЫ РИБОНУКЛЕИНОВЫХ КИСЛОТ
Известны несколько видов клеточных РНК: транспортная РНК (т-РНК), информационная РНК (и-РНК), рибосомная РНК (р-РНК), si РНК и другие. Они различаются местоположением в клетке, составом и размерами, а также своими функциями. В составе нуклеопротеинов ядра и цитоплазмы обнаруживаются небольшие, стабильные молекулы РНК. Кроме клеточных РНК, имеются вирусные РНК, входящие в состав многих вирусов животных и растений.
На долю т-РНК приходится 10–20 % от суммы клеточных РНК; их молекулярная масса 30 000, цепь включает 75–90 нуклеотидных звеньев. Основная роль т-РНК состоит в том, что они транспортируют аминокислоты из цитоплазмы к месту синтеза белка — в рибосомы. Число т-РНК превышает число α-аминокислот, участвующих в построении белков.
В класс малых si РНК ( small interfering — малые интерферирующие РНК) включают молекулы, содержащие от 20 до 30 нуклеотидов. Особенностью этих молекул является то, что они, в отличие от большинства других клеточных РНК, состоящих всего из одной цепи нуклеотидов, являются двунитчатыми. Нуклеотиды противоположных цепей si РНК соединяются друг с другом по тем же принципам комплементарности, которые формируют двухцепочечные структуры ДНК в хромосомах. Кроме того, по концам каждой из цепей si РНК всегда остается два неспаренных нуклеотида. В 2002 г. была установлена их способность
подавлять экспрессию генов у животных.
В 2006 г. за исследование механизма действия si РНК, выражающегося в нейтрализации отдельных генов на этапе передачи генетической информации и синтеза белка, двум американским ученым Эндрю Файеру и Крейгу Мелло была присуждена Нобелевская премия в области физиологии и медицины. Это достижение открывает заманчивые перспективы в использовании данной технологии в генной инженерии при изучении роли отдельных генов, путем их «выключения», а также лечении ряда вирусных, эндокринных и других заболеваний.
НАРУШЕНИЯ, ВОЗНИКАЮЩИЕ В ДНК ПОД ВЛИЯНИЕМ
ФАКТОРОВ ОКРУЖАЮЩЕЙ СРЕДЫ
Уже на ранних стадиях эволюции, очевидно, ДНК заменила РНК в качестве носителя генетической информации. Это обусловлено большей устойчивостью ДНК, связанной с заменой рибозы на дезоксирибозу, и двухцепочечным строением ДНК. Благодаря гидрофобным взаимодействиям и водородным связям между двумя комплементарными полинуклеотидными цепями ДНК, реакционноспособные азотистые основания, последовательность
которых кодирует информацию, становятся менее доступными.
Однако, несмотря на свои особенности строения, ДНК постоянно подвергается химическим изменениям, как спонтанным, так и индуцируемым мутагенами и даже клеточными метаболитами. Еще одной причиной повреждения ДНК являются радиация и ультрафиолетовое облучение. Большинство изменений ДНК несовместимо с нормальным функционированием клеток: они либо приводят к вредным мутациям, либо блокируют репликацию ДНК и вызывают гибель клеток. Поэтому все клетки имеют специальные системы репарации ДНК.
В ДНК сравнительно часто и спонтанно происходят апуринизация и дезаминирование оснований. Так, ДНК каждой клетки человеческого организма ежедневно теряет около 5000 пуринов. Результатом апуринизации является АР-сайт (англ. Apurinic-apyrimidinic) — дезоксирибоза, лишенная основания.
При дезаминировании цитозин превращается в урацил, аденин — в гипоксантин,
а гуанин — в ксантин.

Многие вещества, обладающие канцерогенным действием, алкилируют, например, метилируют, основания ДНК. Наиболее частые продукты этих реакций — О6-метил-гуанин, 7-метилгуанин и 3-метил-аденин. Первое из этих изменений мутагенно. А два других делают более лабильной N-гликозидную связь и могут способствовать апуринизации.

Основным нарушением, возникающим под действием ультрафиолетового излучения, является насыщение двойных связей азотистых оснований, нарушение ароматичности и плоскостной структуры. В результате образуются пиримидиновые димеры из двух соседних пиримидинов цепи ДНК.