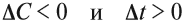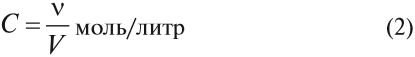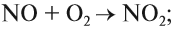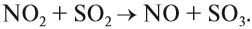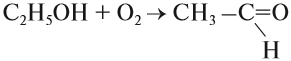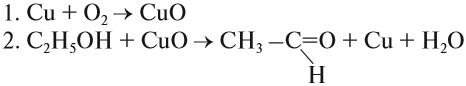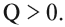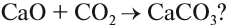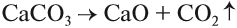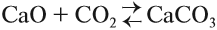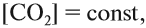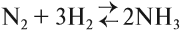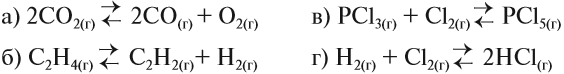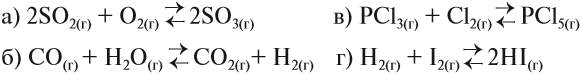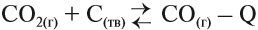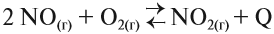Что называют скоростью химической реакции приведите примеры реакций протекающих с высокой и низкой
Вопросы к параграфу 3 — ГДЗ по Химии 9 класс Учебник Рудзитис, Фельдман
Авторы: Рудзитис Г.Е., Фельдман Ф.Г.
§ 3. Скорость химических реакций
Вопросы и задания
1. Что такое скорость химической реакции и как её определяют?
Скорость химической реакции определяется концентрацией одного из реагирующих или образующихся веществ в единицу времени.
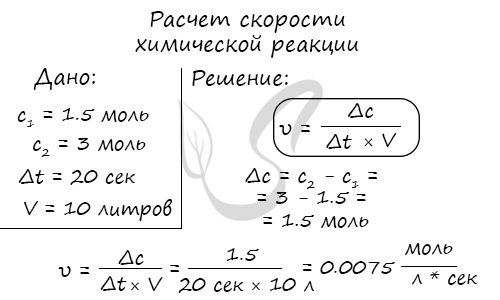
Скорость химической реакции можно найти по формуле:
2. Приведите примеры реакций, замедление или ускорение которых имеет положительное или отрицательное значение для производства либо в быту.
3. В таблице 1 указаны условия, влияющие на скорость химических реакций, и даны примеры. Назовите для каждого условия один-два дополнительных примера, составьте уравнения реакций и дайте обоснование их осуществления.
Природа реагирующих веществ.
Кальций и азот очень легко реагируют, а азот с кислородом — медленно и при определённых условиях (высокая температура, электрический разряд):
Концентрация реагирующих веществ.
Если добавить к соде концентрированную кислоту, пузырьки газа выделяются сильнее, чем при добавлении разбавленного раствора:
Площадь поверхности реагирующих веществ.
При разжигании костра мелкие щепки загорятся быстрее, чем полено или бревно.
Растворение оксида меди в кислоте происходит быстрее при нагревании, чем без него.
Присутствие катализатора или ингибитора.
Производство аммиака ускоряется при использовании катализатора пористого железа.
Ржавление железа замедляется ингибиторами коррозии.
Урок №4. Скорость химических реакций. Первоначальные представления о катализе
Для оценки скорости необходимо изменение концентрации одного из веществ.
Гомогенные системы (однородные) – газ/газ, жидкость/жидкость – реакции идут во всём объёме.
Гетерогенные (неоднородные) системы – твёрдое/жидкость, газ/твёрдое, жидкость/газ – реакции идут на поверхности раздела фаз.
С корость химической реакции в гомогенной системе
Скорость химической реакции в гетерогенной системе
Таким образом, скорость химической реакции показывает изменение количества вещества в единицу времени, в единице объёма или на единице поверхности раздела фаз. Наибольший интерес представляют реакции, протекающие в однородной (гомогенной) среде.
ФАКТОРЫ, ВЛИЯЮЩИЕ НА СКОРОСТЬ РЕАКЦИИ
Закон действующих масс: Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ.
При повышении концентрации хотя бы одного из реагирующих веществ скорость химической реакции возрастает в соответствии с кинетическим уравнением.
aA + bB = cC + dD
, где A, B, C, D – газы, жидкости
Кинетическое уравнение примет вид:
υ=k‧C a (A) ‧C b (B)
, где k – коэффициент скорости реакции
Причиной повышения скорости является увеличение числа столкновений реагирующих частиц за счёт увеличения частиц в единице объёма.
КАТАЛИЗАТОРЫ И ИНГИБИТОРЫ
гомогенный катализ (катализатор образует с реагирующими веществами гомогенную систему, например, газовую смесь);
гетерогенный катализ (катализатор и реагирующие вещества находятся в разных фазах; катализ идет на поверхности раздела фаз).
Для увеличения площади соприкосновения реагирующих веществ, их измельчают. Наибольшей степени измельчения достигают путем растворения веществ. Быстрее всего вещества реагируют в растворах.
Например, металлы магний и железо реагируют с соляной кислотой одинаковой концентрации с различной скоростью. Это связано с разной химической активностью металлов.
ПЛОЩАДЬ СОПРИКОСНОВЕНИЯ РЕАГИРУЮЩИХ ВЕЩЕСТВ
Для увеличения площади соприкосновения реагирующих веществ, их измельчают. Наибольшей степени измельчения достигают путем растворения веществ. Быстрее всего вещества реагируют в растворах.
ПРИРОДА РЕАГИРУЮЩИХ ВЕЩЕСТВ
Например, металлы магний и железо реагируют с соляной кислотой одинаковой концентрации с различной скоростью. Это связано с разной химической активностью металлов.
Скорость химической реакции
Скорость реакции отражает изменение концентраций реагирующих веществ за единицу времени. Единицы измерения для гомогенной реакции: моль/л * сек. Физический смысл в том, что каждую секунду какое-то количество одного вещества превращается в другое в единице объема.
Мне встречались задачи, где была дана молярная концентрация вещества до реакции и после, время и объем. Требовалось посчитать скорость реакции. Давайте решим подобное несложное задание для примера:
Влияние природы реагирующих веществ
При изучении агрегатных состояний веществ возникает вопрос: где же быстрее всего идут реакции: между газами, растворами или твердыми веществами?
Запомните, что самая высокая скорость реакции между растворами, в жидкостях. В газах она несколько ниже.
Если реакция гетерогенная: жидкость + твердое вещество, газ + твердое вещество, жидкость + газ, то большую роль играет площадь соприкосновения реагирующих веществ.
Химическая активность также играет важную роль. Например, отвечая на вопрос: какой из металлов Li или K быстрее прореагирует с водой? Мы отдадим предпочтение литию, так как в ряду активности металлов он стоит левее калия, а значит литий активнее калия.
Иногда для верного ответа на вопрос о скорости реакции требуется знание активности кислот. Мы подробнее обсудим эту тему в гидролизе, однако сейчас я замечу: чем сильнее (активнее) кислота, тем быстрее идет реакция.
Например, реакцию магния с серной кислотой протекает гораздо быстрее реакции магния с уксусной кислотой. Причиной этому служит то, что серная кислота относится к сильным (активным) кислотам, а активность уксусной кислоты меньше, она является слабой кислотой.
Как я уже упомянул, слабые и сильные кислоты и основания изучаются в теме гидролиз.
Влияние изменения концентрации
Замечу деталь, которая может оказаться важной, если в реакции участвуют газы: при увеличении давления концентрация вещества на единицу объема возрастает (представьте, как газ сжимается). Поэтому увеличение давление, если среди исходных веществ есть газ, увеличивает скорость реакции.
Закон действующих масс устанавливает соотношение между концентрациями реагирующих веществ и их продуктами. Скорость простой реакции aA + bB → cC определяют по уравнению:
Записанное выше следствие закона действующих масс нужно не только «зазубрить», но и понять. Поэтому мы решим пару задач, где потребуется написать подобную формулу.
Окисление диоксида серы протекает по уравнению: 2SO2(г) + O2 = 2SO3(г). Как изменится скорость этой реакции, если объемы системы уменьшить в три раза?
По итогу решения становится ясно, что скорость реакции в таком случае возрастет в 27 раз.
Решим еще одну задачу. Дана реакция синтеза аммиака: N2 + ЗН2 = 2NH3. Как изменится скорость прямой реакции образования аммиака, если уменьшить концентрацию водорода в два раза?
В результате решения мы видим, что при уменьшении концентрации водорода в два раза скорость реакции замедлится в 8 раз.
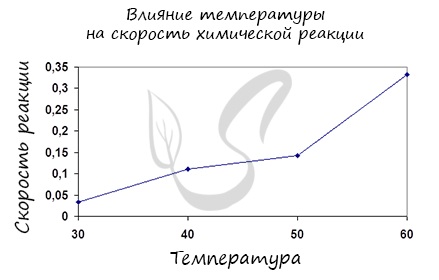
Влияние изменения температуры на скорость реакции
Постулат, который рекомендую временно взять на вооружение: «Увеличение температуры увеличивает скорость абсолютно любой химической реакции: как экзотермической, так и эндотермической. Исключений нет!»
Правило Вант-Гоффа, голландского химика, позволяет точно оценить влияние температуры на скорость химической реакции. Оно звучит так: «При повышении температуры на каждые 10 градусов константа скорости гомогенной элементарной реакции увеличивается в два — четыре раза»
Если по итогам решения задач у вас получится температурный коэффициент меньше 2 или больше 4, то, скорее всего, где-то вы допустили ошибку. Используйте этот факт для самопроверки.
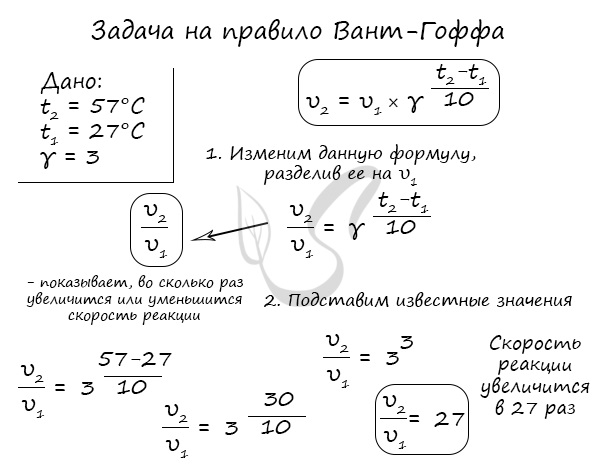
Для тренировки решим пару задач, в которых потребуется использование правило Вант-Гоффа.
Как изменится скорость гомогенной реакции при повышении температуры от 27°C до 57°C при температурном коэффициенте, равном трем?
Иногда в задачах требуется рассчитать температурный коэффициент, как, например, здесь: «Рассчитайте, чему равен температурный коэффициент скорости, если известно, что при понижении температуры от 250°C до 220°C скорость реакции уменьшилась в 8 раз».
Катализаторы и ингибиторы
Ингибиторы применяют для замедления коррозии металла, окисления топлива, старения полимеров. Многие лекарственные вещества являются ингибиторами.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Блиц-опрос по теме Скорость химической реакции
Что называют скоростью химической реакции приведите примеры реакций протекающих с высокой и низкой
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
Задание 1
Что называется скоростью химической реакции? Скоростью химической реакции называют изменение концентрации вещества в единицу времени.
Приведите примеры реакций, протекающих с высокой и низкой скоростями.
Реакции горения протекают с высокой скоростью, а реакции окисления, например, меди и серебра на воздухе ― с низкой скоростью.
С + O2 = CO2 Реакция протекает быстро.
Ag+ O2 = Ag2O Реакция протекает медленно.
2Cu+ O2 = 2CuO Реакция протекает медленно.
Дополнительное задание
Найдите в Интернете видео опыта каталитической реакции. Запишите уравнение реакции, укажите, какой катализатор был использован для ее проведения. Оксид марганца (IV) MnO 2
2H2O2 MnO₂ ⟶ 2H2O + O2 ↑
Урок 5. Скорость химической реакции
Зависимость скорости химической реакции от различных факторов
Понятие «скорость» довольно часто встречается в литературе. Из физики известно, что чем большее расстояние преодолеет материальное тело (человек, поезд, космический корабль) за определённый отрезок времени, тем выше скорость этого тела.
А как измерить скорость химической реакции, которая никуда «не идёт» и никакое расстояние не преодолевает? Для того чтобы ответить на этот вопрос, следует выяснить, а что всегда меняется в любой химической реакции? Поскольку любая химическая реакция — это процесс изменения вещества, то исходное вещество в ней исчезает, превращаясь в продукты реакции. Таким образом, в ходе химической реакции всегда изменяется количество вещества, уменьшается число частиц исходных веществ, а значит, и его концентрация (С).
Задание ЕГЭ. Скорость химической реакции пропорциональна изменению:
А теперь сравните свой ответ с правильным:
скорость химической реакции равна изменению концентрации реагирующего вещества в единицу времени
где С1 и С0 — концентрации реагирующих веществ, конечная и начальная, соответственно; t1 и t2 — время эксперимента, конечный и начальный отрезок времени, соответственно.
Поскольку реагирующие вещества всегда расходуются в данной реакции, то
Таким образом, отношение этих величин всегда отрицательно, а скорость не может быть величиной отрицательной. Поэтому в формуле появляется знак «минус», который одновременно говорит о том, что скорость любой реакции с течением времени (при неизменных условиях) всегда уменьшается.
Итак, скорость химической реакции равна:
Возникает вопрос, в каких единицах следует измерять концентрацию реагирующих веществ (С) и почему? Для того чтобы ответить на него, нужно понять, какое условие является главным для протекания любой химической реакции.
Для того чтобы частицы прореагировали, необходимо, чтобы они, как минимум, столкнулись. Поэтому чем выше число частиц* (число молей) в единице объёма, тем чаще они сталкиваются, тем выше вероятность химической реакции.
* О том, что такое «моль», читай в уроке 29.1.
Поэтому при измерении скоростей химических процессов используют молярную концентрацию веществ в реагирующих смесях.
Молярная концентрация вещества показывает, сколько молей его содержится в 1 литре раствора
Итак, чем больше молярная концентрация реагирующих веществ, тем больше частиц в единице объёма, тем чаще они сталкиваются, тем выше (при прочих равных условиях) скорость химической реакции. Поэтому основным законом химической кинетики (это наука о скорости химических реакций) является закон действующих масс.
Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ.
Для реакции типа А + В →… математически этот закон можно выразить так:
Если реакция более сложная, например, 2A + B → или, что тоже самое А + А + В → …, то
Таким образом, в уравнении скорости появился показатель степени «два», который соответствует коэффициенту 2 в уравнении реакции. Для более сложных уравнений большие показатели степеней, как правило, не используют. Это связано с тем, что вероятность одновременного столкновения, скажем, трёх молекул А и двух молекул В крайне мала. Поэтому многие реакции протекают в несколько стадий, в ходе которых сталкивается не более трёх частиц, и каждая стадия процесса протекает с определённой скоростью. Эту скорость и кинетическое уравнение скорости для неё определяют экспериментально.
Вышеприведённые уравнения скорости химической реакции (3) или (4) справедливы только для гомогенных реакций, т. е. для таких реакций, когда реагирующие вещества не разделяет поверхность. Например, реакция происходит в водном растворе, и оба реагирующих вещества хорошо растворимы в воде или для любой смеси газов.
Другое дело, когда происходит гетерогенная реакция. В этом случае между реагирующими веществами имеется поверхность раздела, например, углекислый газ реагирует с водным раствором щёлочи. В этом случае любая молекула газа с равной вероятностью может вступить в реакцию, поскольку эти молекулы быстро и хаотично двигаются. А частицы жидкого раствора? Эти частицы двигаются чрезвычайно медленно, и те частицы щёлочи, которые находятся «на дне», практически не имеют шансов вступить в реакцию с углекислым газом, если раствор не перемешивать постоянно. Реагировать будут только те частицы, которые «лежат на поверхности». Значит, для гетерогенных реакций —
скорость реакции зависит от величины площади поверхности раздела, которая увеличивается при измельчении.
Поэтому очень часто реагирующие вещества измельчают (например, растворяют в воде), пищу тщательно пережёвывают, а в процессе приготовления — растирают, пропускают через мясорубку и т. д. Не измельчённый пищевой продукт практически не усваивается!
Таким образом, с максимальной скоростью (при прочих равных условиях) протекают гомогенные реакции в растворах и между газами, (если эти газы реагируют при н. у.), причём в растворах, где молекулы располагаются «рядом», а измельчение такое же, как в газах (и даже больше!), — скорость реакции выше.
Задание ЕГЭ. Какая из реакций протекает с наибольшей скоростью при комнатной температуре:
В данном случае нужно найти, какой процесс является гомогенным.
Следует отметить, что скорость химической реакции между газами или гетерогенной реакции, в которой участвует газ, зависит и от давления, поскольку при увеличении давления газы сжимаются, и концентрация частиц увеличивается (см. формулу 2). На скорость реакций, в которых газы не участвуют, изменение давления влияния не оказывает.
Задание ЕГЭ. На скорость химической реакции между раствором кислоты и железом не оказывает влияния
И наконец, скорость реакции зависит и от реакционной способности веществ. Например, если с веществом реагирует кислород, то при прочих равных условиях, скорость реакции будет выше, чем при взаимодействии этого же вещества с азотом. Дело в том, что реакционная способность кислорода заметно выше, чем у азота. Причину этого явления мы рассмотрим в следующей части Самоучителя (урок 14).
Задание ЕГЭ. С большей скоростью идёт химическая реакция между соляной кислотой и
Вопрос. Как вы полагаете, почему скорость реакции так резко возрастает при нагревании?
Скорость реакции возрастает потому, что, во-первых, увеличивается число столкновений частиц, а во-вторых, увеличивается число активных столкновений. Именно активные соударения частиц приводят к их взаимодействию. Для того чтобы произошло такое соударение, частицы должны обладать определённым запасом энергии.
Энергия, которой должны обладать частицы, для того чтобы произошла химическая реакция, называется энергией активации.
Эта энергия расходуется на преодоление сил отталкивания между внешними электронами атомов и молекул и на разрушение «старых» химических связей.
Возникает вопрос: как повысить энергию реагирующих частиц? Ответ простой — повысить температуру, поскольку при повышении температуры возрастает скорость движения частиц, а, следовательно, их кинетическая энергия.
при повышении температуры на каждые 10 градусов скорость реакции возрастает в 2–4 раза.
ВАНТ-ГОФФ Якоб Хендрик (30.08.1852–1.03.1911) — голландский химик. Один из основателей физической химии и стереохимии. Нобелевская премия по химии № 1 (1901).
Следует заметить, что это правило (не закон!) было установлено экспериментально для реакций, «удобных» для измерения, то есть для таких реакций, которые протекали не слишком быстро и не слишком медленно и при температурах, доступных экспериментатору (не слишком высоких и не слишком низких).
Вопрос. Как вы полагаете, как можно быстрее приготовить картофель: отварить его или обжарить в слое масла?
Если мы хотим сохранить пищевые продукты, — мы их охлаждаем или замораживаем.
Для того чтобы как следует уяснить себе смысл описываемых явлений, можно сравнить реагирующие молекулы с группой учеников, которым предстоит прыгать в высоту. Если им поставлен барьер высотой 1 м, то ученикам придётся как следует разбежаться (повысить свою «температуру»), чтобы преодолеть барьер. Тем не менее всегда найдутся ученики («неактивные молекулы»), которые взять этот барьер не смогут.
Что делать? Если придерживаться принципа: «Умный в гору не пойдёт, умный гору обойдёт», то следует просто опустить барьер, скажем, до 40 см. Тогда любой ученик сможет преодолеть барьер. На молекулярном уровне это означает: для того чтобы увеличить скорость реакции, нужно уменьшить энергию активации в данной системе.
В реальных химических процессах эту функцию выполняет катализатор.
Катализатор — это вещество, которое изменяет скорость химической реакции, оставаясь при этом неизменным к концу химической реакции.
Катализатор участвует в химической реакции, взаимодействуя с одним или несколькими исходными веществами. При этом образуются промежуточные соединения, и изменяется энергия активации. Если промежуточное соединение более активно (активный комплекс), то энергия активации понижается, а скорость реакции увеличивается.
Например, реакция между SO2 и О2 происходит очень медленно, при нормальных условиях практически не идёт. Но в присутствии NO скорость реакции резко возрастает. Сначала NO очень быстро реагирует с O2:
полученный диоксид азота быстро реагирует с оксидом серы (IV):
Задание 5.1. Покажите на этом примере, какое вещество является катализатором, а какое — активным комплексом.
И наоборот, если образуются более пассивные соединения, то энергия активации может возрасти настолько, что реакция при данных условиях практически происходить не будет. Такие катализаторы называются ингибиторами.
На практике применяются оба типа катализаторов. Так особые органические катализаторы — ферменты — участвуют абсолютно во всех биохимических процессах: переваривании пищи, сокращении мышц, дыхании. Без ферментов невозможно существование жизни!
Ингибиторы необходимы для того, чтобы защитить металлические изделия от коррозии, жиросодержащие пищевые продукты от окисления (прогоркания). Некоторые лекарства также содержат ингибиторы, которые угнетают жизненные функции микроорганизмов и тем самым уничтожают их.
Катализ может быть гомогенным и гетерогенным. Примером гомогенного катализа служит действие NO (это катализатор) на процесс окисления диоксида серы. Примером гетерогенного катализа может служить действие нагретой меди на спирт:
Эта реакция идёт в две стадии:
Задание 5.2. Определите, какое вещество в этом случае является катализатором? Почему этот вид катализа называется гетерогенным?
На практике чаще всего используется гетерогенный катализ, где катализаторами служат твёрдые вещества: металлы, их оксиды и др. На поверхности этих веществ имеются особые точки (узлы кристаллической решётки), где, собственно и происходит каталитическая реакция. Если эти точки закрыть посторонними веществом, то катализ прекращается. Это вещество, губительное для катализатора, называется каталитическим ядом. Другие вещества — промоторы — наоборот, усиливают каталитическую активность.
Катализатор может изменить направление химической реакции, то есть, меняя катализатор, можно получать разные продукты реакции. Так, из спирта C2H5OH в присутствии оксидов цинка и алюминия можно получить бутадиен, а в присутствии концентрированной серной кислоты — этилен.
Таким образом, в ходе химической реакции изменяется энергия системы. Если в ходе реакции энергия выделяется в виде теплоты Q, такой процесс называется экзотермическим:
Для эндотермических процессов теплота поглощается, т. е. тепловой эффект Q Обратимость химических процессов. Принцип Ле-Шателье
* ЛЕ ШАТЕЛЬЕ Анри Луи (8.10.1850–17.09.1936) — французский физико-химик и металловед. Сформулировал общий закон смещения равновесия (1884).
Реакции бывают обратимыми и необратимыми.
Необратимыми называют такие реакции, для которых не существует условий, при которых возможен обратный процесс.
Примером таких реакций могут служить реакции, которые происходят при скисании молока, или когда сгорела вкусная котлета. Как невозможно пропустить мясной фарш назад через мясорубку (и получить снова кусок мяса), также невозможно «реанимировать» котлету или сделать свежим молоко.
Но зададим себе простой вопрос: является ли необратимым процесс:
Для того чтобы ответить на этот вопрос, попробуем вспомнить, можно ли осуществить обратный процесс? Да! Разложение известняка (мела) с целью получить негашёную известь СаО используется в промышленном масштабе:
Таким образом реакция является обратимой, так как существуют условия, при которых с ощутимой скоростью протекают оба процесса:
Более того, существуют условия, при которых скорость прямой реакции равна скорости обратной реакции.
В этих условиях устанавливается химическое равновесие. В это время реакция не прекращается, но число полученных частиц равно числу разложившихся частиц. Поэтому в состоянии химического равновесия концентрации реагирующих частиц не изменяются. Например, для нашего процесса в момент химического равновесия
знак [ ] означает равновесная концентрация.
Возникает вопрос, что произойдёт с равновесием, если повысить или понизить температуру, изменить другие условия? Ответить на подобный вопрос можно, зная принцип Ле-Шателье:
если изменить условия (t, p, c), при которых система находится в состоянии равновесия, то равновесие сместится в сторону того процесса, который противодействует изменению.
Другими словами, равновесная система всегда противится любому воздействию извне, как противится воле родителей капризный ребёнок, который делает «всё наоборот».
Рассмотрим пример. Пусть установилось равновесие в реакции получения аммиака:
Вопросы. Одинаково ли число молей реагирующих газов до и после реакции? Если реакция идёт в замкнутом объёме, когда давление больше: до или после реакции?
Очевидно, что данный процесс происходит с уменьшением числа молекул газов, значит, давление в ходе прямой реакции уменьшается. В обратной реакции — наоборот, давление в смеси увеличивается.
Зададим себе вопрос, что произойдёт, если в этой системе повысить давление? По принципу Ле-Шателье пойдёт та реакция, которая «делает наоборот», т. е. понижает давление. Это — прямая реакция: меньше молекул газа — меньше давление.
Итак, при повышении давления равновесие смещается в сторону прямого процесса, где давление понижается, так как уменьшается число молекул газов.
Задание ЕГЭ. При повышении давления равновесие смещается вправо в системе:
Если в результате реакции число молекул газов не меняется, то изменение давления на положение равновесия не оказывает влияние.
Задание ЕГЭ. Изменение давления оказывает влияние на смещение равновесия в системе:
Положение равновесия этой и любой другой реакции зависит от концентрации реагирующих веществ: увеличивая концентрацию исходных веществ и уменьшая концентрацию полученных веществ, мы всегда смещаем равновесие в сторону прямой реакции (вправо).
Задание ЕГЭ. Химическое равновесие в системе
сместится влево при:
Процесс синтеза аммиака экзотермичен, то есть сопровождается выделением теплоты, то есть повышением температуры в смеси.
Вопрос. Как сместится равновесие в этой системе при понижении температуры?
Рассуждая аналогично, делаем вывод: при понижении температуры равновесие сместится в сторону образования аммиака, так как в этой реакции теплота выделяется, а температура повышается.
Вопрос. Как изменится скорость химической реакции при понижении температуры?
Очевидно, что при понижении температуры резко понизится скорость обеих реакций, т. е. придётся очень долго ждать, когда же установится желаемое равновесие. Что делать? В этом случае необходим катализатор. Он хотя и не влияет на положение равновесия, но ускоряет наступление этого состояния.
Задание ЕГЭ. Химическое равновесие в системе
смещается в сторону образования продукта реакции при:
Выводы
Скорость химической реакции зависит от:
Равновесие устанавливается, когда скорость прямой реакции равна скорости обратного процесса. В этом случае равновесная концентрация реагирующих веществ не меняется. Состояние химического равновесия зависит от условий и подчиняется принципу Ле-Шателье.