Что называют активированным комплексом
Активированный комплекс
Полезное
Смотреть что такое «Активированный комплекс» в других словарях:
АКТИВИРОВАННЫЙ КОМПЛЕКС — в химии то же, что переходное состояние … Большой Энциклопедический словарь
активированный комплекс — (хим.), то же, что переходное состояние. * * * АКТИВИРОВАННЫЙ КОМПЛЕКС АКТИВИРОВАННЫЙ КОМПЛЕКС, в химии то же, что переходное состояние (см. ПЕРЕХОДНОЕ СОСТОЯНИЕ) … Энциклопедический словарь
активированный комплекс — aktyvintasis kompleksas statusas T sritis chemija apibrėžtis Nepatvarus, iš reaguojančiųjų medžiagų susidarantis ir skylantis į reakcijos produktus kompleksas. atitikmenys: angl. activated complex rus. активированный комплекс … Chemijos terminų aiškinamasis žodynas
АКТИВИРОВАННЫЙ КОМПЛЕКС — (хим.), то же, что переходное состояние … Естествознание. Энциклопедический словарь
активированный комплекс — см. переходное состояние … Химические термины
Комплекс стимуляции анафазы — Комплекс стимуляции анафазы[1] Комплекс, стимулирующий анафазу (англ. … Википедия
Комплекс SCF — Схема комплекса SCF Комплекс SCF (аббревиатура слагается из начальных букв трёх субъединиц комплекса: Skp1, Cul1, F box) белковое соединение, играющее существенную роль в регуляции … Википедия
Активный комплекс — в химии, то же, что Активированный комплекс … Большая советская энциклопедия
Уман Комплекс Д.И. — Уман Комплекс Д.И. Действующее вещество ›› Фактор IX комплекс (Factor IX complex) Латинское название Uman Complex D.I. АТХ: ›› B02BD Факторы свертывания крови Фармакологическая группа: Коагулянты (в т.ч. факторы свертывания крови), гемостатики… … Словарь медицинских препаратов
ПЕРЕХОДНОЕ СОСТОЯНИЕ — (активированный комплекс), конфигурация системы атомных ядер и электронов, участвующих в элементарном акте хим. реакции, в момент преодоления системой энергетич. барьера, разделяющего её начальное и конечное состояния. Теорию П. с. применяют для… … Естествознание. Энциклопедический словарь
Большая советская энциклопедия (БСЭ)
Активированный комплекс
Протекание элементарного акта может быть рассмотрено на примере газовой бимолекулярной реакции (См. Бимолекулярные реакции) образования йодистого водорода из водорода и паров иода:
Как показывает квантовомеханическая теория, при сближении молекул H2 и I2 на расстояние, сравнимое с молекулярными размерами, они отталкиваются друг от друга с силой, быстро растущей при уменьшении расстояния. Подавляющее большинство столкновений молекул H2 и I2 в газовой смеси не приводит к реакции, потому что энергия теплового движения молекул оказывается недостаточной для преодоления отталкивания. У некоторой, весьма малой, доли молекул интенсивность теплового движения случайно много больше средней; этим создаётся возможность настолько тесного сближения молекул H2 и I2, что возникают новые химические связи между атомами Н и I, а существовавшие прежде химические связи Н-Н и I-I разрываются. Две образовавшиеся молекулы HI отталкиваются друг от друга и поэтому расходятся, чем завершается элементарный акт реакции. Переход от расположения связей 

расположение атомов в А. к. будет таким же, как и для прямой реакции (1), но направления движения атомов в активированных комплексах реакций (1) и (2) взаимно противоположны.
Энергетические соотношения при элементарном акте реакции можно схематически представить с помощью графика, на котором потенциальная энергия реагирующей системы U изображена как функция т. н. реакционной координаты х, описывающей взаимное расположение атомов.
Поскольку интервал Δх мал, то и с+ и τ пропорциональны Δх, так что их отношение не зависит от значения произвольно выбранной величины Δх. Величины с+ и τ вычисляются методами статистической механики, при этом используют ряд упрощающих предположений, из которых главным является допущение, что протекание реакции не нарушает статистически равновесное распределение молекул по состояниям.
Исходные понятия метода А. к. были разъяснены выше на примере гомогенной газовой реакции, но метод применяют и к скоростям реакций в растворах, гетерогенно-каталитических реакций и вообще к вычислению скоростей во всех случаях, когда превращение связано с необходимостью случайного концентрирования энергии теплового движения в количестве, значительно превышающем среднюю энергию молекул при данной температуре.
Сопоставление теории абсолютных скоростей реакций с опытными данными, как и теоретический анализ её предпосылок, показывает, что эта теория, будучи не вполне точной, вместе с тем является удачным приближением, ценным своей простотой.
Лит.: Глесстон С., Лейдлер К., Эйринг Г., Теория абсолютных скоростей реакции, пер. с англ., М., 1948.
Теория активированного комплекса
Теория активированного комплекса или переходного состояния основана на том, что элементарный акт взаимодействия молекул состоит в постепенной перестройке химических связей, при котором начальная конфигурация атомов в исходных молекулах переходит в конечную у продуктов реакции при непрерывном изменении межатомных расстояний.
Количественную теорию, основанную на этих представлениях, с использованием математического аппарата статистической термодинамики, так называемую теорию абсолютных скоростей реакций, предложили Г.Эйринг и М. Поляни и (1935).
Рассмотрим механизм реакцию
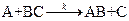
Согласно теории активированного комплекса при сближении атома А с молекулой ВС ослабляется связь В—С и возникает связь А—В. Процесс завершается образованием молекулы АВ и атома С, для чего система должна пройти через активированный комплекс АВС 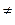
Качественные представления об элементарном акте как о сложном процессе перестройки химических связей при сближении молекул, а также представления о поверхности потенциальной энергии и координате реакции называют теорией активированного комплекса или переходного состояния.
Строгая количественная теория, основанная на этой физической модели механизма элементарного акта, должна состоять в теоретическом расчете энергетической поверхности реакции методами квантовой механики и в теоретической оценке на этой основе энергии активации и предэкспоненциального множителя. Сделать это пока не удается, из-за математических трудностей. Поэтому пользуются приближенной математической моделью, так называемой теорией абсолютных скоростей реакций.
Согласно этой теории, скорость любой химической реакции равна скорости перехода активированного комплекса через потенциальный барьер, т.е. скорости распада активированного комплекса в продукты реакции. При этом молекула активированного комплекса проходит путь d (рис. 8).
При выводе выражения для константы скорости в теории активированного комплекса элементарную реакцию рассматривают как одномерное поступательное движение по координате реакции в направлении продуктов реакции. При этом сделаны следующие длпущения:
1. В ходе химической реакции на вершине потенциального барьера образуется активированный комплекс ( 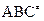
2. Активированный комплекс на участке 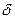
3. Движение по пути реакции может быть описано в терминах классической механики без учета квантовых эффектов.
4. Элементарная реакция происходит адиабатически, то есть без перехода на другую поверхность потенциальной энергии.
Таким образом, активированный комплекс рассматривается как обычная молекула, у которой одна колебательная степень свободы заменена на поступательную в направлении продуктов реакции.
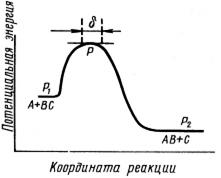 Рис. 8. Путь процесса на основе модели актвированного комплекса. d – область существования активированного комплекса Рис. 8. Путь процесса на основе модели актвированного комплекса. d – область существования активированного комплекса |
Процесс перехода активированного комплекса в продукты реакции – реакция первого порядка.
Основным уравнением теории абсолютных скоростей реакции (без вывода) является уравнение, связывающее константу скорости реакции со свойствами переходного состояния через суммы по состояниям:
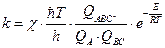
где 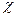
Предполагается, что химическая реакция протекает без нарушения равновесного распределения молекул реагентов по энергиям, а между реагентами и активированным комплексом существует динамическое равновесие, поэтому концентрацию активированных комплексов можно выразить через термодинамическую константу равновесия.
Если ввести обозначение:
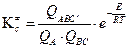
то наиболее общее уравнение теории абсолютных скоростей реакции можно записать:
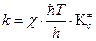
где 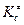
В зависимости от того, как рассчитывают константу равновесия, различают статистический(4.217) и термодинамический (4.218) аспекты теории активированного комплекса.
Что значит «активированный комплекс»
Энциклопедический словарь, 1998 г.
Большая Советская Энциклопедия
группировка атомов в решающий момент элементарного акта химической реакции. Понятием об А. к. широко пользуются в теории скоростей химических реакций. Протекание элементарного акта может быть рассмотрено на примере газовой бимолекулярной реакции образования йодистого водорода из водорода и паров иода: H2+I2 = 2HI═════════════════(
Как показывает квантовомеханическая теория, при сближении молекул H2 и I2 на расстояние, сравнимое с молекулярными размерами, они отталкиваются друг от друга с силой, быстро растущей при уменьшении расстояния. Подавляющее большинство столкновений молекул H2 и I2 в газовой смеси не приводит к реакции, потому что энергия теплового движения молекул оказывается недостаточной для преодоления отталкивания. У некоторой, весьма малой, доли молекул интенсивность теплового движения случайно много больше средней; этим создаётся возможность настолько тесного сближения молекул H2 и I2, что возникают новые химические связи между атомами Н и I, а существовавшие прежде химические связи Н≈Н и I≈I разрываются. Две образовавшиеся молекулы HI отталкиваются друг от друга и поэтому расходятся, чем завершается элементарный акт реакции. Переход от расположения связей ═к расположению ═происходит не внезапно, а постепенно: по мере сближения молекул H2 и I2 связи Н≈Н и I≈I ослабевают и одновременно усиливаются связи Н≈I. Отталкивание Н≈Н от I≈I сменяется отталкиванием Н≈I от Н≈I в момент, когда новое расположение связей начинает превалировать над старым. Таким образом, в ходе элементарного акта возникает конфигурация атомов, являющаяся критической в том смысле, что если она достигнута, то дальнейшее движение атомов происходит беспрепятственно, не требуя запаса энергии. Совокупность атомов в этой конфигурации и называется «активированным комплексом» (Г. Эйринг, США, 1935) или «переходным состоянием» (М. Г. Эванс и М. Поляни, Англия, 1935). Для обратной реакции
расположение атомов в А. к. будет таким же, как и для прямой реакции (1), но направления движения атомов в активированных комплексах реакций (1) и (2) взаимно противоположны.
Энергетические соотношения при элементарном акте реакции можно схематически представить с помощью графика, на котором потенциальная энергия реагирующей системы U изображена как функция т. н. реакционной координаты х, описывающей взаимное расположение атомов.
Задавшись некоторым весьма малым интервалом Dх (рис.) и считая, что конфигурация атомов отвечает А. к., если координата х имеет значение, лежащее в пределах этого интервала, можно ввести понятия ≈ концентрация активированных комплексов прямой реакции в данной реагирующей системе с+ и их время жизни t. За время t в единице объёма происходит с+ актов прямой реакции. Т. к. скорость прямой реакции r+. есть число соответствующих актов реакции в единице объёма в единицу времени, то
Поскольку интервал Dх мал, то и с+ и t пропорциональны Dх, так что их отношение не зависит от значения произвольно выбранной величины Dх. Величины с+и t вычисляются методами статистической механики, при этом используют ряд упрощающих предположений, из которых главным является допущение, что протекание реакции не нарушает статистически равновесное распределение молекул по состояниям.
Уравнение (3) выражает основную идею теоретической трактовки скоростей реакций на основе концепции А. к. Оно не только позволяет судить о зависимости скорости реакции от концентраций веществ ≈ участников реакции, от температуры и др. факторов, но устанавливает абсолютное значение скорости. Поэтому метод А. к. часто называют теорией абсолютных скоростей реакций. В некоторых сравнительно немногочисленных реакциях перестройка химических связей происходит затрудненно, так что достижение конфигурации А. к. ещё не гарантирует осуществление акта реакции. Чтобы учесть существование таких реакций, называемых неадиабатными, в правую часть равенства (3) вводят добавочный множитель, «коэффициент прохождения» или «трансмиссионный коэффициент»; в случае неадиабатных реакций он много меньше единицы.
Исходные понятия метода А. к. были разъяснены выше на примере гомогенной газовой реакции, но метод применяют и к скоростям реакций в растворах, гетерогенно-каталитических реакций и вообще к вычислению скоростей во всех случаях, когда превращение связано с необходимостью случайного концентрирования энергии теплового движения в количестве, значительно превышающем среднюю энергию молекул при данной температуре.
Сопоставление теории абсолютных скоростей реакций с опытными данными, как и теоретический анализ её предпосылок, показывает, что эта теория, будучи не вполне точной, вместе с тем является удачным приближением, ценным своей простотой.
Лит.: Глесстон С., Лейдлер К., Эйринг Г., Теория абсолютных скоростей реакции, пер. с англ., М., 1948.
Транслитерация: aktivirovannyiy kompleks
Задом наперед читается как: скелпмок йыннаворивитка
Активированный комплекс состоит из 22 букв
Понятие о теории активированного комплекса (переходного состояния)
Влияние температуры на скорость химической реакции
Скорость химической реакции увеличивается с повышением температуры. Приблизительно оценить влияние температуры на скорость реакции можно по правилу Вант-Гоффа:
при повышении температуры на каждые 10 градусов скорость реакции увеличивается в 2 ¸ 4 раза.

Для биологических процессов важен определенный температурный интервал, вне которого процесс прекращается. В этом интервале увеличение температуры активизирует протекание жизненно важных процессов до оптимального, а последующее повышение температуры быстро снижает скорость процесса вплоть до прекращения жизнедеятельности организма. Это связано с необратимой тепловой денатурацией белков биологических тканей, а также с инактивацией ферментов (биологических катализаторов).
Более точно зависимость скорости реакции от температуры выражается уравнением Аррениуса. Уравнение Аррениуса в дифференциальной форме:
где kск константа скорости реакции
R – универсальная газовая постоянная: R=8,314 Дж/моль∙К
Энергия активации — та избыточная энергия (по сравнению со средней энергией молекул), которой должны обладать сталкивающиеся молекулы, чтобы быть способными к химической реакции (рис.)
Активация вызывается повышением температуры, действием электрического поля, действием квантов света и т.д. Энергия активации Еа постоянна в данном температурном интервале и определяется механизмом реакции.

Теоретические представления о механизме химических реакций.
Понятие о теории активных соударений.
Для того чтобы произошла химическая реакция, необходимо, чтобы частицы столкнулись. Скорость реакции пропорциональна общему числу двойных столкновений в единицу времени в единице объема
где q – коэффициент пропорциональности.
В теории соударений используются следующие допущения:
1. Частицы бесструктурны – это шары с радиусом r;
2. В момент соударения молекулы ведут себя как упругие шары. Т.е. суммарная энергия молекул до и после соударения остается постоянной, но может перераспределяться между молекулами.
3. Реагируют только молекулы, которые обладают энергией активации.
4. Число двойных активных столкновений определяется соотношением:

где zобщ – общее число столкновений,
zакт – число активных столкновений,


5. Процесс превращения исходных веществ в продукты происходит мгновенно в момент соударения активных молекул.
6. Скорость реакции А+В=С
Роль стерического фактора:
Стерический фактор характеризует вероятность реакции между молекулами, энергия которых 

откуда предэкспоненциальный множитель А=Рz0.
Недостатки теории активных соударений.
1) бесструктурность частиц – они рассматриваются как шары
2) элементарный акт рассматривается как мгновенный, в действительности это сложный процесс перераспределения связей, требующий определенного времени.
Теория активных соударений объясняет много разнообразных факторов, но не объясняет влияния на скорость реакции растворителя, давления, добавок инертных газов, не позволяет сделать теоретическую оценку стерического фактора.
Понятие о теории активированного комплекса (переходного состояния)
Теория основывается на квантовых представлениях о строении молекул и химической связи. Она должна решить следующие задачи:
1) рассмотреть энергетику взаимодействия реагирующих частиц с целью определения энергии активации;
2) рассчитать константы скорости химической реакции при известной энергии активации.
Рассмотрим бимолекулярную реакцию
Считается, что частицы уже активированы, т.е. рассматриваем сам элементарный акт реакции, происходящий во времени.
При сближении активированных молекул взаимодействие между ними начинается еще до столкновения – старая связь ослабевает, но еще не разрушена, при этом одновременно образуется новая связь. Таким образом, образуется трехатомный конгломерат (активированный комплекс), который находится в равновесии с исходными веществами и затем распадается на продукты.
Активированный комплекс устойчив во всех направлениях, кроме пути реакции. Т.е. активированный комплекс может распасться только на продукты реакции.
Путь или координата реакции – это взаимосвязанное изменение совокупности межъядерных расстояний при переходе от начальной конфигурации атомов к конечной, сопровождающееся минимальным изменением потенциальной энергии. Сечение поверхности потенциальной энергии вдоль пути реакции называется профилем пути реакции
Из хода кривой видно, что в процессе элементарного акта химического превращения система должна преодолеть потенциальный барьер, равный энергии активации. Истинная энергия активации 

Для определения 
Расчет константы скорости элементарной реакции при заданной энергии активации основан на постулатах:
1. Распределение молекул по энергиям и скоростям подчиняется распределению Максвелла-Больцмана. Превращение активных комплексов в продукты реакции не нарушает этого распределения, т.е. доля активных частиц в ходе реакции не изменяется, и поэтому концентрацию активных комплексов можно вычислить из распределения Максвелла-Больцмана.
2. Реакция протекает адиабатически. Адиабатическое приближение состоит в том, что система взаимодействующих атомов делится на две подсистемы – медленную подсистему ядер и быструю подсистему электронов, которая успевает быстро, безынерционно перестроиться при изменении конфигурации ядер. Поэтому можно рассматривать только одну поверхность потенциальной энергии для ядер, которые и должны преодолеть энергетический барьер в ходе реакции.
3. Активированный комплекс находится в равновесии с исходными веществами
Активированный комплекс существует не при определенном значении межъядерных расстояний, а в каком-то интервале δ, следовательно, время жизни комплекса
Серьезным недостатком теории переходного состояния является отсутствие экспериментальных данных о строении активированного комплекса, что затрудняет ее применение. Несмотря на это, благодаря сравнительной простоте математического аппарата она является наиболее широко используемой теорией кинетики элементарных химических реакций, позволяет правильно объяснить и полуколичественно предсказать много закономерностей для кинетики химических реакций.
Катализ
Явление катализа – это изменение скорости реакции под действием некоторых веществ, которые к концу реакции остаются в химически неизменном виде.
1) положительный – под действием некоторых веществ скорость реакции увеличивается;
2) отрицательный: под действием некоторых веществ скорость реакции уменьшается, такие вещества называются ингибиторами;
3) автокатализ: катализатором являются продукты реакции;
4) гомогенный: катализатор и реагенты находятся в одной фазе (газ или раствор);
5) гетерогенный: катализатор и реагенты находятся в разных фазах;
6) ферментативный: катализатором является биологический фермент.
1) катализатор принимает участие в химической реакции, образуя промежуточные продукты, но в конце реакции выделяется в химически неизменном виде. Физическое состояние катализатора, входящего в активный комплекс, может существенно изменяться, например, уменьшатся размеры зерен твердого катализатора, изменится структура поверхностных слоев;
2) катализатор не смещает положение равновесия, а лишь увеличивает скорость прямой и обратной реакции в равной степени;
3) действие катализатора является специфичным (селективным);
4) катализатор увеличивает скорость реакции за счет уменьшения Еакт, ведет реакцию по пути с меньшим энергетическим барьером.
Гомогенный катализ
Рассмотрим схему реакции, протекающей без катализатора:
В присутствии катализатора реакция протекает в несколько стадий:
1.
2.
3.
Это уравнение лежит в основе кинетики гомогенных каталитических реакций. Из уравнения видно, что скорость процесса прямо пропорциональна концентрации катализатора, исключение составляют лишь случаи, когда катализатор находится в большом избытке, в результате чего скорость процесса лимитируется не кинетическими, а физическими закономерностями, например, диффузией растворенного вещества к катализатору.
Энергетический профиль каталитической реакции представлен на рисунке 4.
Рис.4. Энергетические профили
реакций с катализатором и без него.
Е1 – энергия активации некаталитической реакции,
Е2 – каталитической реакции
В ранних исследованиях предполагалось, что поверхность катализатора энергетически однородна (Лэнгмюр). В дальнейшем была экспериментально доказана адсорбционная неоднородность поверхности. Возникло представление о том, что каталитически активны только определенные участки поверхности, на которых имеются адсорбционные центры. Здесь вещество способно образовать активное для протекания данного каталитического процесса промежуточное поверхностное соединения, благодаря чему понижается энергия активации реакции.
Гетерогенный катализ
В случае гетерогенного катализа реакции происходят на границе раздела фаз.
Гетерогенный катализ состоит из следующих стадий:
1. массоперенос реагентов к катализатору;
2. абсорбция – образование абсорбированного комплекса между реагентом и катализатором;
3. каталитическая реакция – образование продукта в основном адсорбированном состоянии;
4. десорбция продукта;
5. внутренний массоперенос (изнутри катализатора);
6. внешний массоперенос (из области реакции).
Общая скорость каталитической реакции определяется скоростью самой медленной из этих стадий. Если не рассматривать диффузию и считать, что равновесие «адсорбция ↔ десорбция» устанавливается быстро, то скорость каталитической реакции определяется скоростью реакции в адсорбционном слое, где роль реагента играют свободные адсорбционные центры. Простейший механизм гетерогенного катализа описывается схемой:

Для придания катализаторам большей избирательности, термической стойкости, механической прочности и активности их часто применяют в форме многокомпонентных систем: смешанных, на носителях, промотированных катализаторов.
Каталитические яды — это вещества, понижающие активность катализатора.
Активность катализаторов оценивают либо количеством вещества (в молях), реагирующих в единицу времени под воздействием единицы массы катализатора, или количеством вещества (в молях), реагирующих в единицу времени под воздействием единицы поверхности катализатора.
Ферментативный катализ
Ферментативными реакциями называются такие химические процессы в биологических системах, скорость которых регулируется веществами биологического происхождения. Это белковые молекулы, называемые ферментами или энзимами.
Ферментативный катализ играет огромную роль в жизнедеятельности организма. Широкое применение получили ферментные препараты при нарушениях функции желудочно-кишечного тракта, связанных с недостаточной выработкой пищеварительных ферментов (пепсин, панкреатин). При ожогах, гнойных ранах, гнойно-воспалительных заболеваниях легких, когда необходимо разрушить накопившиеся в большом количестве белковые образования, применяются протолитические ферменты, приводящие к быстрому гидролизу белков и способствующие рассасыванию гнойных скоплений. Для лечения инфекционных заболеваний используются препараты лизоцина, которые разрушают оболочку некоторых болезнетворных бактерий. Очень важные ферменты, которые рассасывают тромбы (сгустки крови внутри кровеносных сосудов) – плазмин, трипсин, химотрипсин, на их основе с разными добавками созданы различные лекарственные препараты – стрептокиназа, стрептаза, и т.п., широко применяемые в медицине.
Выделения ферментов в особый класс катализаторов обусловлен особыми свойствами этих веществ:
1) высокая специфичность;
2) эффективность действия;
3) биологические катализаторы образуются и разрушаются в процессе
жизнедеятельности организма.
По своей каталитической активности биологические катализаторы в тысячи раз превышают неорганические. Специфичность действия связана с особенностями структуры фермента и субстрата. Одни части каталитической системы выполняют функции, главным образом связанные с пространственной организацией системы, другие в этой организационной системе осуществляют собственно катализ. Т.е., как и при неферментативном катализе, в каталитической реакции участвует не вся белковая молекула в целом, а лишь определенные ее участки – активные центры фермента.
Простейшая схема ферментативного катализа включает обратимое образование промежуточного комплекса фермента (Е) с реагирующим веществом (субстратом S) и разрушение этого комплекса с образованием продуктов реакции (Р):

Течение химических реакций может быть заторможено присутствием некоторых веществ. Ингибиторы ферментативного катализа, способны образовывать комплексы с ферментом или фермент-субстратным комплексом.
Дата добавления: 2019-11-25 ; просмотров: 804 ; Мы поможем в написании вашей работы!