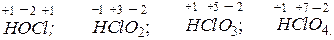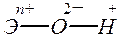Что называется сродством к электрону
Электронное сродство
Сродство к электрону выражают в килоджоулях на моль (кДж/моль) или в электронвольтах на атом (эВ/атом).
В отличие от ионизационного потенциала атома, имеющего всегда эндоэнергетическое значение, сродство атома к электрону описывается как экзоэнергетическими, так и эндоэнергетическими значениями (см. табл.).
| Элемент | ε | Элемент | ε | Элемент | ε |
|---|---|---|---|---|---|
| H | -0,75 | Na | -0,78 | K | -0,92 |
| He | 0,30 | Mg | 0,32 | Ca | 0,40 |
| Li | -0,58 | Al | -0,52 | Sc | 0,14 |
| Be | 0,19 | Si | -1,39 | Ti | -0,40 |
| B | -0,33 | P | -0,78 | V | -0,94 |
| C | -1,12 | S | -2,07 | Cr | -0,98 |
| N | 0,27 | Cl | -3,61 | Mn | 1,07 |
| О | -1,47 | Br | -3,36 | Fe | -0,58 |
| F | -3,45 | I | -3,06 | Co | -0,94 |
| Ne | 0,55 | Ni | -1,28 | ||
| Cu | -1,80 |
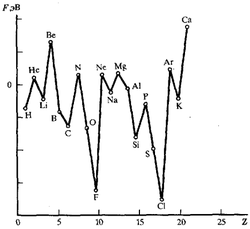
Наибольшим сродством к электрону обладают p-элементы VII группы. Наименьшее сродство к электрону у атомов с конфигурацией s 2 (Be, Mg, Zn) и s 2 p 6 (Ne, Ar) или с наполовину заполненными p-орбиталями (N, P, As):
| Li | Be | B | C | N | O | F | Ne | |
|---|---|---|---|---|---|---|---|---|
| Электронная конфигурация | s 1 | s 2 | s 2 p 1 | s 2 p 2 | s 2 p 3 | s 2 p 4 | s 2 p 5 | s 2 p 6 |
| ε, эВ | -0,59 | 0,19 | -0,30 | -1,27 | 0,21 | -1,47 | -3,45 | 0,22 |
Небольшие расхождения в цифрах между табл. 1 и табл. 2 обусловлены тем, что данные взяты из разных источников, а также погрешностью измерений.
Литература
Структурная химия
Полезное
Смотреть что такое «Электронное сродство» в других словарях:
ЭЛЕКТРОННОЕ СРОДСТВО — см. Сродство к электрону. Физическая энциклопедия. В 5 ти томах. М.: Советская энциклопедия. Главный редактор А. М. Прохоров. 1988 … Физическая энциклопедия
электронное сродство — elektroninis giminiškumas statusas T sritis Standartizacija ir metrologija apibrėžtis Dydis, proporcingas energijai, išsiskiriančiai atomui arba jonui prisijungus elektroną. atitikmenys: angl. electron affinity vok. Elektronenaffinität, f rus.… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
электронное сродство — elektroninis giminiškumas statusas T sritis Standartizacija ir metrologija apibrėžtis Energijų skirtumas tarp laisvojo elektrono begalybėje ir elektrono, esančio dielektriko ar puslaidininkio laidumo juostos žemiausiame lygmenyje. atitikmenys:… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
электронное сродство — elektroninis giminiškumas statusas T sritis fizika atitikmenys: angl. electron affinity vok. Elektronenaffinität, f rus. электронное сродство, n pranc. affinité électronique, f … Fizikos terminų žodynas
отрицательное электронное сродство — neigiamasis elektroninis giminiškumas statusas T sritis radioelektronika atitikmenys: angl. negative electron affinity vok. negative Elektronenaffinität, f rus. отрицательное сродство к электрону, n; отрицательное электронное сродство, n pranc.… … Radioelektronikos terminų žodynas
положительное электронное сродство — teigiamasis elektroninis giminiškumas statusas T sritis radioelektronika atitikmenys: angl. positive electron affinity vok. positive Elektronenaffinität, f rus. положительное сродство к электрону, n; положительное электронное сродство, n pranc.… … Radioelektronikos terminų žodynas
Сродство к электрону — электронное сродство, способность некоторых нейтральных атомов, молекул и радикалов свободных (См. Радикалы свободные) присоединять добавочные электроны, превращаясь в отрицательные Ионы. Мерой этой способности для частиц каждого… … Большая советская энциклопедия
сродство к электрону — elektroninis giminiškumas statusas T sritis Standartizacija ir metrologija apibrėžtis Dydis, proporcingas energijai, išsiskiriančiai atomui arba jonui prisijungus elektroną. atitikmenys: angl. electron affinity vok. Elektronenaffinität, f rus.… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
сродство к электрону — elektroninis giminiškumas statusas T sritis Standartizacija ir metrologija apibrėžtis Energijų skirtumas tarp laisvojo elektrono begalybėje ir elektrono, esančio dielektriko ar puslaidininkio laidumo juostos žemiausiame lygmenyje. atitikmenys:… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
отрицательное сродство к электрону — neigiamasis elektroninis giminiškumas statusas T sritis radioelektronika atitikmenys: angl. negative electron affinity vok. negative Elektronenaffinität, f rus. отрицательное сродство к электрону, n; отрицательное электронное сродство, n pranc.… … Radioelektronikos terminų žodynas
Энергия сродства к электрону
Эне́ргией сродства́ а́тома к электро́ну, или просто его сродством к электрону (ε), называют энергию, выделяющуюся в процессе присоединения электрона к свободному атому Э в его основном состоянии с превращением его в отрицательный ион Э − (сродство атома к электрону численно равно, но противоположно по знаку энергии ионизации соответствующего изолированного однозарядного аниона).
Сродство к электрону выражают в килоджоулях на моль (кДж/моль) или в электронвольтах на атом (эВ/атом).
В отличие от ионизационного потенциала атома, имеющего всегда эндоэнергетическое значение, сродство атома к электрону описывается как экзоэнергетическими, так и эндоэнергетическими значениями (см. табл.).
| Элемент | ε | Элемент | ε | Элемент | ε |
|---|---|---|---|---|---|
| H | -0,75 | Na | -0,78 | K | -0,92 |
| He | 0,30 | Mg | 0,32 | Ca | 0,40 |
| Li | -0,58 | Al | -0,52 | Sc | 0,14 |
| Be | 0,19 | Si | -1,39 | Ti | -0,40 |
| B | -0,33 | P | -0,78 | V | -0,94 |
| C | -1,12 | S | -2,07 | Cr | -0,98 |
| N | 0,27 | Cl | -3,61 | Mn | 1,07 |
| О | -1,47 | Br | -3,36 | Fe | -0,58 |
| F | -3,45 | I | -3,06 | Co | -0,94 |
| Ne | 0,55 | Ni | -1,28 | ||
| Cu | -1,80 |
Наибольшим сродством к электрону обладают p-элементы VII группы. Наименьшее сродство к электрону у атомов с конфигурацией s 2 (Be, Mg, Zn) и s 2 p 6 (Ne, Ar) или с наполовину заполненными p-орбиталями (N, P, As):
| Li | Be | B | C | N | O | F | Ne | |
|---|---|---|---|---|---|---|---|---|
| Электронная конфигурация | s 1 | s 2 | s 2 p 1 | s 2 p 2 | s 2 p 3 | s 2 p 4 | s 2 p 5 | s 2 p 6 |
| ε, эВ | -0,59 | 0,19 | -0,30 | -1,27 | 0,21 | -1,47 | -3,45 | 0,22 |
Небольшие расхождения в цифрах между табл. 1 и табл. 2 обусловлены тем, что данные взяты из разных источников, а также погрешностью измерений.
Литература
Полезное
Смотреть что такое «Энергия сродства к электрону» в других словарях:
энергия сродства к электрону — elektroninio giminiškumo energija statusas T sritis fizika atitikmenys: angl. energy of electron affinity vok. Energie der Elektronenaffinität, f rus. энергия сродства к электрону, f pranc. énergie d’affinité électronique, f … Fizikos terminų žodynas
ЭНЕРГИЯ СРОДСТВА — может быть либо атома или молекулы к электрону, либо анионов или молекул к протону. Наиболее важны Э. с. атома к электрону и анионов и молекул к протону. Обычно выражается в эв на единицу (атом, молекулу, ион) или ккал/г·атом. Э. с. атома к… … Геологическая энциклопедия
Энергия связи — (для данного состояния системы) разность между полной энергией связанного состояния системы тел или частиц и энергией состояния, в котором эти тела или частицы бесконечно удалены друг от друга и находятся в состоянии покоя: где … … Википедия
ЭНЕРГИЯ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ — энергия (U), затрачиваемая на разрыв кристаллической решетки на ее составляющие с переносом на расстояние отсутствия взаимодействия, взятая с обратным знаком. Если решетка ионная, то это энергия разрыва на соответствующие ионы, если атомная или… … Геологическая энциклопедия
сродство к электрону — способность некоторых атомов и молекул присоединять добавочный электрон и превращаться в отрицательные ионы. Мерой сродства к электрону служит выделяющаяся при этом энергия. Наибольшим сродством к электрону обладают атомы галогенов (до 3 4 эВ). * … Энциклопедический словарь
СРОДСТВО К ЭЛЕКТРОНУ — способность нек рых нейтральных атомов, молекул и свободных радикалов присоединять добавочные эл ны, превращаясь в отрицат. ионы. Мерой этой способности служит положит. энергия С. к э. c, равная разности энергии нейтрального атома (молекулы) в… … Физическая энциклопедия
СРОДСТВО К ЭЛЕКТРОНУ — способность некоторых атомов и молекул присоединять добавочный электрон и превращаться в отрицательные ионы. Мерой сродства к электрону служит выделяющаяся при этом энергия. Наибольшим сродством к электрону обладают атомы галогенов (до 3 4 эВ).… … Большой Энциклопедический словарь
СРОДСТВО К ЭЛЕКТРОНУ — энергия (символ Е), которая выделяется или поглощается при присоединении электрона к изолированному атому (или иону), молекуле, радикалу без передачи частице кинетической энергии; выражается в Дж, кДж. Величина сродства к электрону важна для… … Большая политехническая энциклопедия
СРОДСТВО К ЭЛЕКТРОНУ — см. Энергия сродства. Геологический словарь: в 2 х томах. М.: Недра. Под редакцией К. Н. Паффенгольца и др.. 1978 … Геологическая энциклопедия
ФИЗИКА ТВЕРДОГО ТЕЛА — раздел физики, изучающий структуру и свойства твердых тел. Научные данные о микроструктуре твердых веществ и о физических и химических свойствах составляющих их атомов необходимы для разработки новых материалов и технических устройств. Физика… … Энциклопедия Кольера
Сродство к электрону
Полезное
Смотреть что такое «Сродство к электрону» в других словарях:
сродство к электрону — способность некоторых атомов и молекул присоединять добавочный электрон и превращаться в отрицательные ионы. Мерой сродства к электрону служит выделяющаяся при этом энергия. Наибольшим сродством к электрону обладают атомы галогенов (до 3 4 эВ). * … Энциклопедический словарь
СРОДСТВО К ЭЛЕКТРОНУ — энергия (символ Е), которая выделяется или поглощается при присоединении электрона к изолированному атому (или иону), молекуле, радикалу без передачи частице кинетической энергии; выражается в Дж, кДж. Величина сродства к электрону важна для… … Большая политехническая энциклопедия
СРОДСТВО К ЭЛЕКТРОНУ — способность некоторых атомов и молекул присоединять добавочный электрон и превращаться в отрицательные ионы. Мерой сродства к электрону служит выделяющаяся при этом энергия. Наибольшим сродством к электрону обладают атомы галогенов (до 3 4 эВ).… … Большой Энциклопедический словарь
СРОДСТВО К ЭЛЕКТРОНУ — способность нек рых нейтральных атомов, молекул и свободных радикалов присоединять добавочные эл ны, превращаясь в отрицат. ионы. Мерой этой способности служит положит. энергия С. к э. c, равная разности энергии нейтрального атома (молекулы) в… … Физическая энциклопедия
СРОДСТВО К ЭЛЕКТРОНУ — см. Энергия сродства. Геологический словарь: в 2 х томах. М.: Недра. Под редакцией К. Н. Паффенгольца и др.. 1978 … Геологическая энциклопедия
сродство к электрону — – энергия, которая выделяется или поглощается при присоединении электрона к изолированному атому или иону в газовой фазе при Т = 0 К без передачи частице кинетической энергии. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
сродство к электрону — elektroninis giminiškumas statusas T sritis Standartizacija ir metrologija apibrėžtis Dydis, proporcingas energijai, išsiskiriančiai atomui arba jonui prisijungus elektroną. atitikmenys: angl. electron affinity vok. Elektronenaffinität, f rus.… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
сродство к электрону — elektroninis giminiškumas statusas T sritis Standartizacija ir metrologija apibrėžtis Energijų skirtumas tarp laisvojo elektrono begalybėje ir elektrono, esančio dielektriko ar puslaidininkio laidumo juostos žemiausiame lygmenyje. atitikmenys:… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
сродство к электрону — elektroninis giminingumas statusas T sritis chemija apibrėžtis Dydis, proporcingas energijai, išsiskiriančiai arba sugeriamai atomui (jonui) prisijungus elektroną. atitikmenys: angl. electron affinity rus. сродство к электрону … Chemijos terminų aiškinamasis žodynas
СРОДСТВО К ЭЛЕКТРОНУ — частицы (молекулы, атома, иона), миним. энергия А, необходимая для удаления электрона из соответствующего отрицат. иона на бесконечность. Для частицы X С. к э. относится к процессу: С. к э. равно энергии ионизации Eотрицат. иона X (первому… … Химическая энциклопедия
Сродство к электрону



Неметаллические, или окислительные свойства элементов характеризует сродство к электрону. Сродством к электрону Е называется энергия, которая выделяется при присоединении электрона к атому, молекуле или радикалу. Она выражается в тех же единицах, что и энергия ионизации. Чем больше сродство к электрону, т.е. чем больше энергии выделилось при присоединении электрона, тем прочнее удерживается электрон взявшей его частицей, тем сильнее выражены у элемента окислительные свойства.
Атомы элементов – окислителей, принимая электроны, превращаются в отрицательно заряженные ионы. Энергия сродства к электрону атомов (как и энергия ионизации) закономерно изменяется в соответствии с характером электронных структур атомов.
В пределах периода с ростом порядкового номера элемента атомный радиус уменьшается, так как заполняется электронами один и тот же энергетический уровень, а заряд ядра растет, следовательно, увеличивается и притяжение ядром внешних электронов. Наибольшее уменьшение радиусов наблюдается у элементов малых периодов, у которых происходит заполнение электронами внешнего энергетического уровня. В больших периодах у d– и f–элементов наблюдается более плавное уменьшение радиусов при увеличении заряда ядра атома.
В связи с уменьшением атомного радиуса у р–элементов, уменьшением числа электронов, недостающих до завершения внешнего уровня, и увеличением силы притяжения электронов ядром в периодах слева направо возрастает у элементов сродство к электрону, а следовательно, и окислительные, т.е. неметаллические свойства. Самым высоким сродством к электрону обладают галогены (элементы VIIA группы), т.к. при присоединении одного электрона к нейтральному атому они приобретают законченную электронную конфигурацию благородного газа.
В пределах подгруппы с увеличением порядкового номера элемента (сверху вниз) атомный радиус увеличивается, поэтому ослабевает сила притяжения ядром принимаемых электронов и вместе с этим уменьшается сродство к электрону, а следовательно, и окислительные (неметаллические) свойства элементов. Поэтому самым сильным окислителем является фтор. И если с синтезом новых элементов, т.е. с дальнейшим развитием периодической системы Д.И. Менделеева, мы можем ожидать элемент с более выраженными металлическими свойствами, чем у франция, то более активного, чем фтор, неметалла быть не может.
Для решения вопроса о том, какой из атомов легче отдает или принимает электроны, учитывают оба фактора: и энергию ионизации, и сродство к электрону. Такой обобщающей характеристикой элемента служит электроотрицательность – ЭО, которую принимают равной полусумме энергии ионизации и сродства к электрону:
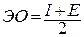
Электроотрицательность характеризует способность атомов элементов принимать электроны при образовании ионной связи или оттягивать на себя общую электронную пару при образовании ковалентной связи. Чем выше электроотрицательность элемента, тем сильнее проявляются у него эти тенденции. При учете обеих энергий нивелируется неоднозначное изменение энергии ионизации у элементов одного периода с ростом порядкового номера и электроотрицательность изменяется однозначно в пределах периода и подгруппы. Электроотрицательность возрастает в направлении слева направо для элементов каждого периода и уменьшается в направлении сверху вниз для элементов одной подгруппы периодической системы Д.И. Менделеева.
Учитывая сложность определения величины сродства к электрону, американский ученый Полинг предложил термохимическую систему, согласно которой электроотрицательности атомов А и В определяют, исходя из энергий связей А – В, А – А и В – В.
Зная закономерности изменения электроотрицательности элементов, мы можем судить и о закономерности изменения свойств соединений, образуемых элементами (табл.2).
Электроотрицательность элементов по Полингу
| Н 2,1 | ||||||
| Li 1,0 | Be 1,5 | B 2,0 | C 2,5 | N 3,0 | O 3,5 | F 4,0 |
| Na 0,9 | Mg 1,2 | Al 1,5 | Si 1,8 | P 2,1 | S 2,5 | Cl 3,0 |
| K 0,8 | Ca 1,0 | Ga 1,6 | Ge 1,8 | As 2,0 | Se 2,4 | Br 2,8 |
| Rb 0,8 | Sr 1,0 | In 1,7 | Sn 1,8 | Sb 1,9 | Te 2,1 | I 2,5 |
| Cs 0,8 | Ba 0,9 | Tl 1,8 | Pb 1,8 | Bi 1,9 | Po 2,0 | At 2,2 |
| Fr 0,7 | Ra 0,9 |
Приведенные молекулы образованы элементами одной подгруппы – хлором, бромом и иодом. Так как электроотрицательность в пределах подгруппы уменьшается сверху вниз, то наибольшая ЭО будет у хлора, поэтому самая полярная связь будет в молекуле HCl, и соляная кислота будет самой сильной из приведенных кислот.
С другой стороны, в этих молекулах атомы галогенов проявляют отрицательную степень окисления, равную –1, т.е. мы условно считаем, что каждый из них принял по одному электрону от атома водорода, поэтому все соединения могут проявлять восстановительные свойства. Так как электроотрицательность убывает от хлора к брому и далее к иоду, то взятый электрон будет удерживаться наиболее прочно ядром атома хлора (он взят на наиболее близкий к ядру, третий, уровень), а наименее прочно – ядром атома иода. Поэтому восстановительные свойства в большей степени проявляются HI (это очень сильный восстановитель, часто используемый в органической химии).
Рассмотрим кислородсодержащие кислоты хлора, в молекулах которых хлор проявляет различные степени окисления:
хлорноватистая хлористая хлорноватая хлорная
кислота; кислота; кислота; кислота.
Во всех этих кислотах хлор, проявляя положительную степень окисления, может быть окислителем. Изменение кислотных свойств и окислительной способности данных соединений можно выразить следующей схемой:
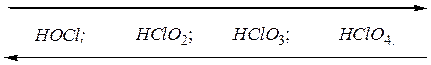
Усиление окислительной активности.
С увеличением степени окисления хлора устойчивость его кислородных кислот растет, растет и сила кислот: самая слабая кислота – хлорноватистая, самая сильная – хлорная. Хлорная кислота – самая сильная кислота из всех известных кислот вообще.
Окислительные свойства в этом ряду соединений, наоборот, ослабевают. Наиболее сильный окислитель – хлорноватистая кислота, наименее сильный – хлорная кислота.
Такая закономерность – усиление кислотных свойств гидроксида (и, соответственно, ослабление его основных свойств) с ростом степени окисления элемента характерна не только для хлора, но и для других элементов. В первом приближении эту закономерность можно объяснить, рассматривая все связи в молекулах гидроксидов как чисто ионные:
В этом ряду самой сильной кислотой будет HOCl, а самой слабой – HOI.
Поскольку предположение о чисто ионной природе всех связей в молекулах гидроксидов может быть высказано со значительной долей погрешности, рассмотренная схема влияния заряда и размеров иона Э n + на характер диссоциации молекулы Э(ОН)n не может служить основой для количественной оценки кислотно-основных свойств гидроксидов. Однако при сопоставлении кислотно-основных свойств различных гидроксидов, образуемых данным элементом в разных степенях окисления, или при сопоставлении свойств аналогичных гидроксидов, образуемых элементами одной и той же подгруппы периодической системы, эта схема в большинстве случаев приводит к правильным качественным выводам.