Что называется сплавом железа с углеродом
Сталь (сплав железа с углеродом)
Для феррита характерны относительно низкие прочность и твёрдость, но высокие пластичность и ударная вязкость. Цементит хрупок, но весьма твёрд и прочен. Перлит обладает ценным сочетанием прочности, твёрдости, пластичности и вязкости. Соотношение между этими фазами в структуре С. определяется главным образом содержанием в ней углерода; различные свойства этих фаз и обусловливают многообразие свойств С. Так, С., содержащая
0,1% С (в её структуре преобладает феррит), характеризуется большой пластичностью; С. этого типа используется для изготовления тонких листов, из которых штампуют части автомобильных кузовов и др. деталей сложной формы. С., в которой содержится
Классификация сталей. В современной металлургии С. выплавляют главным образом из чугуна и стального лома. По типу сталеплавильного агрегата (кислородный конвертер, мартеновская печь, электрическая дуговая печь) С. называется кислородно-конвертерной, мартеновской или электросталью. Кроме того, различают металл, выплавленный в основной или кислой (по характеру футеровки) печи; С. при этом называется соответственно основной или кислой (например, кислая мартеновская С.).
По характеру застывания металла в изложнице различают спокойную, полуспокойную и кипящую С. Поведение металла при кристаллизации обусловлено степенью его раскисленности: чем полнее удалён из С. кислород, тем спокойнее протекает процесс затвердевания; при разливке малораскисленной С. в изложнице происходит бурное выделение пузырьков окиси углерода ‒ С. как бы «кипит». Полуспокойная С. занимает промежуточное положение между спокойной и кипящей С. Каждый из этих видов металла имеет достоинства и недостатки; выбор технологии раскисления и разливки С. определяется её назначением и технико-экономическими показателями производства.
Маркировка сталей. Единой мировой системы маркировки С. не существует. В СССР проведена большая работа по унификации обозначений различных марок С., что нашло отражение в государственных стандартах и технических условиях. Марки углеродистой С. обыкновенного качества обозначаются буквами Ст и номером (Ст0, Ст1, Ст2 и т.д.). Качественные углеродистые С. маркируются двузначными числами, показывающими среднее содержание С в сотых долях процента: 05, 08, 10, 25, 40 и т.д. Спокойную С. иногда дополнительно обозначают буквами сп, полуспокойную ‒ пс, кипящую ‒ кп (например, СтЗсп, Ст5пс, 08кп). Буква Г в марке С. указывает на повышенное содержание Mn (например, 14Г, 18Г). Автоматные С. маркируются буквой А (А12, А30 и т.д.), углеродистые инструментальные С. ‒ буквой У (У8, У10, У12 и т.д. ‒ здесь цифры означают содержание С. в десятых долях процента).
Лит.: Сталеплавильное производство. Справочник, под ред. А. М. Самарина, т. 1‒2, М., 1964; Меськин В. C., Основы легирования стали, 2 изд., М., 1964; Гудремон Э., Специальные стали, пер. с нем., 2 изд., т. 1‒2, М., 1966; Дреге В., Сталь как конструкционный материал, пер. с нем., М., 1967; Гуляев А. П., Чистая сталь, М., 1975.
Лит.: Тульские «златокузнецы». [Альбом], Л., 1974.
Сплавы железа с углеродом
Диаграмма состояния железоуглеродистых сплавов дает представление о строении основных конструкционных сплавов — сталей и чугунов.
Ферритом называется твердый раствор углерода в а- железе. Содержание углерода в феррите очень невелико — максимальное 0,02% при температуре 727°С. Благодаря столь малому содержанию углерода свойства феррита совпадают со свойствами железа (низкая твердость и высокая пластичность). Твердый раствор углерода в высокотемпературной модификации Feα (т.е. в Feδ) часто называют δ- ферритом или высокотемпературным ферритом.
Аустенит — это твердый раствор углерода в γ- железе. Максимальное содержание углерода в аустените составляет 2,14% (при температуре 1147°С). Имеет твердость НВ 220.
Цементит— это химическое соединение железа с углеродом (карбид железа) Fe3C. В нем содержится 6,67 % углерода (по массе). Имеет сложную ромбическую кристаллическую решетку. Характеризуется очень высокой твердостью (НВ 800), крайне низкой пластичностью и хрупкостью.
Рис. 15 Пластинчатый перлит
Рис. 16 Зернистый перлит
Перлит— это механическая смесь феррита с цементитом. Содержит 0,8% углерода, образуется из аустенита при температуре 727°С. Имеет пластинчатое строение, т.е. его зерна состоят из чередующихся пластинок феррита и цементита. Перлит является эвтектоидом.
Эвтектоид— это механическая смесь двух фаз, образующаяся из твердого раствора (а не из жидкого сплава, как эвтектика).
Ледебуритпредставляет собой эвтектическую смесь аустенита с цементитом. Содержит 4,3% углерода, образуется из жидкого сплава при температуре 1147°С. При температуре 727°С аустенит, входящий в состав ледебурита превращается в перлит и ниже этой температуры ледебурит представляет собой механическую смесь перлита с цементитом.
Фаза цементита имеет пять структурных форм: цементит первичный, образующийся из жидкого сплава; цементит вторичный, образующийся из аустенита; цементит третичный, образующийся из феррита; цементит ледебурита; цементит перлита.
Диаграмма Fe-Fe3C. На рис. 17 приведена диаграмма состояния сплавов железа с цементитом. На горизонтальной оси концентраций отложено содержание углерода от 0 до 6,67%. Левая вертикальная ось соответствует 100% содержанию железа. На ней отложены температура плавления железа и температуры его полиморфных превращений. Правая вертикальная ось (6,67% углерода) соответствует 100% содержанию цементита. Буквенное обозначение точек диаграммы принято согласно международному стандарту и изменению не подлежит.

Железоуглеродистые сплавы в зависимости от содержания углерода делятся на техническое железо (до 0,02% С), сталь (от 0,02 до 2,14 % С) и чугун (от 2,14 до 6,67% С). Сталь, содержащая до 0,8% С называется доэвтектоидной, 0,8% С — эвтектоидной и свыше 0,8% С — заэвтектоидной. Чугун, содержащий от 2,14 до 4,3% С называется доэвтектическим, ровно 4,3% — эвтектическим и от 4,3 до 6,67% С — заэвтектическим.
Структура техническою железа представляет собой зерна феррита или феррит с небольшим количеством третичного цементита. Обязательной структурной составляющей стали является перлит. Структура доэвтектоидной стали, состоит из равномерно распределенных зерен феррита и перлита. Эвтектоидная сталь состоит только из перлита. Структура заэвтектоидной стали представляет собой зерна перлита, окруженные сплошной или прерывистой сеткой вторичного цементита. Для чугуна характерно наличие ледебурита в структуре. Структура доэвтектического чугуна состоит из перлита, вторичного цементита и ледебурита, эвтектическою — из ледебурита и заэвтектического — из ледебурита и первичного цементита.
Три основных вида термической обработки: отжиг, закалка, отпуск (старение). Их назначение.
Таким образом, путем изменения режима термической обработки удается получать различные физико-механические свойства металлов. К основным операциям термической обработки относят отжиг, нормализацию, закалку и отпуск.
Отжиг – термическая обработка заключающаяся в нагреве металла до определенных температур, выдержка и последующего очень медленного охлаждения вместе с печью. Применяют для улучшения обработки металлов резанием, снижения твердости, получения зернистой структуры, а также для снятия напряжений, устраняет частично (или полностью) всякого рода неоднородности, которые были внесены в металл при предшествующих операциях (механическая обработка, обработка давлением, литье, сварка), улучшает структуру стали.
Отжиг первого рода. Это отжиг при котором не происходит фазовых превращений, а если они имеют место, то не оказывают влияния на конечные результаты, предусмотренные его целевым назначением. Различают следующие разновидности отжига первого рода: гомогенизационный и рекристаллизационный. Гомогенизационный – это отжиг с длительной выдержкой при температуре выше 950С (обычно 1100–1200єС) с целью выравнивания химического состава. Рекристаллизационный – это отжиг наклепанной стали при температуре, превышающей температуру начала рекристаллизации, с целью устранения наклепа и получение определенной величины зерна. Отжиг второго рода. Это отжиг, при котором фазовые превращения определяют его целевое назначение. Различают следующие виды: полный, неполный, диффузионный, изотермический, светлый, нормализованный (нормализация), сфероидизирующий (на зернистый перлит). Полный отжиг производят путем нагрева стали на 30–50 °С выше критической точки, выдержкой при этой температуре и медленным охлаждением до 400–500 °С со скоростью 200 °С в час углеродистых сталей, 100°С в час для низколегированных сталей и 50 °С в час для высоколегированных сталей. Структура стали после отжига равновесная, устойчивая. Неполный отжиг производится путем нагрева стали до одной из температур, находящейся в интервале превращений, выдержкой и медленным охлаждением. Неполный отжиг применяют для снижения внутренних напряжений, понижения твердости и улучшения обрабатываемости резанием. Диффузионный отжиг. Металл нагревают до температур 1100–1200С, так как при этом более полно протекают диффузионные процессы, необходимые для выравнивания химического состава. Изотермический отжиг заключается в следующем: сталь нагревают, а затем быстро охлаждают (чаще переносом в другую печь) до температуры, находящейся ниже критической на 50–100С. Нормализация – заключается в нагреве металла до температуры на (30–50) С выше критической точки и последующего охлаждения на воздухе. Высокоуглеродистые стали подвергают нормализации с целью устранения цементитной сетки. Закалка – это нагрев до оптимальной температуры, выдержка и последующее быстрое охлаждение с целью получения неравновесной структуры. В результате закалки повышается прочность и твердость и понижается пластичность стали. Отпуск стали является завершающей операцией термической обработки, формирующей структуру, а следовательно, и свойства стали. Отпуск заключается в нагреве стали до различных температур (в зависимости от вида отпуска, но всегда ниже критической точки), выдержке при этой температуре и охлаждении с разными скоростями. Назначение отпуска – снять внутренние напряжения, возникающие в процессе закалки, и получить необходимую структуру. В зависимости от температуры нагрева закаленной детали различают три вида отпуска: высокий, средний и низкий. Высокий отпуск производится при температурах нагрева выше 350–600 °С, но ниже критической точки; такой отпуск применяется для конструкционных сталей. Средний отпуск производится при температурах нагрева 350 – 500°С; такой отпуск широко применяется для пружинной и рессорной сталей. Низкий отпуск производится при температурах 150–250 °С. Твердость детали после закалки почти не изменяется; низкий отпуск применяется для углеродистых и легированных инструментальных сталей, для которых необходимы высокая твердость и износостойкость. Старение – это процесс изменения свойств сплавов без заметного изменения микроструктуры. Если изменение твердости, пластичности и прочности протекает при комнатной температуре, то такое старение называется естественным. Если же процесс протекает при повышенной температуре, то старение называется искусственным.
Общие понятия об отжиге: разновидности, назначение.
СПЛАВЫ ЖЕЛЕЗА С УГЛЕРОДОМ



Сплавы железа с углеродом являются основой так называемых черных сплавов — сталей и чугунов, которые служат важнейшими конструкционными материалами в технике. Структура и свойства любого сплава зависят прежде всего от свойств базового компонента и элементов-добавок, а также от характера их взаимодействия.
Чистое железо — металл серебристо-белого цвета; тугоплавкий. Температура плавления железа 1539°С. Железо имеет две полиморфные модификации, a и g.
При температурах ниже 910°С железо имеет объемно-центрированную кубическую решетку. Эту модификацию называют a-железо; a-железо магнитно до температуры 768°С (точка Кюри).
При нагреве железа его объемно-центрированная кубическая решетка при 910°С превращается в гранецентрированную кубическую решетку, a-железо превращается в g железо; g-железо существует при температуре 910-1392°С.
Углерод является неметаллическим элементом. Температура плавления углерода 3500°С. Углерод в природе может существовать в двух полиморфных модификациях: алмаз и графит. Форма алмаза в сплавах не встречается.
В железоуглеродистых сплавах в свободном виде углерод находится в форме графита. Кристаллическая структура графита слоистая. Прочность и пластичность его весьма низкие.
Углерод растворим в железе в жидком и твердом состояниях, может образовывать химическое соединение — цементит, может находиться в свободном виде в форме графита.
Железоуглеродистые сплавы могут иметь следующие структурные составляющие.
Феррит (Ф) — твердый раствор внедрения углерода и других элементов в a-железе. Имеет объемно-центрированную кубическую решетку. Растворимость углерода в феррите очень мала: при комнатной температуре до 0,005 %; наибольшая растворимость 0,02 % при 727°С. Феррит высокопластичен и мягок, хорошо обрабатывается давлением в холодном состоянии.
Аустенит (А) — твердый раствор углерода и других элементов в g-железе. Существует только при высоких температурах. Предельная растворимость углерода в g-железе 2,14% при температуре 1147°С и 0,8 % при 727°С. Эта температура является нижней границей существования аустенита в железоуглеродистых сплавах. Аустенит высокопластичен, но более тверд, чем феррит.
Цементит (Ц)— химическое соединение железа с углеродом (карбид железа Fe3C). В цементите содержится 6,67 % углерода. Температура плавления цементита около 1600°С. Имеет сложную кристаллическую решетку. Самая твердая и хрупкая составляющая железоуглеродистых сплавов. Цементит неустойчив и в определенных условиях распадается с образованием свободного углерода в виде графита по реакции: Fe3C > 3Fe + С.
Чем больше цементита в железоуглеродистом cплаве, тем выше его твердость.
Графит — аллотропическая модификация углерода. Графит мягок, прочность его очень низкая. В чугунах и графитизированной стали содержится в виде включений различных форм. Форма графитовых включений влияет на механические и технологические свойства сплава.
Перлит (П) — механическая смесь феррита и цементита, содержащая 0,8 % углерода. Образуется при перекристаллизации (распаде) аустенита при температуре 727°С. Этот распад называется эвтектоидным, а перлит — эвтектоидом. Перлит обладает высокими прочностью, твердостью и повышает механические свойства сплава.
Ледебурит — механическая смесь аустенита и цементита, содержащая 4,3 % углерода. Образуется в результате эвтектического превращения при температуре 1147°С. При температуре 727°С аустенит превращается в перлит, и после охлаждения ледебурит представляет собой смесь перлита с цементитом. Ледебурит имеет высокую твердость и большую хрупкость. Содержится во всех белых чугунах.
Диаграмма состояния железо — цементит представлена в упрощенном виде на рис. 14. Она показывает фазовый состав и структуру железоуглеродистых сплавов с концентрацией от чистого железа до цементита (6,67 % углерода).
В рассматриваемой системе существуют следующие фазы: жидкий сплав, твердые растворы (феррит и аустенит), химических соеденений
(в упрощенном виде): А — аустенит, П — перлит, Л — ледебурит,
Ф.— феррит, Ц — цементит
Жидкий сплав (Ж. С.) существует выше линии ликвидус ACD. Цементит Fe3C (Ц) — вертикальная линия DFKL. Область феррита (Ф) располагается левее линии GPQ. Область аустенита (А) — AESG.
На диаграмме точка А (1539°С) соответствует температуре плавления железа, а точка D (1600°С) — температуре плавления цементита. Точка С (911 °С) — температура полиморфного превращения железа a 
Точка С соответствует предельному содержанию углерода в аустените (2,14 % при температуре 1147°С). При понижении температуры растворимость углерода в аустените уменьшается полинии ES. В точке S она составляет 0,8 % при 727°С.
Точка Р — предельное содержание углерода в феррите 0,02 % при 727°С. При охлаждении до комнатной температуры растворимость углерода в феррите уменьшается по линии PQ до 0,005 %.
При температуре 1147°С жидкий сплав, содержащий 4,3 % углерода, кристаллизуется с образованием эвтектики (механической смеси двух фаз аустенита и цементита). При этом образуется структура ледебурита. Точка С на диаграмме — точка эвтектики, линия ECF— линия кристаллизации эвтектики.
При температуре 727°С аустенит, содержащий 0,8 % углерода, распадается на две фазы — цементит и феррит, т. е. происходит эвтектоидное превращение. При этом образуется структура, называемая перлитом. На диаграмме точка S — точка эвтектоида, линия PSK— линия эвтектоидного превращения.
Рассмотрим кристаллизацию сплавов, содержащих различное количество углерода.
Сплавы,содержащие до 2,14% углерода, кристаллизуются в интервале температур, ограниченном линиями АС (линия ликвидус) и АЕ (линия солидус). После затвердевания сплавы имеют однофазную структуру — аустенит.
При кристаллизации доэвтектических сплавов, содержащих от 2,14 до 4,3% С, из жидкой фазы при температурах, соответствующих линии ликвидус АС, сначала выделяются кристаллы аустенита. При температуре 1147°С оставшаяся жидкость, имеющая эвтектический состав (4,3 % С), кристаллизуется, образуя эвтектику ледебурит. После затвердевания доэвтектические сплавы состоят из аустенита и ледебурита.
В заэвтектических сплавах, содержащих от 4,3 до 6,67 % С, с понижением температуры до линии ликвидус CD зарождаются и растут кристаллы цементита. При температуре 1147°С жидкость достигает эвтектической концентрации и затвердевает с образованием ледебурита. После затвердевания заэвтектические чугуны состоят из первичного цементита (кристаллизовавшегося из жидкого сплава) и ледебурита.
Эвтектический сплав (4,3% C) кристаллизуется при постоянной температуре с образованием только эвтектики — ледебурита (А + Fe3C).
После затвердевания железоуглеродистые сплавы претерпевают фазовые и структурные изменения. Это связано с полиморфным превращением железа и с изменением растворимости углерода в аустените и в феррите с понижением температуры.
Сплавы, содержащие до 0,02% С (точка Р), испытывают при охлаждении и при нагреве полиморфное превращение a 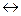
Сплавы, содержащие 0,02—0,8% С, называют доэвтектоидными. Эти стали после кристаллизации состоят из аустенита. При температурах ниже линии GOS начинают расти зерна феррита. При достижении 727°С аустенит, не претерпевший превращения, имеет эвтектоидную концентрацию (0,8 % С) и распадается с одновременным выделением из него феррита и цементита, образующих эвтектоидную структуру перлит. После окончательного охлаждения доэвтектоидные сплавы имеют структуру феррит + перлит.
В эвтектоидном сплаве (0,8% С) при температуре 727°С (точка S) весь аустенит превращается в перлит.
При охлаждении заэвтектоидных сплавов(от 0,8 до 2,14% С) до температур, соответствующих линии SE, из аустенита выделяется цементит (вторичный) в результате уменьшения растворимости углерода в аустените. При температуре 727°С аустенит, содержащий 0,8 % С, превращается в перлит. После охлаждения заэвтектоидные сплавы состоят из перлита и цементита.
В доэвтектических сплавах вследствие уменьшения растворимости углерода при охлаждении (линия SE) происходит частичный распад аустенита с выделением кристаллов вторичного цементита. При 727°С аустенит эвтектоидного состава превращается в перлит. Структура доэвтектических сплавов после окончательного охлаждения состоит из перлита, вторичного цементита и ледебурита (перлит + цементит).
Эвтектический сплав (4,3 % С) при температурах ниже 727°С состоит только из ледебурита (перлит + цементит).
Заэвтектические сплавы после полного охлаждения состоят из первичного цементита и ледебурита (перлит + цементит).
При температурах ниже 727° С железоуглеродистые сплавы имеют различную структуру, но фазовый состав их одинаков. Они состоят из двух фаз феррита и цементита.
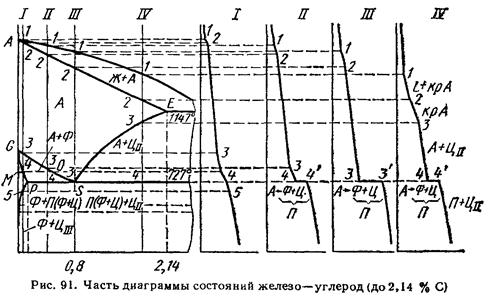
Все сплавы, содержащие до 2,14%С, после окончания кристаллизации имеют структуру аустенита. В сплавах, содержащих до 0,1 % С (до точки Н), при охлаждении вначале происходит кристаллизация Fеδ (С) с последующим превращением его в аустенит. В сплавах, содержащих 0,1—0,5 % С (до точки В), образование аустенита происходит по линии HJВ при 1499 °С по перитектической реакции ЖB + ФH ↔ АJ. Поэтому часто пользуются более упрощенной диаграммой Fе—Fе3С, где линия солидуса АHJЕ представлена в виде простой линии АЕ (рис. 91).
На рис. 91 изображена левая часть диаграммы Fе—Fе3С.
Сплав I содержит меньше 0,02% С, т. е. расположен левее точки Р. Он представляет собой технически чистое железо.
Кристаллизация аустенита начинается в точке 1 и заканчивается в точке 2. До точки 3 в сплаве I не происходит никаких фазовых превращений: сплав просто охлаждается.
Чем больше в стали углерода, т. е. чем ближе располагается сплав к точке 5, тем большее время необходимо для этого превращения (отрезок 4-4′ на кривой охлаждения будет больше) и в структуре сплава будет больше перлита. После охлаждения структура таких сплавов состоит из Ф+ П.
Сплав III содержит 0,8 % С, т. е. по составу отвечает точке эвтектоидного превращения 5. При его охлаждении до 727 °С аустенит не испытывает никаких превращений, поэтому при температуре 727 °С весь аустенит превратится в перлит,
При 727°С (точка 4) происходит эвтектоидное превращение. Таким образом, после окончательного охлаждения сплав будет иметь структуру П + ЦII. По сравнению с ЦIII выделение ЦII происходит при более высоких температурах, когда скорости диффузии велики. Поэтому ЦII образуется по границам зерен в виде сетки.
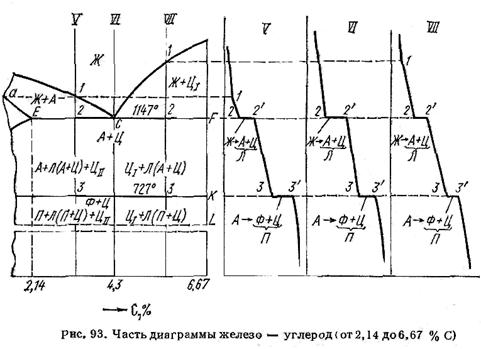
Особенностью всех сплавов с содержанием углерода от 2,14 до 6,67 % является наличие в их структуре ледебурита (рис. 93).
Кривая охлаждения сплава V типична для всех сплавов, содержащих от 2,14 до 4,3 % углерода (т. е. расположенных от точки Е до точки С). Кристаллизация зерен аустенита начинается в точке 1 и заканчивается в точке 2. С понижением температуры состав аустенита изменяется по линии солидуса от точки а до точки Е, а состав жидкой фазы — от точки 1 до точки С. При 1147 °С (точка 2) оставшаяся жидкость претерпевает эвтектическое превращение
При температурах между линиями ЕСF и РSК сплав имеет структуру А + Л (А + Ц) + ЦII. И в этих сплавах образуется ЦII, так как при охлаждении состав аустенита также будет изменяться по линии GS.
При 727 °С (линия РSК) происходит эвтектоидное превращение АS ↔ эвтектоид(ФР + ЦK) и ниже этой температуры сплав будет иметь структуру П + Л (П + Ц) + ЦII. Вторичный цементит сливается с цементитом ледебурита.
При охлаждении сплава VI (4,3 % С) при температуре 1147 о С (точка С) вся жидкость превращается в ледебурит, который с понижением температуры испытывает превращения, аналогичные сплаву V.
В сплавах, содержащих углерода от 4,3 до 6,67 % (сплав VII), в точке 1 начинается образование кристаллов цементита. Чтобы отметить характер выделения, такой цементит называют первичным и обозначают ЦI. Поскольку при кристаллизации ЦI выделяется из жидкой фазы, его кристаллы обычно бывают крупными (грубые выделения). В точке 2 происходит эвтектическое превращение. Структура сплава между линиями ЕСF и РSК ЦI + Л (А + Ц), При 727 о С происходит эвтектоидное превращение аустенита. Окончательная структура сплава (ниже 727°С) ЦI + Л (П + Ц). Химические и физические свойства ЦI, ЦII и ЦIII одинаковы. Влияние на механические свойства сплавов оказывает различие в размерах, количестве и расположении этих выделений.
Влияние углерода и примесей на свойства сталей
Углеродистые стали являются основными. Их свойства определяются количеством углерода и содержанием примесей, которые взаимодействуют с железом и углеродом.
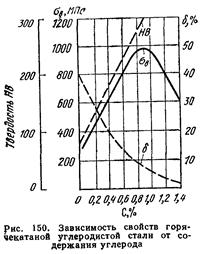
Влияние углерода на свойства сталей показано на рис. 10.1.
С ростом содержания углерода в структуре стали увеличивается количество цементита, при одновременном снижении доли феррита. Это приводит к уменьшению пластичности, к повышению прочности и твердости. Прочность повышается до содержания углерода около 1%, а затем она уменьшается, так как образуется грубая сетка цементита вторичного.
Углерод влияет на вязкие свойства. Увеличение содержания углерода повышает порог хладоломкости и снижает ударную вязкость.
Повышаются электросопротивление, снижаются магнитная проницаемость и плотность магнитной индукции.
Рис.10.1. Влияние углерода на свойства сталей
Углерод оказывает влияние и на технологические свойства. Повышение содержания углерода ухудшает литейные свойства стали (для изготовления отливок используются стали с содержанием углерода до 0,4 %), обрабатываемость давлением и резанием, свариваемость. Следует учитывать, что стали с низким содержанием углерода также плохо обрабатываются резанием.
В углеродистых сталях всегда присутствуют примеси, которые делятся на четыре группы.
1. Постоянные примеси: кремний, марганец, сера, фосфор.
Марганец и кремний вводятся в процессе выплавки стали для раскисления, они являются технологическими примесями.
Содержание марганца не превышает 0,5…0,8 %. Марганец повышает прочность, не снижая пластичности, и резко снижает красноломкость стали, вызванную влиянием серы. Он способствует уменьшению содержания сульфида железа FeS, так как образует с серой соединение сульфид марганца MnS. Частицы сульфида марганца располагаются в виде отдельных включений, которые деформируются и оказываются вытянутыми вдоль направления прокатки.
Содержание кремния не превышает 0,35…0,5 %. Кремний, дегазируя металл, повышает плотность слитка. Кремний растворяется в феррите и повышает прочность стали, особенно повышается предел текучести, 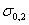
Содержание фосфора в стали 0,025…0,05 %. Фосфор, растворяясь в феррите, искажает кристаллическую решетку и увеличивает предел прочности 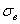
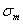
Располагаясь вблизи зерен, увеличивает температуру перехода в хрупкое состояние, вызывает хладоломкость, уменьшает работу распространения трещин. Повышение содержания фосфора на каждую 0,01 % повышает порог хладоломкости на 20…25 o С.
Хладноломкость Ст3кп – 0 о С, а у Ст3сп – «-40 о С», поэтому применение кипящей стали для северных районов не допустимо.
Фосфор обладает склонностью к ликвации, поэтому в центре слитка отдельные участки имеют резко пониженную вязкость. Для некоторых сталей возможно увеличение содержания фосфора до 0,10…0,15 %, для улучшения обрабатываемости резанием.
Сера S – уменьшается пластичность, свариваемость и коррозионная стойкость. Р–искажает кристаллическую решетку.
Содержание серы в сталях составляет 0,025…0,06 %. Сера – вредная примесь, попадает в сталь из чугуна. Сера нерастворима в железе, она образует с ним химическое соединение – сульфид железа FeS, которое, в свою очередь, образует с железом легкоплавкую эвтектику (Fе + FеS) с температурой плавления988 o С. Поэтому при нагреве стальных заготовок для пластической деформации выше 900 °С эвтектика плавится, нарушаются связи между зернами, сталь становится хрупкой. При деформации в местах расположения эвтектики возникают надрывы и трещины, заготовка разрушается – явление красноломкости (повышение хрупкости при высоких температурах).
Для уменьшения вредного влияния серы добавляют марганец (соединение MnS имеет tпл=1620 о С, пластично и не вызывает красноломкости).
Сера снижает механические свойства, особенно ударную вязкость а 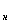
Азот и кислород находятся в стали в виде хрупких неметаллических включений: окислов (FeO, SiO2, Al2O3 ) нитридов (Fe 2N), в виде твердого раствора или в свободном состоянии, располагаясь в дефектах (раковинах, трещинах).
Примеси внедрения (азот N, кислород О) повышают порог хладоломкости и снижают сопротивление хрупкому разрушению. Неметаллические включения (окислы, нитриды), являясь концентраторами напряжений, могут значительно понизить предел выносливости и вязкость.
Очень вредным является растворенный в стали водород, который значительно охрупчивает сталь. Он приводит к образованию в катанных заготовках и поковках флокенов.
Флокены – тонкие трещины овальной или округлой формы, имеющие в изломе вид пятен – хлопьев серебристого цвета. Металл с флокенами нельзя использовать в промышленности, при сварке образуются холодные трещины в наплавленном и основном металле. Если водород находится в поверхностном слое, то он удаляется в результате нагрева при 150…180 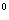
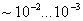
Сталь считают легированной хромом или никелем, если содержание этих элементов составляет 1 % или более.
При содержании ванадия, молибдена, титана, ниобия и других элементов более 0,1—0,5 % стали считают легированными этими элементами.
Сталь является легированной и в том случае, если в ней содержатся только элементы, характерные для углеродистой стали, марганец или кремний, но их количество должно превышать 1 %.
В конструкционных сталях легирование осуществляют с целью улучшения механических свойств — прочности, пластичности и т. д. Кроме того, при введении в сталь легирующих элементов меняются физические, химические и другие ее свойства.
Нужный комплекс свойств достигается не только легированием, но и рациональной термической обработкой, в результате которой получается необходимая структура.
Как правило, легирующие элементы существенно повышают стоимость стали, а некоторые из них к тому же являются дефицитными металлами, поэтому добавление их в сталь должно быть строго обосновано.