Что называется гидроксильным показателем и как он определяется
Понятие водородного и гидроксильного показателей
Равновесной концентрацией ионов водорода или гидроксила можно количественно охарактеризовать степень кислотности или щёлочности любого раствора. Чаще принято характеризовать растворы концентрацией ионов водорода:
Для удобства проведения расчётов – избавление от отрицательных степеней – в значениях концентраций ионов водорода и гидроксила предложено применять вместо подлинных значений концентраций [Н + ] и [ОН – ] их отрицательные логарифмы.
При увеличении концентрации водородных ионов величина рН уменьшается, при увеличении концентрации гидроксил-ионов величина рН увеличивается, т.е. в кислой среде рН 7.
Индикаторы – вещества, изменяющие свою окраску при взаимодействии с одним из реагирующих веществ реакции. Под интервалом (областью перехода) индикатора понимают промежуток значений рН, в котором происходит заметное изменение окраски индикатора. В таблице приведены интервалы некоторых индикаторов.
| Индикатор |  Область перехода ∆ Область перехода ∆ |  Цвет индикатора в средах кислой щелочной Цвет индикатора в средах кислой щелочной |
| Метиловый оранжевый | 3,2 – 4,4 | красный жёлтый |
| Лакмус | 5 – 8 | красный синий |
| Фенолфталеин | 8,2 – 10,0 |  бесцветный малиновый бесцветный малиновый |
| Метиловый красный | 4,2 – 6,2 | красный жёлтый |
Буферные растворы
Растворы, сохраняющие практически неизменными величины рН при разбавлении, либо при добавлении к ним небольших количеств кислот или щелочей называются буферными. Буферные растворы именуются часто буферными смесями, так как по составу они представляют смеси электролитов с одноимёнными ионами:
1. Слабой кислоты и одноимённой её соли. Например, ацетатный буфер:
СН3СООН и СН3СООNa.
2. Слабого основания и соли с одноимёнными катионами. Например, аммиачный буфер: NH4OH и NH4Cl.
3. Гидросолей многоосновных кислот с одноимёнными катионами. Например, NaН2РО4 и Na2НРО4.
4. Составы буферных смесей разнообразны и могут быть ещё более сложными.
Регулирующий механизм рН буферных растворов основан на смещении устанавливающихся в них равновесий. Например, в аммиачном буфере имеются следующие равновесные процессы: NH4OH D NH4 + + OH –
Расчётные формулы для вычисления рН буферных растворов представлены в таблице 3 приложения.
Гидролиз солей
Гидролизом называется ионообменное взаимодействие соли с водой, в результате которого образуются малодиссоциирующие соединения (ионы или молекулы). Продуктами гидролиза могут быть слабая кислота (или кислотные остатки) и слабое основание (или основные остатки).
При рассмотрении солей как продуктов взаимодействия кислоты с основанием в зависимости от силы их можно выделить 4 типа солей, образованных:
1) сильной кислотой и сильным основанием;
2) сильным основанием и слабой кислотой;
3) слабым основанием и сильной кислотой;
4) слабым основанием и слабой кислотой.
В зависимости от типов солей возможны 4 случая их гидролиза:
1. Соли, образованные сильным основанием и сильной кислотой (например, K2SO4, NaNO3, KCl, NaCl) гидролизу не подвергаются, так как при взаимодействии их с водой слабые электролиты не образуются. В таких растворах равновесие в процессе диссоциации воды не нарушается, реакция среды остаётся нейтральной.
Катионы натрия с водой не взаимодействуют.
Na2CO3 + Н2О D NaНCO3 +NaОН.
Анионы NO3 – сильной кислоты с водой не взаимодействуют. Катион Fe 3+ является катионом слабого основания Fe(ОН)3, основной остаток FeOH +2 взаимодействует с молекулами воды с образованием малодиссоциирующего продукта – основного остатка FeOH +2 :
Fe(NO3)3 + Н2О D (FeOH)( NO3)2 + НNO3.
Итак, при растворении в воде солей, образованных слабым основанием и
4. Если соль образована слабым основанием и слабой кислотой, происходит гидролиз её по катиону слабого основания и по аниону слабой кислоты – полный необратимый гидролиз до конечных продуктов гидролиза. Например, если сульфид алюминия Аl2S3, полученный сжиганием алюминия в порошке серы, бросить в воду, то моментально произойдёт бурная реакция гидролиза
Аl2S3: Аl2S3 + 6Н2О = 2Al(OH)3 + 3H2S.
В результате образуется осадок Al(OH)3 и выделится сероводород. Этот гидролиз необратим, поэтому реакцией обмена в растворе Аl2S3 получить нельзя. Вместо него образуются продукты гидролиза.
Уравнения необратимого гидролиза составляют только в молекулярной форме.
Расчётные формулы для вычисления рН растворов гидролизующихся солей представлены в таблице 3 приложения.
Дата добавления: 2016-09-06 ; просмотров: 4138 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Физиология и нарушения кислотно-основного состояния (методические материалы к практическим и семинарским занятиям)
Информация
Справочное пособие содержит информацию о физиологии кислотно- основного состояния (КОС). Представлена информация о методах лабораторной диагностики нарушений КОС. Перечислены варианты нарушений и методы коррекции. Предназначается для врачей всех специальностей, курсантов ФПК и студентов медвузов.
Физиология кислотно-основного состояния
В норме сильных кислот образуется 50 – 100 ммоль/сутки. При избыточном образовании они вызывают тяжелые нарушения. Это происходит при анаэробном окислении глюкозы.
В норме окисление глюкозы происходит аэробно: С6Н12О2 + 6О2 = 6Н2О + 6СО2 + 38 АТФ
Рис. 1. Доставка 02 к тканям и первые стадии элиминации CO2
Рис. 2. В легких бикарбонат снова превращается в С02 и выводится
Транспорт кислорода из легких к тканям и из тканей к легким обусловлен изменениями, которые воздействуют на сродство кислорода к гемоглобину. На уровне тканей из-за снижения рН это сродство уменьшается (эффект Бора) и вследствие этого улучшается отдача кислорода. В крови легочных капилляров сродство гемоглобина к кислороду увеличивается из-за снижения рС02 и возрастания рН по сравнению с аналогичными показателями венозной крови, что приводит к повышению насыщения артериальной крови кислородом.
Первичные изменения КЩС и компенсаторные реакции
IV.Водородный и гидроксильный показатели растворов



Расчет pH и pOH растворов сильных кислот.
Cильные кислоты в растворе диссоциируют полностью:
c(B) – молярная концентрация кислоты, моль/л;
α – степень диссоциации;
Кислотность среды водного раствора сильной кислоты характеризуют водородным показателем рН:
Водородный и гидроксильный показатели взаимосвязаны:
Пример 11.ОпределитеpOH 0,1н раствора Н2SO4, степень электролитической диссоциации которой равна 90%.
Решение. Н2SO4 – сильный электролит, процесс диссоциации описывается уравнением: H2SO4 = 2H + + SO4 2- ; NH + = 2;
1. Определим молярную концентрацию кислоты:
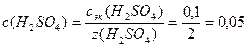
3.Определим рН раствора кислоты:
4. pOH = 14 – pH = 14 – 1,05= 12,95
Пример 12. Определите концентрацию гидроксид-ионов 5%-ного раствора HCl, степень электролитической диссоциации HCl равна 80%, плотность раствора 1,03 г/мл.
1. Определим молярную концентрацию HCl:
Примем m(р-ра)=100г, тогда m(HCl)= 5г,
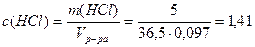
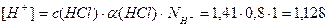
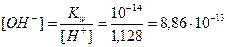
Пример 13. В 3л раствора содержится 0,015 моль HCl и 0,075 моль H2SO4, a(HCl)=1, a(H2SO4)=1. Определите pOH раствора.
Решение.Раствор содержит две сильные кислоты, уравнения их диссоциации:
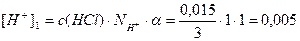
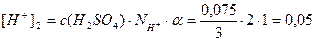
[H + ] = [H + ]1 + [H + ]2 = 0,005 + 0,05 = 0,055 моль/л;
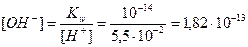
Пример 14.Рассчитайте pH раствора, полученного при смешивании 50 мл 0,1М HCl, 15мл 0,1M NaOH и 935мл H2O.
Решение. При смешивании щелочи и кислоты в растворе происходит реакция нейтрализации:
NaOH + HCl = NaCl + H2O
Реакция среды раствора будет определяться избытком
кислоты или щелочи, оставшейся после реакции.
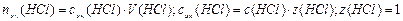
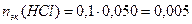
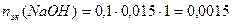
3. Взаимодействующие в ходе реакции вещества подчиняются закону эквивалентов: nэк(HCl) = nэк(NaOH). Следовательно, после реакции в растворе останется избыток HCl в количестве:
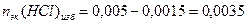
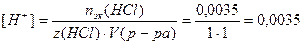
Ионное произведение воды. Водородный и гидроксильный показатели. Что они характеризуют. Принцип действия индикаторов
Ионное произведение воды.Тщательно очищенная от посторонних примесей вода обладает определенной, хотя и незначительной, электрической проводимостью, заметно возрастающей с повышением температуры.
Наличие электрической проводимости может быть объяснено только тем, что молекулы воды, частично распадаются на ионы, т.е. вода является слабым электролитом. Процесс диссоциации воды может быть записан Н2О+Н2О=Н3О+ОН‾.
Этот процесс называется самоионизацией или автопротолизом.
Константа диссоциации воды может быть вычислена по уравнению (8.16)
Учитывая, что степень распада молекул воды крайне мала, активность ионов в уравнении можно заменить их концентрациями, а концентрацию нераспавшихся молекул воды можно считать равной общей концентрации молекул воды. Концентрацию молекул можно рассчитать, разделив массу 1 литра воды на массу ее моля: 1000/18=55,5 моль/л.
Считая эту величину постоянной, можно уравнение записать в виде (8.17а)
Где Кв – ионное произведение воды. Так как в соответствии с уравнением диссоциации концентрация ионов Н+ и ОН‾ в воде одинаковы, их можно определить, зная ионное произведение воды. [Н+]=[ОН‾]=√Кв=10^(-7) моль/л.
Диссоциация воды – процесс эндотермический, поэтому константа Кв сильно зависит от температуры.
При расчетах, связанных с водными растворами электролитов, используют не концентрации, а активности ионов: (8.17б)
Как всякая константа равновесия, константа Кв не зависит от активностей ионов Н+ и ОН‾ в растворе. Так, если в воду добавить кислоты, активность ионов Н+ резко возрастает. Тогда за счет подавления диссоциации воды равновесие этого процесса сместиться влево и активность ионов ОН‾ в растворе уменьшится, но ионное произведение остается неизменным.
Таким образом, в водных растворах активность ионов Н+ и ОН‾ при постоянной температуре связаны между собой. Достаточно указать активность одного из них, чтобы определить активность другого, пользуясь выражением.
Для характеристики кислотности (щелочности) среды введен специальный параметр – водородный показатель, или рН. Водородным показателем, или рН, называется взятый с обратным знаком десятичный логарифм активности ионов водорода в растворе(8.18):
Водородный показатель нейтральной среды равен 7, если рН>7 – щелочная среда, рН
Константа диссоциации кислотного индикатора запишется в виде:
Некоторые наиболее распространенные индикаторы
Взаимосвязь водородного и гидроксильного показателя
Теория растворимости
При растворении молекулы или ионы вещества распределяются более или менее равномерно между молекулами растворителя. Например, в кристаллическом хлориде натрия среднее расстояние между нонами натрия и хлора равно 2,8 А. В 1 М растворе растворитель разделяет ноны и поэтому ионы натрия и хлора удалены друг от друга на 10 А. На трудность разделения таких ионов указывают высокие температуры плавления (800°С) и кипения (1413°С) чистого хлорида натрия.
Работа, необходимая для разделения двух противоположно заряженных пластинок, при введении между ними вещества уменьшается на величину, которая называется диэлектрической проницаемостью среды.
Молекулы воды, находящиеся между двумя нонами (или заряженными пластинами конденсатора), представляют собой маленькие диполи, ориентированные друг к другу разноименными зарядами («голова к хвосту») так, что они частично нейтрализуют ионные заряды и. таким образом, стабилизируют систему. Поэтому можно ожидать, что сольватирующая способность и диэлектрическая проницаемость будут изменяться параллельно.
Предельная растворимость многих веществ в воде (или в других растворителях) представляет собой постоянную величину, соответствующую концентрации насыщенного раствора при данной температуре. Она является качественной характеристикой растворимости и приводится в справочниках в граммах на 100 г растворителя (при определённых условиях).
Растворимость зависит от природы растворяемого вещества и растворителя, температуры и давления.
Природа растворяемого вещества.
Кристаллические вещества подразделяются на:
Влияние температуры. Если растворение вещества является экзотермическим процессом, то с повышением температуры его растворимость уменьшается (Например, Ca (OH) 2 в воде) и наоборот. Для большинства солей характерно увеличение растворимости при нагревании.
Практически все газы растворяются с выделением тепла. Растворимость газов в жидкостях с повышением температуры уменьшается, а с понижением увеличивается.
Влияние давления. С повышением давления растворимость газов в жидкостях увеличивается, а с понижением уменьшается.
Классификация веществ по степени диссоциации
Исходя из степени диссоциации все электролиты делятся на две группы.
Составьте уравнения диссоциации веществ:
Взаимосвязь водородного и гидроксильного показателя
Какая реакция среды при гидролизе соли, образованной сильной кислотой и слабым основанием. Приведите пример, напишите уравнение гидролиза. В соли, образованной слабым основанием и сильной кислотой (FeCl2, NH4Cl, Al2 (SO4) 3, MgSO4) гидролизу подвергается катион:
FeCl2 + HOH =>Fe (OH) Cl + HCl,
В результате гидролиза образуется слабый электролит, ион H и другие ионы. рН раствора