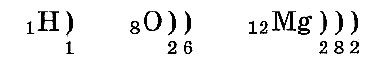Что называется электронной оболочкой
Электронная оболочка
Электронная оболочка атома — область пространства вероятного местонахождения электронов, характеризующихся одинаковым значением главного квантового числа n и, как следствие, располагающихся на близких энергетических уровнях. Число электронов в каждой электронной оболочке не превышает определенного максимального значения.
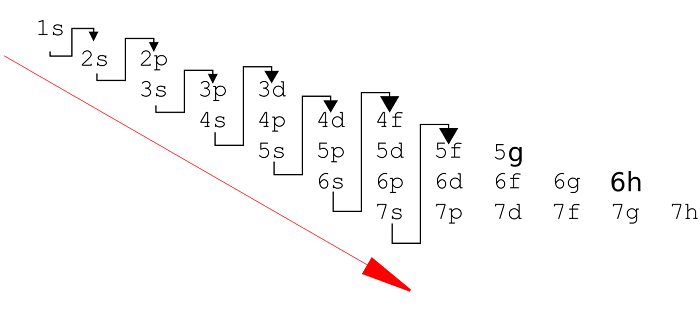
Порядок заполнения электронных оболочек (орбиталей с одинаковым значением главного квантового числа n) определяется правилом Клечковского, порядок заполнения электронами орбиталей в пределах одного подуровня (орбиталей с одинаковыми значениями главного квантового числа n и орбитального квантового числа l) определяется Правилом Хунда.
Содержание
Оболочки
Электронные оболочки обозначаются буквами K, L, M, N, O, P, Q или цифрами от 1 до 7. Подуровни оболочек обозначаются буквами s, p, d, f, g, h, i или цифрами от 0 до 6. Электроны внешних оболочек обладают большей энергией, и, по сравнению с электронами внутренних оболочек, находятся дальше от ядра, что делает их более важными в анализе поведения атома в химических реакциях и в роли проводника, так как их связь с ядром слабее и легче разрывается.
Количество электронов в каждой оболочке
Данное количество вычисляется по формуле:
| 1 | 2 | 3 | 4 | 5 | 6 | Итого |
|---|---|---|---|---|---|---|
| 1 (K) | 2 | 2 | ||||
| 2 (L) | 2 | 6 | 8 | |||
| 3 (M) | 2 | 6 | 10 | 18 | ||
| 4 (N) | 2 | 6 | 10 | 14 | 32 | |
| 5 (O) | 2 | 6 | 10 | 14 | 18 | 50 |
Подуровни оболочек
Каждая оболочка состоит из одного или нескольких подуровней, каждый из которых состоит из атомных орбиталей. К примеру, первая оболочка (K) состоит из одного подуровня «1s». Вторая оболочка (L) состоит из двух подуровней, 2s и 2p. Третья оболочка — из «3s», «3p» и «3d». Возможные варианты подуровней оболочек приведены в следующей таблице:
| Обозначение подуровня | l | Макс. кол-во электронов | Содержание в оболочках | Историческое наименование |
|---|---|---|---|---|
| s | 0 | 2 | В каждой | sharp |
| p | 1 | 6 | Во всех, начиная со 2 | principal |
| d | 2 | 10 | Во всех, начиная с 3 | diffuse |
| f | 3 | 14 | Во всех, начиная с 4 | fundamental |
| g | 4 | 18 | Во всех, начиная с 5 | |
| h | 5 | 22 | Во всех, начиная с 6 | |
| i | 6 | 26 | Во всех, начиная с 7 |
Валентные оболочки
Валентная оболочка — самая внешняя оболочка атома. Электроны этой оболочки зачастую неверно называют валентными электронами, то есть электронами, определяющими поведение атома в химических реакциях. С точки зрения химической активности, наименее активными считаются атомы, в которых валентная оболочка окончательно заполнена (инертные газы). Наибольшей химической активностью обладают атомы, в которых валентная оболочка состоит всего из одного электрона (щелочные металлы), и атомы, в которых одного электрона не хватает для окончательного заполнения оболочки (галогены).
На самом деле всё немного иначе. Поведение атома в химических реакциях определяют электроны, обладающие большей энергией, то есть те электроны, которые расположены дальше от ядра. Электроны внутренних подуровней оболочек имеют меньшую энергию, чем электроны внешних подуровней. Несмотря на то, что электроны подуровня оболочки 3d могут не принадлежать к т. н. валентной оболочке, они могут иметь энергию большую, чем электроны подуровня оболочки 4s, что делает их валентными электронами.
ЭЛЕКТРОННАЯ ОБОЛОЧКА
Совокупность Э. о. представляет собой э л е к т р о н н у ю к о н ф и г у р а ц и ю атома или иона. Электронные конфигурации атомов разл. элементов приводятся в периодической системе элементов Менделеева. В. П. Шевелько.
Полезное
Смотреть что такое «ЭЛЕКТРОННАЯ ОБОЛОЧКА» в других словарях:
Электронная оболочка — атома область пространства вероятного местонахождения электронов, характеризующихся одинаковым значением главного квантового числа n и, как следствие, располагающихся на близких энергетических уровнях. Число электронов в каждой электронной… … Википедия
электронная оболочка — elektroninis apvalkalas statusas T sritis chemija apibrėžtis Išorinis atomo elektronų sluoksnis. atitikmenys: angl. electron shell; electronic shell rus. электронная оболочка … Chemijos terminų aiškinamasis žodynas
электронная оболочка — elektronų sluoksnis statusas T sritis fizika atitikmenys: angl. electron shell; electronic shell vok. Elektronenschale, f rus. электронная оболочка, f pranc. écorce électronique, f; couche électronique, f … Fizikos terminų žodynas
электронная оболочка — elektroninis apvalkalas statusas T sritis fizika atitikmenys: angl. electron shell; electronic shell vok. Elektronenschalle, f rus. электронная оболочка, f pranc. écorce électronique, f; couche électronique, f … Fizikos terminų žodynas
электронная оболочка — Совокупность одноэлектронных состояний в атоме, имеющих определённые значения квантовых чисел n и l и возникающих при описании атома в приближении самосогласованного поля … Политехнический терминологический толковый словарь
электронная оболочка атома — ▲ оболочка ↑ атом, состоять из, электрон термы. синглет. триплет. мюоний. мезоатом. молекула. молекулярный. химическое соединение. | атомно молекулярный. фазовое состояние … Идеографический словарь русского языка
внешняя электронная оболочка — išorinis elektronų sluoksnis statusas T sritis radioelektronika atitikmenys: angl. outer electron shell vok. äußere Elektronenschale, f rus. внешняя электронная оболочка, f pranc. couche externe d électrons, f … Radioelektronikos terminų žodynas
внутренняя электронная оболочка — vidinis elektronų sluoksnis statusas T sritis radioelektronika atitikmenys: angl. inner electron shell vok. innere Elektronenschale, f; innere Schale, f rus. внутренняя электронная оболочка, f pranc. gaine interne d électrons, f … Radioelektronikos terminų žodynas
заполненная оболочка — заполненная оболочка; замкнутая оболочка Электронная оболочка, в которой все состояния заняты … Политехнический терминологический толковый словарь
замкнутая оболочка — заполненная оболочка; замкнутая оболочка Электронная оболочка, в которой все состояния заняты … Политехнический терминологический толковый словарь
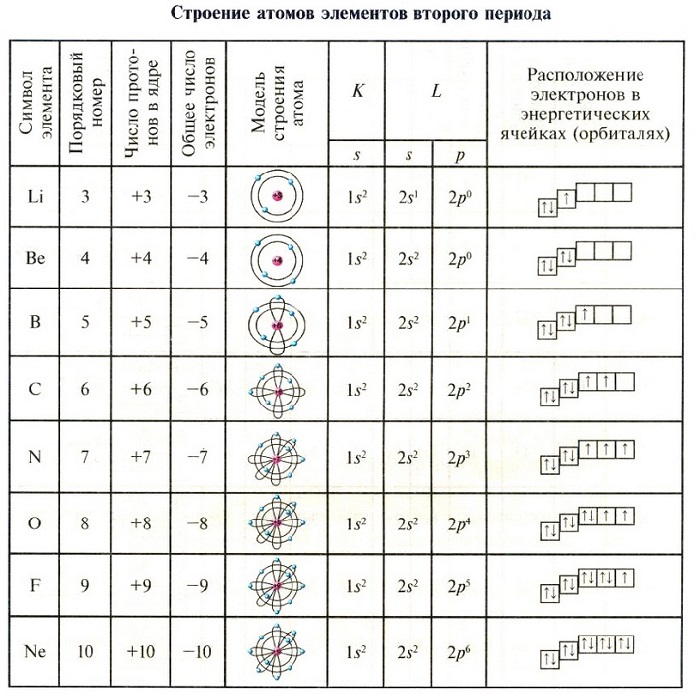
Строение электронной оболочки атома
Атом состоит из ядра и электронной оболочки.
Электронная оболочка атома – это совокупность всех электронов в данном атоме.
Химические свойства элементов определяются строением электронных оболочек их атомов.
В 20-х годах ХХ в. ученые установили, что электрон имеет двойственную природу: он является одновременно частицей и волной (имеет свойства частицы и свойства волны).
Представление о двойственной природе электрона привело к созданию квантово-механической теории строения атома.
Согласно этой теории, электрон (как и другие микрочастицы) не имеет определенной траектории движения. Можно говорить только о вероятности нахождения электрона в разных частях атомного пространства.
Часть атомного пространства, в которой вероятность нахождения данного электрона наибольшая (равна 90%), называется атомной орбиталью.
Каждый электрон в атоме занимает определенную орбиталь и образует электронное облако, которое является совокупностью различных положений быстро движущегося электрона.
Атомная орбиталь и облако электрона, который занимает эту орбиталь, имеют одинаковый размер, одинаковую форму и одинаковое направление в пространстве.
Для характеристики орбиталей и электронов используются квантовые числа.
Энергия и размер орбитали и электронного облака характеризуются главным квантовым числом n.
Главное квантовое число принимает значения целых чисел от 1 до ∞(бесконечности): n = 1, 2, 3, 4, 5, 6, 7…∞
Орбитали, которые имеют одинаковое значение n, близки между собой по энергии и по размеру.
Совокупность орбиталей, которые имеют одинаковое значение главного квантового числа, — это энергетический уровень.
Энергетические уровни обозначаются большими буквами латинского алфавита.
Совокупность электронов, которые находятся на одном энергетическом уровне, — это электронный слой.
На одном энергетическом уровне могут находиться орбитали (электронные облака), которые имеют различные геометрические формы.
Форма орбиталей и облаков характеризуется побочным (орбитальным) квантовым числом l.
Для орбиталей данного энергетического уровня побочное (орбитальное) квантовое число принимает значения целых чисел от 0 до n-1.
Орбитали, для которых l = 0, имеют форму шара (сферы) и называются s-opбиталями (условно изображаются в виде окружности):
s –орбитали имеются на всех энергетических уровнях.
На K-уровне (на первом энергетическом уровне) имеется только s-орбиталь.
Орбитали, для которых l=1, имеют форму гантели и называются р-орбиталями:
р-Орбитали имеются на всех энергетических уровнях, кроме первого (K) уровня.
Орбитали с большими значениями l имеют более сложную форму и обозначаются так:
l = 2: d-орбитали;
l = 3: f-орбитали.
d-Орбитали есть на всех энергетических уровнях, кроме первого (K) и второго (L) уровней.
f-Oрбитали есть на всех энергетических уровнях, кроме первого (K), второго (L) и третьего (М) уровней.
Энергия орбиталей (Е), которые находятся на одном энергетическом уровне, но имеют различную форму, неодинакова:
Итак, каждая орбиталь и электрон, который находится на этой орбитали, характеризуются тремя квантовыми числами: главным n, побочным l и магнитным m1.
Электрон характеризуется еще одним — спиновым квантовым числом (от англ. to spin — кружить, вращать).
Спиновое квантовое число (спин электрона) ms, характеризует вращение электрона вокруг своей оси и принимает только два значения: +1/2 и – 1/2.
Схематично это можно показать так:
Электрон со спином +1/2 — условно изображают так: ↑; со спином —1/2: ↓
Принцип Паули гласит:
В атоме не может быть двух электронов с одинаковым набором всех четырех квантовых чисел.
Поэтому на одной орбитали не может быть больше двух электронов; эти два электрона имеют одинаковый набор трех квантовых чисел (n, l, m1) и должны отличаться спинами (спиновым квантовым числом ms:
Два электрона, которые находятся на одной орбитали, называются спаренными (или неподеленной электронной парой). Спаренные электроны являются электронами с противоположными (антипараллельными) спинами.
Что называется электронной оболочкой
Ключевые слова конспекта: строение электронных оболочек атомов первых 20 элементов Периодической системы Д.И. Менделеева, завершенный электронный слой, валентный слой, энергетические уровни, правило октета, орбиталь,
Электронная оболочка атома — это все электроны атома. Электроны в электронной оболочке атома расположены слоями. Электроны в разных слоях различаются энергией взаимодействия с ядром атома. Чем дальше от ядра находится электрон, тем меньше энергия его взаимодействия с ядром.
Вместимость электронных слоев различная. В слое № 1, или в первом слое, у всех элементов, кроме водорода, находится 2 электрона. (В атоме водорода всего 1. электрон, и он — в первом слое.) Во втором слое может находиться не больше восьми электронов. В третьем слое максимально может расположиться 18 электронов. В четвертом слое максимально бывает 32 электрона.
Завершенный электронный слой — это слой в атоме, содержащий максимально возможное для него число электронов.
Электронные слои заполняются так: сначала первый, потом второй и последующие — по мере уменьшения энергии их взаимодействия с ядром. Расположение по слоям электронов в атомах водорода, кислорода и магния:
Число электронных слоев атома равно номеру периода химического элемента в таблице Менделеева. Поэтому у атома водорода один электронный слой, у кислорода — два слоя, а у магния — три слоя.
Валентный слой — это внешний электронный слой. У водорода это 1-й слой, у кислорода — 2-й слой, у магния — 3-й слой. Валентные электроны — это электроны внешнего слоя. Внешний слой всегда содержит не больше восьми электронов. Восьми-электронный внешний слой характеризуется повышенной устойчивостью. (Это — «правило октета».)
Зная максимальное число электронов в каждом электронном слое атома, можно составить схему расположения электронов по слоям в заданном элементе. Электронные слои атомов называют энергетическими уровнями.
Химические свойства атомов определяются свойствами их электронов. Движение электронов в атоме описывают с привлечением понятия орбитали. Каждый электрон в атоме находится на своей орбитали.
Орбиталь — это часть электронного облака, создаваемого электронами при движении в атоме. Орбиталь — это пространство около ядра, где чаще всего находится электрон.
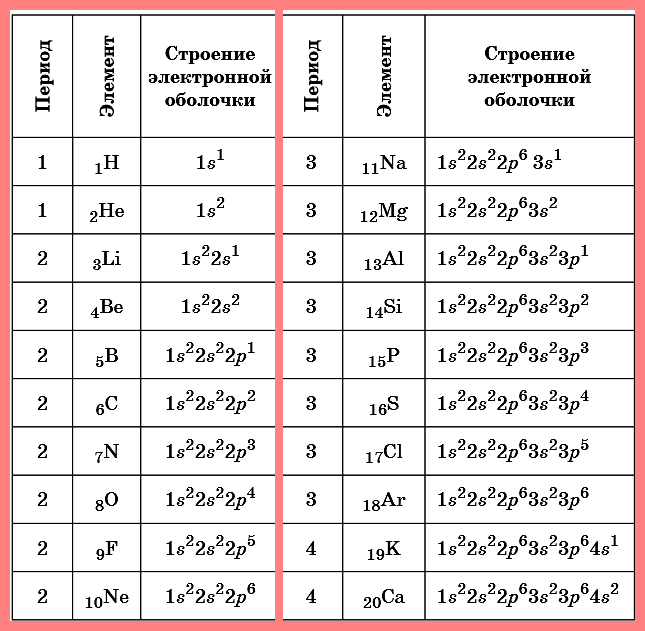
Таблица. Строение электронных оболочек атомов
первых 20 элементов Периодической системы Д.И. Менделеева
Фтор — элемент 2-го периода, т.к. в его электронной формуле два электронных слоя. Сумма всех надстрочных индексов — 9 (общее число электронов), это и атомный номер фтора. Элементы, у которых очередные электроны помещаются на s- и р-орбиталях, относятся к главным подгруппам таблицы Менделеева. Сумма электронов 2-го внешнего слоя дает номер группы — VII.
Конспект урока «Строение электронных оболочек атомов».
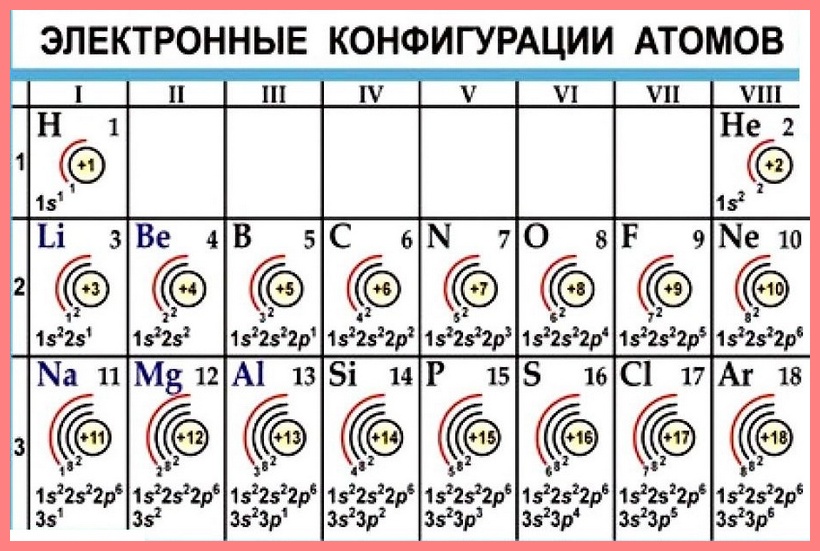
Строение электронных оболочек атомов химического элемента зависит от его месторасположения в периодической таблице Д. И. Менделеева.
Химия неразрывно связана с изучением мельчайших частиц вещества. В данной статье рассмотрим, как заполняются электронами орбитали атома.
Строение атома
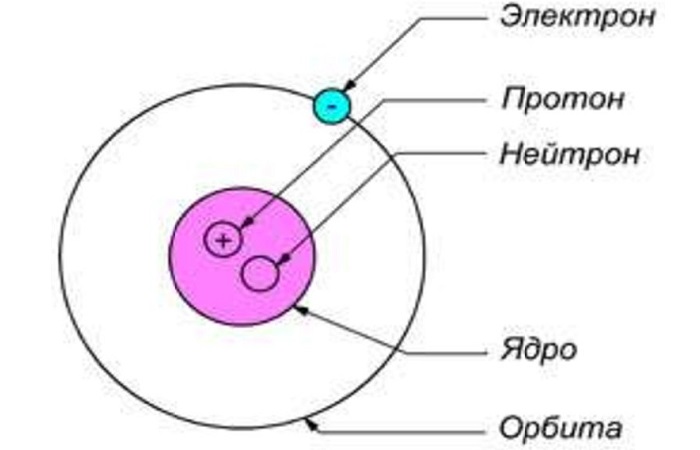
Атом любого вещества состоит из ядра (с положительным зарядом) и электронов (с отрицательным зарядом), расположенных вокруг него в виде электронного облака.
Ядро состоит из протонов и нейтронов. Значения зарядов противоположных частиц по абсолютному значению равны, в результате чего атом нейтрален. Вся его масса сосредоточена в центре.
Количество протонов элемента всегда равно его порядковому номеру таблицы Д. И. Менделеева. Масса протона равна 1,00728 а.е.м., а заряд соответствует +1 условной единице.
Масса нейтрона составляет 1,00866 а.е.м., а заряд нейтрален.
Строение электронной оболочки атома
Вид электронного облака зависит от орбит, по которым движутся отрицательные частицы. Область пространства, где вероятность их присутствия больше 90%, называется орбиталью.
Существует несколько типов орбиталей. S – шаровидная, p – гантелеобразная, d и f – сложная.
Они группируются в виде слоев. Эти слои отличаются друг от друга расстоянием от ядра и энергией. Чем ближе находится слой к ядру, тем меньше его энергия.
Внешний уровень может содержать не больше 8-ми электронов. В соответствии с правилом октета, это так называемый валентный слой, который характеризуется повышенной устойчивостью.
Принципы заполнения электронами орбиталей атома
Электронные оболочки заполняются по принципу возрастания энергии системы. Сначала заполняется уровень, расположенный ближе всего к ядру, а затем остальные, в порядке увеличения расстояния от него.
Первый уровень состоит из одной s-орбитали, а остальные из s-, p-, d- и f-подуровней, которые имеют 1, 3, 5 и 7 орбиталей. На каждой из них может находиться максимум 2 электрона. Таким образом, они могут содержать не более 2, 6, 10 и 14 электронов соответственно.
Если у элемента внешним является полностью заполненный s-подуровень, то его называют s-элементом.
Если у элемента внешним является полностью заполненный p-подуровень, то его называют p-элементом.
В соответствии с правилом Хунда отрицательные частицы располагаются на однотипных орбиталях одного ряда таким образом, чтобы суммарный спин был максимален. Следовательно, при заполнении ряда каждый электрон в первую очередь старается занять отдельную ячейку.
Если занять отдельный орбиталь не удается, он присоединяется к ряду уже другой отрицательной частицы.
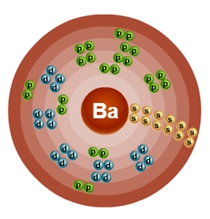
Определить структуру элемента можно по таблице Д. И. Менделеева. На примере химического элемента бария Ba (класс мягких металлов), видно, что он расположен в восьмом периоде, что означает наличие 8 энергетических уровней.
Порядковый номер 56 соответствует общему количеству электронов.
Заполнение орбиталей выглядит следующим образом:
1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 5s 2 5p 6 6s 2
Если нарисовать схему данного элемента, то она будет иметь следующий вид:
Следует отметить, что свойства и структура расположения частиц определяют химические и физические свойства вещества. Взаимодействие различных веществ также зависит от того, какой вид и структуру имеет электронное облако вещества.