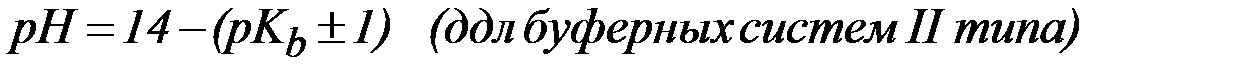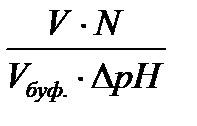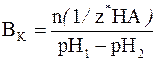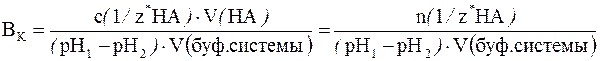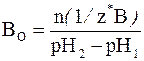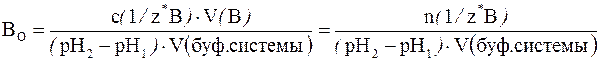Что называется буферной емкостью буферного раствора
Буферная емкость. От каких факторов зависит.



Буферная емкость(В) измеряется количеством кислоты или щелочи (моль или ммоль эквивалента), добавление которого к 1 л буферного раствора изменяет рН на единицу.
Буферная емкость зависит от ряда факторов:
1. Чем больше абсолютное содержание компонентов пары основание/сопряженная кислота, тем выше буферная емкость буферного раствора.
2. Буферная емкость зависит от соотношения количеств компонентов буферного раствора, а следовательно, и от рН буфера. Буферная емкость максимальна при равных количествах компонентов буферной системы и уменьшается с отклонением от этого соотношения.
3. При различном содержании компонентов буферные емкости раствора по кислоте и по щелочи отличаются.
Расчет величины рН буферных растворов.
Область (зона) буферного действия отличается от 

Понятие растворимости. Какие факторы влияют на растворимость твердых веществ.
Растворимость вещества (Р)– молярная концентрация вещества в насыщенном растворе.
Растворимость твердых веществ зависит от:
· природы растворенного вещества и растворителя
Растворимость газов зависит от:
Произведение растворимости малорастворимого сильного электролита. Расчет ПР.
В насыщенном растворе малорастворимого сильного электролита при данной температуре произведение молярных концентраций его ионов, возведенных в степени их стехиометрических коэффициентов, есть величина постоянная и называется произведением растворимости.
Буферная емкость. Количественное определение буферной емкости. Зона буферного действия.



Буферная ёмкость (В) выражается количеством моль-эквивалентов сильной кислоты или щелочи, которое следует добавить к одному литру буфера, чтобы сместить рН на единицу.
В =
В – буферная ёмкость,
nЭ – количество моль-эквивалента сильной кислоты или щелочи,
рНН – начальное значение рН ( до добавления кислоты или щелочи)
рНК – конечное значение рН (после добавления кислоты или щелочи)
На практике буферная ёмкость рассчитывается по формуле:
В =
V – объём кислоты или щелочи,
N – эквивалентная концентрация кислоты или щелочи,
Vбуф.— объём буферного раствора,
Δ рН – изменение рН.
Интервал значений рН, выше и ниже которого буферное действие прекращается, называется зоной буферного действия.
Она равна рН = рК ± 1
(Буферная ёмкость зависит от концентрации электролитов и соотношения компонентов буфера. Наибольшей буферной ёмкостью обладают растворы с большей концентрацией компонентов и соотношением компонентов, равным единице.)
Буферные растворы. Буферная емкость. Механизм действия буферных растворов. Применение их в анализе. Роль буферных растворов в процессах жизнедеятельности
В лабораторной практике часто приходится работать с растворами, которые имеют определенное значение рН. Такие растворы называют буферными.
Буферные растворы – растворы, рН которых практически не изменяется при добавлении к ним небольших количеств кислот и оснований или при их разбавлении.
Буферные растворы могут быть четырех типов:
1. Слабая кислота и её соль. Например, ацетатный буферный раствор СН3СООН + СН3СООNа (рН=4,7).
2. Слабое основание и его соль. Например, аммиачный буферный раствор NH4OH + NH4Cl (рН=9,2).
3. Раствор двух кислых солей. Например, фосфатный буферный раствор NaH2PO4 + Na2HPO4 (рН=8). В этом случае соль играет роль слабой кислоты.
Аминокислотные и белковые буферные растворы.
Механизм действия.
СН3СООNа + НСl = СН3СООН + NаСl
При добавлении к ацетатному буферному раствору щелочи (например, NaОН) происходит реакция:
Буферная емкость.
Всякий буферный раствор практически сохраняет постоянство рН лишь до прибавления определенного количества кислоты или щелочи, то есть обладает определенной буферной емкостью.
Буферная емкость – то предельное количество (моль) сильной кислоты или щелочи, которое можно добавить к 1 л буферного раствора, чтобы рН его изменился не более чем на единицу.
Приготовление.
Буферные свойства проявляются очень слабо, если концентрация одного компонента в 10 раз и более отличается от концентрации другого. Поэтому буферные растворы часто готовят смешением растворов равной концентрации обоих компонентов либо прибавлением к раствору одного компонента соответствующего количества реагента, приводящего к образованию равной концентрации сопряженной формы.
Для приготовления аммиачной буферной смеси смешивают 100 мл раствора NH4Cl с массовой долей его 10% и 100 мл раствора NH4OH с массовой долей 10% и разбавляют полученную смесь дистиллированной водой до 1 л.
Применение.
Буферные растворы широко применяются в химическом анализе, биохимическом анализе для создания и поддержания определенного значения рН среды при проведении реакций.
Например, ионы Ва 2+ отделяют от ионов Са 2+ осаждением дихромат-ионами Сr2О7 2- в присутствии ацетатного буферного раствора; при определении многих катионов металлов с помощью трилона Б методом комплексонометрии используют аммиачный буферный раствор.
Буферные растворы обеспечивают постоянство биологических жидкостей и тканей. Главными буферными системами в организме являются гидрокарбонатная, гемоглобиновая, фосфатная и белковая. Причем, действие всех буферных систем взаимосвязано. Поступившие из вне или образовавшиеся в процессе обмена веществ ионы водорода связываются одним из компонентов буферных систем. Однако, при некоторых заболеваниях может происходить изменение значения рН крови. Смещение значения рН крови в кислую область от нормальной величины рН 7,4 называется ацидозом, в щелочную область – алкалозом. Ацидоз возникает при тяжелых формах сахарного диабета, длительной физической работе и при воспалительных процессах. При тяжелой почечной или печеночной недостаточности или при нарушении дыхания может возникнуть алкалоз.
Величина буферной емкости зависит от концентраций компонентов буферной системы и от их соотношения



Способность буферных систем противодействовать резкому изменению рН при добавлении к ним сильной кислоты или основания является ограниченной. Буферная смесь поддерживает рН постоянным только при условии, что количество вносимых в раствор сильной кислоты или щелочи не превышает определенной величины. В противном случае наблюдается резкое изменение рН, т.е. буферное действие раствора прекращается.
Это связано с тем, что в результате протекающей реакции изменяется соотношение молярных концентраций компонентов буферной системы: с(кислоты)/с(соли) или с(основания)/с(соли).
При этом концентрация компонента, реагирующего с добавленной кислотой или щелочью, уменьшается, а концентрация второго компонента возрастает, т.к. он дополнительно образуется в ходе реакции.
Количественно буферное действие раствора характеризуется с помощью буферной емкости (В). При этом различают буферную емкость по кислоте (Вк.) и буферную емкостьпо основанию или щелочи (Во.).
Буферной емкостью по кислоте является то количество химических эквивалентов сильной кислоты, которое нужно добавить к 1 литру (1 дм 3 ) буферной системы, чтобы уменьшить её рН на единицу. Ее можно рассчитать по следующей формуле:
где n(1/z* HA) – число молей химических эквивалентов сильной кислоты, добавленное к 1 дм 3 буферной системы; рН1 – водородный показатель системы до добавления сильной кислоты; рН2 – водородный показатель системы после добавления сильной кислоты.
В более общем случае (если брать не 1 дм 3 буферной системы, а любой другой ее объем, выраженный в литрах или дм 3 ) формула для подсчета буферной емкости будет иметь следующий вид:
где с(1/z* НА) – молярная концентрация химического эквивалента сильной кислоты в добавляемом растворе; V(НА) – объем (дм 3 ) добавленного раствора сильной кислоты; V(буф. системы) – объем буферного раствора, к которому добавляют раствор кислоты.
Соответственно, буферной емкостью по основанию является то количество химических эквивалентов сильного основания (щелочи), которое нужно добавить к 1 литру (1 дм 3 ) буферной системы, чтобы вызвать увеличение ее рН на единицу:
где n(1/z* В) – число молей химических эквивалентов основания, которое добавили к 1 дм 3 буферного раствора; рН1 – водородный показатель раствора до добавления основания; рН2 – водородный показатель раствора после добавления основания.
В более общем случае (если брать не 1 дм 3 буферной системы, а любой другой ее объем) формула для подсчета буферной емкости по основанию примет следующий вид:
где с(1/z* В) – молярная концентрация химического эквивалента основания в добавляемом растворе; V(В) – объем (дм 3 ) добавленного раствора сильного основания; V(буф. системы) – объем буферного раствора (дм 3 ), к которому добавляют раствор сильного основания.
Чем более концентрированным является буферный раствор, тем выше его буферная емкость, т.к. в этом случае добавление небольших количеств сильной кислоты или щелочи не вызовет существенного изменения концентраций его компонентов, а значит и их соотношения.
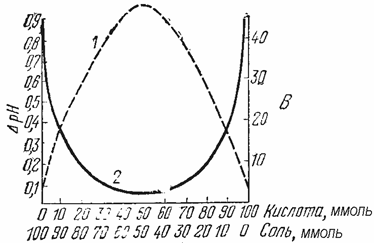
Из буферных растворов с одинаковым суммарным содержанием химического количества их компонентов наибольшей емкостью будут обладать те, которые составлены из равного числа молей слабой кислоты и её соли или слабого основания и его соли (рис. 35). В таких растворах молярные концентрации компонентов будут одинаковые, а значит соотношение с(кислоты)/с(соли) = 1 и с(основания)/с(соли) = 1.
Рис. 35. Изменение буферной емкости (1) и изменение рН кислотной буферной системы при добавлении к ней определенного количества сильной кислоты (2) в зависимости от содержания её компонентов
Данные растворы будут иметь примерно одинаковые значения буферной емкости как по кислоте, так и по основанию.
Если же соотношение концентраций компонентов буферной системы не равно 1, то значения ее буферной емкости по основанию и кислоте будут отличаться друг от друга (причем тем существеннее, чем в большей степени соотношение с(кислоты)/с(соли) и с(основания)/с(соли) отклоняется от единицы).
Например, если в кислотной буферной системе солевой компоненты содержится больше, чем слабой кислоты, то ее буферная емкость по кислоте будет выше, чем по основанию, т.е. Вк. > Во.
Соответственно, буферная емкость по кислоте для основной буферной системы будет больше, чем по основанию, в том случае, если содержание солевой компоненты в этом случае будет меньше, чем слабого основания.
Таким образом, можно сделать вывод, что в данных случаях буферная емкость выше по тому веществу, которое реагирует с избыточным компонентом буферного раствора.
Если буферная система не обладает достаточной буферной емкостью, ее можно повысить, увеличив концентрацию обоих компонентов в необходимое количество раз.
Буферные системы, их классификация и механизм действия. Буферные растворы. Уравнение Гендерсона-Гассельбаха.
Буферные системы (смеси или растворы) по составу бывают двух основных типов:
а) из слабой кислоты и ее соли, образованной сильным основанием;
б) из слабого основания и его соли, образованной сильной кислотой.
На практике часто применяют следующие буферные смеси: ацетатный буфер CH3COOH + CH3COONa, бикарбонатный буфер H2CO3+NaHCO3, аммиачный буфер NH4OH +NH4Cl, белковый буфер белок кислота + белок соль, фосфатный буфер NaH2PO4 + Na2 HPO4
Рассмотрим механизм буферного действия. При добавлении соляной кислоты к ацетатному буферу происходит взаимодействие с одним из компонентов смеси (СНзСООН); Из уравнения (а), сильная кислота заменяется эквивалентным количеством слабой кислоты (в данном случае НСl заменяется СН3СООН). В соответствии с законом разведения Оствальда повышение концентрации уксусной кислоты понижает степень ее диссоциации, а в результате этого концентрация ионов Н + в буфере увеличивается незначительно. При добавлении к буферному раствору щелочи концентрация водородных ионов и рН изменяется также незначительно. Щелочь при этом будет реагировать с другим компонентом буфера, (СН3СООН) по реакции нейтрализации. В результате этого добавленная щелочь заменяется эквивалентным количеством слабоосновной соли, в меньшей — степени влияющей на реакцию среды. Анионы СНзСОО
, образующиеся при диссоциации этой соли, будут оказывать некоторое Угнетающее действие на диссоциацию уксусной кислоты.
Буферные растворы в зависимости от своего состава делятся на 2 основных типа: кислотные и основные.
31.Емкость буферных растворов и факторы, определяющие её. Буферные системы крови. Водородкарбонатный буфер. Фосфатный буфер.
Способность растворов поддерживать постоянное значение pH небезгранична. Буферные смеси можно различить по силе оказываемого ими сопротивления по отношению к действию кислот и оснований, вводимых в буферный раствор.
Количество кислоты или щелочи, которое нужно добавить к 1 л буферного раствора, чтобы значение его pH изменилось на единицу, называют буферной емкостью.
Таким образом, буферная емкость является количественной мерой буферного действия раствора. Буферный раствор имеет максимальную буферную емкость при pH = pK кислоты или основания, образующей смесь при соотношении ее компонентов, равном единице. Чем выше исходная концентрация буферной смеси, тем выше ее буферная емкость. Буферная емкость зависит от состава буферного раствора, концентрации и соотношения компонентов.
Нужно уметь правильно выбрать буферную систему. Выбор определяется необходимым интервалом pH. Зона буферного действия определяется силовым показателем кислоты (основания) ±1 ед.
При выборе буферной смеси необходимо учитывать химическую природу ее компонентов, так как вещества раствора, к которым добав-
ляется буферная система, могут образовывать нерастворимые соединения, взаимодействовать с компонентами буферной системы.