Что называется бензольным кольцом
Что такое бензольное кольцо
Содержание статьи
Специфика строения бензола
В далеком 1825 году, Майкл Фарадей английский естествоиспытатель, исследовал ворвань. При ее термическом разложении выделилось вещество с сильным запахом. Молекулярная его формула была С6Н6. Именно это соединение сегодня называют простейшим ароматическим углеводородом, или бензолом.
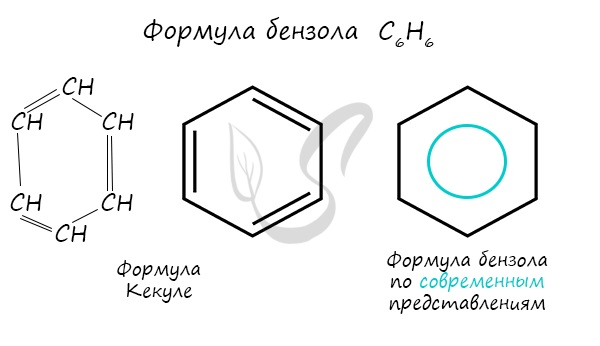
Структурная формула, предложенная уже немецким химиком Кекуле в 1865 году, получила широкое распространение. Она представляет собой чередующиеся одинарные и двойные связи между атомами углерода, замыкаясь в кольцо. Когда Кекуле работал над этой темой, во сне он увидел змею, что кусала себя хвост. Благодаря этому сну он сумел создать бензольное кольцо структурно, определил пространственное положение атомов углерода относительно друг друга.
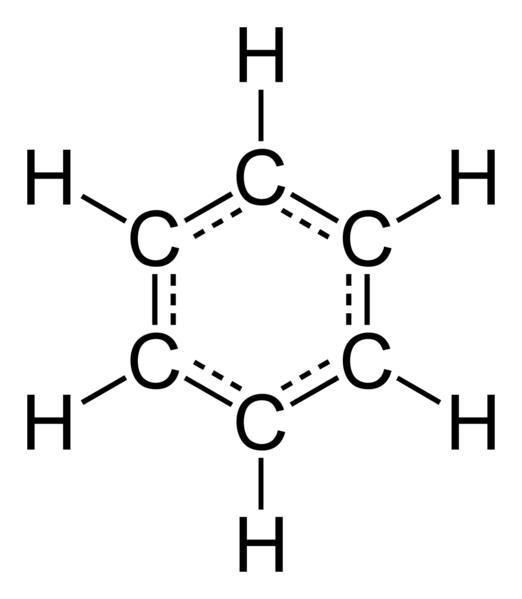
В молекуле бензола привычные одинарные и двойные связи между атомами углерода отсутствуют, они одинаково равноценны, представляют собой промежуточные, так называемые полуторные, связи. С их помощью образованное единственное бензольное кольцо, в других веществах этот вид связи не встречается. Особенностью бензольного кольца является то, что все атомы, входящие в состав этого вещества, находятся в одной плоскости, и каркас его образуют атомы углерода, создавая правильный шестиугольник. Все валентные углы составляют 120 градусов, они равны.
Орбитали бензола
Каждый атом углерода в молекуле бензола имеет одинаковую электронную плотность. Состояние каждого из них – sр2-гибридизация. Из этого видно, что гибридизированы всего три орбитали, одна – s, и две – р. Одна р-орбиталь остается негибридной. Две гибридные р-орбитали перекрыты с двумя смежными атомами углерода, s-орбиталь водорода перекрывается с третьей орбиталью. Негибридная р-орбиталь имеет форму гантели, она расположена под углом в 90 градусов к s-орбитали.
В результате того, что у бензола р-орбиталь каждого атома углерода перекрывается с двумя смежными аналогичными р-орбиталями атомов, получается, что смежные электроны между собой взаимодействуют, образуют р-электронное облако, единое для всех атомов. Графически оно изображается в виде кольца внутри правильного шестигранника.
Физико-химические свойства бензола
Бензол со своими гомологами представляют собой специфически пахнущие жидкости, не имеющие цвета. Их удельный вес меньше, чем у воды, в ней они не растворяются, но в органических жидкостях, таких как ацетон, эфир и спирт, растворяются легко.
Прочность у ядра бензола очень высокая, благодаря этому он легко вступает в операции замещения. Атомы водорода в ядре очень подвижны, по этой причине реакции сульфирования, галогенирования, нитрования протекают достаточно легко.
Бензол и его гомологи
Важно заметить, что двойные связи в молекуле бензола не фиксированы, а постоянно перемещаются по кругу.
Долгое время структурная формула бензола оставалась тайной. Предложенная Кекуле формула с тремя двойными связями не могла объяснить то, что бензол не вступает в реакции присоединения. Как уже было сказано выше, по современным представлениям двойные связи в молекуле бензола постоянно перемещаются, поэтому более верно рисовать их в виде кольца.
Номенклатура и изомерия аренов
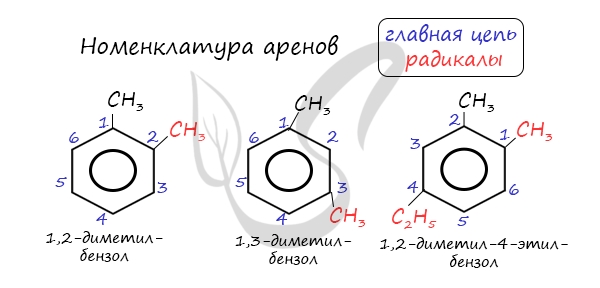
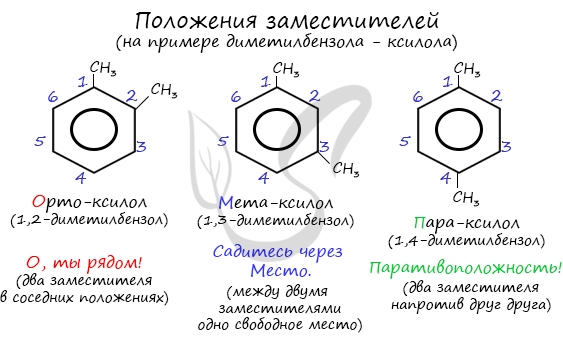
Для аренов характерна структурная изомерия, связанная с положением заместителей. Например, два заместителя в бензольном кольце могут располагаться в разных положениях.
Название положения заместителей в бензольном кольце формируется на основе их расположения относительно друг друга. Оно обозначается приставками орто-, мета- и пара. Ниже вы найдете мнемонические подсказки для их успешного запоминания 😉
Получение аренов
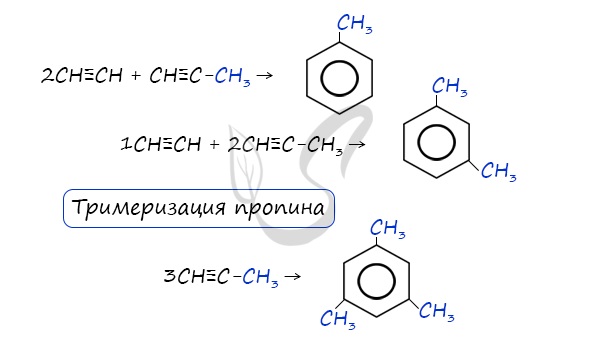
В случае, если к ацетилену добавить пропин, то становится возможным получение толуола. Увеличивая долю пропина, в конечном итоге можно добиться образования 1,3,5-триметилбензола.
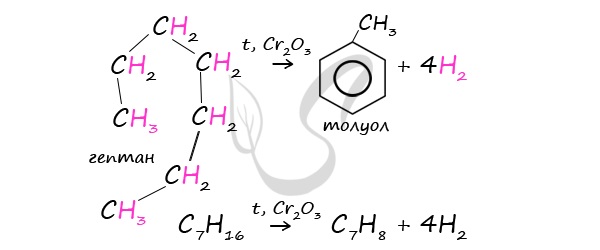
При дегидроциклизации гептана получается толуол.
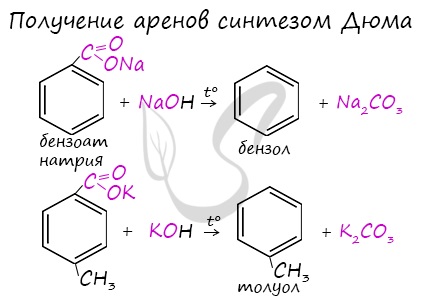
Синтез Дюма заключается в сплавлении солей карбоновых кислот с щелочами. В результате такой реакции возможно образование различных органических веществ, в том числе аренов.
Химические свойства аренов
Запомните, что, в отличие от других непредельных соединений, бензол и его гомологи не обесцвечивают бромную воду и раствор перманганата калия.
При повышенной температуре и наличии катализатора, водород способен разорвать двойные связи в бензольном кольце и превратить арен в циклоалкан.
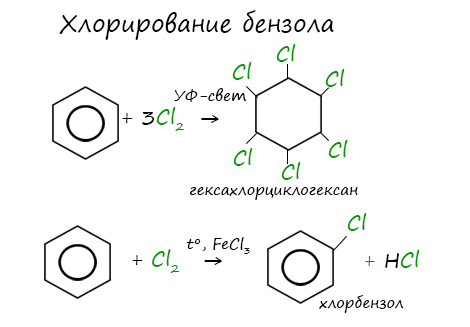
Реакция бензола с хлором на свету приводит к образованию гексахлорциклогексана, если же использовать только катализатор, то образуется хлорбензол.
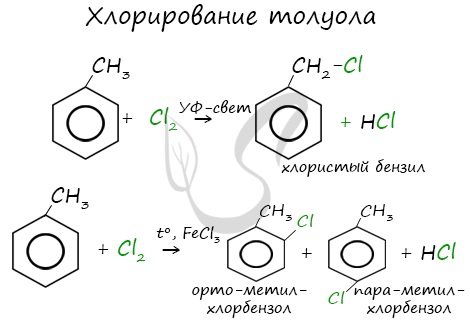
Реакции с толуолом протекают иначе: при УФ-свете хлор направляется в радикал метил и замещает атом водорода в нем, при действии катализатора хлор замещает один атом водорода в бензольном кольце (в орто- или пара-положении).
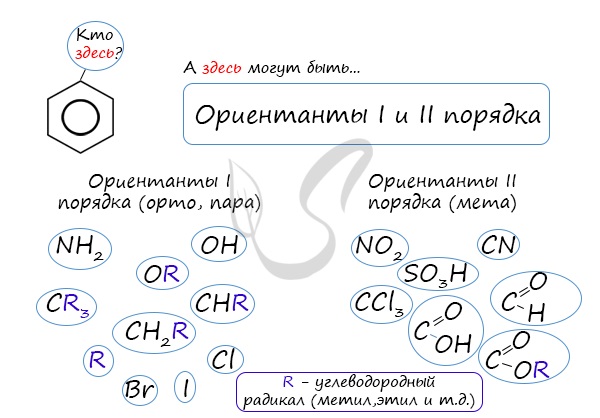
Почему хлор направляется именно в орто- и пара-положения относительно метильной группы? Здесь самое время коснуться темы ориентантов I (орто-, пара-ориентантов) и II порядков (мета-ориентанты).
К ориентантам первого порядка относятся группы: NH2, OH, OR, CR3, CHR2, CH2R, галогены. К ориентантам второго: NO2, CN, SO3H, CCl3, CHO, COOH, COOR.
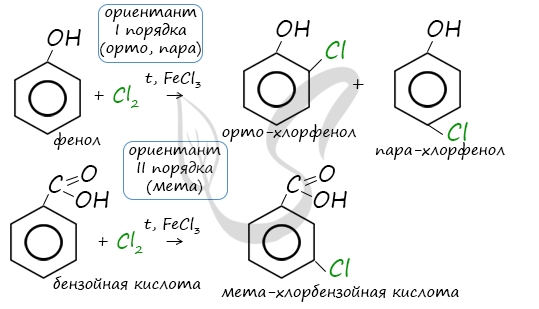
Например, ориентант I порядка, гидроксогруппа OH, обеспечивает протекание хлорирования в орто- и пара-положениях. А карбоксильная группа COOH, ориентант II порядка, обуславливает хлорирование в мета-положениях.
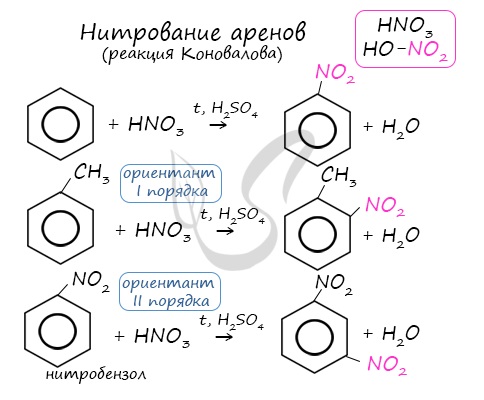
Арены вступают в реакции нитрования, протекающие при повышенной температуре и в присутствии серной кислоты, обладающей водоотнимающими свойствами.
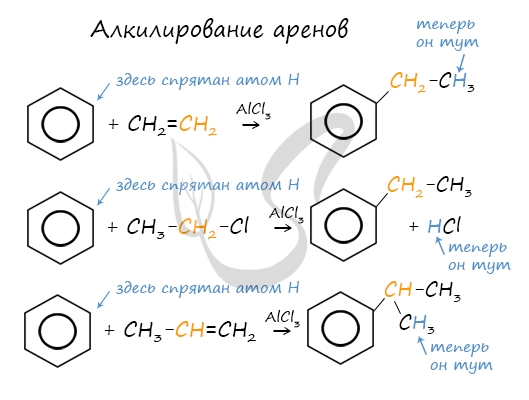
Алкилирование аренов осуществляется путем введения алкильного радикала в молекулу бензола. Алкильным радикалом чаще всего выступает алкен или галогеналкан. В подобных реакциях используют катализатор AlCl3.
В случае если для алкилирования используется алкен, то с молекулой бензола соединяется наименее гидрированный атом углерода алкена, прилежащий к двойной связи. Один атом водорода переходит из бензольного кольца к радикалу.
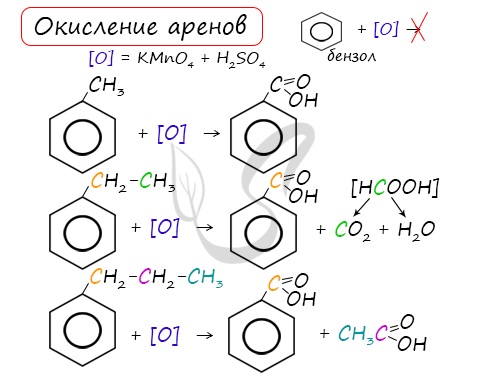
Арены, как и все органические вещества, сгорают с образованием углекислого газа и воды.
При неполном окислении гомологи бензола способны окисляться до бензойной кислоты (при подкислении раствора серной кислотой). Сам бензол не вступает в реакцию окисления с KMnO4, не обесцвечивает его раствор.
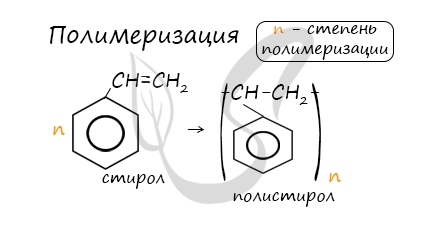
В реакцию полимеризации способен вступать стирол (винилбензол), в радикале которого содержится двойная связь.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Ароматические УВ. Бензол
Ароматические УВ (арены) – это УВ, молекулы которых содержат одно или несколько бензольных колец.
Примеры ароматических УВ:
Арены ряда бензола (моноциклические арены)
Общая формула: CnH2n-6, n≥6
Простейшим представителем ароматических УВ является бензол, его эмпирическая формула С6Н6.
Электронное строение молекулы бензола
Общая формула моноциклических аренов CnH2n-6 показывает, что они являются ненасыщенными соединениями.
В 1856 г. немецкий химик А.Ф. Кекуле предложил циклическую формулу бензола с сопряженными связями (чередуются простые и двойные связи) — циклогексатриен-1,3,5:
Такая структура молекулы бензола не объясняла многие свойства бензола:
Современная теория для объяснения строения молекулы С6Н6 использует представление о гибридизации орбиталей атома углерода.
Каждый атом углерода имеет один р-электрон, который не участвует в гибридизации. Негибридизованные р-орбитали атомов углерода находятся в плоскости, перпендикулярной плоскости σ-связей. Каждое р-облако перекрывается с двумя соседними р-облаками, и в результате образуется единая сопряженная π-система (вспомните эффект сопряжения р-электронов в молекуле бутадиена-1,3, рассмотренный в теме «Диеновые углеводороды»):
Сочетание шести σ-связей с едиой π-системой называется ароматической связью.
Цикл из шести атомов углерода, связанных ароматической связью, называется бензольным кольцом, или бензольным ядром.
В соответствии с современными представлениями об электронном строении бензола молекулу С6Н6 изображают следующим образом:
Физические свойства бензола
Бензол при обычных условиях — бесцветная жидкость; t o пл= 5,5 о С; t o кип. = 80 о С; имеет характерный запах; не смешивается с водой, хороший растворитель, сильно токсичен.
Химические свойства бензола
Ароматическая связь определяет химические свойства бензола и других ароматических УВ.
6π-электронная система является более устойчивой, чем обычные двухэлектроиные π-связи. Поэтому реакции присоединения менее характерны для ароматических УВ, чем для непредельных УВ. Наиболее характерными для аренов являются реакции замещения.
I. Реакции замещения
1.Галогенирование
2.Нитрование
Реакцию осуществляют смесью концентрированных азотной HNO3 и серной H2SO4 кислот (нитрующая смесь):
3.Сульфирование
4.Алкилирование (замещение атома «Н» на алкильную группу) – реакции Фриделя-Крафтса, образуются гомологи бензола:
Вместо галогеналканов можно использовать алкены (в присутствии катализатора – AlCl3 или неорганической кислоты):
II. Реакции присоединения
1.Гидрирование
2.Присоединение хлора
III. Реакции окисления
2. Неполное окисление (KMnO4 или K2Cr2O7 в кислой среде). Бензольное кольцо устойчиво к действию окислителей. Реакция не происходит.
Получение бензола
1) переработка нефти и угля;
2) дегидрирование циклогексана:
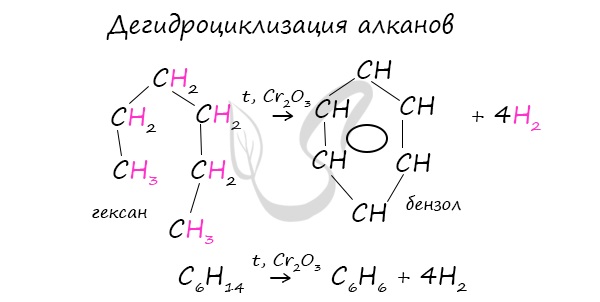
3) дегидроциклизация (ароматизация) гексана:
В лаборатории:
Сплавление солей бензойной кислоты со щелочами:
Изомерия и номенклатура гомологов бензола
Любой гомолог бензола имеет боковую цепь, т.е. алкильные радикалы, связанные с бензольным ядром. Первый гомолог бензола представляет собой бензольное ядро, связанное с метильным радикалом:
Толуол не имеет изомеров, поскольку все положения в бензольном ядре равноценны.
Для последующих гомологов бензола возможен один вид изомерии – изомерия боковой цепи, которая может быть двух видов:
1) изомерия числа и строения заместителей;
2) изомерия положения заместителей.
Физические свойства толуола
Толуол — бесцветная жидкость с характерным запахом, не растворимая в воде, хорошо растворяется в органических растворителях. Толуол менее токсичен, чем бензол.
Химические свойства толуола
I. Реакции замещения
1.Реакции с участием бензольного кольца
Метилбензол вступает во все реакции замещения, в которых участвует бензол, и проявляет при этом более высокую реакционную способность, реакции протекают с большей скоростью.
Метильный радикал, содержащийся в молекуле толуола, является заместителем рода, поэтому в результате реакций замещения в бензольном ядре получаются орто- и пара-производные толуола или при избытке реагента — трипроизводные общей формулы:
а) галогенирование
При избытке галогена можно получить ди- и три- замещенные производные в соответствии с правилами ориентации:
б) нитрование
в) сульфирование
г) алкилирование
2. Реакции с участием боковой цепи
Метильная группа в метилбензоле может вступать в реакции, характерные для алканов:
При дальнейшем хлорировании можно получить дихлорметилбензол и трихлорметилбензол:
II. Реакции присоединения
Гидрирование
III.Реакции окисления
2. Неполное окисление
В отличие от бензола его гомологи окисляются некоторыми окислителями; при этом окислению подвергается боковая цепь, в случае толуола – метильная группа. Мягкие окислители типа MnO2 окисляют его до альдегидной группы, более сильные окислители (KMnO4) вызывают дальнейшее окисление до кислоты:
Любой гомолог бензола с одной боковой цепью окисляется сильным окислителем типа KMnO4 в бензойную кислоту, т.е. происходит разрыв боковой цепи с окислением отщепившейся части ее до СО2; например:
При наличии нескольких боковых цепей каждая из них окисляется до карбоксильной группы и в результате образуются многоосновные кислоты, например:
Получение толуола:
В промышленности:
1) переработка нефти и угля;
2) дегидрирование метилциклогексана:
3) дегидроциклизация гептана:
В лаборатории:
1) алкилирование по Фриделю-Крафтсу;
2) реакция Вюрца-Фиттига (взаимодействие натрия со смесью галогенбензола и галогеналкана):
Похожее
Добавить комментарий Отменить ответ
Репетитор по химии. Занятия проходят онлайн по Скайпу. По всем вопросам пишите в Ватсапп: +7 928 285 70 42
Что называется бензольным кольцом
6. АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ (АРЕНЫ)
Ароматическими первоначально называли органические соединения. которые или сами имели приятный запах, или же выделялись из природных веществ, обладающих приятным запахом. В последствии среди них были обнаружены соединения с приятным и неприятным запахом, а также соединения без запаха. Однако название за большой группой органических соединений, проявляющих сходные с бензолом свойства, сохранилось.
К ароматическим углеводородам или аренам относятся соединения, молекулы которых содержат одно или несколько бензольных колец.
В зависимости от числа бензольных циклов, входящих в состав молекулы, различают одноядерные (моноциклические) и многоядерные (полициклические) арены.
Простейшим представителем одноядерных ароматических соединений является бензол (С6Н6).
Впервые бензол был получен английским ученым М. Фарадеем в 1825 г. из светильного газа, образующегося в процессе переработки каменного угля. Однако строение его молекулы в течение многих лет оставалось загадкой для химиков. Несмотря на то, что формула С6Н6 предполагает достаточно выраженный ненасыщенный характер, бензол, в отличие от непредельных соединений, оказался относительно инертным веществом. Он сравнительно устойчив к нагреванию и действию окислителей, практически не вступает в характерные для ненасыщенных соединений реакции присоединения. Наоборот, для бензола более характерными оказались не свойственные непредельным соединениям реакции замещения.
Составу С6Н6 приписывались разные структурные формулы, но все они не объясняли в полной мере химических свойств бензола.
В 1865 г. немецкий химик Кекуле предложил формулу бензола, представляющую собой цикл из шести атомов углерода с чередующимися простыми и двойными связями:
Формула Кекуле предполагает равноценность всех атомов углерода и водорода в молекуле.
В соответствии с формулой Кекуле бензол должен иметь два 1,2-дизамещенных изомера:
Экспериментально же было установлено, что 1,2-дизамещенные производные бензола не имеют изомеров положения, т. е. они существуют в виде одного соединения.
Для объяснения этого противоречия в 1872 г. Кекуле выдвинул осцилляционную гипотезу, согласно которой двойные связи в молекуле не фиксированы, а непрерывно перемещаются (осциллируют) между двумя возможными положениями:
Правильно отображая некоторые свойства бензола, формула Кекуле тем не менее не согласовывалась с рядом установленных фактов. Все это возвращало химиков к пересмотру структуры бензола.
Образование замкнутой сопряженной системы (ароматического секстета) является для молекулы бензола энергетически выгодным. Экспериметально установлено, что сопряжение в цикле приводит к уменьшению энергии на 150.7 кДж/моль, по сравнению с рассчитанной для циклогексатриена. Эта разность составляет энергию сопряжения.
В бензольном кольце нет простых и двойных связей в прямом понимании этого слова. Такую связь называют ароматической. Если длина простой связи С–С в алканах составляет 0,154 нм, длина двойной связи в алкенах – 0,134 нм, то длина С–С связи в молекуле бензола равна 0,140 нм, т. е. является промежуточной между длиной одинарной и двойной связи.
Совокупность специфических свойств бензола – высокая стабильность, инертность в реакциях присоединения, склонность к реакциям замещения, получила общее название «ароматичность», или «ароматические свойства».
Что же требуется для того, чтобы мы имели право отнести соединение к ароматическому ряду?
а) для проявления ароматического характера молекула должна прежде всего иметь плоское строение;
б) молекула должна иметь замкнутую сопряженную систему;
в) количество π- электронов должно соответствовать формуле 4n+ 2, где п = 0, 1, 2, 3 и т. д. (данная закономерность была сформулирована в 1931 г. немецким ученым Э. Хюккелем).
Номенклатура и изомерия
По заместительной номенклатуре ИЮПАК одноядерные арены рассматривают как производные бензола.
При наличии в кольце двух и более заместителей их положение указывают цифрами. Нумерацию атомов углерода бензольного кольца осуществляют таким образом, чтобы заместители имели возможно меньшие номера.
В дизамещенных производных бензола наряду с цифровым обозначением положений заместителей применяют приставки: орто-(о-) положение – 1,2; мета-(м-) положение – 1,3 и пара-(п-) положение – 1,4.
Кроме названий по заместительной номенклатуре сохранились и тривиальные названия: толуол, ксилол, кумол и др.
Одновалентные радикалы аренов имеют общее название – арилы (Аr). Двухвалентные радикалы бензола называют фениленами (о-, м-, п-)
Изомерия гомологов бензола обусловлена разными структурами, числом и положением заместителей в бензольном кольце.
Для однозамещенных гомологов бензола характерна изомерия, связанная с разной структурой заместителя.
Дизамещенные производные бензола существуют в трех изомерных формах, в зависимости от взаимного расположения в бензольном кольце (изомеры положения).
Для тризамешенных бензолов с одинаковыми заместителями в бензольном кольце существуют также три изомера:
Способы получения аренов
1. Циклотримеризация алкинов
Ацетилен пропускают над активированным углем при повышенной температуре. Реакция была открыта Зелинским.
2. Обработка ацетона конц. H2S04
3. Дегидрогенизация алициклических соединений
Эта реакция показывает взаимосвязь между ароматическими и алициклическими соединениями.
4. Реакция Вюрца – Фиттига
Эта реакция чаще всего используется для получения гомологов бензола.
5. Алкилирошние ароматических углеводородов по Фриделю – Крафтсу.
Бензол и его низшие гомологи представляют собой жидкости, обладающие специфическим запахом. Ароматические углеводороды не растворимы в воде и хорошо растворяются в органических растворителях. Многие из них сами являются хорошими растворителями для других органических веществ. Из-за высокого содержания углерода горят коптящим пламенем.
Реакционная способность бензола и его гомологов определяется главным образом наличием в структуре замкнутой π- электронной системы, которая является областью повышенной электронной плотности. Ароматические углеводороды, как и алкены, обладают нуклеофильным характером. Однако, в отличие от ненасыщенных соединений, при взаимодействии с электрофильными реагентами арены более склонны к реакциям замещения, а не присоединения, поскольку при этом сохраняется их ароматический характер. Эти реакции носят название реакций электрофильного замещения SE.
Реакции присоединения для аренов менее характерны, так как они приводят к нарушению ароматичности, с трудом вступают ароматические углеводороды и в реакции окисления.
I. Реакции электрофильного замещения (SE)
Образование σ- комплекса является наиболее высокоэнергетичной стадией реакции, определяющей ее скорость. σ- Комплекс не устойчив, он отщепляет протон от атома углерода, связанного с электрофилом, благодаря чему восстанавливается ароматичность бензольного кольца.
К наиболее важным реакциям SЕ относятся реакции нитрования, сульфирования, галогенирования, алкилирования и ацилирования.
1. Нитрование. В качестве нитрующих агентов чаше используют концентрированную азотную кислоту или смесь концентрированной азотной и серной кислот (нитрующая смесь):
Атакующей электрофильной частицей в реакции является ион нитрония N02+, который образуется в результате кислотно-основного взаимодействия между азотной и серной кислотами, где азотная кислота играет роль основания:
2. Сульфирование – это процесс замещения атома водорода в бензольном ядре на сульфогруппу – S03H. Для сульфирования бензола и его гомологов применяют концентрированную серную кислоту или олеум (раствор триоксида серы S03 в серной кислоте):
Особенности механизма сульфирования аренов изучены недостаточно. Однако экспериментальные данные свидетельствую о том, что атакующей электрофильной частицей служит триоксид серы SO3
3. Галогенирование. Бензол и его гомологи хлорируются, бромируются и йодируются. Замещение атома водорода в бензольном ядре на атом хлора или брома осуществляют в присутствии катализаторов – кислот Льюиса (А1С13, FeBr,, ZnCl2 и др.):
Под действием катализатора молекула галогена поляризуется. Атакующей электрофильной частицей служит либо комплекс поляризованной молекулы галогена с кислотой Льюиса, либо катион галогена, образующийся в процессе ионизации данного комплекса:
4. Алкилирование по Фриделю – Крафтсу. Для введения алкильной группы в молекулу ароматического соединения в качестве электро-фильных реагентов чаше всего используют галогеналканы. Взаимодействие происходит в присутствии катализаторов – кислот Льюиса:
Атакующей электрофильной частицей является карбкатион, который образуется при взаимодействии алкилирующего агента и катализатора:
Для алкилирования аренов также могут быть использованы спирты (реакции протекают в присутствии кислот Льюиса или минеральных кислот – H3P04, H2S04) или алкены (в этом случае алкилирование требует присутствия кислот Льюиса и минеральной кислоты как источника протонов).
По своему механизму реакция алкилирования аналогична реакциям нитрования, сульфирования и галогенирования.
5. Ацилирование по Фриделю – Крафтсу. Ацилированием называют процесс введения в молекулу органического соединения ацильной группы RCO.
Ацилирование бензола и его гомологов обычно осуществляют галогенангидридами карбоновых кислот в присутствии кислот Льюиса:
Электрофилом, атакующим бензольное кольцо, является либо ацилиевый ион 

Для введения ацильной группы могут быть использованы и ангидриды карбоновых кислот.
II. Реакции присоединения
Реакции присоединения не характерны для аренов, они протекают в жестких условиях.
1. Гидрирование. При повышенных температуре и давлении, в присутствии катализаторов (мелкопористый никель – никель Ренея) бензол и его гомологи присоединяют три молекулы водорода:
Остановить реакцию на стадии образования продуктов частичного гидрирования невозможно, поскольку они гидрируются значительно легче, чем сам бензол.
2. Хлорирование. При интенсивном солнечном освещении или под действием ультрафиолетового излучения бензол присоединяет хлор. Реакция протекает по радикальному механизму с образованием гексахлорциклогексана:
III. Реакции окисления
1. Окисление бензольного цикла. Бензольное кольцо устойчиво к действию окислителей. В обычных условиях ни перманганат калия, ни азотная кислота, ни оксид хрома (VI), ни другие сильные окислители не окисляют бензол. В жестких же условиях, например, при действии кислорода воздуха в присутствии оксида ванадия (V205), при температуре 400-500 º С бензольное ядро окисляется, образуя малеиновый ангидрид:
2. Окисление гомологов бензола. Алкилбензолы, в отличие от незамещенного бензола, окисляются значительно легче. В этом случае при действии сильных окислителей (КМn04, K2Cr2O7 и др.) подвергаются окислению боковые цепи:
Продуктами реакции являются ароматические карбоновые кислоты. Каждый алкильный радикал в бензольном кольце, независимо от длины углеродной цепи, окисляется до карбоксильной группы.
3. Озонирование. Подобно алкенам, бензол и его гомологи реагируют с озоном, образуя продукты присоединения, – триозониды:
Триозониды взрывоопасны. Это маслянистые жидкости, они нестойкие и под действием влаги разрушаются с образованием дикарбонильных соединений и продуктов их дальнейшего окисления – дикарбоновых кислот.
Правила ориентации в бензольном ядре
В молекуле незамещенного бензола электронная плотность распределена равномерно, поэтому электрофильный реагент может атаковать в равной степени любой из шести атомов углерода.
По влиянию на направление реакций электрофильного замещения и реакционную способность бензольного кольца заместители можно разделить на две группы – заместители I рода (орто-, пара- ориентанты) и заместители II рода (мета-ориентанты).
Заместители I рода – атомы и атомные группы, проявляющие положительный индуктивный (+I) или положительный мезомерный (+M) эффекты (доноры электронов):
Заместители I рода (за исключением галогенов) увеличивают электронную плотность в бензольном кольце, тем самым активируют его в реакциях SE и направляют следующие заместители в орто- и пара- положения.
Заместители II рода – группы, проявляющие отрицательный индуктивный (-1) или отрицательный мезомерный (-М) эффекты (электроноакцепторы):
При введении третьего заместителя необходимо учитывать природу двух уже имеющихся в бензольном ядре.
Ориентация в дизамещенных производных бензола
В зависимости от электронной природы заместителей и их взаимного расположения различают согласованную и несогласованную ориентацию.
При согласованной ориентации оба заместителя направляют новый заместитель в одни и те же положения бензольного кольца. Согласованная ориентация характерна для дизамещенных производных бензола, в которых соблюдаются условия:
При несогласованной (несовпадающей) ориентации один из заместителей направляет новую группу в одни, а другой – в иные положения бензольного кольца. Предпочтительное направление замещения можно определить, используя следующие правила:
1) если один из заместителей является ориентантом I рода, он определяет направление замещения:
2) если оба заместителя являются ориентантами I рода, направление замещения определяется более сильным ориентантом:
3) если оба заместителя являются ориентантами II рода, замещение осуществляется с трудом, а место вхождения третьего заместителя определяется более сильным ориентантом:
Наряду с электронной природой заместителей на соотношение продуктов замещения оказывают влияние пространственные факторы.
Ароматические углеводороды, содержащие два и более бензольных ядер, относятся к многоядерным аренам.
В зависимости оттого, каким образом связаны бензольные кольца, многоядерные арены делятся на две группы:
МНОГОЯДЕРНЫЕ АРЕНЫ С КОНДЕНСИРОВАННЫМИ БЕНЗОЛЬНЫМИ ЦИКЛАМИ
Конденсированные многоядерные арены содержат в своем составе два или более бензольных ядра, имеющих общие атомы углерода.
Наиболее важными представителями конденсированных аренов являются нафталин, антрацен и фенантрен.
Нафталин состоит из двух конденсированных бензольных колец. Два атома углерода (9 и 10) общие для двух колец.
В отличие от бензола атомы углерода в молекуле нафталина неравноценны. Положения 1, 4, 5, 8 равнозначны, их принято обозначать буквой α и называть α- положениями. Положения 2, 3, 6 и 7 также равнозначны и их обозначают буквой β и называют β- положениями.
Для монозамешенного нафталина возможно 2 изомера ( α- и β-), а при наличии двух одинаковых заместителей – 10 изомеров.
Радикалы нафталина называют нафтилами:
1. Природные источники. В промышленности нафталин, главным образом, получают из каменноугольной смолы, где его содержание составляет около 10 %. Наряду с нафталином из каменноугольной смолы выделяют также некоторые его моно- и диметильные производные.
2. Получение нафталина из ацетилена. При пропускании ацетилена через нагретые до 700–800 º С трубки наряду с бензолом образуется также и нафталин.
Нафталин – бесцветное кристаллическое вещество с характерным запахом, сублимируется при 81 °С. Не растворяется в воде, растворяется в органических растворителях. Применяется в быту для борьбы с молью, в химии красителей, для получения лекарств, пластмасс, глифталевых смол.
Электронное строение нафталина сходно со строением бензола. Его молекула плоская. Дипольный момент равен нулю, но электронная плотность распределена не так равномерно, как в молекуле бензола. Более высокая электронная плотность α- положений нафталина делает их более реакционноспособными по сравнению с β- положениями.
Длина связей в молекуле нафталина разная.
Химические свойства нафталина
Нафталин, как и бензол, проявляет свойства ароматических соединений и для него характерны, прежде всего, реакции электрофильного замещения, но он также легко вступает в реакции присоединения и окисления.
1. Реакции электрофильного замещения. В реакции электрофильного замещения (нитрование, сульфирование, галогенирование) нафталин вступает значительно легче бензола. При этом образуются в основном продукты α- замещения. Это обусловлено тем, что в α- положении нафталинового ядра выше электронная плотность и при атаке в α- положение образуется более стабильный σ- комплекс, чем в β- положении:
Как видно, при атаке α- положения делокализация положительного заряда в α- комплексе происходит с сохранением ароматичности одного из бензольных ядер в возможных резонансных структурах.
В случае атаки электрофилом β- положення, лишь в одном случае возможно сохранение ароматичности бензольного ядра. Следовательно, замещение по α- положению энергетически более выгодно.
Нитрование. Нафталин довольно легко нитруется нитрующей смесью с образованием в основном α- изомера:
Сульфирование. Для сульфирования нафталина используют концентрированную H2S04, причем в зависимости от температуры, при которой проводится реакция, получают α- или β- продукты замещения. При температуре 80 º С реакционной среды образуется α- нафталинсульфокислота, а при 160 °С – β- нафталинсульфокислота:
При нагревании α- изомера до температуры 160 °С он полностью превращается в β- нафталинсульфокислоту.
Галогенирование. При температуре 90–110 °С в присутствии катализатора – FeCl3, нафталин хлорируется с образованием преимущественно α- хлорнафталина. Реакция протекает по механизму SE:
Галогенирование нафталина возможно и без катализатора. Тогда вначале протекает реакция присоединения галогена, а затем отщепления галоген водорода. Например, при взаимодействии брома с нафталином, бром присоединяется в положения 1 и 4, а затем продукт присоединения отщепляет молекулу бромводорода, образуя α- бромнафталин:
Правила ориентации в нафталиновом ядре
Правила ориентации в нафталиновом ядре имеют свои особенности.
Направление электрофильного замещения в монозамещенных производных нафталина определяется электронной природой уже имеющегося заместителя и большей реакционной способностью ос-положения.
При наличии в нафталиновом ядре электронодонорного заместителя электронная плотность повышается прежде всего в том кольце, с которым связан заместитель, и поэтому реакция электрофильного замещения происходит именно в этом кольце. Замещение, прежде всего, идет по 4 положению ( α- положение).
Электроноакцепторный заместитель понижает электронную плотность в нафталиновом ядре и прежде всего в том кольце, с которым он связан. Поэтому реакции идут с участием атомов углерода второго бензольного ядра.
Так как ос-положения более реакционноспособны, то замещение происходит преимущественно в положения 5 и 8.
Например, нитрирование 1-нитронафталина нитрующей смесью приводит к образованию смеси изомеров:
2. Реакции присоединения
Реакция восстановления. Присоединение водорода идет вначале по α- положению. Затем образуется 1,2,3,4-тетрагидронафталин, который при 200 °С гидрируется с образованием декагидронафталина – декалина:
Тетралин используется как топливо и растворитель для жиров и смол Декалин используется как растворитель для лаков, является заменителем скипидара.
3. Реакции окисления
В отличие от бензольного, нафталиновое ядро легко окисляется и при окислении гомологов нафталина окисляется само ядро. Например:
Окисление нафталина в присутствии V205 приводит к образованию фталевого ангидрида:
Это многоядерное соединение, состоящее из трех линейно конденсированных бензольных колец.
В молекуле антрацена нумеруются лишь атомы углерода, несушие водород. Положения 1,4, 5, 8 – называют α- положениями; 2, 3, 6, 7 – β- положениями; 9, 10 – γ- положениями или μ- ( мезо – средний) положениями. При одном заместителе в ядре возможно 3 изомера – α, β, γ.
Антрацен находится в каменноугольном дегте, а именно в антраценовом масле, в количестве 0,5 %, откуда его и добывают в промышленности.
В лаборатории можно получить антрацен по реакции Фриделя – Крафтса из бензола и 1,1,2,2-тетрабромэтана в присутствии А1Br3:
Антрацен – это бесцветное кристаллическое вещество, tпл равна 217 °С, перегоняющееся с водяным паром, растворимо в бензоле, эфире, нерастворимо в Н,0. Растворы обладают голубой флюоресценцией.
1. Реакция восстановления. Антрацен легко присоединяет водород с образованием 9,10-дигидроантрацена. Дальнейшее его гидрирование приводит к пергидроантрацену.
2. Реакции замещения. Галогенирование антрацена происходит по механизму присоединения-отщепления. Например:
Нитрование антрацена азотной кислотой в среде уксусной кислоты при комнатной температуре ведет к образованию 9-нитроантрацена. В результате сульфирования антрацена серной кислотой при нагревании образуются α- и β- изомеры, которые являются более устойчивыми, чем γ-.
3. Реакция окисления. Антрацен очень легко окисляется концентрированной азотной кислотой или хромовой смесью до антрахинона.
Антрахинон – это желтое кристаллическое вещество, обладающее свойствами хинонов.
Структурным изомером антрацена является фенантрен. В антрацене три бензольных кольца соединены линейно, тогда как в фенантрене они соединяются ангулярно, т. е. под углом.
С увеличением числа ароматических колец в многоядерных соединениях растет число монозамешенных изомеров: так для нафталина возможны два продукта ( α, β). для антрацена – три. для фенантрена – 5.
Цифрами обозначены положения, в которых могут находиться заместители.
Получают фенантрен в основном из каменноугольной смолы.
Физические свойства фенантрена
Фенантрен – это твердое кристаллическое вещество с tпл 101 º С, tкип 340,2 °С. Растворяется в эфире, бензоле, трудно – в спирте. Растворы имеют голубую флуоресценцию.
Фенантрен, как и антрацен, обладает более слабым ароматическим характером, чем нафталин, и тем более, чем бензол. Электронная плотность в его молекуле распределяется неравномерно, ароматичность среднего бензольного кольца здесь настолько нарушена, что связь между 9 и 10 атомами углерода приобретает характер двойной связи. Реакции замещения протекают по механизму присоединения-отщепления.
Так. вначале присоединяется бром в 9 и 10 положениях с последующим отщеплением HBr и образованием 9-бромфенантрена:
9,10-Дибром-9,10-дигидрофенантрен может быть выделен в свободном состоянии.
При окислении фенантрена образуется фенанренхинон. При дальнейшем окислении идет разрыв связи С9–С10 и образуется дифеновая кислота:
При восстановлении фенантрена образуется продукт, который носит название пергидрофенантрен.
Конденсированная система пергидрофенантрена и циклопентана называется циклопентанпергидрофенантрен, или стеран.
Данная структура лежит в основе стероидов.
МНОГОЯДЕРНЫЕ АРЕНЫ С ИЗОЛИРОВАННЫМИ БЕНЗОЛЬНЫМИ ЦИКЛАМИ
Наиболее важными представителями этой группы соединений являются бифенил, дифенилметан и трифенилметан.
1. Бифенил выделяют из каменноугольной смолы, где он содержится в небольшом количестве.
2. Дегидрогенизация бензола. Пары бензола пропускают через раскаленные трубки. Выход бифенила достигает 70 %.
3. Реакция Ульмана. Нагревание йодбензола в присутствии порошка меди:
Бифенил – твердое вещество с tпл 70 °С, легко растворим в спирте. эфире.
Строение. Химические свойства
Вид пространственной изомерии, обусловленный ограничением свободного вращения вокруг простой связи, называется атропизомерией (от греч. атропо – нет поворота).
Нитрогруппа в молекуле 4-нитробифенила уменьшает электронную плотность, прежде всего в бензольном кольце, в котором она находится, поэтому вторая нитрогруппа вступает в незамещенное ядро.
В молекуле дифенилметана два бензольных цикла связаны через метиленовую группу. Нумерацию углеродных атомов в каждом цикле проводят отдельно:
Дифенилметан получают по реакции Фриделя – Крафтса алкилированием бензола бензилхлоридом или дихлорметаном:
Дифенилметан – твердое кристаллическое вещество с tпл 26– 27 º С и запахом герани, он легко растворим в спирте, диэтиловом эфире, хлороформе.
Для дифенилметана характерны реакции с участием бензольных циклов и активной метиленовой группы.
Атомы водорода метиленовой группы в молекуле дифенилметана подвижны вследствие электроноакцепторного действия фенильных групп. В результате дифенилметан легко окисляется:
Бензгидрол является исходным продуктом при получении димедрола – (C6H5)2CHOCH2CH2N(CH3)2HCl –антигистаминного средства.
Водородные атомы метиленовой группы также легко замещаются на галоген:
Дифенилметан используется в парфюмерной промышленности для отдушки мыл; некоторые его производные являются пестицидами.
В молекуле трифенилметана три бензольных цикла связаны через метиновую группу (СН):
Трифенилметан получают по реакции Фриделя–Крафтса из хлороформа и бензола:
Трифенилметан – кристаллическое вещество с tпл 76 °С, трудно растворимое в воде, легко – в органических растворителях.
По химическим свойствам трифенилметан во многом напоминает дифенилметан. Для него также характерны реакции электрофильного замещения с участием бензольных циклов и реакции с участием атома водорода мети новой группы.
Так, при действии амида натрия в жидком аммиаке трифенилметан образует трифенилметилнатрий:
Трифенилметилнатрий окрашен в желтый цвет, он имеет ионное строение, его эфирные растворы проводят электрический ток.
Стабильность трифенилметил-аниона и наличие окраски объясняется тем, что в делокализации отрицательного заряда принимают участие все три бензольных ядра:
При взаимодействии трифенилметана с хлором атом водорода СН-группы замешается на хлор, продуктом реакции является трифенилхлорметан. Атом хлора в его молекуле очень подвижен. При растворении трифенилхлорметана в жидком S02 (растворитель с высокой диэлектрической постоянной) в присутствии А1Сl3 происходит его ионизация с образованием трифенилметил-катиона:
При окислении трифенилметана образуется трифенил карбинол. который подвергается ионизации в концентрированной серной кислоте:
Устойчивость трифенилметил-катиона также обусловлена участием бензольных колец в делокализации положительного заряда за счет сопряжения:
При обработке трифенилхлорметана цинком в бензольном растворе образуется свободный трифенилметильный радикал, находящийся в равновесии со своим димером:
Трифенилметильный радикал – это первый радикал, полученный в свободном виде. Он был получен в 1900 г. американским химиком М. Гомбергом. Столь высокая устойчивость трифенил метила по сравнению с алкильными радикалами объясняется значительной делокализацией неспаренного электрона по всем бензольным кольцам.
Свободный радикал трифенилметила окрашен в желтый цвет.
Красители трифенилметанового ряда
К красителям трифенилметанового ряда относятся бриллиантовый зеленый и фенолфталеин.
Бриллиантиновый зеленый применяется в медицине в виде 1–2 % водных или спиртовых растворов как антисептическое средство, а также при изготовлении бактерицидных пластырей.
Фенолфталеин является представителем гидроксипроизводных трифенилметана. Получают фенолфталеин конденсацией фенола с фталевым ангидридом в присутствии концентрированной кислоты:
Фенолфталеин представляет собой белое кристаллическое вещество с tпл 259–263 °С, практически нерастворимое в воде, хорошо растворимое в этаноле. Фенолфталеин применяется в аналитической практике как кислотно-основный индикатор. В кислой и нейтральной среде он находится в бесцветной лактонной форме, в шелочной среде (при рН 8,2–10,0) приобретает малиновую окраску вследствие образования хиноидной структуры.
Фенолфталеин применяется в медицине как слабительное средство при хронических запорах.