Что значит сотовое легкое
Сотовое легкое (изменения по типу пчелиных сот)
Сотовое легкое представляет собой деструктивные и фиброзные изменения легочной ткани, содержащие многочисленные кистозные воздушные пространства с толстыми фиброзными стенками, отражающие поздние стадии различных заболеваний легких с полной потерей нормальной архитектоники ацинуса. Флейшнеровское сообщество определяет под данным термином группы кистозных воздушных образований (размерами 3-10 мм в диаметре, иногда до 2.5 см), которые обычно располагаются субплеврально и в базальных отделах. Стенки кист хорошо отграничены и имеют толщину 1-3 мм и выстланы метаплазированным эпителием. [2,4].
Диагностика
На рентгенограммах грудной клетки сотовое легкое проявляется как близко расположенные кольцевые тени, как правило, 3-10 мм в диаметре со стенками 1-3 мм в толщину, что напоминает соты. Их обнаружение подразумевает терминальные стадии заболевания легких.
При компьютерной томографии пчелиными сотами называют проявления легочного фиброза (обычной интерстициальной пневмонии) в виде сгруппированных кистозных воздушных пространств, как правило, диаметром порядка 3-10 мм, но иногда и до 2,5 см. Изменения, как правило, расположены субплеврально и характеризуются четко отграниченными стенками. Изменения по типу пчелиных сот отражают необратимые изменения при интерстициальных болезнях легких и подразумевают плохой прогноз. Термин должен использоваться с осторожностью, так как может оказать серьезное влияние на характер лечения.
Дифференциальный диагноз
Этимология
Впервые термин появился в 1949 году в исследованиях N Oswald и T Parkinson [3].
Диагностика и лечение идиопатического легочного фиброза
Общая информация
Краткое описание
Прежнее название: идиопатический фиброзирующий альвеолит не рекомендуется к использованию в связи с патоморфологическими особенностями заболевания – быстрым формированием фиброза.
Дата разработки протокола: 04.2013 г.
Категория пациентов: пациенты, страдающие идиопатическим фиброзом легких
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Диагностика
II. МЕТОДЫ, ПОДХОДЫ, ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Экстренная госпитализация производится без предварительного (амбулаторного) лабораторно-инструментального исследования.
Инструментальные критерии ИЛФ: основываются на характерных признаках обычной интерстициальной пневмонии (ОИП) по данным КТВР (таблица 1), гистопатологических критериях ОИП (таблица 2), данных функционального исследования.
Таблица 1. Критерии КТВР для картины ОИП [1, 4, 5].
| Картина ОИП (Все четыре признака) | Возможный рисунок ОИП (все три критерия) | Противоречит ОИП (любой из семи признаков) |
| Вероятная ОИП | Возможная ОИП (все три критерия) | Не ОИП (любой из шести критериев) |
Дифференциальный диагнозЛечениеРоль легочной реабилитации: улучшение функционального статуса и индивидуальных характеристик течения болезни. Обобщенные результаты рандомизированного двойного слепого плацебо-контролируемого исследования IFIGENIA продемонстрировали целесообразность присоединения к терапии ГКС у больных ИЛФ N-ацетилцистеина в высоких дозах (1800 мг в сутки) [13]. N-ацетилцистеин замедляет снижение ЖЕЛ и DLCO. Препарат позволяет более успешно, чем только иммуносупрессивная терапия, стабилизировать клинико-функциональные показатели у больных ИЛФ и смягчить нежелательные эффекты, вызываемые ГКС и цитостатиками. В то же время монотерапия N-ацетилцистеином не показана в связи с отсутствием эффекта [13]. ГоспитализацияИнформацияИсточники и литератураИнформацияРецензенты: Указание на отсутствие конфликта интересов: Разработчики данного протокола подтверждают отсутствие конфликта интересов, связанных с предпочтительным отношением к той или иной группе фармацевтических препаратов, методов обследования или лечения пациентов с идиопатическим легочным фиброзом. Сотовое легкое – один из видов легочного фиброзаИдиопатический легочный фиброз (ИЛФ) – это одна из форм воспаления легких, которая приводит к прогрессивному изменению в альвеолярной паренхиме. Сотовое легкое – это деформация легочной ткани в виде множественных мелких кист. Оно развивается в следствии формирования ИЛФ и является одним из его характерных признаков. Внешняя симптоматика проявляется не сразу, а постепенно. Основанием для постановки диагноза является физикальный осмотр, анамнез, рентген и КТ. Лечение может быть консервативным или оперативным. Прогноз, как правило, неблагоприятный. Более подробно об этом читайте ниже и смотрите на приложенном видео. Этиология и патогенезДля того, чтобы лучше понять, что такое сотовое легкое, нужно рассмотреть все причины основной патологии, которая и обуславливает возникновение аномалии. В большинстве случаев фиброзные изменения в легких являются последствиями развития идиопатической интерстициальной пневмонии. Проще говоря при воспалении легких, развиваются осложнения, которые вызывают усугубление основного заболевания и появление патологий вторичного характера, на фоне воспалительного процесса.
Основной причиной формирования врачи считают пристрастие к табаку, причем не важно курит человек сейчас или это было в прошлом. Примерно у каждого пятого пациента выявляют случаи заболевания в семейном анамнезе, что указывает на генетическую предрасположенность. Также увеличивают шансы развития сотового легко следующие обстоятельства: Фиброзные процессы в легком при наличии воспалительного процесса могут быть довольно разнообразны. Кистозная аномалия приводит к тому, что ткань становится похожа на пчелиные ячейки (показано на фото), поэтому такая аномалия получила название «сотового легкого». Этот процесс выявляется у всех больных ИЛФ и прогрессирует по мере развития. СимптоматикаПризнаки сотового легкого появляются постепенно (от полугода до нескольких лет). Основу клиники составляют: Утолщения дистальных фаланг пальцев рук получившие названия «барабанных палочек» наблюдаются у каждого второго заболевшего (см. фото). Редко встречающиеся такие признаки: Других проявлений нет, но ситуация резко ухудшается на терминальной стадии – у больного развиваются тяжелые формы легочной и сердечной недостаточности. Клиническая диагностика сотового легкогоИдиопатический легочный фиброз часто пропускают, потому что его клинические признаки схожи с иными патологиями: Поэтому для верного определения заболевания требуется ряд специфических анализов и процедур, которые обозначены в нижерасположенной таблице. Таблица. Диагностика ИЛФ: | При выслушивании явно наличие хрипов по типу «треск целлофана». Это дает повод подозревать о наличие фиброзного процесса. | |
| На негативе заметно диффузное усиление легочного рисунка в нижних и периферических зонах легкого. Видны кистозные поражения (сотовое легкое) и другие признаки тканевых изменений. | ||
| Компьютерная томография (КТ) высокого разрешения дает возможность получить снимки самой высокой четкости, на которых клиницисты хорошо визуализируют аномальные изменения. | ||
| В редких случаях требуется проведения забора легочной ткани (оперативным путем) для гистологического исследования. |
Обратите внимание. Что лабораторные анализы крови и мочи в диагностике идиопатического легочного фиброза играют незначительную роль. Внешние клинические признаки неспецифичны (кашель, треск в легких при выслушивании), они часто определяются и при других заболеваниях дыхательных путей.
Лечение
В основе консервативной терапии лежит назначение противофиброзных препаратов. На данный момент популярны пирфенидон и нинтеданиб – новые антифибротические лекарства, однако, их невозможно приобрести в ряде стран. Поддерживающие меры предполагают лечение кислородом и легочную реабилитацию
Обратите внимание. Больным рекомендуется работать с психологом. Занятия в группах дают определенную пользу, поскольку помогают справиться со стрессом.
Достаточно много препаратов против ИЛФ находятся в разработке, поэтому врачам рекомендовано направлять пожилых больных в программы клинических исследований.
В некоторых случаях можно ставить вопрос о трансплантации легких, что необходимо делать еще на стадии постановки первичного диагноза. Это возможно при условии, если возраст больного менее 65 лет и у него нет серьезных сопутствующих хронических заболеваний.
Прогноз
В большинстве случаев неблагоприятный. Средняя выживаемость с момента постановки диагноза составляет около 3 лет.
Факторы, которые могут повлиять на сокращение длительности жизни: мужской пол, пожилой возраст, другие хронические заболевания, усугубляющие здоровье. Стремительно ухудшают состояние больного усугубление легочной недостаточности, скопление воздуха или газов в плевральной полости и тромбоэмболия легочных сосудов. Также определенную опасность представляют инфекционные заболевания.
Развитие онкологического осложнения при данном диагнозе более вероятно нежели у больных фиброзом без сотового легкого, но причиной смерти, как правило, становится не рак, а прогрессия легочной недостаточности.
Идиопатический легочный фиброз (ИЛФ): современный подход к классификации и диагностике
Идиопатический легочный фиброз (ИЛФ) – это вариант идиопатической интерстициальной пневмонии (ИИП), характеризующийся неуклонным прогрессирующим течением и высокой смертностью. В отличие от большинства ИИП, иммуносупрессивная терапия не оказывает влияния на скорость прогрессирования ИЛФ. В течение последнего десятилетия установлена эффективность двух антифибротических препаратов в лечении ИЛФ – пирфенидона и нинтеданиба. Чтобы своевременно начать патогенетическую терапию, необходимо как можно быстрее установить диагноз ИЛФ на основании диагностического алгоритма, предполагающего анализ клинических, лабораторных и инструментальных данных, прежде всего результатов компьютерной томографии высокого разрешения (КТВР). При недостаточной информативности последней может быть использована малоинвазивная трансбронхиальная криобиопсия легкого, которая по точности сопоставима с хирургической биопсией легкого. Продолжается поиск молекулярно-биологических и генетических маркеров ИЛФ.
Согласно классификации Американского торакального общества/Европейского респираторного общества (ATS):1–112. /ERS):1–112. ) [1], идиопатический легочный фиброз (ИЛФ) представляет собой форму идиопатической интерстициальной пневмонии (ИИП) (табл. 1). Доля ИЛФ составляет 20-30% в структуре всех ИИП, а заболеваемость – от 7 до 17 случаев на 100 000 населения [2]. Мужчины болеют несколько чаще, чем женщины (соотношение мужчин/женщин приблизительно 1,5:1) [3]. ИЛФ развивается в основном у людей среднего и пожилого возраста: возраст 65% пациентов на момент постановки диагноза составляет 60 лет и более [4].
| Частые формы ИИП |
| Идиопатический легочный фиброз (ИЛФ) |
| Идиопатическая неспецифическая интерстициальная пневмония |
| Респираторный бронхиолит, ассоциированный с интерстициальным заболеванием легких |
| Десквамативная интерстициальная пневмония |
| Криптогенная организующая пневмония |
| Острая интерстициальная пневмония |
| Редкие формы ИИП |
| Идиопатическая лимфоцитарная интерстициальная пневмония |
| Идиопатический плевропаренхиматозный фиброэластоз |
| Неклассифицируемые формы (ИИП) |
В 2018 году P. Wolters и соавт. предложили выделять 4 варианта легочного фиброза в зависимости от патогенеза заболевания (табл. 2) [5]. ИЛФ характеризуется прогрессирующим течением с развитием дыхательной недостаточности и среди всех ИИП обладает самым неблагоприятным прогнозом: средняя выживаемость составляет от 2 до 5 лет [6,7]. Высокая смертность пациентов с ИЛФ объясняется особенностями патогенеза заболевания – преобладанием фиброза при незначительной выраженности воспалительных изменений [8,9]. Основным механизмом, приводящим к развитию прогрессирующего легочного фиброза, является персистирующее повреждение альвеолярного эпителия с последующим нарушением процессов его регенерации, избыточным отложением компонентов внеклеточного матрикса, активацией фибробластов и миофибробластов [10]. Указанные изменения определяют неэффективность традиционной иммуносупрессивной терапии у пациентов с ИЛФ [11]. Тем не менее, в настоящее время достигнуты значительные успехи в лечении ИЛФ, связанные с применением антифибротических препаратов – пирфенидона (антагониста трансформирующего фактора роста бета – TGF β) и нинтеданиба (множественного ингибитора тирозинкиназ), замедляющих уменьшение легочных объемов, в первую очередь, форсированной жизненной емкости легких (ФЖЕЛ), и улучшающих выживаемость без прогрессирования заболевания [12]. При отсутствии противопоказаний трансплантация легких также рассматривается в качестве варианта лечения у пациентов с прогрессирующим ИЛФ, осложнившимся тяжелой дыхательной недостаточностью [13,14].
| Группа 1: ЛФ, индуцированный дисфункцией эпителиальных клеток | ИЛФ |
| Группа 2: ЛФ, индуцированный дисфункцией клеток воспалени | Системная склеродермия, ревматоидный артрит, синдром Шегрена, экзогенный аллергический альвеолит, саркоидоз, НСИП |
| Группа 3: ЛФ, вызванный приемом лекарственных препаратов или воздействием профессиональных факторов | Асбестоз, силикоз, лекарственное поражение легких |
| Группа 4: ЛФ, связанный с курением | Десквамативная интерстициальная пневмония, респираторный бронхиолит, ассоциированный с интерстициальным заболеванием легких, Лангерганс-клеточный гистиоцитоз |
Клиническая картина
Основные жалобы у пациентов с ИЛФ – прогрессирующая одышка и сухой кашель, усиливающиеся при физической нагрузке. Реже отмечаются боль и дискомфорт в грудной клетке, повышенная утомляемость, общая слабость, снижение массы тела. В ряде случаев заболевание на начальных этапах протекает бессимптомно, а первыми проявлениями оказываются изменения функциональных легочных параметров [1]. Типичным аускультативным феноменом при ИЛФ является крепитация, преимущественно в задне-базальных отделах легких. У больных c развернутой стадией ИЛФ могут отмечаться признаки вторичной артериальной легочной гипертензии с развитием легочного сердца и правожелудочковой сердечной недостаточности [15].
При ИЛФ может определяться незначительное повышение СОЭ. Несмотря на наличие прогрессирующей дыхательной недостаточности, выраженное увеличение концентрации гемоглобина наблюдается крайне редко. уменьшением всех легочных объемов в сочетании со снижением диффузионной способности легких (DLCO). Одним из ранних проявлений ИЛФ может быть изолированное снижение DLCO при относительной сохранности легочных объемов. Также к ранним проявлениям ИЛФ относят увеличение альвеолоартериального градиента по кислороду, что часто характеризуется нормальными показателями сатурации крови в покое и десатурацией при физической нагрузке [16].
Диагностический алгоритм
Диагноз ИЛФ основывается на отсутствии известных причин легочного фиброза и наличии картины обычной интерстициальной пневмонии (ОИП) [17]. Даже при наличии гистологической картины ОИП при хирургической биопсии легкого (ХБЛ) окончательный диагноз требует исключения других патологических состояний, ассоциированных с развитием ОИП, включая диффузные заболевания соединительной ткани, пневмокониозы, поражение легких, связанное с приемом лекарственных препаратов, семейный легочный фиброз [18]. При отсутствии данных за альтернативный диагноз, согласно действующим клиническим рекомендациям [4], диагноз ИЛФ устанавливают на основании характерных данных компьютерной томографии высокого разрешения (КТВР) и, при необходимости, результатов биопсии легкого (табл. 3). Следует отметить, что в представленной гистологической классификации выделены «возможный ИЛФ» и «вероятный ИЛФ», когда невозможно однозначно подтвердить или исключить наличие ИЛФ. В таком случае показана повторная оценка данных КТВР и биопсии легкого для уточнения диагноза.
| КТ-картина | Гистологические данные | Диагноз |
|---|---|---|
| ОИП | ОИП | ИЛФ |
| Вероятная ОИП | ||
| Возможная ОИП | ||
| Неклассифицируемый фиброз | ||
| Не соответствует ОИП | Не-ИЛФ | |
| Возможная ОИП | ОИП Вероятная ОИП | ИЛФ |
| Возможная ОИП | Вероятный ИЛФ | |
| Неклассифицируемый фиброз | ||
| Не соответствует ОИП | Не-ИЛФ | |
| Не соответствует ОИП | ОИП | Возможный ИЛФ |
| Вероятная ОИП | Не-ИЛФ | |
| Возможная ОИП | ||
| Неклассифицируемый фиброз | ||
| Не соответствует ОИП |
КТ-диагностика
КТВР играет ключевую роль в диагностике ИЛФ и позволяет установить диагноз приблизительно в 2/3 случаев. В ряде исследований было показано, что КТ-картина типичной ОИП по данным КТВР согласуется с наличием гистологической картины типичной ОИП по данным биопсии легкого в 90-100% случаев [4]. Наличие достоверных КТ-признаков ОИП в настоящее время считают достаточным для диагностики ИЛФ без биопсии легкого. Проведение хирургической биопсии легкого (ХБЛ) рекомендуется при наличии КТ-картины, не типичной для ОИП. В таких случаях диагноз устанавливают на основании сочетания данных КТВР и гистологической картины (табл. 3). Таким образом, точная интерпретация данных КТВР является необходимым условием для постановки диагноза [1].
В настоящее время выделяют три КТ-варианта ОИП «типичная ОИП», которая исключает необходимость проведения ХБЛ, «возможная ОИП» и «не соответствует ОИП». При наличии последних двух вариантов требуется проведение ХБЛ [19].
КТ-картина типичной ОИП включает в себя преимущественно базальные и периферические ретикулярные изменения с образованием сотового легкого в сочетании с тракционными бронхоэктазами или без них. Критериями «сотового легкого» считают преимущественно субплевральные кисты диаметром 3-10 мм с четкими, относительно толстыми стенками (1-3 мм), расположенные слоями. Все КТ-признаки, рассматриваемые как «не соответствующие» ОИП, должны отсутствовать (рис. 1). Если все вышеуказанные критерии выполнены, данные КТВР достаточны для диагностики ОИП, а необходимости в проведения биопсии легкого нет [4]. Относительно признаков типичной ОИП заключения разных специалистов обычно хорошо согласуются [20,21]. Тем не менее, следует отметить, что ОИП и ИЛФ не являются синонимами, так как КТизменения, характерные для ОИП, могут отмечаться при ряде других заболеваний, прежде всего диффузных заболеваниях соединительной ткани.
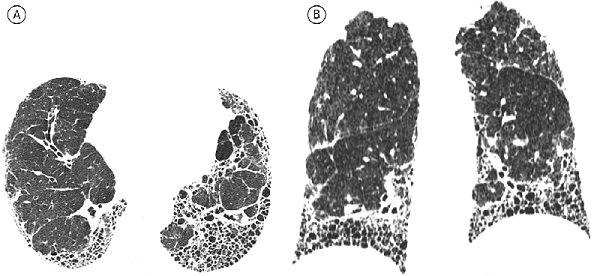
При возможной ОИП наблюдаются преимущественно базальные и периферические ретикулярные изменения без формирования зон сотового легкого. При этом изменения, не соответствующие ОИП, отсутствуют (рис. 2). Картина возможной ОИП менее специфична для ИЛФ, чем картина типичной ОИП. В данном случае дифференциальный диагноз следует проводить, в первую очередь, с неспецифической интерстициальной пневмонией (НСИП), для которой характерны отсутствие участков сотового легкого, преобладание затемнений по типу «матового стекла» над ретикулярными изменениями, относительная сохранность субплевральных зон. Участки сотовой трансформации редко встречаются при НСИП. В одном исследовании они были выявлены менее чем у 5% пациентов с идиопатической НСИП [23].
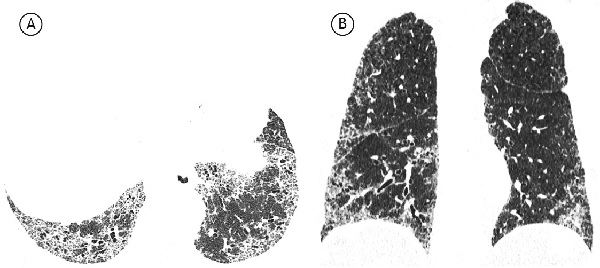
Изменения по данным КТВР, которые считают не соответствующими ОИП, включают в себя следующие: а) преобладание изменений в верхних и средних отделах легких; б) преимущественно перибронховаскулярные изменения; в) значительные по размеру зоны затемнения по типу «матового стекла», распростра ненность которых превышает таковую ретикулярных изменений; г) двусторонние очаговые изменения, преимущественно в верхних отделах легких; д) наличие кист (множественных, двусторонних) вне зон фиброза; е) картина мозаичного затемнения легочной ткани/ наличие «воздушных ловушек» (двусторонние изменения в трех и более долях); ж) наличие зон консолидации (рис. 3).
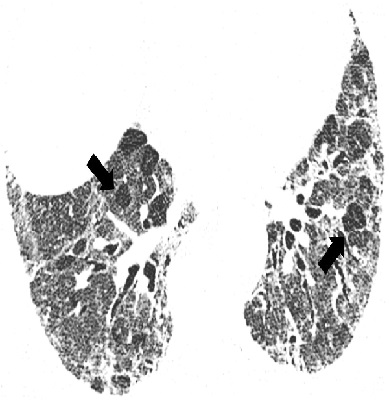
Несмотря на высокую вероятность наличия ИЛФ при типичной ОИП по данным КТВР, отсутствие зарактерной КТ-картины не должно служить основанием для исключения диагноза ИЛФ [22]. В 2017 г. D. Lynch и соавт. предложили новую КТ-классификацию ОИП, в которой впервые выделена группа неопределенной ОИП (табл. 4) [24].
| Типичная ОИП | Вероятная ОИП | Неопределенная ОИП | Наименее вероятно соответствует ОИП |
|---|---|---|---|
| Преобладание в базальных и субплевральных отделах (редко диффузные изменения); часто неоднородное распределение Зоны «сотового легкого»; ретикулярные изменения с периферическими тракционными бронхо эктазами и бронхиолоэктазами; отсутствие данных за альтернативный диагноз | Преобладание в базальных и субплевральных отделах; часто неоднородное распределение Ретикулярные изменения с периферическими тракционным бронхоэктазами и бронхиолоэктазами; отсутствие зон «сотового легкого»; отсутствие данных за альтернативный диагноз | Вариабельное или диффузное распределение Наличие фиброза в сочетании с небольшими по объему изменениями, не соответствующими ОИП | Преобладание в верхних и средних отделах легких; перибронховаскулярное распределение с относительной сохранностью субплевральных зон Любое из нижеперечисленного: преобладание зон консолидации; значительные по размеру зоны затемнения по типу «матового стекла» (при отсутствии обострения ИЛФ); диффузные очаговые или кистозные изменения; выраженное мозаичное затемнение легочной ткани с наличием «воздушных ловушек» |
Клиническое течение ИЛФ может быть различным. У большинства пациентов отмечается медленно прогрессирующее течение, однако у некоторых пациентов происходит стабилизация патологического процесса, тогда как у других отмечается довольно быстрое прогрессирование заболевания. Что касается выраженности легочных изменений по данным КТВР, то зоны затемнения по типу «матового стекла» чаще всего трансформируются в ретикулярные изменения, которые, в свою очередь, могут прогрессировать и формировать зоны «сотового легкого», размер которых со временем обычно увеличивается. Следует отметить, что общий паттерн легочных изменений также может изменяться: так, КТкартина возможной ОИП может трансформироваться в типичную ОИП [22].
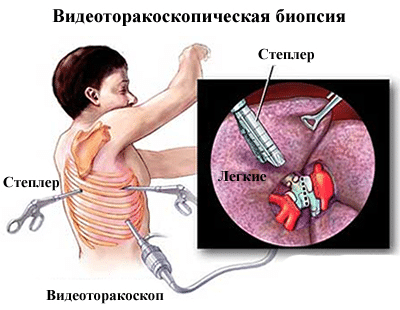
Биопсия легкого
Если однозначные данные о наличии ИЛФ при КТВР отсутствуют, то для подтверждения диагноза показано выполнение хирургической биопсии легких, которую чаще проводят с помощью видеоторакоскопической методики. С целью повышение эффективности биопсия легких должна производиться из разных долей легких. Хотя ХБЛ является наиболее достоверным методом определения гистологической картины ИИП, ее проведение связано с риском возникновения ряда осложнений, наиболее тяжелым из которых является обострение ИЛФ, особенно у пациентов с тяжелой дыхательной и/или сердечной недостаточностью [25]. В связи с этим решение о ее проведении должно приниматься индивидуально с учетом клинической картины, возможных преимуществ для постановки точного диагноза, а также согласия пациента.
В течение последнего десятилетия для гистологического подтверждения диагноза ИЛФ и других вариантов ИИП разработана методика трансбронхиальной криобиопсии легкого (ТБКБЛ). Ее основными преимуществами являются малоинвазивность, отсутствие необходимости в проведении интубации и ингаляционного наркоза и, вследствие этого, низкая частота развития осложнений в сочетании с возможностью получения большого по объему биоптата легкого, достаточного, в абсолютном большинстве случаев, для гистологической верификации диагноза [26]. Так, у пациентов без типичной картины ОИП по данным КТВР проведение ТБКБЛ позволяло установить диагноз приблизительно в 2/3 случаев, что сопоставимо с эффективностью ХБЛ в сходной ситуации [27]. При этом для ТБКБЛ характерны более низкий риск периоперационных осложнений (чаще всего отмечают развитие пневмоторакса и не угрожающего жизни кровотечения в месте проведения биопсии) и смерти, более короткий период госпитализации, что позволяет проводить ТБКБЛ у пациентов с высоким уровнем анестезиологического риска и наличием противопоказаний к ХБЛ [28].Таким образом, внедрение ТБКБЛ в клиническую практику может расширить показания к биопсии легкого и повысить диагностическую точность алгоритма обследования пациентов с подозрением на ИЛФ.
При морфологическом исследовании у пациентов с подозрением на ИЛФ G. Raghu и соавт. выделяют пять возможных гистологических паттернов заболевания (табл. 5) [29,4]. В сочетании с рентгенологическими данными они используются для подтверждения/исключения диагноза ИЛФ (табл. 3) [4,30].
Дифференциальный диагноз
У пациентов с подозрением на ИЛФ должен проводиться тщательный дифференциальный диагноз. При выявлении КТ-картины, соответствующей вероятной или возможной ОИП, что происходит довольно часто, в круг дифференциального диагноза следует включать, в первую очередь, хронический экзогенный аллергический альвеолит и фибротический вариант НСИП. Тем не менее, у части пациентов рекомендованная в данном случае ХБЛ не проводится в связи с наличием противопоказаний (тяжелой дыхательной недостаточности, сопутствующих заболеваний, возрастных ограничений) или нежеланием пациента.
При проведении дифференциального диагноза важно также исключить поражение легких в рамках системного заболевания соединительной ткани, в частности, ревматоидного артрита, системной склеродермии, дерматомиозита, синдрома Шегрена [31], в том числе при наличии КТ-картины типичной ОИП. При наличии у пациента отдельных клинических проявлений или повышения уровня лабораторных аутоиммунных маркеров, не соответствующих конкретному системному заболеванию соединительной ткани, может быть установлен диагноз интерстициальной пневмонии с аутоиммунными чертами [32].
Генетические маркеры ИЛФ
В настоящее время выявлен ряд мутаций и полиморфизмов генов, участвующих в ремоделировании легочной ткани и регуляции врожденного и приобретенного иммунитета, ассоциированных с развитием ИЛФ [33]. К ним относятся, в частности, мутации в генах, кодирующих сурфактантные протеины А и D (S):1–112. P-A и S):1–112. PD), описанные при семейных формах ИЛФ [34]. В ряде исследований выявлена ассоциация генетических полиморфизмов с прогнозом заболевания: в частности, наличие отдельных однонуклеотидных полиморфизмов в гене TLR-3 (Toll-подобный рецептор 3-го типа) ассоциировано с более быстрым прогрессированием заболевания [35]. Также при ИЛФ описан ряд полиморфизмов в генах муцина 5B (MUC5B) и TOLLIP (протеин, взаимодействующий с Toll-подобным рецептором) [36]. Хотя исследование генетических полиморфизмов не является частью диагностического алгоритма при ИЛФ, продолжается поиск генетических маркеров, способных служить предикторами различных вариантов течения заболевания и ответа на терапию.
Обострение ИЛФ
Обострение ИЛФ – это тяжелое жизнеугрожающее состояние, проявляющееся в виде быстрого нарастания дыхательной недостаточности у пациентов с ранее установленным диагнозом ИЛФ [37]. Как правило, характеризуется крайне тяжелым течением; смертность в ряде исследований достигала 85% [38]. В отличие от стабильного или медленно прогрессирующего течения ИЛФ, критерии диагностики его обострения определены менее четко. Согласно данным Н. Collard и соавт. [39], критерии обострения ИЛФ включают в себя наличие предшествующего или впервые выявленного ИЛФ с резким нарастанием одышки, развитием дыхательной недостаточности за предшествующие 30 дней без установленной причины, а также появление новых зон затемнения легочной ткани по типу «матового стекла» и/или консолидации на фоне имевшихся ранее изменений, соответствующих ОИП – зон ретикулярных изменений и «сотового легкого» (рис. 4) [40]. Тем не менее, вышеуказанные критерии обладают низкой специфичностью, в связи с чем при подозрении на обострение ИЛФ должен проводиться дифференциальный диагноз с инфекционным процессом, тромбоэмболией легочной артерии и ее ветвей, пневмотораксом, а также острой левожелудочковой недостаточностью с развитием отека легких [41].
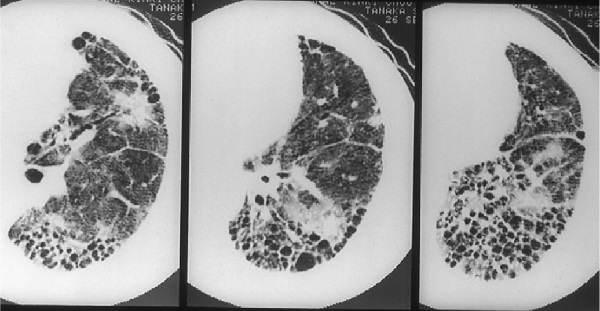
Заключение
Появление новых методов лечения, в частности, антифибротических препаратов, и неэффективность традиционной иммуносупрессивной терапии при ИЛФ подчеркивают важность как можно более ранней постановки диагноза и начала терапии. В течение последнего десятилетия был достигнут значительный прогресс в разработке диагностических алгоритмов для пациентов с ИЛФ. Этому способствовало повышение качества визуализационных методов, более полное понимание роли биопсии легких и разработка гистологических критериев ИЛФ. Все вышеперечисленные параметры должны исследоваться мультидисциплинарной командой специалистов, что в настоящий момент является стандартом диагностики ИЛФ. Несмотря на достигнутые успехи, в диагностике ИЛФ остаются нерешенные вопросы, в основном касающиеся применения инвазивных методов диагностики, в частности, хирургической биопсии легкого. Необходимо продолжать поиск молекулярно-биологических и генетических маркеров ИЛФ и разработку малоинвазивных биопсийных методов для максимально раннего установления диагноза, определения прогноза и разработки стратегии терапии ИЛФ.