Что значит радиоактивный элемент
Радиоактивный элемент
Основные сведения
Радиоактивными элементами в строгом смысле являются все элементы, идущие в таблице Менделеева после свинца (включая висмут), а также элементы технеций и прометий. Следующие элементы содержат в природных смесях хотя бы один радиоактивный изотоп: калий, кальций, ванадий, германий, селен, рубидий, цирконий, молибден, кадмий, индий, теллур, лантан, неодим, самарий, европий, гадолиний, лютеций, гафний, вольфрам, рений, осмий, платина, висмут, торий, уран (в список не включены дочерние элементы из рядов урана и тория, такие как радий, радон и астат, а также образующиеся в атмосфере под действием космических лучей, такие как углерод-14).
Все элементы, идущие за ураном, называются трансурановыми элементами. Есть предположения, что некоторые далёкие трансурановые элементы могут быть не радиоактивными или, во всяком случае, иметь достаточно долгоживущие изотопы, чтобы присутствовать в природе.
Многие радиоактивные элементы имеют важное практическое значение. Уран и плутоний используют как делящийся материал в атомных реакторах и в ядерном оружии. Некоторые радиоактивные элементы применяют для изготовления атомных электрических батареек со сроком непрерывной работы до нескольких лет. Долгоживущие изотопы природных радиоактивных элементов используются в геохронологии.
Использование радиоактивных элементов в России регламентируется «Санитарными правилами перевозки, хранения, учёта и работы с радиоактивными веществами (РВ)». Впервые в стране формы предупредительного санитарного надзора и получения объектами предварительного разрешения городской СЭС на приобретение радиоактивных веществ были разработаны и внедрены Розановой Ниной Александровной, заведующей в 1960 годах радиологической лабораторией, выделенной в самостоятельный отдел ГорСЭС (ныне Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека по городу Москве Роспотребнадзор).
Виды и характеристики радиоактивных металлов
Радиоактивные металлы занимают значительную часть периодической таблицы Менделеева. Одни о них говорят со страхом, другие с интересом. Данные элементы обладают уникальными свойствами, за которые ценятся научным сообществом, но вредны для человека. Излучение, которое исходит от этих металлов, провоцирует разрушение внутренних органов.

Какие элементы относятся к радиоактивным?
Группа радиоактивных элементов в периодической таблице Менделеева начинается от свинца и заканчивается последней ячейкой. Излучение происходит из-за определенного периода полураспада — преобразования металлического ядра в дочернее. Радиоактивные элементы:
Среди них присутствуют цветные и черные радиоактивные металлы.
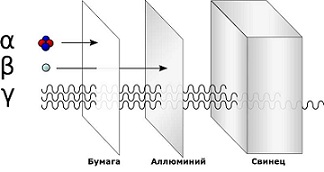
Существуют три вида радиоактивного излучения — альфа, бета, гамма. Они отличаются длиной волны, проникающей способностью. Если альфа излучение может сдержать плотная бумага или картон, то гамма излучение остановит только слой свинца.
История открытия
Открытием радиации человечество обязано прусскому физику Вильгельму Рентгену. В 1895 году он смог увидеть радиоактивное излучение. Благодаря работам этого ученого был разработан рентгеновский аппарат.
Изучение радиоактивности продолжил Анри Беккерель в 1896 году. Этот ученый проводил эксперименты с солями урана. Прорыв в данной области произошел через 2 года. Пьер Кюри получил первый чистый радиоактивный материал — радий. После открытия этого элемента ученый не смог продолжить его изучение, поскольку умер от излучения.
Следующее продвижение в этой области произошло в 1934 году. В этот год ученые смогли синтезировать искусственный радиоактивный изотоп. Сейчас эта область является одной из самых актуальных. Ее изучением занято огромное количество ученых, крупных научных организаций.
Запасы и месторождения
Запасы и месторождения представителей радиоактивной группы:
Большинство радиоактивных металлов редко встречаются в природе, добывать их сложно.
Добыча и промышленное получение
В чистом виде естественные радиоактивные металлы найти невозможно. Чаще их синтезируют из урановых руд. Это затратный, трудоемкий процесс, состоящий из нескольких этапов:
После обработки из тонны руды получается несколько грамм чистого вещества. Проводить подобные процедуры можно только в специальных цехах.
Свойства и характеристики
Знание характеристик радиоактивных металлов поможет выявить уникальные свойства этих элементов, понять, где их лучше применять.
Уран растворяется в азотной и соляной кислоте, не взаимодействует с щелочами. При нагревании может вступать в реакции с азотом, фосфором.
Радий
По химической активности радий можно сравнить с барием. На воздухе быстро окисляется. При соединении с водой возникает бурная реакция с нагреванием жидкости.
Плутоний
Сферы применения
Радиоактивные металлы применяются в разных направлениях. С их помощью проводят эксперименты, изучают влияние на другие материалы, живые организмы. Часто используются для выработки энергии в реакторах.
Влияние на организм
Радиоактивное излучение разрушает внутренние органы. Естественные механизмы защиты организма справляются только с малыми дозами излучения. Когда они становятся большими, развивается лучевая болезнь, повышается риск поражения организма раком.
Радиоактивные металлы обладают уникальными свойствами. Их изучением ученые занимаются постоянно. Исследователи находят новые способы получения металлов, сферы для их применения.
Радиоактивные элементы
Описание, применение, влияние на человеческий организм
Организации Москвы
Прочие медицинские услуги
Медицинские НИИ
Продолжительность жизни, человека и других живых существ.
Этюды оптимизма. И. И. Мечников
Посольства
— популярные туристические направления
Финансовые организации
ЦБ России
Московские отделения банков
это химические элементы, имеющие нестабильные атомные ядра, которые самопроизвольно распадаются, превращаясь в атомные ядра других элементов и при этом испуская частицы (электроны, протоны, позитроны, нейтроны) и кванты электромагнитного излучения (рентгеновские и гамма-лучи), которые могут вызывать мутагенные, канцерогенные, тератогенные и другие изменения в живых организмах, а также негативные экологические явления.
Здесь приведены данные о некоторых радиоактивных элементах, в обнаруженных в местах радиоактивного загрязнения на территории Москвы.
Цезий-137, Cs-137
Цезий-137, известен также как радиоцезий — один из главных компонентов радиоактивного загрязнения биосферы. Содержится в радиоактивных выпадениях, радиоактивных отходах, сбросах заводов, перерабатывающих отходы атомных электростанций. Интенсивно сорбируется почвой и донными отложениями; в воде находится преимущественно в виде ионов. Содержится в растениях и организме животных и человека.
В организме животных 137Cs накапливается главным образом в мышцах и печени
Выброс цезия-137 в окружающую среду происходит в основном в результате ядерных испытаний и аварий на предприятиях атомной энергетики
Известны случаи загрязнения внешней среды в результате небрежного хранения источников цезия-137 для медицинских и технологических целей.
Биологическое действие
Внутрь живых организмов цезий-137 в основном проникает через органы дыхания и пищеварения. Хорошей защитной функцией обладает кожа
Поглощённая доза излучения измеряется энергией ионизирующего излучения, переданного массе облучаемого вещества.
Единица поглощённой дозы – грей (Гр), равный 1 джоулю, поглощённому 1 кг вещества
1 Гр = 1Дж/кг = 100 рад.
Развитие радиационных поражений у человека можно ожидать при поглощении дозы примерно в 2 Гр и более. Симптомы во многом схожи с острой лучевой болезнью при гамма-облучении: угнетённое состояние и слабость, диарея, снижение массы тела, внутренние кровоизлияния
Радионуклиды Cs-137, проникая в организм человека, инкорпорируются жизненно важными органами. При этом, в клетках происходят дистрофические и некробиотические изменения, связанные в первую очередь с нарушением энергетических механизмов и приводящие к нарушениям жизненно-важных функций организма. Тяжесть поражения находится в прямой зависимости от количества Cs-137 инкорпорированного организмом и отдельными органами. Эти поражения могут представлять опасность, прежде всего, как индукторы мутаций в генетическом аппарате половых и соматических клеток.
Способность Cs-137 вызывать мутации в половых клетках, будет являться в будущих поколениях основой для возникновения внутриутробной гибели зародыша, врожденных пороков развития, патологии плода и новорожденного, заболеваний взрослого организма, связанных с недостаточной генной активностью.
Это внутреннее облучение организма также чрезвычайно опасно и тем, что оно сочетается со способностью радионуклидов Cs-137 и продуктов их распада в виде бария, воздействовать на биологические структуры, взаимодействовать с рецепторным аппаратом клеточных мембран, изменять состояние регуляторных процессов.
Выявлена зависимость между частотой нарушений сердечной деятельности у детей и содержанием радионуклидов в их организме. Следует обратить особое внимание на то, что присутствие даже относительно небольших количеств Cs-137 в организме детей 10-30 Бк/кг (при этом, в ткани сердца концентрация данного радионуклида значительно большая) приводит к увеличению в два раза числа детей с электрокардиографическими нарушениями.
В этой связи, факторы внешней среды, подавляющие функцию систем, регулирующих (стимулирующих) активность генетического аппарата клеток, будут являться индукторами (провокаторами) возникновения многих заболеваний. Cs-137 способен в относительно небольших количествах, подавлять активность регуляторных систем организма, и прежде всего, иммунной системы.
Период полураспада цезия-137 составляет 30 лет.
Радий, Ra-226
радиоактивный изотоп химического элемента радия с атомным номером 88 и массовым числом 226. Принадлежит к радиоактивному семейству урана-238
Наиболее устойчивым изотопом является радий-226 (226Ra), образующийся при распаде урана. Период полураспада радия-226 составляет 1600 лет, в процессе распада образуется радиоактивный газ радон.
Радий-226 является источником альфа-излучения и считается потенциально опасным для костной ткани человека.
В ничтожных концентрациях присутствует в природных водах.
Применение
Соли радия используются в медицине как источник радона (см. РАДОН) для приготовления радоновых ванн.
Содержание в организме
Радий сильно токсичен. Около 80% поступившего в организм радия накапливается в костной ткани. Большие концентрации радия вызывают остеопороз, самопроизвольные переломы и опухоли.
Развиваются опухоли костной ткани и органов, заключённых в костной капсуле (кроветворная ткань, гипофиз) или топографически близких к ней (слизистая ротовой полости, гайморова полость).
Кобальт-60, Co-60
Кобальт-60, радиокобальт — радиоактивный нуклид химического элемента кобальта с атомным номером 27 и массовым числом 60. В природе практически не встречается из-за малого периода полураспада. Открыт в конце 1930-х годов
У радиоактивного кобальта много «профессий». Все более широкое применение в промышленности находит, например, гамма-дефектоскопия, т.е. контроль качества продукции путем просвечивания ее гамма-лучами, источником которых служит изотоп кобальт-60. Такой метод контроля позволяет с помощью сравнительно недорогой и компактной аппаратуры легко выявлять трещины, поры, свищи и другие внутренние дефекты массивных отливок, сварных швов, узлов и деталей, находящихся в труднодоступных местах. В связи с тем, что гамма-лучи распространяются источником равномерно во все стороны, метод дает возможность контролировать одновременно большое число объектов, а цилиндрические изделия проверять сразу по всему периметру.
Радиоактивный кобальт используют для контроля и регулирования уровня расплавленного металла в плавильных печах, уровня шихтовых материалов в домнах и бункерах, для поддержания уровня жидкой стали в кристаллизаторе установок непрерывной разливки.
Прибор, называемый гамма-толщиномером, быстро и с большой степенью точности определяет толщину обшивки судовых корпусов, стенок труб, паровых котлов и других изделий, когда к их внутренней поверхности невозможно подобраться и поэтому обычные приборы оказываются бессильны.
Находит кобальт применение и в медицине. Крупицы изотопа кобальт-60, помещенные в медицинские «пушки», не причиняя вреда организму человека, бомбардируют гамма-лучами внутренние злокачественные опухоли, губительно влияя на быстро размножающиеся больные клетки, приостанавливая их деятельность и тем самым ликвидируя очаги страшной болезни.
В аппарате для облучения глубокозалегающих злокачественных опухолей, «кобальтовой пушке» ГУТ-400 (гамма-установка терапевтическая), количество кобальта-60 соответствует по своей активности 400 г радия. Это очень большая величина, такого количества радия нет ни в одной лаборатории. Но именно высокая активность позволяет предпринимать попытки лечения опухолей, расположенных в глубине организма больного.
Однако, несмотря на свою столь обширную плезность радиация есть радиация и бесконтрольное облучение приводит к описанным выше печальным последствиям.
Торий-232, Th-232
Торий-232 — природный радиоактивный нуклид химического элемента тория с атомным номером 90 и массовым числом 232.
Является наиболее долгоживущим изотопом тория, альфа-радиоактивен с периодом полураспада 1,405·10 10 (14 млрд.) лет.
Торий-232 является альфа – излучателем
Активность одного грамма этого нуклида составляет 4 070 Бк.
В виде препарата торотраста суспензия диоксида тория использовалась в качестве контрастного вещества при ранней рентгенодиагностике. В настоящее время препараты тория-232 классифицируются как канцерогенные
Поступление тория в желудочно-кишечный тракт (тяжелый металл, к тому же радиоактивный!) не вызывает отравления. Объясняется это тем, что в желудке – кислая среда, и в этих условиях соединения тория гидролизуются. Конечный продукт – нерастворимая гидроокись тория, которая выводится из организма. Острое отравление способна вызвать лишь нереальная доза в 100 г тория.
Однако чрезвычайно опасно попадание тория в кровь. Следствием этого могут быть заболевания кроветворной системы, образование специфических опухолей.
Плутоний-239, Pu-239
Плутоний-239 (англ. plutonium-239) — радиоактивный нуклид химического элемента плутония с атомным номером 94 и массовым числом 239.
В природе встречается в чрезвычайно малых количествах в урановых рудах.
Активность одного грамма этого нуклида составляет приблизительно 2,3 ГБк.
Плутоний-239 имеет период полураспада 24 100 лет.
Плутоний-239 используют:
— в качестве ядерного топлива в ядерных реакторах на тепловых и особенно на быстрых нейтронах;
— при изготовлении ядерного оружия;
— в качестве исходного вещества для получения трансплутониевых элементов.
Плутоний был открыт в конце 1940 г.
Хотя плутоний, по-видимому, химически токсичен, как и любой тяжелый металл, этот эффект выражается слабо по сравнению с его радиотоксичностью. Токсические свойства плутония появляются как следствие альфа-радиоактивности.
Альфа частицы представляют серьезную опасность только в том случае, если их источник находится в теле (т.е. плутоний должен быть принят внутрь). Хотя плутоний излучает еще и гамма-лучи и нейтроны, которые могут проникать в тело снаружи, уровень их слишком мал, чтобы причинить сильный вред.
Альфа-частицы повреждают только ткани, содержащие плутоний или находящиеся в непосредственном контакте с ним. Значимы два типа действия: острое и хроническое отравления. Если уровень облучения достаточно высок, ткани могут страдать острым отравлением, токсическое действие проявляется быстро. Если уровень низок, создается накопляющийся канцерогенный эффект.
Плутоний очень плохо всасывается желудочно-кишечным трактом, даже когда попадает в виде растворимой соли, впоследствии она все равно связывается содержимым желудка и кишечника. Загрязненная вода, из-за предрасположенности плутония к осаждению из водных растворов и к формированию нерастворимых комплексов с остальными веществами, имеет тенденцию к самоочищению.
Радиоактивные элементы
Строго говоря, радиоактивным элементом следует называть такой химический элемент, все изотопы которого радиоактивны. Однако на практике этим термином часто называют всякий элемент, в природной смеси которого присутствует хотя бы один радиоактивный изотоп, то есть если элемент проявляет радиоактивность в природе. Кроме того, радиоактивными оказываются все изотопы всех синтезированных на сегодняшний день искусственных элементов.
Радиоактивными элементами в строгом смысле являются все элементы, идущие в таблице Менделеева после свинца (включая висмут), а также элементы технеций и прометий. Следующие элементы содержат в природных смесях хотя бы один радиоактивный изотоп: калий, кальций, ванадий, германий, дубний селен, рубидий, цирконий, молибден, кадмий, индий, теллур, лантан, неодим, самарий, гадолиний, лютеций, гафний, вольфрам, рений, осмий, платина, висмут, торий, уран (в список не включены дочерние элементы из рядов урана и тория, такие как радий, радон и астат, а также образующиеся в атмосфере под действием космических лучей, такие как углерод-14).
Все элементы, идущие за ураном, называются трансурановыми элементами. Есть предположения, что некоторые далёкие трансурановые элементы могут быть не радиоактивными или, во всяком случае, иметь достаточно долгоживущие изотопы, чтобы присутствовать в природе.
Многие радиоактивные элементы имеют важное практическое значение. Уран и плутоний используют как делящийся материал в атомных реакторах и в ядерном оружии. Некоторые радиоактивные элементы применяют для изготовления атомных электрических батареек со сроком непрерывной работы до нескольких лет. Долгоживущие изотопы природных радиоактивных элементов используются в геохронологии.
См. также
Полезное
Смотреть что такое «Радиоактивные элементы» в других словарях:
РАДИОАКТИВНЫЕ ЭЛЕМЕНТЫ — химические элементы (криптон 85, цезий 137, рутений 106, стронций 90, йод 131) с нестабильным атомным ядром, которые при самопроизвольном распаде испускают характерное излучение. Могут вызывать мутагенные, канцерогенные, тератогенные и другие… … Экологический словарь
РАДИОАКТИВНЫЕ ЭЛЕМЕНТЫ — хим. элементы, все изотопы которых радиоактивны (см. ). К ним относятся технеций, прометий, полоний и все последующие элементы конца таблицы Д. И. Менделеева до урана, а также «трансурановые» элементы, что составляет больше 1 /4 всех известных… … Большая политехническая энциклопедия
РАДИОАКТИВНЫЕ ЭЛЕМЕНТЫ — химические элементы, все изотопы которых радиоактивны (технеций, прометий, полоний и все следующие за ним элементы в периодической системе Менделеева) … Большой Энциклопедический словарь
РАДИОАКТИВНЫЕ ЭЛЕМЕНТЫ — химические элементы, все изотопы которых радиоактивны: технеций, прометий, полоний и все последующие элементы периодической системы Д. И. Менделеева. Р. э., расположенные (в периодической системе химических элементов) за ураном, называются… … Российская энциклопедия по охране труда
Радиоактивные элементы — химические элементы, все изотопы которых радиоактивны. К числу Р. э. принадлежат Технеций (атомный номер 43), Прометий (61), Полоний (84) и все последующие элементы в периодической системе Менделеева. К 1975 известно 25 Р. э. Те из них,… … Большая советская энциклопедия
радиоактивные элементы — химические элементы, все изотопы которых радиоактивны (технеций, прометий, полоний и все следующие за ним элементы в периодической системе химических элементов). * * * РАДИОАКТИВНЫЕ ЭЛЕМЕНТЫ РАДИОАКТИВНЫЕ ЭЛЕМЕНТЫ, химические элементы, все… … Энциклопедический словарь
РАДИОАКТИВНЫЕ ЭЛЕМЕНТЫ — хим. элементы, все изотопы к рых радиоактивны. К числу Р. э. относят технеций Тс (ат. н. Z=43), прометий Pm (Z=61), полоний Ро (Z=84) и все последующие элементы периодич. системы Менделеева. Те из них, к рые расположены в системе Менделеева за… … Большой энциклопедический политехнический словарь
РАДИОАКТИВНЫЕ ЭЛЕМЕНТЫ — хим. элементы, все нуклиды к рых радиоактивны (технеций, прометий, полоний и все следующие за ним элементы в периодич. системе хим. элементов) … Естествознание. Энциклопедический словарь
радиоактивные элементы — химические элементы, все изотопы которых радиоактивны … Большой медицинский словарь
ЭЛЕМЕНТЫ ЦИКЛИЧЕСКИЕ — по Вернадскому, гр. из 44 хим. элементов, геохим. история которых может быть выражена круговыми процессами (циклами). Э. ц. составляют более 99,7% массы земной коры. В эту гр. не включались: благородные газы (5), благородные металлы (7),… … Геологическая энциклопедия
Радиоактивные металлы
Радиоактивные металлы — это металлы, которые самопроизвольно излучают поток элементарных частиц во внешнюю среду. Этот процесс называют альфа(α), бета(β), гамма(γ) излучением или просто радиоактивным излучением.
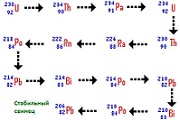
Все радиоактивные металлы со временем распадаются и превращаются в стабильные элементы (иногда проходя целую цепочку превращений). У разных элементов радиоактивный распад может длиться от нескольких миллисекунд до нескольких тысяч лет.
Рядом с названием радиоактивного элемента часто указывается массовое число его изотопа. Например, Технеций-91 или 91 Tc. Разные изотопы одного и того же элемента как правило имеют общие физические свойства и различаются лишь длительностью радиоактивного распада.

Список радиоактивных металлов
| Название рус. | Название eng. | Самый стабильный изотоп | Период распада |
|---|---|---|---|
| Технеций | Technetium | Tc-91 | 4.21 x 10 6 лет |
| Прометий | Promethium | Pm-145 | 17.4 года |
| Полоний | Polonium | Po-209 | 102 года |
| Астат | Astatine | At-210 | 8.1 часов |
| Франций | Francium | Fr-223 | 22 минут |
| Радий | Radium | Ra-226 | 1600 лет |
| Актиний | Actinium | Ac-227 | 21.77 лет |
| Торий | Thorium | Th-229 | 7.54 x 10 4 лет |
| Протактиний | Protactinium | Pa-231 | 3.28 x 10 4 лет |
| Уран | Uranium | U-236 | 2.34 x 10 7 лет |
| Нептуний | Neptunium | Np-237 | 2.14 x 10 6 лет |
| Плутоний | Plutonium | Pu-244 | 8.00 x 10 7 лет |
| Америций | Americium | Am-243 | 7370 лет |
| Кюрий | Curium | Cm-247 | 1.56 x 10 7 лет |
| Беркелий | Berkelium | Bk-247 | 1380 лет |
| Калифорний | Californium | Cf-251 | 898 лет |
| Эйнштейний | Einsteinium | Es-252 | 471.7 дней |
| Фермий | Fermium | Fm-257 | 100.5 дней |
| Менделевий | Mendelevium | Md-258 | 51.5 дней |
| Нобелий | Nobelium | No-259 | 58 минут |
| Лоуренсий | Lawrencium | Lr-262 | 4 часа |
| Резенфордий | Rutherfordium | Rf-265 | 13 часов |
| Дубний | Dubnium | Db-268 | 32 часа |
| Сиборгий | Seaborgium | Sg-271 | 2.4 минуты |
| Борий | Bohrium | Bh-267 | 17 секунд |
| Ганий | Hassium | Hs-269 | 9.7 секунд |
| Мейтнерий | Meitnerium | Mt-276 | 0.72 секунды |
| Дармштадий | Darmstadtium | Ds-281 | 11.1 секунды |
| Рентгений | Roentgenium | Rg-281 | 26 секунд |
| Коперниций | Copernicium | Cn-285 | 29 секунд |
| Унунтрий | Ununtrium | Uut-284 | 0.48 секунд |
| Флеровий | Flerovium | Fl-289 | 2.65 секунд |
| Унунпентий | Ununpentium | Uup-289 | 87 миллисекунд |
| Ливерморий | Livermorium | Lv-293 | 61 миллисекунда |
Радиоактивные элементы делятся на естественные (существующие в природе) и искусственные (получаемые в результате лабораторного синтеза). Естественных радиоактивных металлов не много — это полоний, радий, актиний, торий, протактиний и уран. Их наиболее стабильные изотопы встречаются в природе, чаще в виде руды. Все остальные металлы из списка созданы человеком.
Самый радиоактивный металл
Самый радиоактивный металл на данный момент — ливерморий. Его изотоп Ливерморий-293 распадается всего за 61 милисекунду. Впервые этот изотоп был получен в Дубне, в 2000 году.
Другой очень радиоактивный металл — унунпентий. Изотоп унунпентий-289 имеет чуть больший период распада (87 милисекунд).
Что такое радиация
Всем известно, что радиация очень опасна и лучше держаться подальше от радиоактивного излучения. С этим трудно поспорить, хотя в реальности мы постоянно подвержены влиянию радиации, где бы не находились. В земле залегает довольно большое количество радиоактивной руды, а из космоса на Землю постоянно прилетают заряженные частицы.
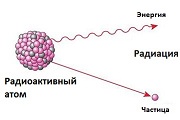
Кратко говоря, радиация это самопроизвольное испускание элементарных частиц. От атомов радиоактивного вещества отделяются протоны и нейтроны, «улетая» во внешнюю среду. Ядро атома при этом постепенно изменяется, превращаясь в другой химический элемент. Когда все нестабильные частицы отделяются от ядра, атом перестает быть радиоактивным. Например, торий-232 в конце своего радиоактивного распада превращается в стабильный свинец.
Наука выделяет 3 основных вида радиоактивного излучения
Альфа излучение(α) — поток альфа-частиц, положительно заряженных. Они сравнительно большие по размеру и плохо проходят даже через одежду или бумагу.
Бета излучение(β) — поток бета-частиц, негативно заряженных. Они довольно малы, легко проходят через одежду и проникают внутрь клеток кожи, что наносит большой вред здоровью. Но бета-частицы не проходят через плотные материалы, такие как алюминий.
Гамма излучение(γ) — это высокочастотная электромагнитная радиация. Гамма-лучи не имеют заряда, но содержат очень много энергии. Скопление гамма-частиц излучает яркое свечение. Гамма-частицы проходят даже через плотные материалы, что делает их очень опасными для живых существ. Их останавливают только самые плотные материалы, например, свинец.
Все эти виды излучения так или иначе присутствуют в любой точке планеты. Они не представляют опасности в малых дозах, но при высокой концентрации могут причинить очень серьезный ущерб.
Изучение радиоактивных элементов


Первооткрывателем радиоактивности является Вильгельм Рентген. В 1895 году этот Прусский физик впервые наблюдал радиоактивное излучение. На основе этого открытия был создан знаменитый медицинский прибор, названый в честь ученого.
В 1896 г изучение радиоактивности продолжил Анри Беккерель, он экспериментировал с солями урана.
В 1898 г Пьер Кюри в чистом виде получил первый радиоактивный металл — Радий. Кюри хоть и открыл первый радиоактивный элемент, однако, не успел толком его изучить. И выдающиеся свойства радия привели к быстрой гибели ученого, который беспечно носил свое «детище» в нагрудном кармане. Великое открытие отомстило своему первооткрывателю — Кюри умер в возрасте 47 лет от мощной дозы радиоактивного облучения.
В 1934 г был впервые синтезирован искусственный радиоактивный изотоп.
Сейчас изучением радиоактивности занимаются множество ученых и организаций.
Добыча и синтез


Даже естественные радиоактивные металлы не встречаются в природе в чистом виде. Их синтезируют из урановой руды. Процесс получения чистого металла чрезвычайно трудоемок. Состоит он из нескольких стадий:
В итоге, из тонны урановой руды можно получить всего несколько граммов урана.
Синтез искусственных радиоактивных элементов и их изотопов проходит в специальных лабораториях, в которых создаются условия для работы с подобными веществами.
Практическое применение
Чаще всего, радиоактивные металлы используют для выработки энергии.
Ядерные реакторы — это устройства, использующие уран для нагревания воды и создания потока пара, который вращает турбину, с помощью чего вырабатывается электричество.