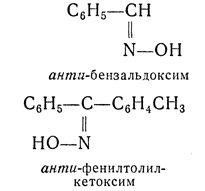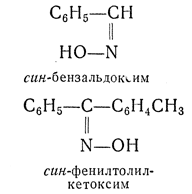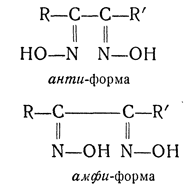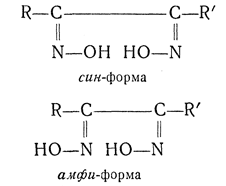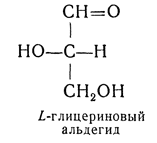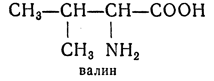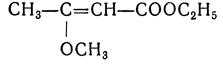Что значит приставка гипо в химии
ГИПО. (приставка)
Смотреть что такое «ГИПО. (приставка)» в других словарях:
гипо. — ГИПО. [от греч. hypo под, внизу]. Первая часть сложных слов. Вносит зн.: уменьшение чего л., снижение по отношению к какой л. норме. гиподинамический, гипосенсибилизация, гипохлоридный. * * * гипо. (от греч. hypó под, внизу), приставка,… … Энциклопедический словарь
ГИПО. — ГИПО. (от греческого hypo под, внизу), приставка, означающая: 1) находящийся внизу (например, гиподерма); 2) пониженный против нормы (например, гипотония) … Современная энциклопедия
ГИПО. — ГИПО. (от греч. hypo под внизу), приставка, означающая: 1) находящийся внизу (напр., гиподерма).2) Пониженный против нормы (напр., гипотония) … Большой Энциклопедический словарь
. гипо — [греч. hypo – внизу, снизу, под] Приставка, указывающая на понижение против нормы, напр., гипотония. Большой словарь иностранных слов. Издательство «ИДДК», 2007 … Словарь иностранных слов русского языка
Гипо — (лат. hypo ) приставка, обозначающая недостаток, дефицит. Источник: КОНТРОЛЬ ПРОГРАММЫ ПРОФИЛАКТИКИ ЙОДДЕФИЦИТНЫХ ЗАБОЛЕВАНИЙ ПУТЕМ ВСЕОБЩЕГО ЙОДИРОВАНИЯ СОЛИ. МЕТОДИЧЕСКИЕ УКАЗАНИЯ. МУ 2.3.7.1064 01 (утв. Главным государственным санитарным… … Официальная терминология
Гипо. — ГИПО. (от греческого hypo под, внизу), приставка, означающая: 1) находящийся внизу (например, гиподерма); 2) пониженный против нормы (например, гипотония). … Иллюстрированный энциклопедический словарь
гипо… — Приставка, употребляющаяся для указания на уменьшение чего л. против нормы, например: гиповитаминоз, гиподинамия, гипотония, гипофункция. [От греч. ‛υπο под] … Малый академический словарь
Гипо- (Hypo-) — приставка. См. гип Источник: Медицинский словарь … Медицинские термины
гипо — приставка, пишется всегда слитно … Орфографический словарь русского языка
Некоторые важнейшие приставки (префиксы) и окончания (суффиксы)
-аза — окончание в названиях энзимов или ферментов (мальтаза, амилаза, лактаза); присоединяется к названию (или корню названия) вещества, на которое действует энзим.
алло- — приставка, обозначающая, что данное соединение по химическому строению сходно с другим. Например, кофеин и аллокофеин. В случаях геометрической изомерии соединений с двойной связью обозначает более стабильную форму, в которую соединение превращается при нагревании: фумаровую кислоту можно назвать алломалеиновой, так как она является более стабильным изомером, образующимся при нагревании малеиновой кислоты.
-ал — окончание названий альдегидов по Женевской и Льежской номенклатурам.
амфи- — приставка, обозначающая положения 2,6 для двузамещенных нафталина. Применяется также для наименования некоторых стереоизомеров диоксимов (см. анти-).
-ан — окончание названий предельных (парафиновых) углеводородов.
ана- — приставка для обозначения 1,5-двузамещенных нафталина.
анти- — приставка, применяемая для обозначения стереоизомеров. Например, антивинная (мезовинная) кислота. Часто также применяется для обозначения стереоизомерных оксимов и гидразонов и указывает на диагональное расположение групп по отношению к плоскости двойной связи; в противоположность этому приставкой син- в ряду оксимов и гидразонов обозначают одностороннее расположение групп:
В ряду диоксимов кроме анти- и син-форм возможны еще амфи-формы:
(ср. также транс- и цис-).
аци- — приставка, обозначающая кислотную таутомерную форму нитросоединений.
би- — приставка, обозначающая удвоение радикала, например: бифенил.
бис-, трис-, тетракис- — приставки, указывающие на наличие двух, трех, четырех и т. д. сложных радикалов, например: бис-(диметиламино)-этан.
виц- — сокращение от вицинальный (соседний, рядовой).
втор- — сокращение от вторичный.
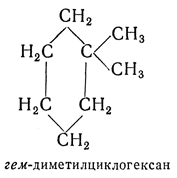
гем- — приставка, обозначающая (для полиметиленовых, динитро- и др. соединений) замещение двух атомов водорода у одного и того же атома углерода. Например:
гомо- — наиболее часто — приставка для обозначения гомологов, которые отличаются на одну группу СН2. Например, салициловая кислота С6Н4(ОН)СООН и гомосалициловая кислота С6Н4(ОН)СН2СООН, цистеин CH2(SH)CH(NH2)COOH и гомоцистеин CH2(SH)CH2CH(NH2)COOH.
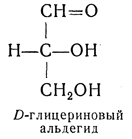
D — обозначение (от слова dexter — правый), указывающее на принадлежность одного из пары зеркальных изомеров (энантиомеров) к ряду соединений с определенной пространственной конфигурацией (D-ряд, или ряд D-глицеринового альдегида). Зеркальные изомеры с противоположной пространственной конфигурацией обозначают символом L (от слова laevus— левый), что также указывает на принадлежность их к стерическому ряду (L-ряд, или ряд L-глицеринового альдегида). Проекционные формулы зеркально-изомерных глицериновых альдегидов:
d — сокращение от слова dexter (правый); первоначально применялось для обозначения оптически активных соединений, вызывающих правое вращение плоскости поляризации света; оптические антиподы, вызывающие левое вращение, обозначали символом l — сокращение от слова laevus (левый). Затем символы d и l стали применять для обозначения принадлежности зеркальных изомеров по их пространственным конфигурациям к определенным стерическим рядам, и в этом значении они встречаются в литературе, наряду с символами D и L (d-ряд или D-ряд; l-ряд или L-ряд, см. выше). В последние годы во избежание путаницы для обозначения соответствующих пространственных конфигураций символы d и l стремятся заменить символами D и L. Символы d и l предложено сохранить в их первоначальном значении для обозначения правого и левого вращения плоскости поляризации, наряду со знаками (+) и (—).
-диен — окончание для обозначения наличия двух двойных связей в молекуле, например пентадиен-1,3 СН3—СН=СН—СН=СН2.
-диин — окончание для обозначения наличия двух тройных связей в молекуле, например гексадиин-2,4 СН3—С≡С—С≡С—СН3.
-диол — окончание, характерное для названий двухатомных спиртов (гликолей), например гександиол-1,5 СН3СНОНСН2СН2СН2СН2ОН.
DL или dl — сокращения слов dexter — laevus (правый — левый) для обозначения рацемических смесей или соединений оптических антиподов.
-ен — окончание для названий углеводородов с двойной связью, например пентен-2 СН3СН=СНСН2СН3. По номенклатуре IUPAC 1957 это окончание имеют также ароматические углеводороды, например: бензен (бензол), толуен (толуол), нафтален (нафталин), фенантрен и т. д.
i — сокращение от inactive (неактивный). Приставка, показывающая, что вещество оптически недеятельно (рацемат, мезо-форма). В иностранной литературе часто встречается как сокращенное обозначение приставки изо- (см. ниже).
изо- — приставка, указывающая на разветвленное строение цепи атомов углерода.
-ил — окончание для названий одновалентных радикалов: метил СН3—, этил С2Н5—, пропил С3Н7— и т. д.
-илен — окончание для названий углеводородов этиленового ряда: этилен СН2=СН2, пропилен СН3СН=СН2 и т. д. Такое же окончание имеют и названия некоторых двухвалентных радикалов, например: метилен —СН2—; этилен — СН2—СН2—; триметилен — СН2—СН2—СН2— и т. п.
-илиден — окончание для названий двухвалентных радикалов: этилиден
ВАЖНЕЙШИЕ ПРИСТАВКИ И ОКОНЧАНИЯ
-ит — окончание названий многоатомных спиртов: эритрит, пентит, гексит, маннит и т. д.
ката—приставка для обозначения 1,7-двузамещенных нафталина.
мезо- (иногда греческая буква «мю» μ) — приставка, указывающая на срединное положение замещающих групп в трициклических конденсированных системах, например: 9- или мезо-метилакридин (стр. 365); служит также для обозначения стереоизомеров соединений с двумя или несколькими асимметрическими атомами, оптически неактивных по внутренней компенсации вследствие общей симметрии молекулы (мезо-изомеры, мезо-формы).
мета- (м-) — приставка для обозначения 1,3-двузамещенных бензола, а иногда и других шестичленных циклов.
N — перед названием азотсодержащих соединений указывает на непосредственную связь радикала с азотом, например N-метилпиррол.
н- (или н.) обозначает, что молекула имеет нормальное (неразветвленное) строение цепи атомов углерода.
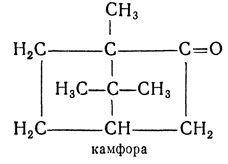
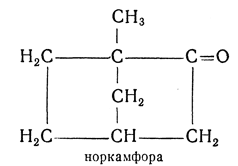
нор— приставка, обозначающая близкие производные, например камфора и норкамфора:
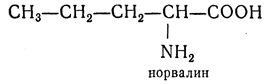
Обозначает также соединение с нормальной (неразветвленной) цепью (в отличие от изомера, имеющего разветвленную цепь), например:
О — перед названием радикала указывает на соединение его с кислородом, например О-метилацетоуксусный эфир:
-оза — окончание названий углеводов, главным образом моносахаридов и олигосахаридов, например: глюкоза, сахароза.
-ол—окончание в систематических названиях спиртов.
омега- (со) — приставка, обозначающая, что заместитель связан с крайним атомом углерода цепи; например ω-нитростирол С6Н5СН = СНNО2.
-он — окончание в систематических названиях кетонов.
орто- (о-) —приставка для обозначения 1,2-двузамещенных бензола, а иногда и других шестичленных циклов.
пара- (п-) —приставка для обозначения 1,4-двузамещенных бензола, а иногда и других шестичленных циклов.
перв— сокращение от первичный.
пери—приставка для обозначения 1,8-двузамещенных нафталина.
поли—приставка для обозначения полимеров, например полиэтилен (—СН2—СН2—)п, полибутадиен (—СН2—СН = СН—СН2—)п и т. п.
псевдо- (иногда греческая буква «пси» ψ) — приставка, обозначающая изомерную форму, например бутилен СН2 = СН—СН2—СН3 и псевдобутилен
СН3СН=СНСН3; кумол (изопропилбензол) и псевдокумол (1,2,4-триметилбензол).
прос- — приставка для названий 2,7-двузамещенных нафталина.
симм- — сокращение от симметричный; например симм-диметилэтилен СН3СН=СНСН3.
син — приставка для обозначения геометрических изомеров, обычно оксимов или гидразонов (см. анти-).
тер- — приставка для обозначения трех бензольных колец, соединенных в пара-положении; например терфенил.
-тиол — окончание названий тиоспиртов, или меркаптанов.
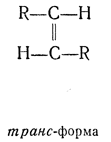
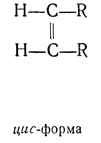
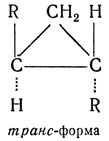
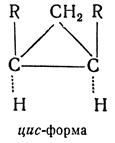
транс- — приставка для обозначения пространственных изомеров, указывающая на положение замещающих групп по разные стороны плоскости двойной связи, плоскости полиметиленового цикла и т. п. В противоположность этому приставка цис- обозначает одностороннее расположение групп в таких изомерах:
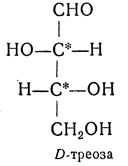
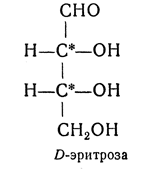
трео- — приставка, обозначающая, что в соединении два смежных асимметрических центра имеют одинаковую конфигурацию (как у моносахарида треозы); в противоположность этому приставка эритро- указывает на различную конфигурацию этих центров (как у моносахарида эритрозы):
трет- — сокращение от третичный.
-триен — окончание, показывающее наличие в молекуле трех двойных связей. -триин — окончание, показывающее наличие в молекуле трех тройных связей. -триол — окончание названий трехатомных спиртов, например пропантриол (глицерин) СН2ОНСНОНСН2ОН. трис- — см. бис-.
цис- — приставка для обозначения пространственных изомеров (см. транс-), цикло- — приставка для обозначения циклического строения:
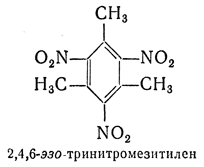
эзо- — приставка, показывающая, что замещающие группы присоединены к кольцу, например:
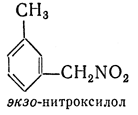
экзо- — приставка, показывающая, что замещающие группы находятся в боковой цепи, например:
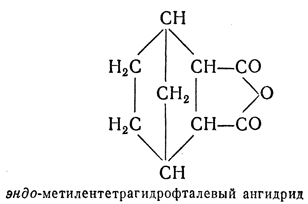
эндо- — приставка, показывающая, что группа расположена внутри кольца, например:
эпи- — приставка для обозначения 1,6-двузамещенных нафталина; применяется также для обозначения диастереоизомерных альдоз, отличающихся конфигурацией групп только у асимметрического атома углерода, соседнего с альдегидной группой (эпимерные альдозы; например, манноза может быть названа эпиглюкозой); указывает также на наличие внутримолекулярной мостиковой связи; например эпихлоргидрин
Номенклатура неорганических соединений (по правилам ИЮПАК)
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Номенклатура неорганических соединений (по правилам ИЮПАК).
ИЮПАК – международный союз теоретической и прикладной химии. Правила ИЮПАК 1970 г. являются международной моделью, по которой создаются номенклатурные правила для химических соединений на языке соответствующей страны. Эти правила являются компромиссными, т.к. допускают не только систематические, но и тривиальные наименования, т.е. они не в полной мере совершенны. Вместе с тем, правила ИЮПАК передают эмпирическую формулу, а иногда и основные структурные свойства соединения, отражая таким образом состав и очевидные свойства вещества.
Названия для групп элементов.
Элементы классифицируются как металлы, полуметаллы и неметаллы. Применение названия «металлоид» не рекомендуется.
Допускается использование следующих групповых названий: щелочные металлы (от Li до Fr), щелочноземельные металлы (от Ca до Ra), галогены (от F до At), халькогены (от О до Ро), благородные газы (от Не до Rn). Переходные элементы – элементы, атомы которых имеют незаполненную d-оболочку, или образующие катионы с незаполненной d – оболочкой. Редкоземельные элементы – металлы – Sc, Y, элементы от La до Lu. Лантаноиды – элементы от La до Lu, аналогично используются названия актиноиды, ураноиды и кюроиды.
Систематические названия для соединений.
Систематические названия соединений образуются путем указания составляющих и их соотношений в соответствии со следующими принципами. Многие природные химические соединения по существу бинарны, остальные соединения можно считать бинарными с точки зрения номенклатуры.
Электроположительная составляющая (катион) в формулах и названиях всегда занимает первое место, например, NaCl – натрий хлорид. Для соединений, содержащих более одного катиона и более одного аниона, внутри каждого класса составляющих должен быть алфавитный порядок их символов. Кислоты рассматриваются как водородные соли. Чтобы определить место комплексных ионов, во внимание принимается только символ центрального атома.
Если электроотрицательная составляющая – моноатомная или гомополиатомная, ее название изменяется в окончании на –ид. В формулах и названиях бинарных соединений неметаллов на первое место следует помещать составляющую, стоящую раньше (левее) в следующем ряду:
Rn, Xe, Kr, B, Si, C, Sb, As, P, N, H, Te, Se, S, At, J, Br, Cl, O, F.
Для бинарных соединений название элемента, стоящего дальше в этом ряду, изменяется в окончании на –ид, например, HCl – водород хлорид, OF2 – кислород дифторид.
Летучие гидриды, кроме элементов VII группы, кислорода и азота, можно называть с использованием суффикса –ан, например, Si2H6 – дисилан.
Допускаются названия вода, аммиак, гидразин, фосфин, арсин, стибин, висмутин.
Если электроотрицательная составляющая является гетерополиатомной, ее следует обозначить окончанием –ат. Термины сульфат, фосфат и т.д. обозначают, как правило, отрицательную группу с серой или фосфором в качестве центрального атома независимо от его состояния и количества и природы лигандов. Комплекс заключается в квадратные скобки [ ], но это не всегда обязательно.
Na2[SO4 ] – динатрий тетраоксосульфат
Na2 [S2O3 ] – динатрий триоксотиосульфат
K [PF2O2 ] – калий диоксодифторфосфат
Во многих случаях (если нет особой необходимости) эти названия могут быть сокращены, например, натрий сульфат, натрий тиосульфат.
N2O – диазот оксид, азот (I) оксид
NO2 – азот диоксид, азот (IV) оксид
V2O3 – диванадий триоксид, ванадий (III) оксид
VO1,5 – ванадий сесквиоксид, ванадий (III) оксид
V2O5 – диванадий пентаоксид, ванадий (V) оксид
N2S5 – диазот пентасульфид, азот (V) сульфид
FeCl2 – железо дихлорид или феррум дихлорид, железо (II) хлорид или феррум (II) хлорид
K4[ Ni(CN)4 ] – калий тетрацианоникколат (0).
«Функциональная» терминология, например, употребление названия «азотный ангидрид» для N2O5 не рекомендуется.
Названия для катионов и анионов.
Моноатомные катионы следует обозначать по названию элемента без его изменения для добавления суффикса. Например:
Cu 1+ – медь (I) ион
Сu 2+ – медь (II) ион
I + – иод (I) катион
Полиатомные катионы, образованные из моноатомных катионов путем добавления к ним других ионов, нейтральных атомов или молекул (лигандов), могут рассматриваться как комплексы. Например:
[Al(H2O)6 ] 3+ – гексаакваалюминий ион
[ COCl(NH3)5 ] 2+ пентаамминхлорокобальт (II) ион.
Названия для полиатомных катионов, возникающих при добавлении к моноатомным анионам большего числа протонов, чем требуется для получения нейтральной частицы, образуются путем добавления окончания –оний к корню названия элемента аниона: оксоний, фосфоний, арсоний, стибоний, сульфоний, селеноний, теллуроний, фтороний, иодоний ионы.
Исключением из этого правила является название аммоний для NH4 +
Названия для моноатомных анионов состоят из названия элемента с окончанием –ид:
Рекомендуется для названий моноатомных ионов всегда употреблять окончание – ид, когда заряд иона соответствует вышеуказанному.
Некоторые полиатомные анионы имеют названия, оканчивающиеся на –ид:
Названия для других многоатомных анионов должны состоять из корня названия центрального атома с окончанием –ат. Атомы и группы, присоединенные к центральному атому, обычно рассматриваются как лиганды в комплексе, например, [Sb(OH)6] – гексагидроксоантимонат (V) ион.
Название кислорода в анионах принято опускать, а присутствие этого элемента и пропорции указывать посредством приставок гипо-, пер- и т.д., а иногда также и суффикса –ит вместо –ат (для обозначения низших степеней окисления). Суффикс –ит можно сохранить в следующих традиционных названиях:
Номенклатура оснований и гидратов.
Номенклатура оснований подчиняется в принципе тем же правилам, что и для бинарных соединений. Наименования оснований складываются из названия электроположительной составляющей и слова гидроксид. Для металлов, имеющих различные степени окисления и образующих несколько оснований, к слову гидроксид добавляют приставки моно, ди и т.д. или указывают степень окисления:
КОН – калий гидроксид
Мо(ОН)2 – магний гидроксид
Fe(ОН)2 – железо гидроксид, железо (II) гидроксид.
Термины «смешанные оксиды» и смешанные гидроксиды» не рекомендуются. Такие соединения нужно назвать двойными, тройными и т.д.
У оксидов и гидроксидов металлы перечисляются в алфавитном порядке, например, AlLiMn2O4(OH)4 – алюминий литий димарганец (IV) тетрагидроксид тетраоксид.
Окончание -ат теперь является принятым окончанием для анионов и его не следует использовать для молекулярных соединений. Однако одно исключение признается. В соответствии со своим окончанием гидрат теперь твердо применяется для соединений, содержащих кристализационную воду, и допускается для обозначения воды, связанной неопределенным образом. Названия гидратов можно образовывать из названий отдельных соединений, записывая их через дефис и указывая в конце число молекул арабскими цифрами, разделенными дробной чертой:
3CdSO4· 8H2O – кадмий сульфат-гидрат (3/8)
Na2CO3 ·10H2O – натрий карбонат-гидрат (1/10) или натрий карбонат декагидрат
В случае, если имеются данные о структуре, возможно, например, такое обозначение: Fe(H2O)6SO4·H2O – гексаакважелезо (II) сульфат моногидрат.
Номенклатура кислот.
Номенклатура кислот имеет давнюю историю с прочно укоренившимися традициями. Правила ИЮПАК сохраняют наиболее полезные из старых названий, и в то же время в них делается попытка дать руководство для более рациональных названий новых соединений.
Кислоты, от которых образованы названия анионов с окончанием –ид, рассматриваются как двойные и псевдодвойные соединения водорода, например, H2S – водород сульфид, HCN – водород цианид.
В ряде случаев различие между разными степенями окисления характеристических атомов в оксокислотах указывается приставками. Но это обозначение не следует распространять за пределы случаев, перечисленных ниже.
Приставка гипо- применяется, чтобы обозначить более низкую степень окисления: HСlO гипохлористая кислота, HВrO – гипобромистая кислота, HJO – гипоиодистая кислота. В русской химической терминологии для этих соединений укоренились соответственно названия: хлорноватистая, бромноватистая, иодноватистая кислоты.
Приставка пер- применяется, чтобы обозначить более высокую степень окисления и сохраняется только для HСlO4 (перхлорная кислота) и для соответствующих кислот других элементов VII группы. Применение приставки пер- не должно распространяться на элементы других групп.
Приставки орто– и мета- применяются, чтобы распознать кислоты, различающиеся по «содержанию воды». Одобряются следующие названия:
H3BO3 – ортоборная кислота
H2SiO4 – ортокремниевая кислота
H3PO4 – ортофосфорная кислота
H5IO6 – ортопериодная кислота
H6TeO6 – ортотеллуровая кислота
(HBO2)n – метаборная кислота
(H2SiO3)n – метакремниевая кислота
(HPO3)n – метафосфорная кислота
Приставка пиро- применяется для обозначения кислоты, состоящей из двух молекул ортокислоты с вычетом одной молекулы воды. Название пирофосфорная кислота можно сохранить для H4P2O7, хотя название дифосфорная кислота предпочтительнее.
Когда приставка пероксо- применяется с тривиальными названиями кислот, она указывает замещение иона – О – ионом – О – О –. Например:
HNO4 – пероксоазотная кислота
Кислоты, образованные из оксокислот путем замещения кислорода серой, называются тиокислотами. Когда замещено более одного атома кислорода, количество атомов серы желательно указывать:
HSCN – тиоциановая кислота
Кислоты, содержащие другие лиганды, а не кислород и серу, обозначаются обычно по номенклатуре координационных соединений.
Нижеприведенный список содержит принятые названия для некоторых оксокислот и их пероксо- и тио- производных.
H2CO3 – угольная кислота
HOCN – циановая кислота
HNCO – изоциановая кислота
HONC – гремучая кислота
HNO3 – азотная кислота
HNO2 – азотистая кислота
H2NO2 – нитроксильная кислота
H2N2O2 – гипоазотистая кислота
H3PO5 – пероксомонофосфорная кислота
H2PHO3 – фосфоновая кислота
H3AsO4 – мышьяковая кислота
H2SO4 – серная кислота
H2S2O7 – дисерная кислота
H2S2O3 – тиосерная кислота
H2SO3 – сернистая кислота
H2SeO4 – селеновая кислота
H2SeO3 – селенистая кислота
H2CrO4 – хромовая кислота
H2Cr2O7 – дихромовая кислота
HСlO3 – хлорновая кислота
HBrO4 – пербромная кислота
HBrO3 – бромноватая кислота
HIO3 – иодноватая кислота
HMnO4 – пермарганцовая кислота
H2ReO4 – рениевая кислота
Номенклатура солей.
Простые соли относятся к классу бинарных соединений, и их названия образуют из названий составных ионов.
Названия солей, содержащих не полностью замещенный в кислоте водород («кислые соли»), с добавлением слова «водород». В случае необходимости перед водородом указывается числовой префикс. За водородом без пробела следует название аниона:
NaHCO3 – натрий водородкарбонат
LiH2PO4 – литий диводородфосфат
KHS – калий водородсульфид
В формулах двойных, тройных и др. солей катионы, кроме водорода, перечисляются в алфавитном порядке. Водород называется последним среди катионов. Если необходимо отметить присутствие какого-либо конкретного гидратированного катиона, его рассматривают как комплексный ион и указывают в названии в порядке алфавита:
KMgF3 – калий магний фторид
NaTl (NO3)2 – натрий таллий (I) нитрат или натрий таллий динитрат
Na(UO2)3[Zn(H2O)6](C2H3O2)9 – нонаацетат гексааквацинк натрий триуранил (VI)
BiClO – висмут оксид хлорид
MgCl(OH) – магний гидроксид хлорид
VOSO4 – ванадий (IV) оксид сульфат
ZrCl2O · 8H2O – цирконий оксид дихлорид октагидрат
Комплексные соли. Номенклатура комплексных соединений.
В названиях координационных соединений центральный атом следует указывать после лигандов.
Название соединений с комплексным анионом, например К3[Fе(СН)6], комплексным катионом [Li(H2О)4]NO3 и нейтральным комплексом [Pt(C2H4)(NH3)Cl2], в целом, строится так же, как и названия соответствующих солей или других сложных соединений. Для сравнения приведем названия этих комплексных соединений и соответствующих «некомплексных» аналогов:
Названия лигандов, являющихся нейтральными молекулами, обычно берутся без изменения.
Стехиометрические отношения можно указывать с помощью стехиометрических префиксов или не указывать вообще:
K3[Fe(CN)6] – гексацианоферрат (III) калия или трикалий гексацианоферрат
K4[Fe(CN)6] – гексацианоферрат (II) калия или тетракалий гексацианоферрат
Для сложных лигандов, которые сами содержат числительные, употребляют особые числительные: бис – 2, трис – 3, тетракис – 4:
[Co(NH3)3(NO2)3] 3+ – тринитротриамминкобальт (III)
K2[Zn(CNS)4] – тетрароданоцинкат(II) калия
[Zn(H2O)4](NO3)2 – тетрааквацинка (II) нитрат
K[Au(OH)4] – тетрагидроксоаурат (III) калия
[Pt(P(C6H5)3)2Cl2] – дихлорбистрифенилфосфинплатина (III)
Na2[Fe(CN)5NO] – нитрозилпентацианоферрат (III) натрия
K3[Fe(CN)5CO] – карбонилпентацианоферрат (II) калия
В соответствии с рекомендациями Международного союза теоретической и прикладной химии название комплексного аниона начинают с указания состава внутренней сферы. Во внутренней сфере, прежде всего называют лиганды – анионы, прибавляя к их латинскому названию окончание «о». Например: С1 – – хлоро, CN – – циано, SО3 2- – сульфито, ОН – – гидроксо
CH3COO – – ацетато
CH3OSOO – – метилсульфито
F – – фторо
I – – иодо
O2 – – оксо
H – – гидридо или гидро
OH – – гидроксо
O2 2 – – пероксо
Далее называют нейтральные лиганды. При этом пользуются терминами: для координированного аммиака – аммин, для воды – аква, для оксида углерода (II) – карбонил. Число лигандов указывают греческими числительными: 1 – моно, 2 – ди, 3 – три, 4 – тетра, 5 – пента, 6 – гекса. Затем называют комплексообразователь, используя корень его латинского названия и окончание ат, после чего римскими цифрами указывают (в скобках) степень окисления комплексообразователя. После обозначения состава внутренней сферы называют внешнесферные катионы.
В случае неэлектролитов (комплексообразователь и лиганды образуют не внутреннюю, а единственную комплексную сферу с нулевым зарядом) вместе с лигандами степень окисления центрального атома не приводят, так как она однозначно определяется, исходя из электронейтральности комплекса.
Если центральный атом входит в состав комплексного катиона, то используют русское название элемента и в скобках указывают его степень окисления. Приведем другие примеры: