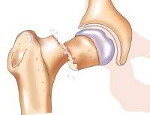
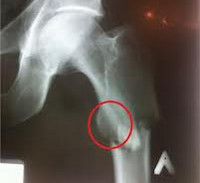
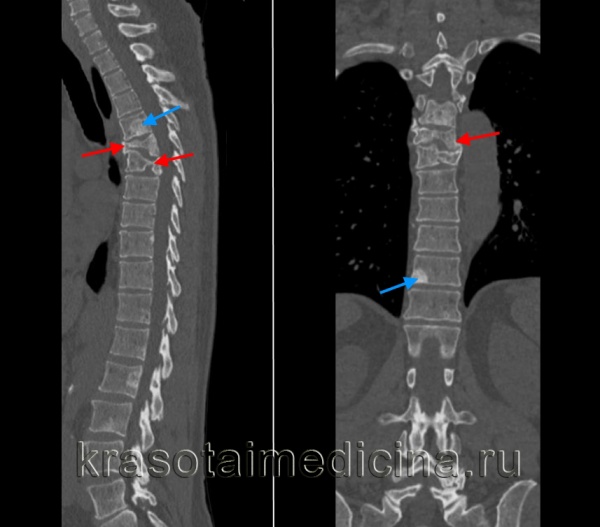
Что значит патологический перелом
Патологические переломы
Патологические переломы возникают у детей с заболеваниями костей скелета при воздействии незначительной травмирующей силы. Причиной таких переломов могут быть несовершенное костеобразование, фиброзная и хрящевая остеодисплазия, авитаминоз (рахит, цинга), воспалительные заболевания (остеомиелит, туберкулез) и др.
Патогенез (что происходит?) во время Патологических переломов:
Симптомы Патологических переломов:
Клинически несовершенное костеобразование проявляется искривлением конечностей вследствие множественных повторяющихся переломов или надломов костей, мышечной гипотрофии, наличием голубых склер, иногда «янтарных зубов» и понижением слуха. При врожденной форме уже у новорожденного обращает на себя внимание искривление конечностей с прогибом костей кнаружи или кпереди. В области переломов нередко пальпируется плотная костная мозоль. Число переломов у таких «стеклянных детей» бывает значительным. Несмотря на хрупкость костей, переломы быстро срастаются, однако в результате мышечной гипотрофии, неполной адаптации костных отломков, «эластичности» костной мозоли возникают деформации костей. Для заболевания характерны мягкость и податливость костей черепа у детей раннего возраста, что является причиной деформации головы у детей старшего возраста (в основном в переднезаднем направлении),
Диагностика Патологических переломов:
На рентгенограмме кости представляются нежными и тонкими, особенно тонкий кортикальный слой: губчатое вещество прозрачное и имеет едва заметный рисунок. Ясно бывают видны сросшиеся переломы. Вследствие множественных переломов конечности деформированы и укорочены.
Лечение Патологических переломов:
При несовершенном костеобразовании лечение переломов сводится в основном к тщательной репозиции, надежной иммобилизации до полной консолидации. Сроки фиксации перелома несколько удлиняются, несмотря на то что образование костной мозоли происходит быстро и в обычные возрастные сроки, но она еще длительное время остается «эластичной», в результате чего сохраняется возможность деформации конечности при сросшемся переломе.
Кроме локального лечения перелома, проводят общеукрепляющее лечение: ультразвуковые облучения, поливитамины, эргокальциферол (витамин D), рыбий жир, препараты кальция, соляной кислоты с пепсином. Целесообразно назначение анаболического гормона ме-тандростенолона (неробол), гормона щитовидной железы тиреокаль-цитонина внутримышечно. Лечение может проводиться и в амбулаторных условиях с соблюдением всех рекомендаций лечащих врачей стационара.
При часто повторяющихся переломах с выраженной и значительной деформацией конечностей рекомендуется оперативное лечение, которое состоит в основном в корригирующей остеотомии, интрамедуллярном остеосинтезе и костной ауто- или аллопластике для стимуляции репаративной регенерации костной ткани.
Кроме несовершенного костеобразования, патологические переломы наблюдаются при заболеваниях, нарушающих нормальную анатомическую структуру кости.
Формирование кисты кости является по существу дистрофическим процессом. Тип кисты зависит от биомеханических условий в том или ином отделе опорно-двигательного аппарата, от остро возникающих при аневризмальных или растянутых во времени солитарных кист нарушений гемодинамики в кости. Большинство солитарных кист локализуется в проксимальных отделах трубчатых костей. Чаще поражаются плечевая (56%) и бедренная (23%) кости. Процесс деструкции развивается медленно, бессимптомно и проявляется патологическим переломом. Большинство аневризмальных кист локализуется в губчатых костях с богатым артериальным кровоснабжением (позвонки; кости таза; концы костей, образующих коленный сустав). В анамнезе у всех больных имеется травма. Первыми симптомами являются легкая боль, ощущение неудобства, скованность. Клинико-рентгенологические проявления кист костей требуют проведения дифференциальной диагностики солитарных кист с фиброзной дисплазией, неостеогенной фибромой, гиперпаратиреозом, эозинофильной гранулемой. Аневризмальные кисты необходимо отличать от хондромиксоидной фибромы, остеогенной саркомы.
Показания к консервативному или оперативному лечению зависят от фазы патологического процесса, обширности поражения и данных кистографии, ангиографии, радиоизотопного исследования, биопсии и др.
При недостатке витаминов D и С возникает патологическая хрупкость костей. При рахите и цинге у детей младшего возраста наблюдаются переломы. Достаточно незначительной травмы или неловкого движения, чтобы у ребенка, болеющего рахитом, произошел перелом. Такие переломы, как правило, возникают в нижней трети бедренной кости и на костях предплечья. Часто они бывают поднадкостничными. Жалобы на боли незначительны, и перелом нередко просматривается; в таких случаях только при развитии мозоли и искривлении конечности выявляется бывший перелом, что подтверждается рентгенограммой.
Полные рахитические переломы срастаются медленно и требуют наряду с надежной иммобилизацией энергичного противорахитического общего лечения.
На рентгенограмме обнаруживается тень вокруг диафиза, которую дает кровоизлияние, а иногда отделение эпифиза от метафиза. Отделение эпифиза, кроме того, определяют на рентгенограмме по изменению положения ядра окостенения: тень ядра окостенения лежит не по средней линии, а смещается в сторону от оси конечности.
Заболевание цингой с поражением костей встречается при неправильном и неполноценном питании, направильном искусственном вскармливании. Иногда дети с поражением костей, обусловленным авитаминозом С, имеют «упитанный» вид; признаки истощения отсутствуют, так как у детей сохранена масса тела, хотя они получают однообразное неполноценное питание.
Общее лечение авитаминоза С, правильное питание, создание покоя выраженной конечности быстро улучшают состояние ребенка.
При воспалительных заболеваниях может разрушиться костная ткань, что ведет к патологическому перелому. К таким заболеваниям у детей относятся остеомиелит и туберкулез. Значительная деструкция костной ткани при остеомиелите может сопровождаться патологическим переломом. Они чаще всего наблюдаются в нижнем метафизе бедренной кости и в области шейки ее или в верхней трети плечевой кости. Кость, измененная патологическим процессом, может сломаться под влиянием незначительного насилия, часто почти неуловимого. Поэтому такого характера переломы называют самопроизвольными (спонтанными).
Распознавание патологического перелома при остеомиелите не представляет трудностей. Часто дети начинают жаловаться на усиление боли в конечности. При полных переломах со смещением определяются патологическая подвижность, деформация и укорочение конечности. Часто перелом обнаруживают случайно, во время перевязок. Уточняет диагноз рентгенологическое исследование.
Патологические переломы при остеомиелите иногда сопутствуют обострению воспалительного процесса, при недостаточной иммобилизации возникают деформации и укорочение конечности, в редких случаях образуются ложные суставы.
К каким докторам следует обращаться если у Вас Патологические переломы:
Патологический перелом
Патологический перелом – это нарушение целостности кости в области ее патологической перестройки. Возникает в результате незначительного травмирующего воздействия: падения с небольшой высоты, неинтенсивного удара или даже обычного напряжения мышц. Причиной развития является остеопороз, остеомиелит, злокачественные и доброкачественные новообразования костной ткани и некоторые другие заболевания. Клинические проявления обычно стертые, может наблюдаться боль, отек, ограничение функции конечности. Диагноз устанавливают на основании рентгенографии, МРТ, КТ, сцинтиграфии, биопсии и других исследований. Лечение чаще оперативное.
МКБ-10
Общие сведения
Патологический перелом – повреждение кости, прочность которой снижена в связи с каким-то заболеванием или патологическим состоянием. Наибольшее значение в силу своей распространенности, вероятных осложнений и возможного неблагоприятного исхода имеют патологические переломы при остеопорозе, нередко возникающие у людей пожилого и старческого возраста. Чаще всего в клинической практике встречаются патологические повреждения позвонков, шейки бедренной кости и дистального эпифиза лучевой кости.
Характерной особенностью данного вида повреждений является затруднение консолидации вследствие патологических изменений костной ткани. Из-за этого больные долго остаются обездвиженными, что становится причиной развития пролежней и застойных пневмоний, формирования тяжелых контрактур и т. д. Это, а также необходимость удаления опухоли при доброкачественных и злокачественных новообразованиях, обуславливает высокую частоту оперативных вмешательств. Лечение патологических переломов в зависимости от причины их возникновения могут осуществлять травматологи-ортопеды и онкологи.
Причины
Чаще всего патологическими переломами осложняются новообразования костей и фиброзные остеодистрофии. По статистике, патологическое нарушение целостности кости наблюдается в 50-60% солитарных кист. Немного реже травматические повреждения возникают при фиброзной дисплазии. При болезни Педжета и болезни Реклингхаузена кости ломаются в 40-50% случаев, при гигантоклеточных опухолях – в 15% случаев.
Своеобразные микропереломы всегда возникают при остеохондропатиях и в большинстве случаев – при врожденном сифилисе и детской цинге. Реже кости ломаются при остеомаляции и рахите и очень редко – при гемофилии. Патологическим переломом можно считать и нарушение целостности формирующейся костной мозоли, то есть, рецидив травматического перелома. Целостность кости также часто нарушается при анкилозах, в таких случаях атрофированная кость ломается поблизости от сустава. Многие специалисты относят к патологическим повреждениям переломы атрофированного и анкилозированного позвоночника при болезни Бехтерева.
Симптомы патологического перелома
Отличительной особенностью таких повреждений является слабая выраженность симптомов по сравнению с обычными травматическими переломами. Возможны незначительные или умеренные боли и нерезкая отечность пораженного сегмента. В ряде случаев такие переломы становятся первым проявлением патологического процесса в кости у людей, ранее считавших себя здоровыми. Достаточно часто патологическому нарушению целостности кости предшествуют костные деформации, неопределенные спонтанные боли или боли при нагрузке.
Значительное смещение фрагментов наблюдается очень редко. Часто возникают компрессионные поражения, надгибы, крупные трещины, вдавления и переломы трубчатых костей в виде подзорной трубы (поперечные повреждения, при которых истонченный корковый слой одного отломка надвигается на другой костный фрагмент). Патологическая подвижность и крепитация при подобных травмах отсутствуют, кровоизлияние может быть слабо выражено или вовсе не выражено. Все перечисленное затрудняет диагностику и становится причиной позднего обращения пациентов к врачам.
Диагностика
Диагноз выставляется с учетом жалоб, характерного анамнеза (незначительная травма), данных осмотра и дополнительных методов обследования. Наибольшее значение имеет рентгенография. Для более точной оценки состояния костей и окружающих мягких тканей также могут использоваться МРТ и КТ. При подозрении на метастазы большое значение приобретает сцинтиграфия, позволяющая в четыре раза чаще обычной рентгенографии выявлять метастатические поражения. При подозрении на остеопороз показана денситометрия. В некоторых случаях характер патологического процесса удается установить только при помощи биопсии.
Определенную диагностическую ценность имеют и лабораторные исследования. Для остеолитических процессов характерно выделение гидроксипромина, гиперкальциурия и гиперкальциемия. При остеопластических поражениях наблюдается снижение уровня кальция и повышение уровня щелочной фосфатазы в сыворотке крови. Вместе с тем, данные анализов в большинстве случаев не специфичны и могут рассматриваться только в качестве дополнительного диагностического критерия.
Лечение патологического перелома
Лечебная тактика определяется с учетом основного заболевания, а также локализации и характера повреждения. Целью хирургического вмешательства может быть сокращение сроков лечения в стационаре, ликвидация болевого синдрома, облегчение ухода за пациентом, ранняя активизация больного и улучшение его психоэмоционального состояния, а также уменьшение вероятности развития осложнений: пролежней, тромбофлебита, трофических язв, застойных пневмоний, гиперкальциемии и т. д.
Метод оперативного вмешательства выбирают с учетом особенностей патологического процесса. При доброкачественных опухолях выполняют резекцию пораженного участка (в ряде случаев – с замещением образовавшегося дефекта алло- или гомотрансплантатом) в сочетании с накостным или внутрикостным остеосинтезом. При онкологических поражениях на первый план нередко выходит не увеличение продолжительности, а улучшение качества жизни пациента.
Вместе с тем, при успешном лечении основного заболевания патологические переломы, являющиеся осложнением злокачественных опухолей, достаточно успешно срастаются, что также необходимо учитывать при выборе оперативной тактики. При поражении сустава или околосуставной области по возможности осуществляют эндопротезирование, при нарушении целостности диафиза – сегментарную резекцию в сочетании с укреплением поврежденного участка костным цементом или замещением дефекта трансплантатом. Отломки фиксируют, используя гвозди, пластины, штифты, винты или устанавливая аппараты Илизарова.
Патологический перелом
Патологический перелом – это перелом, причиной которого стала не травма, а болезнь.
Что такое патологический перелом?
Некоторые болезни существенно ослабляют наши кости. В результате, повседневные действия, на которые мы привыкли не обращать внимание, могут спровоцировать повреждение и перелом кости. Это может быть сильный кашель, попытка выйти из машины, или слишком тяжелая сумка.
Причины и симптомы патологического перелома
У патологических переломов нет особенных признаков. Они сопровождаются теми же симптомами, что и обычные переломы, связанные с травмой. К ним можно отнести:
— сильную боль в области перелома;
— синяки и отечность возле места перелома;
— онемение, покалывание и слабость в области перелома.
Существует множество причин патологических переломов. Самой распространенной из них является остеопороз. Остеопороз – заболевание, которое ослабляет ваши кости, из-за чего они начинают ломаться. Эта болезнь протекает бессимптомно, а первые признаки появляются только на поздних стадиях, когда кости уже слишком хрупкие и слабые. К другим симптомам остеопороза можно отнести:
— частые переломы в области тазобедренного сустава, позвоночника или запястья. Остеопороз – довольно распространенное заболевание, и, как правило, женщин оно поражает чаще, чем мужчин. По данным Национального фонда остеопороза, с патологическими переломами, связанными с этой болезнью, будут иметь дело около 50% женщин и 25% мужчин.
Симптомы рака зависят от его типа и стадии, но общие признаки включают:
— появление твердых комочков под кожей;
— отек и боль в месте распространения опухоли;
— увеличение лимфатических узлов;
— лихорадку, потливость, озноб;
— необъяснимую потерю веса;
— проблемы с кишечником;
— появление ран, которые не заживают;
— кашель или простуда, которые не лечатся.
Остеомаляция поддается лечению.
— чувство усталости и раздражительности;
— боль, отек и покраснение в месте поражения кости.
Менее распространенные болезни, которые могут стать причиной патологического перелома:
— доброкачественные опухоли и кисты;
Диагностика и лечение патологического перелома
Диагностика патологического перелома ничем не отличается от диагностики обычного перелома. Врач проведет физический осмотр, чтобы определить место перелома, а также сделает рентген поврежденной кости, который поможет увидеть сам перелом, и, не исключено, диагностировать его причину.
Анализы, которые помогают установить причину патологического перелома, включают:
— анализ крови для оценки уровня витамина D, кальция и фосфатов;
— биопсия кости для выявления опухоли, кисты, инфекции и т.д.
Лечение патологического перелома ничем не отличается от лечения обычного перелома, но оно должно походить на фоне лечения основной причины повреждения кости.
Все вышеперечисленные причины патологических переломов лечатся по-разному. Пока ваши кости будут восстанавливаться, а перелом заживать, вам придется часто отдыхать и жить в щадящем режиме, не нагружая свое тело, чтобы не спровоцировать еще один перелом.
5 вариантов завтрака, которые помогут избавиться от жира на животе
Неправильные формы микропластика разрушают клетки человека и вызывают аллергию
Бег в районах с плохой экологией так же опасен, как и низкий уровень физической активности
Ученые: Из-за устойчивости к антибиотикам будет ежегодно погибать 10 млн человек
Деятельность, которая может спровоцировать инсульт в течение следующих 60 минут
Исследование: Человек эволюционировал и стал жить долго благодаря постоянной физической нагрузке
Что значит патологический перелом
Введение. Лечение пациентов с доброкачественными опухолями и опухолеподобными заболеваниями костей у детей на сегодняшний день является актуальнейшей проблемой детской костной патологии. Одним из грозных осложнений течения опухолей и опухолеподобных заболеваний костей является патологический перелом. Патологическими считаются переломы, произошедшие под воздействием незначительной травмирующей силы или даже физиологических нагрузок на кость, измененную на фоне болезни [1]. Механизм взаимодействия патологической ткани и кости представляет собой сложный многоэтапный процесс. Под влиянием постепенно растущей в костномозговом канале опухоли, вследствие давления, костная ткань некротизируется, при этом кортикальный слой истончается, местами полностью исчезает, что является причиной перелома [2]. Растущая патологическая ткань продуцирует большое количество факторов, активирующих остеокласты или изменяющих гормональный фон организма с развитием распространенного остеопороза [3].
Риск возникновения патологического перелома в зависимости от характера процесса, по данным разных авторов, колеблется от 3 до 70% [4]. Наиболее часто переломы встречаются при кистах костей — в 50–60% случаев, при неостеогенных фибромах — в 35–40%, при хрящевых опухолях — в 20–30%, при фиброзной дисплазии — в 50%, при остеофиброзной дисплазии (болезни Кампаначчи) — в 30%, при гигантоклеточных опухолях — в 15–40% [5].
Несмотря на обилие современных методик остеосинтеза при переломах длинных костей, на сегодняшний день остается дискутабельным вопрос о методах профилактики и лечения патологических переломов у пациентов детского возраста.
Пациенты и методы
В период с 2000 по 2018 г. в отделении детской костной патологии и подростковой ортопедии ФГБУ «НМИЦ ТО им. Н.Н. Приорова» были прооперированы 82 пациента (51 — женского пола, 30 — мужского) в возрасте от 5 до 18 лет с патологическими переломами длинных костей на фоне аневризмальной кисты у 19 больных, солитарной кисты у 24, неостеогенной фибромы у 7, фиброзной дисплазии — у 20, остеофиброзной дисплазии у 2, гигантоклеточной опухоли у 3, болезни Олье у 6, гемангиомы у 1. Распределение пациентов по нозологическим формам с учетом локализации представлено в таблице. 
Остеосинтез пластиной осуществлялся в 29 случаях, аппарат внешней фиксации применялся у 1 пациента, у 51 больного перелом стабилизировали с помощью интраканальных аллотрансплантатов после удаления патологической ткани.
Комплексное обследование пациентов включало в себя ряд диагностических мероприятий: клинический осмотр; лучевые методы (рентгенография, компьютерная томография, магнитно-резонансная томография); морфологические методы (цитологический, гистологический).
При обследовании пациентов с подозрением на патологический перелом особое внимание обращали на появление жалоб, проявление первых симптомов заболевания, их связь с травмой, характер, интенсивность, иррадиацию боли. Оценивались общее физическое состояние, поза в покое, функция, наличие деформации, укорочения поврежденной конечности.
Патологические переломы в отличие от травматических являются низкоэнергетическими, возникают при воздействии незначительной травмирующей силы или при физиологических нагрузках и обычно сопровождаются меньшим болевым синдромом.
При неостеогенной фиброме патологические переломы возникали в результате травмы (падение с упором на пораженную конечность) и, как правило, проходили через область наибольшего поражения кости. Наиболее часто (у 6 пациентов) перелом образовывался в нижней трети большеберцовой кости. Патологические переломы в 4 случаях сопровождались выраженной болевой реакцией, отеком мягких тканей, нарушением функции конечности и смещением отломков.
У всех 20 пациентов переломы на фоне фиброзной дисплазии независимо от формы заболевания и локализации патологического процесса протекали с выраженным болевым синдромом, резким ограничением движений в прилежащем суставе, отеком мягких тканей и нарушением функции конечности.
Типичным симптомом остеофиброзной дисплазии являлась саблевидная деформация сегмента, связанная с эксцентричным вздутием пораженной кости. Болевой синдром объяснялся наличием микропереломов поврежденного сегмента.
Для патологических переломов при гигантоклеточных опухолях также были характерены выраженный болевой синдром, ограничение движений в близлежащем суставе, отечность в проекции очага поражения.
У 2 пациентов с патологическими переломами на почве болезни Олье и гемангиомы интенсивный болевой синдром был отмечен при значительном смещении костных отломков.
Основная роль в диагностике принадлежала лучевым методам исследования.
Рентгенологическое исследование позволяет выявить локализацию и характер перелома. Рентгенологическое обследование начинали после клинического осмотра и уточнения области исследования. Объем обследования определяли исходя из жалоб, клинической картины и допустимых доз облучения (для детей) (рис. 1). 
Для получения объемного изображения очага поражения, а также выявления истинного расположения костных отломков использовали компьютерную томографию. Послойное сканирование и высокая разрешающая способность с возможностью мультиспиральной реконструкции изображения позволяют достоверно определить размеры и локализацию патологического очага, что особенно важно при внутри- и околосуставных патологических переломах.
Магнитно-резонансную томографию применяли в тех случаях, когда требовалось определить точное расположение сосудисто-нервного пучка в зоне перелома и взаимодействие его структур с костными отломками.
Обязательной во всех случаях была морфологическая верификация диагноза.
Методы лечения
Выбор тактики лечения зависел от локализации, нозологии, размеров патологического очага и возраста пациента. Кроме того, учитывалось наличие смещения костных отломков.
Во всех случаях лечение начинали с морфологической верификации диагноза (трепан-биопсия патологического очага).
Переломы без смещения костных отломков вблизи от функционирующей зоны роста фиксировали консервативно гипсовыми повязками. Если же патологический перелом находился вдали от зоны роста, то тактика лечения зависела от нозологической принадлежности: при кистах костей и фиброзной дисплазии дожидались консолидации, а затем осуществляли хирургическое вмешательство, при других нозологиях сразу переходили к оперативному лечению. Первым этапом осуществляли краевую резекцию кости с удалением патологического очага в пределах здоровой ткани. После чего в той же операционной сессии выполнялся костно-пластический этап операции. Фиксация зоны перелома производилась на осевом трансплантате и гипсовой повязкой.
У пациентов с переломами со смещением отломков также учитывалось наличие функционирующей зоны роста: при смещении костных отломков вблизи от зоны роста лечение проводили в два этапа. На первом этапе выполняли закрытую репозицию с налаживанием системы скелетного вытяжения или фиксацию гипсовыми повязками. На втором этапе, после консолидации перелома, проводили костно-пластическую операцию. Если смещение костных отломков было существенным, а закрытая репозиция не приводила к достаточному устранению смещения, то за одну операционную сессию выполняли открытую репозицию, краевую резекцию кости с удалением патологического очага в пределах здоровой ткани и пластику пострезекционного дефекта с фиксацией спицами и гипсовой повязкой. У пациентов старшей возрастной группы (после 16 лет) фиксацию осуществляли пластиной в зависимости от степени функционирования зоны роста пораженного сегмента. Патологические переломы со смещением отломков, которые находились вне зоны роста, лечили оперативно. Проводили открытую репозицию отломков с их временной фиксацией спицами. Затем выполняли краевую резекцию кости с удалением патологического очага в пределах здоровой ткани и последующим костно-пластическим этапом. Далее следовал окончательный металлоостеосинтез пластиной и винтами.
Таким образом, пластика пострезекционного дефекта была применена у 81 пациента: в 7 случаях аутопластика, в 55 — аллопластика (в 24 — Перфоост, у 31 — замороженные кортикальные трансплантаты), в 16 — Перфоост в комбинации с замороженными кортикальными трансплантатами, в 3 — аутоаллопластика. Металлоостеосинтез применялся при 30 оперативных вмешательствах.
Патологические переломы при кистах кости наблюдались в 42 случаях. Нередко сам перелом являлся первым симптомом заболевания, что давало повод к проведению обследований пациента. Чаще (у 24 пациентов) переломы при кисте кости были без смещения. В таких случаях лечение начинали с адекватной иммобилизации пораженной конечности, поскольку известно, что у больных, перенесших патологический перелом на почве кисты, может произойти репарация патологического очага. Это объясняется посттравматическим дренированием полости кисты через линию перелома, одномоментным снижением внутрикостного давления, которое в течение длительного периода может сохраняться низким. В связи с этим метод консервативного лечения состоит в иммобилизации поврежденной конечности на срок, аналогичный сроку при высокоэнергетическом травматическом переломе, и динамическом наблюдении за областью кистозной трансформации в ожидании самоизлечения или уменьшения объема патологической полости. Репарация патологического очага после консолидации перелома наблюдалась только в 1 случае.
У 23 пациентов после консолидации перелома при расположении патологического очага вблизи функционирующей зоны роста в отделении проводили малоинвазивное пункционное лечение, если же патологический очаг находился вдали от нее, выполняли реконструктивно-пластические операции — краевую резекцию, аллопластику (рис. 2). 
При переломах со смещением (зафиксированы у 19 пациентов), которые возникали в случаях падения пациентов с высоты собственного роста или при прямом ударе в область кисты, после верификации диагноза выполняли оперативное вмешательство: открытую репозицию, краевую резекцию, аллопластику и накостный металлоостеосинтез (рис. 3). 
Патологические переломы при неостеогенных фибромах происходили в 7 случаях, в том числе 4 со смещением, 3 без смещения. Они были связаны как с бессимптомным течением самого заболевания, так и с недооценкой угрозы возникновения патологического перелома при ранее выявленном патологическом очаге. В случаях, когда течение заболевания было осложнено патологическим переломом, тактика лечения зависела от наличия смещения костных отломков. При его отсутствии допускалось консервативное лечение гипсовыми повязками. Поскольку сроки сращения патологических переломов при неостеогенных фибромах аналогичны установленным срокам при высокоэнергетических травматических переломах, а патологический очаг оставался в неизмененном виде, то после консолидации перелома выполняли костно-пластическую операцию. При наличии смещения костных отломков применяли открытую репозицию, краевую резекцию, аллопластику и фиксацию перелома пластиной или аппаратом внешней фиксации (рис. 4). 
При фиброзной дисплазии патологические переломы регистрировались в 20 случаях, из них 4 со смещением, 16 без. Наиболее часто происходили «ползущие переломы» с лоозеровской зоной перестройки в местах наибольшей нагрузки на сегмент, что при отсутствии лечения приводит к многоплоскостным деформациям конечности, таким как деформация проксимального отдела бедренной кости по типу «пастушьей палки». После определения диагноза выполняли реконструктивно-пластические операции с корригирующими остеотомиями на вершине деформации и фиксацией металлоконструкций. Однако оперативное лечение патологических переломов со смещением отломков в остром периоде нецелесообразно. Целесообразно провести репозицию и добиться сращения в сроки, которые превышают таковые при высокоэнергетических травматических переломах на 50%. В таком случае операция менее травматична, кровопотеря не настолько массивна и создаются более выгодные условия для перестройки аллотрансплантатов (рис. 5). 
Остеофиброзная дисплазия (болезнь Кампаначчи) — редкое и медленно прогрессирующее заболевание. В настоящем исследовании было зарегистрировано 2 патологических перелома на фоне остеофиброзной дисплазии: 1 со смещением костных отломков, 1 без таковых. После подтверждения диагноза морфологически осуществлялись открытая репозиция отломков, костная пластика с фиксацией металлоконструкций. Учитывая агрессивный характер течения заболевания и высокий процент возникновения рецидивов даже при полной органотипической перестройке трансплантатов, металлоконструкции не удаляли с целью профилактики возникновения патологических переломов в послеоперационном периоде (рис. 6). 
На фоне гигантоклеточных опухолей патологические переломы были отмечены в 3 случаях: в 2 без смещения костных отломков, в 1 со смещением. При лечении этой группы пациентов особое внимание уделяли предварительной морфологической верификации диагноза с целью исключения признаков озлокачествления. При диагностировании типичной гигантоклеточной опухоли выполняли сохранные костно-пластические операции как с накостным остеосинтезом, так и без него (рис. 7). 
При болезни Олье основные клинические проявления (деформация и укорочение пораженных сегментов скелета) возникают достаточно рано — в возрасте от 2 до 10 лет. Несмотря на то что заболевание диагностировалось в раннем возрасте и больные получали соответствующее оперативное лечение, эта категория пациентов оставалась в зоне риска возникновения патологических переломов, которые имели место в 6 случаях: 4 без смещения, 2 со смещением. При лечении пациентов проводилась краевая резекция кости с удалением патологического очага в пределах здоровой ткани и последующим замещением дефекта трансплантатами. Остеосинтез перелома выполнялся металлоконструкцией (рис. 8). 
Гемангиома длинных костей скелета встречается редко. Чаще всего патологический процесс протекает бессимптомно и является случайной находкой. При эксцентрическом расположении гемангиомы с интракортикальной деструкцией возникают патологические переломы. Такие переломы нами были зафиксированы в 1 случае. Оперативное вмешательство выполнялось в объеме: краевая резекция с последующей костной пластикой и фиксация пластиной (рис. 9). 
Результаты
Результаты лечения были прослежены в сроки от 1 года до 9 лет. Оценку эффективности лечения проводили с учетом онкологических и ортопедических критериев. Критериями эффективности являлись отсутствие жалоб, рецидива заболевания, признаки консолидации патологического перелома, функция оперированной конечности.
Всем пациентам были выполнены сохранные костно-пластические операции, лишь в 1 случае оперативное лечение не проводилось, поскольку была зафиксирована репарация патологического очага после сращения перелома на фоне кисты. Срок иммобилизации в гипсовой повязке составил 6 нед. В ситуациях с остальными пациентами оперативное лечение было необходимо. Учитывая отсутствие смещения или наличие незначительного смещения костных отломков и нозологическую принадлежность основного заболевания, фиксация гипсовыми повязками в 21 случае являлась первым этапом лечения. Фиксация преимущественно продолжалась 1 мес с момента травмы, тем самым осуществлялась консолидация перелома, что обеспечивало создание более благоприятных условий для проведения оперативного лечения. При значительном смещении первым этапом проводились трепан-биопсия для верификации диагноза и закрытая репозиция с целью устранения грубого смещения. После чего пораженная конечность фиксировалась гипсовой повязкой или накладывалась система скелетного вытяжения. После морфологической верификации диагноза пациентам выполнялись открытая репозиция перелома, удаление патологической ткани, аллопластика и по необходимости металлоостеосинтез. Пациентам, прооперированным без металлоостеосинтеза, применяли разгрузку и фиксацию пораженной конечности гипсовой повязкой в течение 3 мес с момента операции. Далее гипсовая повязка снималась и начиналась разработка движений в суставах оперируемой конечности. Полная нагрузка рекомендовалась через 4 мес с момента операции. Применение накостного остеосинтеза позволяло отказаться от использования внешней иммобилизации и начинать раннюю активизацию пациента, приступать к ранней разработке движений в суставах оперированной конечности, что в свою очередь способствовало уменьшению сроков стационарного лечения и облегчению ухода за больным.
При наличии металлофиксатора разработка движений в суставах пораженной конечности начиналась через 1 нед с момента операции, а полная нагрузка — через 1 мес. В послеоперационном периоде проводилось динамическое наблюдение всех пациентов, получивших оперативное лечение в отделении. Контрольные рентгенограммы осуществляли через 3, 6, 9 и 12 мес после операции. Консолидация переломов наблюдалась через 2,5–3 мес с момента операции. Сроки неорганотипической перестройки трансплантатов зависели от ряда факторов: объема пострезекционного дефекта, количества, вида и типа трансплантатов и нозологии заболевания. Наиболее быстро перестраивались аутотрансплантаты в сроки от 8 до 12 мес. При изолированном использовании трансплантатов Перфоост период перестройки занимал в среднем от 12 до 14 мес. В случаях массивной аллопластики при обширных резекциях костей, когда поверхностно деминерализированные аллоимплантаты сочетались с кортикальными замороженными имплантатами, срок перестройки увеличивался до 18 мес.
Сроки удаления металлоконструкций зависели от нозологии патологического процесса. При фиброзной и остеофиброзной дисплазиях, учитывая характер течения заболевания, металлоконструкции оставляли с целью профилактики возникновения деформации и патологических переломов в отдаленном послеоперационном периоде. В остальных случаях металлоконструкции удаляли через 1,5–2 года с момента операции.
В сроки от 3 до 6 мес были зарегистрированы следующие осложнения. При кистах кости: в 5 случаях — рецидив основного заболевания, в 2 — укорочение поврежденного сегмента, по 1 случаю — контрактуры суставов и неврологические расстройства; при фиброзной дисплазии: у 1 пациента — укорочение поврежденного сегмента; при неостеогенной фиброме: у 2 – контрактуры суставов. В отдаленные послеоперационные сроки (9–18 мес) при фиброзной дисплазии была отмечена миграция металлоконструкций в 2 случаях.
Обсуждение
При возникновении патологического перелома перед врачом прежде всего встают вопросы: как это осложнение повлияет на течение основного заболевания и какой тактикой лечения воспользоваться в каждом конкретном случае? На сегодняшний день существуют совершенно противоположные подходы к лечению патологических переломов.
По мнению многих авторов [6–15], в 7–15% случаев у больных, перенесших патологический перелом на почве кисты, происходит самоизлечение — закрытие кистозной полости. Это объясняется посттравматическим дренированием полости кисты через линию перелома, одномоментным снижением внутрикостного давления, которое в течение длительного периода может сохраняться низким, особенно при значительном смещении костных отломков. J. Farber и R. Stanton [16] представили данные о самостоятельном разрешении солитарных костных кист в каждом 4-м случае патологического перелома. В связи с этим предлагаемый метод консервативного лечения состоит в длительной иммобилизации поврежденной конечности и динамическом наблюдении за областью кистозной трансформации в ожидании самоизлечения или уменьшения объема патологической полости. J. Ahn и J. Park [17] провели ретроспективный анализ лечения 52 детей с патологическим переломами костей на почве солитарных кист и выявили, что в подавляющем числе случаев киста сохраняется, а иногда и увеличивается. По данным авторов настоящего исследования [29], из 42 пациентов с патологическими переломами на фоне кист кости репарация была отмечена лишь у 1.
Для стабилизации и заживления патологических переломов, а также предотвращения перелома и заживления костных кист у подростков после пункционной биопсии применяют канюлированные винты [18] или внутрикостные стержни Эдера, позволяющие избежать внешней иммобилизации [19].
В то же время Н.А. Шолохова [20], проанализировав результаты лечения более 80 пациентов с кистами костей, пришла к выводу, что патологический перелом на фоне кист костей не способствует снижению внутрикостного давления и закрытию патологического очага. Нецелесообразно также применение металлических конструкций (канюлированных винтов и стержней) при лечении кист костей в силу того, что эти методики не воздействуют на звенья патогенеза заболевания.
По мнению С.Т. Зацепина [2], при лечении патологических переломов на фоне гигантоклеточных опухолей необходимо отложить оперативное вмешательство на 2 нед с момента возникновения перелома, поскольку при переломе резко возрастает коагуляция крови, что приведет к неизбежной обширной кровопотере во время операции. Методика D. Alkalay и соавт. [21] предполагает двухэтапную операцию: на первом этапе выполняются репозиция после кюретажа и минимальная внутренняя фиксация, на втором — повторный кюретаж, криобработка полости, цементирование и стабильный остеосинтез.
А.В. Иванов и соавт. [22], учитывая, что хондромы фаланг кистей и стоп часто диагностируются при переломах, предлагают применять сразу экскохлеацию или резекцию опухоли, замещение дефекта ауто- или аллотрансплантатами с металлоостеосинтезом минипластинами. И.А. Карпенко и соавт. [23] считают, что для лечения пациентов с этими патологиями наиболее приемлем двухэтапный метод: первый этап — наложение дистракционного аппарата с целью репозиции перелома, второй этап — внутриочаговая резекция с костной пластикой.
При лечении патологических переломов на фоне фиброзной дисплазии большинство авторов отдают предпочтение оперативному лечению — репозиции перелома, удалению патологического очага и стабильной фиксации [24]. Однако R. Wirbel и соавт. [25] описывают случай излечения патологического перелома и остеофиброзной дисплазии в течение 10 мес у ребенка 4,5 лет после внутрикостного остеосинтеза титановым стержнем.
Авторы совершенно обоснованно выделяют возможные риски, способствующие возникновению патологических переломов, и советуют применять металлоостеосинтез пораженного сегмента с целью их профилактики [26].
Так, например, В.М. Шаповалов и соавт. [27] при наличии или риске возникновения патологического перелома на фоне доброкачественных опухолей сочетают костную пластику со стабильной внутренней фиксацией.
В то же время С.Т. Зацепин [2] у пациентов с доброкачественными поражениями, в том числе осложненными патологическими переломами, после обширной внутриочаговой резекции рекомендует выполнять костную пластику свежезамороженными кортикальными аллотрансплантатами с фиксацией на осевом трансплантате.
Л.М. Куфтырев и соавт. [28] отдают предпочтение внутрикостной резекции очага деструкции с последующей свободной аутопластикой из крыла подвздошной кости и фиксацией аппаратом Илизарова.
Таким образом, на сегодняшний день остаются дискутабельными вопросы, касающиеся средств фиксации патологических переломов и методов замещения пострезекционных дефектов. Также не существует единого мнения о методах профилактики возникновения патологических переломов у пациентов с доброкачественными опухолями и опухолеподобными заболеваниями.
Выводы
Поскольку не выработано единого протокола по выбору метода лечения детей и подростков с опухолями и опухолеподобными заболеваниями, течение которых было осложнено патологическими переломами, каждый случай требует дифференцированного подхода к лечению и зависит от характера, локализации перелома, а также возраста пациента и нозологической принадлежности основного заболевания, которое должно быть подтверждено морфологически.