Что значит не синтезируется в организме человека
Значение слова «синтезироваться»
1. Хим. Образоваться (образовываться) путем синтеза (во 2 знач.).
Источник (печатная версия): Словарь русского языка: В 4-х т. / РАН, Ин-т лингвистич. исследований; Под ред. А. П. Евгеньевой. — 4-е изд., стер. — М.: Рус. яз.; Полиграфресурсы, 1999; (электронная версия): Фундаментальная электронная библиотека
Источник: «Толковый словарь русского языка» под редакцией Д. Н. Ушакова (1935-1940); (электронная версия): Фундаментальная электронная библиотека
синтези́роваться
Делаем Карту слов лучше вместе

Спасибо! Я стал чуточку лучше понимать мир эмоций.
Вопрос: кроить — это что-то нейтральное, положительное или отрицательное?
Синонимы к слову «синтезироваться»
Предложения со словом «синтезироваться»
Понятия, связанные со словом «синтезироваться»
Отправить комментарий
Дополнительно
Предложения со словом «синтезироваться»
Тогда начнёт синтезироваться дофамин и простимулирует дальнейшую работу мозга.
Цистеин, тирозин и аргинин – могут в случае крайней необходимости синтезироваться организмом, поэтому их называют «условно незаменимыми».
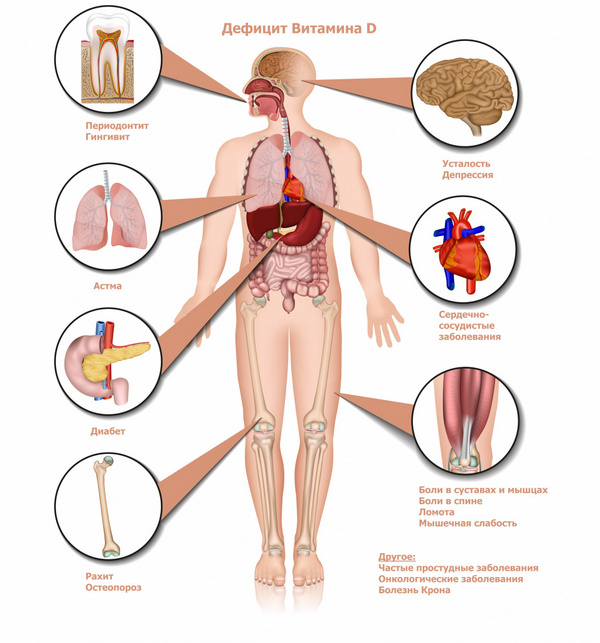
Витамин D способен синтезироваться в коже человека, но при обязательном облучении её солнцем или ультрафиолетовым (кварцевым) облучателем.
Все о гормонах: какие бывают, как работают, как их используют в медицине?
Андрей Смирнов СПИД.ЦЕНТР
Наши тела состоят из миллионов клеток, и для слаженной работы им постоянно нужно обмениваться информацией, чтобы координировать работу разных органов. Для этого у нас есть два принципиально разных канала передачи информации: нервный (с помощью нервных импульсов) и гуморальный — с помощью гормонов и некоторых других веществ. «СПИД.ЦЕНТР» публикует подробный разбор устройства гормонов и их использования в лечении.
Зачем нужны гормоны? Какую роль они играют в организме?
Наши тела состоят из миллионов клеток, и для слаженной работы им постоянно нужно обмениваться информацией, чтобы координировать работу разных органов. Для этого у нас есть два принципиально разных канала передачи информации: нервный (с помощью нервных импульсов) и гуморальный — с помощью гормонов и некоторых других веществ.
Что вы делаете, если нужно сообщить человеку информацию, но он находится на другом конце города? Проще всего позвонить или написать сообщение. Для похожих целей в нашем организме используется нервная система — когда мы хотим, например, поднять руку, мозг «звонит» определенным мышечным волокнам через «телефонные провода» — нервы — и отдает соответствующую команду. Но как быть, если нужно передать какое-то сообщение сразу всем жителям города? Звонить каждому — слишком долго. Для этого у нашего организма есть свои СМИ — их функцию выполняют гормоны.
Название гуморального пути передачи информации происходит от латинского слова humor — «жидкость», так как в этом случае регулирующее вещество (гормон) вырабатывается одними клетками и попадает в жидкие среды организма (кровь, лимфу, межтканевую жидкость). Когда он по ним распространяется, то оказывает влияние на работу других клеток (клеток-мишеней).
Гуморальный путь регуляции эволюционно гораздо более древний, чем нервный. Еще в первых многоклеточных организмах клетки научились общаться между собой с помощью специальных веществ задолго до возникновения прообраза нервной системы.
Чем отличается нервная регуляция от гормональной?
Нервная регуляция работает гораздо быстрее — импульс по нервным волокнам передается за доли секунды. А между тем, как гормон выделится, попадет в кровь и доберется до клетки-мишени, могут проходить десятки секунд. При этом гормоны действуют на мишени гораздо дольше, до тех пор, пока будут оставаться в крови. Это могут быть минуты, часы или даже дни.
К тому же нервная регуляция узконаправленная — нервный импульс передается только определенным группам клеток, связанным нервным окончанием. А когда гормон выделился в кровь, он может влиять на любую клетку с подходящим рецептором.
Поэтому, когда информацию нужно передавать быстро и точно, используется нервный путь, но если надо охватить сразу много клеток, то гуморальный. Например, во время ходьбы мозгу нужно очень быстро и точно напрягать и расслаблять десятки разных мышц, причем каждую их них — в строго определенный момент времени. Для этого отлично подходят нервные импульсы. Но чтобы отрегулировать уровень глюкозы в крови, нужно сообщить сразу всем клеткам организма, с какой скоростью они эту глюкозу могут из крови поглощать, и это гораздо удобнее сделать с помощью гормона.
В нашем организме оба пути регуляции объединены в общую систему нейрогуморальной регуляции и работают синхронно под контролем центральной нервной системы, гипоталамуса и гипофиза.
Чем гормоны отличаются друг от друга?
С точки зрения химической природы гормоны очень сильно различаются — они могут быть производными аминокислот (тироксин, адреналин), стероидами (кортизол, половые гормоны), полипептидами и белками (окситоцин, инсулин). При этом у всех гормонов есть общие свойства.
Гормоны секретируются специализированными железами и влияют на работу других органов и клеток за пределами самой железы.
Гормоны влияют на работу органов и клеток в очень маленьких концентрациях.
Гормоны влияют на клетки, связываясь с рецепторами — специальными белками на поверхности клеток. Если у клетки нет рецептора для соответствующего гормона, она никак не отреагирует на этот гормон.
Гормоны действуют через изменение скорости синтеза ферментов в клетках или через изменение скорости ферментативных реакций в клетках, но при этом сами не являются ферментами.
Как правило, у гормонов много различных физиологических эффектов и они по-разному влияют на органы и ткани.
То или иное вещество может не всегда выступать как гормон. Например, норадреналин — это гормон надпочечников, он влияет на тонус сосудов, работу сердца и других органов. В то же время он выделяется в синапсах и участвует в передаче сигналов между нейронами — в этом случае он уже играет роль нейромедиатора, а не гормона.
Где вырабатываются гормоны?
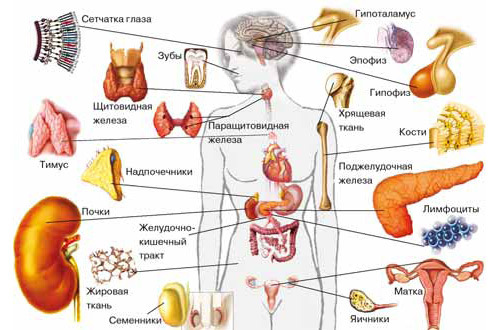
Большинство из них вырабатываются в специальных органах — железах внутренней секреции, или эндокринных железах. Основные из них:
эпифиз (шишковидное тело);
Работа эндокринных желез регулируется гипоталамусом и гипофизом. В общем виде это выглядит так: гипоталамус под влиянием нервных импульсов выделяет специальные вещества — рилизинг-факторы. Они стимулируют выработку гормонов гипофиза (тропинов, или тропных гормонов), и уже под их влиянием другие железы начинают секретировать свои гормоны.
Важный элемент регуляции работы эндокринных желез — отрицательная обратная связь. Гипофиз постоянно контролирует концентрацию каждого гормона в крови, и когда какого-то гормона становится слишком много, он дает команду «горшочек, не вари» нужной железе.
Как связаны гормоны с биоритмами?
Уровень секреции гормонов в организме постоянно меняется. У одних гормонов он не ритмичен и зависит от внешних факторов, так, секрецию инсулина стимулирует прием пищи. Но все же секреция многих гормонов работает с четкой периодичностью — это называют циркадными ритмами. Их изучает отдельная наука — хронобиология.
Суточный ритм организма человека выглядит так: с наступлением темноты повышается секреция гормона сна — мелатонина. Это вещество синтезируется в эпифизе (шишковидной железе), способствует наступлению сна и выделяется всю ночь. Кстати мелатонин может с возрастом меньше синтезироваться — это одна из причин, почему пожилые люди чаще страдают бессонницей. А хронотипы сов и жаворонков появляются именно из-за разных по времени (разница в несколько часов) пиковых концентраций мелатонина и кортизола.
по теме
Лечение
Как устроен иммунитет: Объясняем по пунктам
Когда человек спит, также меньше выделяется гормонов надпочечников (гормонов стресса) и одновременно повышается секреция соматотропного гормона (СТГ) — он отвечает за стимуляцию роста различных тканей. Пик концентрации СТГ приходится на 2-3 часа ночи. Так что утверждение, что мы растем во сне, — научно доказанный факт.
Около 5-7 утра снова повышается выделение гормонов надпочечников, а с восходом солнца перестает синтезироваться мелатонин — все это помогает проснуться. Также на утренние часы приходится пик концентрации тестостерона, с чем связано возникновение утренней эрекции у мужчин.
Помимо суточных ритмов есть и более продолжительные циклы колебания уровня гормонов. Например, изменение уровня женских половых гормонов происходит с периодичностью примерно в 28 дней и регулирует течение менструального цикла. Причем концентрация гормонов существенно меняется на протяжении жизни. В подростковом возрасте гораздо больше синтезируется гормона роста, а в пожилом — существенно меньше вырабатывается половых гормонов.
Как гормоны используют в медицине?
Учитывая мощное и многогранное влияние гормонов на организм, многие из них широко применяются в медицинской практике. Есть несколько основных направлений их использования.
Первый — заместительная гормональная терапия (ЗГТ). Обычно именно ее имеют в виду, сообщая близким трагическим голосом: «Врач назначил мне гормоны» и «Я никогда с них не слезу», готовясь к каким-то ужасным побочным эффектам и необратимым изменениям в организме. На практике все оказывается гораздо прозаичнее: побочных эффектов почти нет или они быстро проходят, человек продолжает обычную жизнь, и ЗГТ на нее практически никак не влияет.
Эта терапия назначается, когда в организме не вырабатывается нужный гормон в необходимых количествах. Учитывая важную роль гормонов, своевременное назначение терапии позволяет избежать серьезных или даже необратимых проблем со здоровьем.
Как правило, гормональная терапия назначается пожизненно, так как в большинстве случаев причины подобных проблем современная медицина еще не научилась решать. И здесь важно не путать причину со следствием: невозможность «слезть с гормонов» связана не с влиянием самой ЗГТ, а с тем, что недостаточность собственной эндокринной функции никуда не исчезнет.
Возможно, страх перед ЗГТ связан с историческими причинами: первые препараты гормонов часто выделяли их желез животных (например, бычий или свиной инсулин), они содержали много примесей и действительно имели не самую хорошую переносимость. Сейчас для ЗГТ используют современные высокоочищенные препараты гормонов человека — они безопасны и эффективны.
В большинстве случаев при назначении гормональной терапии не нужна корректировка доз или отмена других препаратов (например, антиретровирусной терапии), так как ЗГТ имитирует естественную работу эндокринных желез. Но некоторые особенности течения основного заболевания все же нужно учитывать. Например, если лекарство содержит в качестве вспомогательных веществ глюкозу, мальтозу, сахар или другие углеводы, их количество нужно учитывать пациентам, получающим инсулин. Также следует учитывать влияние на активность печеночных ферментов некоторых АРВ-препаратов, например, ингибиторов протеазы. Если соответствующие печеночные ферменты участвуют в расщеплении назначенного гормонального препарата, может потребоваться коррекция дозы гормона — это проверяет и учитывает врач.
Могут ли гормонами лечить заболевания, не связанные с самими гормонами?
Да, это еще одно направление их использования. Например, адреналин повышает артериальное давление благодаря сокращению сосудов и усилению работы сердца. Поэтому его используют для лечения шоковых состояний, когда нужно быстро повысить артериальное давление. А у глюкокортикоидных гормонов мощное противовоспалительное действие, и они подавляют реакции иммунной системы, поэтому их очень широко используют при лечении аллергических заболеваний, бронхиальной астмы и других хронических воспалительных заболеваний.
Во многих случаях «природный» гормон помимо полезного эффекта для лечения заболевания обладает и нежелательными. У мужских половых гормонов есть мощное анаболическое действие — усиливают синтез белка и рост мышц. Это полезно при лечении людей с тяжелой степенью истощения (например, после сильных ожогов). Но в то же время они влияют на половую сферу, повышают агрессивность, могут приводить к чрезмерному увеличению предстательной железы.
Уменьшить ненужные «лишние» эффекты можно с помощью синтетических и полусинтетических аналогов. То есть подбираются вещества, близкие по химической структуре к природному гормону, но при этом у них «нужное» действие более выражено, а «лишние» минимизированы. Именно таким путем из природных мужских половых гормонов получили анаболики — они сильнее стимулируют синтез белка и меньше влияют на половую сферу, чем тестостерон. Сейчас синтетические аналоги гормонов применяют значительно чаще, чем сами природные гормоны.
Также в медицине используют антагонисты гормонов. Это вещества, которые связываются с рецептором природного гормона на поверхности клетки, но при этом характерного влияния не оказывают. Такие вещества часто используют для лечения заболеваний, связанных с избыточной секрецией гормона или когда вредны даже «нормальные» концентрации. Например, некоторые злокачественные опухоли активно растут под влиянием определенных гормонов, и чтобы остановить рост опухоли, нужно «выключить» действие гормона. Так, опухолям предстательной железы для роста часто требуется стимулирующее влияние тестостерона. Один из способов лечения — назначить бикалутамид. Этот препарат связывается с тестостероновыми рецепторами опухоли, блокирует влияние тестостерона и тормозит рост опухоли.
При назначении гормональных препаратов на фоне другой терапии, в том числе и АРВТ, требуется обязательная проверка совместимости препаратов, как и в случае совместного назначения любых других лекарственных средств.
Зачем трансгендерные люди пьют гормоны? И как это работает?
Половые гормоны влияют не только на развитие и функцию репродуктивной системы, но также и на развитие вторичных половых признаков, формируя «мужской» или «женский» внешний облик. Поэтому прием половых гормонов часто является важной частью трансгендерного перехода: такая терапия влияет на внешность гораздо сильнее хирургический операций.
Гормоны в организме человека. За что они отвечают
Гормоны – биологически активные вещества, вырабатывающиеся клетками эндокринных желез (желез внутренней секреции). Оттуда они поступают в кровь и с кровотоком попадают в клетки и ткани-мишени.
Там они связываются со специфическими рецепторами и таким образом регулируют обмен веществ и множество физиологических функций. Так, они отвечают:
Как работает эндокринная система
Разные внешние или внутренние раздражители действуют на чувствительные рецепторы. В результате формируются импульсы, которые действуют на гипоталамус (отдел головного мозга). В ответ на них в гипоталамусе вырабатываются биоактивные вещества, поступающие по локальным сосудам в другой отдел головного мозга – гипофиз.
В ответ на их поступление в гипофизе вырабатываются гормоны гипофиза. Они попадают в кровь и, достигнув с кровотоком конкретной эндокринной железы, стимулируют в ней синтез того или иного гормона. А затем уже этот гормон поступает с кровью к гормональным рецепторам органов-мишеней, как описано выше.
По химическому строению гормоны делят на 4 вида
Стероиды – производные холестерина. Вырабатываются в коре надпочечников (кортикоиды) и половых железах (андрогены, эстрогены). В эту же группу входит кальцитриол.
Производные жирных кислот– эйкозаноиды. К ним относятся простагландины – повышают чувствительность рецепторов к боли и воспалительным процессам, тромбоксаны – участвуют в процессах свертывания крови, лейкотриены – участвуют в патогенезе бронхоспазма.
Производные аминокислот, преимущественно тирозина – гормон стресса адреналин, предшественник адреналина норадреналин и гормоны щитовидной железы.
Белково-пептидные соединения – гормоны поджелудочной железы инсулин и глюкагон, а также гормон роста соматотропин и кортикотропин – стимулятор синтеза гормонов коры надпочечников. В эту же группу входит антидиуретический гормон вазопрессин, «гормон материнства» окситоцин и ТТГ и АКТГ.
По месту образования выделяют гормоны:
По механизму действия различают гормоны:
По биологическим функциям различают гормоны, регулирующие:
Функции основных гормонов в организме
Список по названиям
Тестостерон — вырабатывается и у мужчин, и у женщин. Отвечает:
Эстрогены – женские половые гормоны. Отвечают за формирование первичных половых признаков у женщин. Обеспечивают репродуктивные функции и эмоциональное состояние. У мужчин вырабатываются в жировой ткани живота из тестостерона. Стимулируют синтез коллагена и обеспечивают эластичность кожи. Принимают участие в работе кровеносной системы.
Прогестерон – сохраняет беременность и обеспечивает менструальный цикл у женщин. Кроме этого, и у женщин, и у мужчин он:
Дигидроэпиандростерон – вырабатывается в головном мозге и надпочечниках.
Д-гормон (так называемый витамин Д):
ТТГ — тиреотропный гормон гипофиза. Регулирует выработку гормонов щитовидной железы трийодтиронина Т3 и тироксина Т4. При дисбалансе гормонов щитовидной желез развиваются гипер- и гипотиреоз.
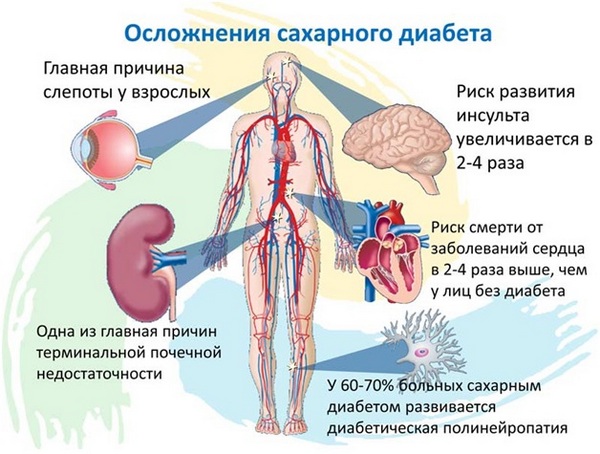
Инсулин – отвечает за усвоение глюкозы клетками. Стимулирует мышечный рост и аппетит. При нехватке инсулина развивается сахарный диабет. Избыток инсулина приводит к инсулинорезистентности (снижение чувствительности инсулинозависимых клеток к действию инсулина с последующим нарушением метаболизма глюкозы и поступления ее в клетки), что ведет к ожирению и развитию сахарного диабета 2 типа.
Дигидротестостерон – влияет на рост волос, образование акне, увеличение простаты у мужчин.
Кортизол – образуется из прогестерона. Адаптирует организм к влиянию стресса, защищает от воспалений, аллергических реакций, поддерживает в норме артериальное давление.
Альдостерон – гормон коры надпочечников; образуется из прогестерона. Отвечает за обмен солей и воды в организме.
СТП (соматотропный гормон) – гормон роста, избыток которого ведет к развитию акромегалии.
В каких случаях нужно сдавать анализы на гормоны
Если баланс эндокринной системы нарушается, в организме развиваются изменения. Нередко достаточно предельно малых отклонений от нормы, чтобы запустить патологический процесс.
Достаточно долго такие патпроцессы могут протекать бессимптомно. Когда же появляется симптоматика, то нередко патогенез уже необратим. Чтобы выявлять бессимптомные гормональные нарушения на ранних стадиях современная доказательная медицина настоятельно рекомендует пакетные проверки. Один раз в 6-12 месяцев достаточно сдать кровь на анализ, чтобы оценить состояние эндокринной системы и не допустить развития гормональных заболеваний.
Кроме этого, о необходимости сдать анализ на гормоны может свидетельствовать ряд признаков:
Также обязательно контролировать уровень гормонов при беременности, чтобы не допустить аномалий развития плода.
При планировании беременности необходимо пройти обследование щитовидной железы: сделать УЗИ щитовидной железы, пройти исследования гормонов ТТГ, Т4 свободный (свободный тироксин) и АТ к ТПО (антитела к тиреопероксидазе)
Во время беременности, если есть нарушение функций щитовидной железы, необходимо 1 раз в триместр проводить скрининг гормона ТТГ и консультироваться у эндокринолога.
Алгоритм метаболизма

Решение организационных вопросов питания у лиц старших возрастов, разработка и назначение индивидуализированных рационов рационального, профилактического и лечебного питания в существенной степени зависит от правильной оценки врачом нутриционного статуса пожилого человека, особенностей состояния обменных процессов. Именно поэтому профессионально грамотный клиницист, участвующий в решении проблем лечебно-профилактического питания у лиц пожилого и старческого возраста, должен быть достаточно хорошо ориентирован в области основ клинической биохимии и физиологии питания стареющего организма.
Белковый обмен
Белки — сложные азотсодержащие биополимеры, мономерами которых служат аминокислоты (органические соединения, содержащие карбоксильные и аминные группы). Их биологическая роль многообразна. Белки выполняют в организме пластические, каталитические, гормональные, транспортные и другие функции, а также обеспечивают специфичность. Значение белкового компонента питания заключается прежде всего в том, что он служит источником аминокислот.
Аминокислоты делятся на эссенциальные и неэссенциальные в зависимости от того, возможно ли их образование в организме из предшественников. К незаменимым аминокислотам относятся гистидин, лейцин, изолейцин, лизин, метионин, фенилаланин, триптофан и валин, а также цистеин и тирозин, синтезируемые соответственно из метионина и фенилаланина. Девять заменимых аминокислот (аланин, аргинин, аспарагиновая и глутамовая кислоты, глутамин, глицин, пролин и серин) могут отсутствовать в рационе, так как способны образовываться из других веществ. В организме также существуют аминокислоты, которые продуцируются путем модификации боковых цепей вышеперечисленных (например, компонент коллагена — гидроксипролин — и сократительных белков мышц — 3-метилгистидин).
Большинство аминокислот имеют изомеры (D- и L-формы), из которых только L-формы входят в состав белков человеческого организма. D-формы могут участвовать в метаболизме, превращаясь в L-формы, однако утилизируются гораздо менее эффективно.
Взаимоотношение аминокислот
По химическому строению аминокислоты делятся на двухосновные, двухкислотные и нейтральные с алифатическими и ароматическими боковыми цепями, что имеет большое значение для их транспорта, поскольку каждый класс аминокислот обладает специфическими переносчиками. Аминокислоты с аналогичным строением обычно вступают в сложные, часто конкурентные взаимоотношения.
Так, ароматические аминокислоты (фенилаланин, тирозин и триптофан) близкородственны между собой. Хотя фенилаланин является незаменимой, а тирозин — синтезируемой из него заменимой аминокислотой, наличие тирозина в рационе как будто бы «сберегает» фенилаланин. Если фенилаланина недостаточно или его метаболизм нарушен (например, при дефиците витамина С) — тирозин становится незаменимой аминокислотой. Подобные взаимоотношения характерны и для серосодержащих аминокислот: незаменимой — метионина — и образующегося из него цистеина.
Триптофан в ходе превращений, для которых необходим витамин В 6 (пиридоксин), включается в структуру НАД и НАДФ, то есть дублирует роль ниацина. Приблизительно половина обычной потребности в ниацине удовлетворяется за счет триптофана: 1 мг ниацина пищи эквивалентен 60 мг триптофана. Поэтому состояние пеллагры может развиваться не только при недостатке витамина РР в рационе, но и при нехватке триптофана или нарушении его обмена, в том числе вследствие дефицита пиридоксина.
Аминокислоты также делятся на глюкогенные и кетогенные, в зависимости от того, могут ли они при определенных условиях становиться предшественниками глюкозы или кетоновых тел (см. табл. 1).
Таблица 1. Классификация аминокислот
| Виды | Эссенциальные аминокислоты | Неэссенциальные аминокислоты |
| Алифатические | Валин (Г), лейцин (К), изолейцин (Г, К) | Глицин (Г), аланин (Г) |
| Двухосновные | Лизин (К), гистидин (Г, К)* | Аргинин (Г)* |
| Ароматические | Фенилаланин (Г, К), триптофан (Г, К) | Тирозин (Г, К)** |
| Оксиаминокислоты | Треонин (Г, К) | Серин (Г) |
| Серосодержащие | Метионин (Г, К) | Цистеин (Г)** |
| Дикарбоновые и их амиды | Глутамовая кислота (Г), глутамин (Г), аспарагиновая кислота (Г), аспарагин (Г) | |
| Иминокислоты | Пролин (Г) |
Обозначения: Г — глюкогенные, К — кетогенные аминокислоты; * — гистидин незаменим у детей до года; ** — условно-незаменимые аминокислоты (могут синтезироваться из фенилаланина и метионина).
Необходимые азотсодержащие соединения
Поступление азотсодержащих веществ с пищей происходит в основном за счет белка и в менее значимых количествах — свободных аминокислот и других соединений. В животной пище основное количество азота содержится в виде белка. В продуктах растительного происхождения большая часть азота представлена небелковыми соединениями, также в них содержится множество аминокислот, которые не встречаются в организме человека и зачастую не могут метаболизироваться им.
Синтез пуриновых оснований
Человек не нуждается в поступлении с пищей нуклеиновых кислот. Пуриновые и пиримидиновые основания синтезируются в печени из аминокислот, а избыток этих оснований, поступивших с пищей, выводится в виде мочевой кислоты.
Прием белка
Обычный (но не оптимальный) ежедневный прием белка у среднестатистического человека составляет приблизительно 100 г. К ним присоединяется примерно 70 г белка, секретируемого в полость желудочно-кишечного тракта. Из этого количества абсорбируется около 160 г. Самим организмом в сутки синтезируется в среднем 240–250 г белка. Такая разница между поступлением и эндогенным преобразованием свидетельствует об активности процессов обратного восстановления исходного сложного химического соединения из «осколков», образовавшихся при его метаболизме (ресинтеза белков из аминокислот, а аминокислот из аммиака и «углеродных скелетов» аминокислот).
Азотное равновесие
Для здорового человека характерно состояние азотного равновесия, когда потери белка (с мочой, калом, эпидермисом и т. п.) соответствуют его количеству, поступившему с пищей. При преобладании катаболических процессов возникает отрицательный азотный баланс, который характерен для низкого потребления азотсодержащих веществ (низкобелковых рационов, голодания, нарушения абсорбции белка) и многих патологических процессов, вызывающих интенсификацию распада (опухолей, ожоговой болезни и т. п.). При доминировании синтетических процессов количество вводимого азота преобладает над его выведением, и возникает положительный азотный баланс, характерный для детей, беременных женщин и реконвалесцентов после тяжелых заболеваний.
После прохождения энтерального барьера белки поступают в кровь в виде свободных аминокислот. Следует отметить, что клетки слизистой оболочки желудочно-кишечного тракта могут метаболизировать некоторые аминокислоты (в том числе глутамовую кислоту и аспарагиновую кислоту в аланин). Способность энтероцитов видоизменять эти аминокислоты, возможно, позволяет избежать токсического эффекта при их избыточном введении.
Аминокислоты, как поступившие в кровь при переваривании белка, так и синтезированные в клетках, в крови образуют постоянно обновляющийся свободный пул аминокислот, который составляет около 100 г.
Путь белка
75 % аминокислот, находящихся в системной циркуляции, представлены аминокислотами с ветвящимися цепями (лейцином, изолейцином и валином). Из мышечной ткани в кровоток выделяются аланин, который является основным предшественником синтеза глюкозы, и глутамин. Многие свободные аминокислоты подвергаются трансформации в печени. Часть свободного пула инкорпорируется в белки организма и при их катаболизме вновь поступает в кровоток. Другие непосредственно подвергаются катаболическим реакциям. Некоторые свободные аминокислоты используются для синтеза новых азотсодержащих соединений (пурина, креатинина, адреналина) и в дальнейшем деградируют, не возвращаясь в свободный пул, в специфичные продукты распада.
Роль печени
Постоянство содержания различных аминокислот в крови обеспечивает печень. Она утилизирует примерно ⅓ всех аминокислот, поступающих в организм, что позволяет предотвратить скачки в их концентрации в зависимости от питания.
Первостепенная роль печени в азотном и других видах обмена обеспечивается ее анатомическим расположением — продукты переваривания попадают по воротной вене непосредственно в этот орган. Кроме того, печень непосредственно связана с экскреторной системой — билиарным трактом, что позволяет выводить некоторые соединения в составе желчи. Гепатоциты — единственные клетки, обладающие полным набором ферментов, участвующих в аминокислотном обмене. Здесь выполняются все основные процессы азотного метаболизма: распад аминокислот для выработки энергии и обеспечения глюконеогенеза, образование заменимых аминокислот и нуклеиновых кислот, обезвреживание аммиака и других конечных продуктов. Печень является основным местом деградации большинства незаменимых аминокислот (за исключением аминокислот с ветвящимися цепями).
Инсулиновый ответ
Синтез азотсодержащих соединений (белка и нуклеиновых кислот) в печени весьма чувствителен к поступлению их предшественников из пищи. После каждого приема пищи наступает период повышенного внутрипеченочного синтеза белков, в том числе альбумина. Аналогичное усиление синтетических процессов происходит и в мышцах. Эти реакции связаны прежде всего с действием инсулина, который секретируется в ответ на введение аминокислот и/или глюкозы.
Некоторые аминокислоты (аргинин и аминокислоты с ветвящимися цепями) усиливают продукцию инсулина в большей степени, чем остальные. Другие (аспарагин, глицин, серин, цистеин) стимулируют секрецию глюкагона, который усиливает утилизацию аминокислот печенью и воздействует на ферменты глюконеогенеза и аминокислотного катаболизма. Благодаря этим механизмам происходит снижение уровня аминокислот в крови после поступления их с пищей. Действие инсулина наиболее выражено для аминокислот, содержащихся в кровотоке в свободном виде (аминокислот с ветвящимися цепями), и малозначимо для тех, которые транспортируются в связанном виде (триптофана). Обратное инсулину влияние на белковый метаболизм оказывают глюкокортикостероиды.
Аминокислоты на «экспорт»
Печень обладает повышенной скоростью синтеза и распада белков по сравнению с другими тканями организма (кроме поджелудочной железы). Это позволяет ей синтезировать «на экспорт», а также быстро обеспечивать лабильный резерв аминокислот в период недостаточного питания за счет распада собственных белков.
Особенность внутрипеченочного белкового синтеза заключается в том, что он усиливается под действием гормонов, которые в других тканях производят катаболический эффект. Так, при голодании белки мышц, для обеспечения организма энергией, подвергаются распаду, а в печени одновременно усиливается синтез белков, являющихся ферментами глюконеогенеза и мочевинообразования.
Избыток белка и голодание
Прием пищи, содержащей избыток белка, приводит к интенсификации синтеза в печени и в мышцах, образованию избыточных количеств альбумина и деградации излишка аминокислот до предшественников глюкозы и липидов. Глюкоза и триглицериды утилизируются как горючее или депонируются, а альбумин становится временным хранилищем аминокислот и средством их транспортировки в периферические ткани.
При голодании уровень альбумина прогрессивно снижается, а при последующей нормализации поступления белка медленно восстанавливается. Поэтому хотя альбумин и является показателем белковой недостаточности, он низкочувствителен и не реагирует оперативно на изменения в питании.
7 из 10 эссенциальных аминокислот деградируют в печени — либо образуя мочевину, либо впоследствии используясь в глюконеогенезе. Мочевина преимущественно выделяется с мочой, но часть ее поступает в просвет кишечника, где подвергается уреазному воздействию микрофлоры. Аминокислоты с ветвящимися цепями катаболизируются в основном в почках, мышцах и головном мозге.
Роль мышц
Мышцы синтезируют ежедневно 75 г белка. У среднего человека они содержат 40 % от всего белка организма. Хотя белковый метаболизм происходит здесь несколько медленнее, чем в других тканях, мышечный белок представляет собой самый большой эндогенный аминокислотный резерв, который при голодании может использоваться для глюконеогенеза.
Мышцы являются основной мишенью воздействия инсулина: здесь под его влиянием усиливается поступление аминокислот, увеличивается синтез мышечного белка и снижается распад.
В процессе превращений в мышцах образуются аланин и глутамин, их условно можно считать транспортными формами азота. Аланин непосредственно из мышц попадает в печень, а глутамин вначале поступает в кишечник, где частично превращается в аланин. Поскольку в печени из аланина происходит синтез глюкозы, частично обеспечивающий мышцу энергией, получающийся круго- оборот получил название глюкозо- аланинового цикла.
К азотсодержащим веществам мышц также относятся высокоэнергетичный креатин-фосфат и продукт его деградации креатинин. Экскреция креатинина обычно рассматривается как мера мышечной массы. Однако это соединение может поступать в организм с высокобелковой пищей и влиять на результаты исследования содержания его в моче. Продукт распада миофибриллярных белков — 3-метилгистидин — экскретируется с мочой в течение короткого времени и является достаточно точным показателем скорости распада в мышцах — при мышечном истощении скорость его выхода пропорционально снижается.
Механизм голодания
В отсутствие пищи синтез альбумина и мышечного белка замедляется, но продолжается деградация аминокислот. Поэтому на начальном этапе голодания мышцы теряют аминокислоты, которые идут на энергетические нужды. В дальнейшем организм адаптируется к отсутствию новых поступлений аминокислот (снижается потребность в зависящем от белка глюконеогенезе за счет использования энергетического потенциала кетоновых тел) и потеря белка мускулатуры уменьшается.
Хотите больше новой информации по вопросам диетологии?
Оформите подписку на информационно-практический журнал «Практическая диетология»!
Роль почек
Почки не только выводят конечные продукты азотного распада (мочевину, креатинин и др.), но и являются дополнительным местом ресинтеза глюкозы из аминокислот, а также регулируют образование аммиака, компенсируя избыток ионов водорода в крови.
Глюконеогенез и функционирование кислотно-щелочной регуляции тесно скоординированы, поскольку субстраты этих процессов появляются при дезаминировании аминокислот: углерод для синтеза глюкозы и азот — для аммиака. Существует даже мнение, что именно производство глюкозы является основной реакцией почек на ацидоз, а образование аммиака происходит вторично.
Белок в нервной ткани
Для нервной ткани характерны более высокие концентрации аминокислот, чем в плазме. Это позволяет обеспечить мозг достаточным количеством ароматических аминокислот, являющихся предшественниками нейромедиаторов.
Некоторые заменимые аминокислоты, такие как глутамат (из которого при участии пиридоксина образуется гамма-аминомасляная кислота) и аспартат, также обладают влиянием на возбудимость нервной ткани. Их концентрация здесь высока, при этом заменимые аминокислоты способны синтезироваться и на месте.
Сон после еды
Специфическую роль играет триптофан, являющийся предшественником серотонина. Именно с повышением концентрации триптофана (а следовательно, и серотонина) связана сонливость после еды. Такой эффект особенно выражен при приеме больших количеств триптофана совместно с углеводистой пищей. Повышенная секреция инсулина снижает уровень в крови аминокислот с ветвящимися цепями, которые при преодолении барьера «кровь — мозг» обладают конкурентными взаимоотношениями с ароматическими аминокислотами, но в то же время не оказывает влияния на концентрацию связанного с альбумином триптофана. Благодаря подобным эффектам препараты триптофана могут использоваться в психиатрической практике.
При заболеваниях печени
Ограничение ароматических аминокислот в рационе, в связи с их влиянием на центральную нервную систему, имеет профилактическое значение при ведении пациентов с печеночной энцефалопатией. Элементные аминокислотные диеты с преимущественным содержанием лейцина, изолейцина, валина и аргинина помогают избежать развития белковой недостаточности у гепатологических больных и в то же время не приводят к возникновению печеночной комы.
Основные пластические функции протеиногенных аминокислот перечислены в таблице 2.
Таблица 2. Основные функции аминокислот
| Аланин | Предшественник глюконеогенеза, переносчик азота из периферических тканей в печень |
| Аргинин | Непосредственный предшественник мочевины |
| Аспарагиновая кислота | Предшественник глюконеогенеза, предшественник пиримидина, используется для синтеза мочевины |
| Глутаминовая кислота | Донор аминогрупп для многих реакций, переносчик азота (проникает через мембраны легче, чем глутамин), источник аммиака, предшественник ГАМК |
| Глицин | Предшественник пуринов, глютатиона и креатинина, входит в состав гемоглобина и цитохромов, нейротрансмиттер |
| Гистидин | Предшественник гистамина, донор углерода |
| Лизин | Предшественник карнитина (транспорт жирных кислот), составляющая коллагена |
| Метионин | Донор метальных групп для многих синтетических процессов (в т. ч. холина, пиримидинов), предшественник цистеина, участвует в метаболизме никотиновой кислоты и гистамина |
| Фенилаланин | Предшественник тирозина |
| Серин | Составляющая фосфолипидов, предшественник сфинголипидов, предшественник этаноламина и холина, участвует в синтезе пуринов и пиримидинов |
| Триптофан | Предшественник серотонина и никотинамида |
| Тирозин | Предшественник катехоламинов, допамина, меланина, тироксина |
| Цистеин | Предшественник таурина (желчные кислоты), входит в состав глютатиона (антиоксидантная система) |
Нормы потребления белка
Современные рекомендации по обеспечению пожилых людей и стариков основными питательными веществами, в первую очередь белками, свидетельствуют о целесообразном некотором снижении суточного количества белковых продуктов в пищевом рационе до 0,75–0,8 г/кг веса. Это связано с тем, что интенсивность основных физиологических функций с каждым десятилетием жизни человека после 50 лет снижается почти на 10 % (Rogers J., Jensen G., 2004), потребность белка уменьшается за счет инволюции синтетических и пластических процессов и ферментообразования, продукции гормонов, ряда биологически активных веществ, обеспечения мышечной деятельности и т. д.
Рекомендуемые нормы потребления для белка с учетом приведенных выше показателей составляют 55–62 г/сут (для мужчины весом 77 кг в возрасте 60–70 лет) и 45–52 г/сут (для женщины весом 65 кг в возрасте 60–70 лет) по выводам IV Американского национального исследования по оценке здоровья и питания (2006).
Вместе с тем установлено, что при сохранении физической активности пожилых людей (профессиональной физической нагрузки, занятий физкультурой, работы на дачном участке и т. п.) для поддержания азотного равновесия организма требуется повышение белкового обеспечения пожилого человека в количестве 1–1,25 г/кг в день. Эта же квота пищевого белка полностью обеспечит потребности пожилого человека, находящегося в состоянии стресса, болезни или ранения (Lowenthal D. T., 1990).
Рис. 1. Влияние пищевых веществ на развитие болезней избыточного питания (по А. А. Покровскому)
Дефицит белка = старение
Важно отметить, что организм пожилого человека очень чувствителен как к дефициту экзогенно поступающих белков, так и к их избытку. В условиях белкового дефицита прогрессирующе развиваются процессы дистрофии и атрофии клеточных структур, в первую очередь мышечной ткани, слизистых оболочек (желудочно-кишечного тракта, дыхательной системы и др.), паренхиматозных органов (поджелудочной железы, печени, эндокринных желез и др.), структур иммунной системы. Белковый дефицит питания активизирует процессы старения организма.
Механизмы патологического действия на организм пожилого и старого человека пищевой белковой перегрузки связаны в первую очередь с белковой «агрессией» печени и связанной с этим несостоятельностью ферментных систем, неполной деполимеризацией всех фракций белка, накоплением в крови токсических продуктов незавершенных окислительно-восстановительных реакций и т. д.
Белковая перегрузка
Интоксикационный процесс метаболического генеза при избыточном белковом питании пожилых и старых людей многократно усиливается по причине развития процессов гнилостной кишечной диспепсии в условиях относительной ферментной недостаточности желудка, поджелудочной железы, тонкой кишки и развития синдромов мальдигестии и мальабсорбции, а также кишечного дисбиоза (Барановский А. Ю., Кондрашина Э. А., 2008).
Белковая пищевая перегрузка в рамках интоксикационного синдрома способствует перевозбуждению центральной нервной системы, иногда — состояниям, близким к неврозам. При этом наблюдается повышенный расход витаминов в организме с формированием витаминной недостаточности.
При длительном высокобелковом питании вначале наблюдается компенсаторное усиление, а затем угнетение секреторной функции желудка и поджелудочной железы, повышается риск развития таких заболеваний, как подагра, мочекаменная болезнь.
В следующем выпуске журнала «Практическая диетология» мы продолжим рассказ о геронтологических особенностях основных видов обмена веществ пациентов пожилого и старческого возраста — углеводном и жировом обмене.
// ПД
Хотите больше новой информации по вопросам диетологии?
Оформите подписку на информационно-практический журнал «Практическая диетология»!