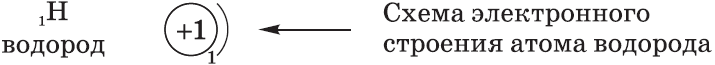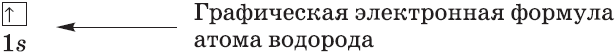Что значит энергетический уровень
Энергетический уровень
Энергетический уровень — собственные значения энергии квантовых систем, то есть систем, состоящих из микрочастиц (электронов, протонов и других элементарных частиц) и подчиняющихся законам квантовой механики. Каждый уровень характеризуется определённым состоянием системы, или подмножеством таковых в случае вырождения. Понятие применимо к атомам (электронные уровни), молекулам (различные уровни, соответствующие колебаниям и вращениям), атомным ядрам (внутриядерные энергетические уровни) и т.д.
Содержание
Электронные энергетические уровни
В современном понятии об орбитальной модели атома, электроны в атоме способны обладать лишь определёнными величинами энергии, и переходить с одного энергетического уровня на другой лишь скачком. Разница между энергетическими уровнями определяет частоту кванта света, выделяемого или поглощаемого при переходе. Каждой паре значений главного квантового числа n и орбитального квантового числа l соответствует определённый уровень энергии, которой может обладать электрон.
Молекулярные энергетические уровни
Внутриядерные энергетические уровни
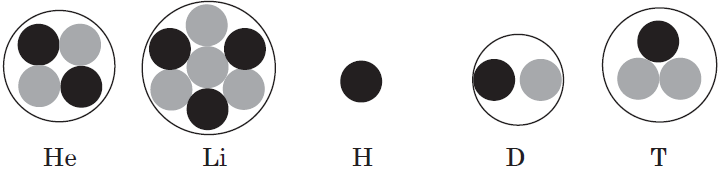
Термин появился благодаря исследованию радиоактивности. Радиационное излучение разделяется на три части: альфа-лучи, бета-лучи и гамма-лучи. Исследования показали, что альфа-излучение состоит из ядер гелия-4 (см. альфа-частица), бета-излучение является потоком быстро движущихся электронов, а гамма-лучи являются электромагнитными. Поскольку энергии переходов между различными электронными уровнями недостаточно для возникновения гамма-лучей, стало понятно, что их источник нужно искать внутри атомного ядра, то есть ядро атома само может обладать различными энергетическими уровнями, при переходах между которыми и происходит излучение гамма-квантов. Гамма-лучи расширили спектр известных электромагнитных волн, и все волны короче 10 −3 нм называются гамма-лучами.
См. также
Полезное
Смотреть что такое «Энергетический уровень» в других словарях:
ЭНЕРГЕТИЧЕСКИЙ УРОВЕНЬ — ЭНЕРГЕТИЧЕСКИЙ УРОВЕНЬ, фиксированное количество энергии, которой обладают ядро атома, ЭЛЕКТРОН, атом или молекула. Например, внутри атома энергия электронов не изменяется беспрерывно. Она выражается в дискретном ряде значений, которые и носят… … Научно-технический энциклопедический словарь
энергетический уровень — — [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN energy levelstate … Справочник технического переводчика
энергетический уровень — – строго определенная энергия, которой характеризуется данный электрон в атоме, соответствующая его расстоянию от ядра. Чем ближе электрон к ядру, тем меньше энергия, которой он обладает. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
энергетический уровень — energijos lygmuo statusas T sritis chemija apibrėžtis Energijos vertė, kurią gali turėti kvantinė sistema stacionariojoje būsenoje. atitikmenys: angl. energy level rus. уровень энергии; энергетический уровень … Chemijos terminų aiškinamasis žodynas
энергетический уровень — energijos lygmuo statusas T sritis fizika atitikmenys: angl. energy level vok. Energieniveau, n rus. уровень энергии, m; энергетический уровень, m pranc. niveau d’énergie, m; niveau énergétique, m … Fizikos terminų žodynas
энергетический уровень — energijos lygmuo statusas T sritis Standartizacija ir metrologija apibrėžtis Energijos vertė, kurią gali turėti kvantinė nuostoviosios būsenos sistema. atitikmenys: angl. energy level vok. Energieniveau, n rus. энергетический уровень, m pranc.… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
Энергетический уровень — см. Уровни энергии … Большая советская энциклопедия
энергетический уровень — Возможное значение полной энергии консервативной квантовой системы.. Иначе: Собственное значение гамильтониана, не зависящего от времени … Политехнический терминологический толковый словарь
энергетический уровень механизации (автоматизации) живого труда — энергетический уровень механизации (автоматизации) труда ΩТ Отношение полезных затрат энергии неживой природы в течение неперекрытого машинного времени к сумме полезных затрат энергии неживой природы и людей в течение штучного времени.… … Справочник технического переводчика
энергетический уровень механизации (автоматизации) средств технологического оснащения — энергетический уровень механизации (автоматизации) СТО ΩП Отношение полезных затрат энергии неживой природы в течение полного машинного времени к сумме полезных затрат энергии неживой природы и людей в течение штучного времени. [ГОСТ 23004… … Справочник технического переводчика
ЭНЕРГЕТИЧЕСКИЙ УРОВЕНЬ
Смотреть что такое «ЭНЕРГЕТИЧЕСКИЙ УРОВЕНЬ» в других словарях:
Энергетический уровень — Энергетический уровень собственные значения энергии квантовых систем, то есть систем, состоящих из микрочастиц (электронов, протонов и других элементарных частиц) и подчиняющихся законам квантовой механики. Каждый уровень характеризуется… … Википедия
энергетический уровень — — [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN energy levelstate … Справочник технического переводчика
энергетический уровень — – строго определенная энергия, которой характеризуется данный электрон в атоме, соответствующая его расстоянию от ядра. Чем ближе электрон к ядру, тем меньше энергия, которой он обладает. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
энергетический уровень — energijos lygmuo statusas T sritis chemija apibrėžtis Energijos vertė, kurią gali turėti kvantinė sistema stacionariojoje būsenoje. atitikmenys: angl. energy level rus. уровень энергии; энергетический уровень … Chemijos terminų aiškinamasis žodynas
энергетический уровень — energijos lygmuo statusas T sritis fizika atitikmenys: angl. energy level vok. Energieniveau, n rus. уровень энергии, m; энергетический уровень, m pranc. niveau d’énergie, m; niveau énergétique, m … Fizikos terminų žodynas
энергетический уровень — energijos lygmuo statusas T sritis Standartizacija ir metrologija apibrėžtis Energijos vertė, kurią gali turėti kvantinė nuostoviosios būsenos sistema. atitikmenys: angl. energy level vok. Energieniveau, n rus. энергетический уровень, m pranc.… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
Энергетический уровень — см. Уровни энергии … Большая советская энциклопедия
энергетический уровень — Возможное значение полной энергии консервативной квантовой системы.. Иначе: Собственное значение гамильтониана, не зависящего от времени … Политехнический терминологический толковый словарь
энергетический уровень механизации (автоматизации) живого труда — энергетический уровень механизации (автоматизации) труда ΩТ Отношение полезных затрат энергии неживой природы в течение неперекрытого машинного времени к сумме полезных затрат энергии неживой природы и людей в течение штучного времени.… … Справочник технического переводчика
энергетический уровень механизации (автоматизации) средств технологического оснащения — энергетический уровень механизации (автоматизации) СТО ΩП Отношение полезных затрат энергии неживой природы в течение полного машинного времени к сумме полезных затрат энергии неживой природы и людей в течение штучного времени. [ГОСТ 23004… … Справочник технического переводчика
Энергетические уровни
Энергетические уровни (слои) электронов в атоме:
У орбиталей, кстати, тоже есть и своя энергия. И если несколько орбиталей имеют равную или близкую энергию, то они образуют свой энергетический слой (уровень). Подобно облакам вокруг планеты, которые могут быть на разной высоте и образовывать разные слои.
Каждый энергетический уровень обозначен за n, от единицы и выше (n = 1, n = 2, n = 3,…). Либо в буквах, тогда первый уровень 1 = K, второй 2 = L, третий 3 = M и далее по латинскому алфавиту.
Например, натрий можно изобразить так:

На одном энергетическом уровне (слое) n может находиться n 2 орбиталей, больше просто не влезет в слой. Т.е. на 1-м уровне 1 орбиталь, на втором 4 орбитали, на третьем, 9 и т.д. А в каждой орбитали, как вы помните, может быть по 2 электрона, значит максимальное количество электронов на электронном уровне атома: N = 2n 2
Логично, что первые электроны занимают сначала первый уровень, потом, весь второй, третий и т.д. И снова нам помогает таблица Менделеева, ведь номер периода (строки) соответствует количеству энергетических уровней в элементе.
Например, только у гелия и водорода всего 1 энергетический уровень, причем в гелии он максимально заполнен электронами (на первом уровне их же всего 2).
Во втором ряду как раз 8 элементов, что логично, ведь на втором уровне может быть всего 8 электронов 2n 2 = 2*2 2 = 8
Ничего страшного, все компенсируется на 4-м уровне, где целых 18 элементов.
В периодической таблице также подписаны все электроны на каждом уровне. Посмотрите, там очень мелко в каждой клетке элементов.
Редактировать этот урок и/или добавить задание Добавить свой урок и/или задание
Добавить интересную новость
Добавить анкету репетитора и получать бесплатно заявки на обучение от учеников
При правильном ответе Вы получите 1 балл
Как узнать, сколько энергетических уровней у элемента?
Выберите всего один правильный ответ.
Добавление комментариев доступно только зарегистрированным пользователям
Lorem iorLorem ipsum dolor sit amet, sed do eiusmod tempbore et dolore maLorem ipsum dolor sit amet, consectetur adipisicing elit, sed do eiusmod tempborgna aliquoLorem ipsum dolor sit amet, consectetur adipisicing elit, sed do eiusmod tempbore et dLorem ipsum dolor sit amet, consectetur adipisicing elit, sed do eiusmod tempborlore m mollit anim id est laborum.
28.01.17 / 22:14, Иван Иванович Ответить +5
Lorem ipsum dolor sit amet, consectetu sed do eiusmod qui officia deserunt mollit anim id est laborum.
Lorem ipsum dolor sit amet, consectetur adipisicing sed do eiusmod tempboLorem ipsum dolor sit amet, consectetur adipisicing elit, sed do eiusmod temLorem ipsum dolor sit amet, consectetur adipisicing elit, sed do eiusmod tempborpborrum.
28.01.17 / 22:14, Иван Иванович Ответить +5
энергетический уровень
Смотреть что такое «энергетический уровень» в других словарях:
ЭНЕРГЕТИЧЕСКИЙ УРОВЕНЬ — ЭНЕРГЕТИЧЕСКИЙ УРОВЕНЬ, фиксированное количество энергии, которой обладают ядро атома, ЭЛЕКТРОН, атом или молекула. Например, внутри атома энергия электронов не изменяется беспрерывно. Она выражается в дискретном ряде значений, которые и носят… … Научно-технический энциклопедический словарь
Энергетический уровень — Энергетический уровень собственные значения энергии квантовых систем, то есть систем, состоящих из микрочастиц (электронов, протонов и других элементарных частиц) и подчиняющихся законам квантовой механики. Каждый уровень характеризуется… … Википедия
энергетический уровень — — [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN energy levelstate … Справочник технического переводчика
энергетический уровень — energijos lygmuo statusas T sritis chemija apibrėžtis Energijos vertė, kurią gali turėti kvantinė sistema stacionariojoje būsenoje. atitikmenys: angl. energy level rus. уровень энергии; энергетический уровень … Chemijos terminų aiškinamasis žodynas
энергетический уровень — energijos lygmuo statusas T sritis fizika atitikmenys: angl. energy level vok. Energieniveau, n rus. уровень энергии, m; энергетический уровень, m pranc. niveau d’énergie, m; niveau énergétique, m … Fizikos terminų žodynas
энергетический уровень — energijos lygmuo statusas T sritis Standartizacija ir metrologija apibrėžtis Energijos vertė, kurią gali turėti kvantinė nuostoviosios būsenos sistema. atitikmenys: angl. energy level vok. Energieniveau, n rus. энергетический уровень, m pranc.… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
Энергетический уровень — см. Уровни энергии … Большая советская энциклопедия
энергетический уровень — Возможное значение полной энергии консервативной квантовой системы.. Иначе: Собственное значение гамильтониана, не зависящего от времени … Политехнический терминологический толковый словарь
энергетический уровень механизации (автоматизации) живого труда — энергетический уровень механизации (автоматизации) труда ΩТ Отношение полезных затрат энергии неживой природы в течение неперекрытого машинного времени к сумме полезных затрат энергии неживой природы и людей в течение штучного времени.… … Справочник технического переводчика
энергетический уровень механизации (автоматизации) средств технологического оснащения — энергетический уровень механизации (автоматизации) СТО ΩП Отношение полезных затрат энергии неживой природы в течение полного машинного времени к сумме полезных затрат энергии неживой природы и людей в течение штучного времени. [ГОСТ 23004… … Справочник технического переводчика
Электронная конфигурация атома
Теория к заданию 1 из ЕГЭ по химии
Понятие атом возникло еще в античном мире для обо значения частиц вещества. В переводе с греческого атом означает «неделимый».
Электроны
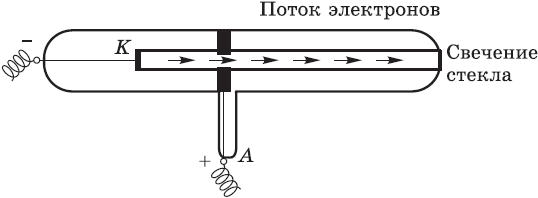
Томсон и Перрен соединяли полюса источника тока с двумя металлическими пластинами — катодом и анодом, впаянными в стеклянную трубку, из которой был откачан воздух. При подаче на пластины-электроды напряжения около 10 тысяч вольт в трубке вспыхивал светящийся разряд, а от катода (отрицательного полюса) к аноду (положительному полюсу) летели частицы, которые ученые сначала назвали катодными лучами, а затем выяснили, что это был поток электронов. Электроны, ударяясь об особые вещества, нанесенные, например, на экран телевизора, вызывают свечение.
Был сделан вывод: электроны вырываются из атомов материала, из которого сделан катод.
Свободные электроны или поток их можно получить и другими способами, например, при накаливании металлической проволоки или при падении света на металлы, образованные элементами главной подгруппы I группы таблицы Менделеева (например, цезий).
Состояние электронов в атоме
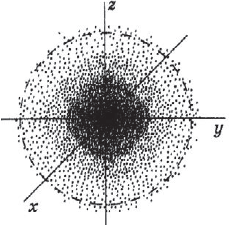
Под состоянием электрона в атоме понимают совокупность информации об энергии определенного электрона в пространстве, в котором он находится. Мы уже знаем, что электрон в атоме не имеет траектории движения, т.е. можно говорить лишь о вероятности нахождения его в пространстве вокруг ядра. Он может находиться в любой части этого пространства, окружающего ядро, и совокупность различных положений его рассматривают как электронное облако с определенной плотностью отрицательного заряда. Образно это можно представить себе так: если бы удалось через сотые или миллионные доли секунды сфотографировать положение электрона в атоме, как при фотофинише, то электрон на таких фотографиях был бы представлен в виде точки. При наложении бесчисленного множества таких фотографий получилась бы картина электронного облака с наибольшей плотностью там, где этих точек больше всего.
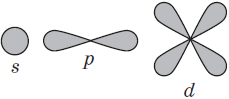
Пространство вокруг атомного ядра, в котором наиболее вероятно нахождение электрона, называется орбиталью.
Оно характеризует энергию электронов, занимающих данный энергетический уровень. Наименьшей энергией обладают электроны первого энергетического уровня, наиболее близкого к ядру. По сравнению с электронами первого уровня электроны последующих уровней характеризуются большим запасом энергии. Следовательно, наименее прочно связаны с ядром атома электроны внеш него уровня.
Число энергетических уровней (электронных слоев) в атоме равно номеру периода в системе Д. И. Менделеева, к которому принадлежит химический элемент: у атомов элементов первого периода один энергетический уровень; второго периода — два; седьмого периода — семь.
Наибольшее число электронов на энергетическом уровне определяется по формуле:
Число подуровней равно значению главного квантового числа: первый энергетический уровень имеет один под уровень; второй — два; третий — три; четвертый — четыре. Подуровни, в свою очередь, образованы орбиталями.
Главное квантовое число, типы и число орбиталей, максимальное число электронов на подуровнях и уровнях.
Ядро атома
Но не только электроны входят в состав атомов. Физик Анри Беккерель обнаружил, что природный минерал, содержащий соль урана, тоже испускает неведомое излучение, засвечивая фотопленки, закрытые от света. Это явление было названо радиоактивностью.
Различают три вида радиоактивных лучей:
Следовательно, атом имеет сложное строение — состоит из положительно заряженного ядра и электронов.
Как же устроен атом?
Расчеты показали, что наблюдаемые явления могли произойти, если бы вся масса атома и весь его положительный заряд были сосредоточены в крохотном центральном ядре. Радиус ядра, как выяснилось, в 100 000 раз меньше радиуса всего атома, той его области, в которой находятся электроны, имеющие отрицательный заряд. Если применить образное сравнение, то весь объем атома можно уподобить стадиону в Лужниках, а ядро — футбольному мячу, расположенному в центре поля.
Атом любого химического элемента сравним с крохотной Солнечной системой. Поэтому такую модель атома, предложенную Резерфордом, называют планетарной.
Протоны и нейтроны
Оказывается, и крошечное атомное ядро, в котором сосредоточена вся масса атома, состоит из частиц двух видов — протонов и нейтронов.
Протоны и нейтроны вместе называют нуклонами (от лат. nucleus — ядро).
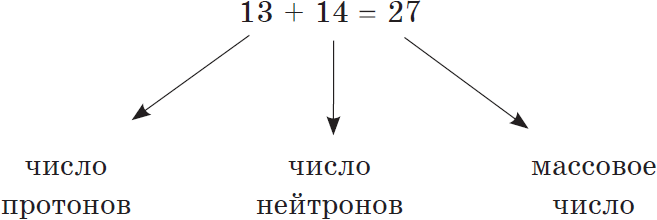
Сумма числа протонов и нейтронов в атоме называется массовым числом. Например, массовое число атома алюминия:
Например, число нейтронов в атоме железа равно:
В таблице представлены основные характеристики элементарных частиц.
Основные характеристики элементарных частиц.
Изотопы
Разновидности атомов одного и того же элемента, имеющие одинаковый заряд ядра, но разное массовое число, называются изотопами.
Слово изотоп состоит из двух греческих слов: isos — одинаковый и topos — место, обозначает «занимающий одно место» (клетку) в Периодической системе элементов.
Химические свойства изотопов хлора совершенно одинаковы, как и изотопов большинства химических элементов, например калия, аргона:
Теперь можно дать современное, более строгое и научное определение химическому элементу.
Химический элемент — это совокупность атомов с одинаковым зарядом ядра.
Строение электронных оболочек атомов элементов первых четырех периодов
Рассмотрим отображение электронных конфигураций атомов элементов по периодам системы Д. И. Менделеева.
Элементы первого периода.
Схемы электронного строения атомов показывают распределение электронов по электронным слоям (энергетическим уровням).
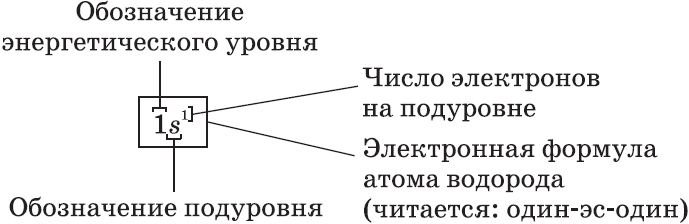
Электронные формулы атомов показывают распределение электронов по энергетическим уровням и под уровням.
Графические электронные формулы атомов показывают распределение электронов не только по уровням и под уровням, но и по орбиталям.
Элементы второго периода.
Элементы третьего периода.
У атомов элементов третьего периода первый и второй электронные слои завершены, поэтому заполняется третий электронный слой, в котором электроны могут занимать 3s-, 3р- и 3d-под уровни.
Строение электронных оболочек атомов элементов третьего периода.
| Символ элемента, порядковый номер, название | Схема электронного строения | Электронная формула | Графическая электронная формула |
| $↙<11> | 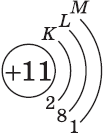 | $1s^2<2>s^2<2>p^6<3>s^1$ | 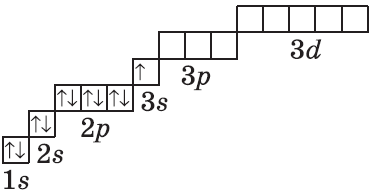 |
| $↙<13> | 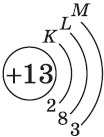 | $1s^2<2>s^2<2>p^6<3>s^2<3>p^1$ | 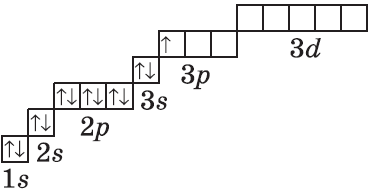 |
| $↙<18> | 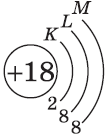 | $1s^2<2>s^2<2>p^6<3>s^2<3>p^6$ | 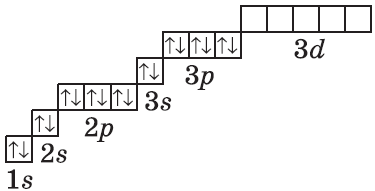 |
Элементы четвертого периода.
$4f$-элементы называют лантаноидами.
$5f$-элементы называют актиноидами.
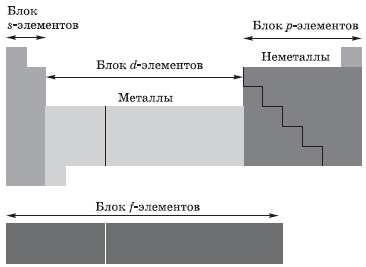
В зависимости от того, какой подуровень атома заполняется электронами последним, все элементы, как вы уже поняли, делят на четыре электронных семейства, или блока:
Электронная конфигурация атома. Основное и возбужденное состояние атомов
Если на орбитали находится один электрон, то он называется неспаренным, если два, то это спаренные электроны, т.е. электроны с противоположными спинами.
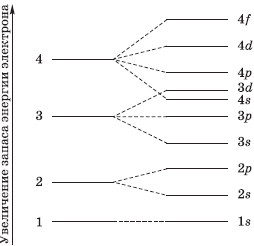
На рисунке показана схема деления энергетических уровней на подуровни.
Иногда в схемах, изображающих распределение электронов в атомах, указывают только число электронов на каждом энергетическом уровне, т.е. записывают сокращенные электронные формулы атомов химических элементов, в отличие от приведенных выше полных электронных формул, например:
Очень часто строение электронных оболочек атомов изображают с помощью энергетических, или квантовых ячеек — записывают так называемые графические электронные формулы. Для этой записи используют следующие обозначения: каждая квантовая ячейка обозначается клеткой, которая соответствует одной орбитали; каждый электрон обозначается стрелкой, соответствующей направлению спина. При записи графической электронной формулы следует помнить два правила: принцип Паули, согласно которому в ячейке (орбитали) может быть не более двух электронов, но с антипараллельными спинами, и правило Ф. Хунда, согласно которому электроны занимают свободные ячейки сначала по одному и имеют при этом одинаковое значение спина, и лишь затем спариваются, но спины при этом, по принципу Паули, будут уже противоположно направленными.