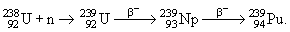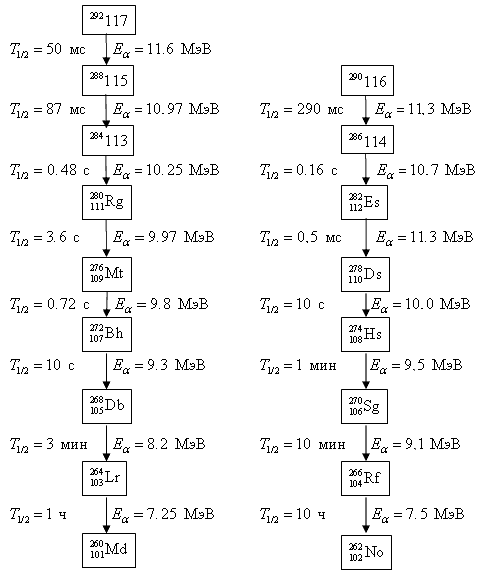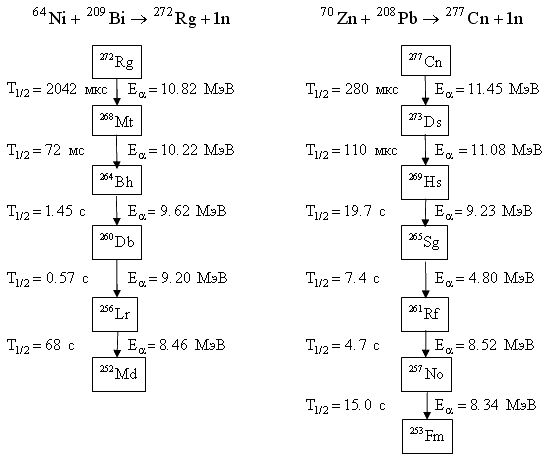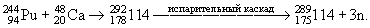Что означает трансурановый элемент
ТРАНСУРАНОВЫЕ ЭЛЕМЕНТЫ
Полезное
Смотреть что такое «ТРАНСУРАНОВЫЕ ЭЛЕМЕНТЫ» в других словарях:
ТРАНСУРАНОВЫЕ ЭЛЕМЕНТЫ — ТРАНСУРАНОВЫЕ ЭЛЕМЕНТЫ, элементы, атомный номер которых больше атомного номера УРАНА (92). Из них наиболее известны элементы группы актиноидов (атомные номера от 89 до 103). Все трансурановые элементы радиоактивны. В природе встречаются только… … Научно-технический энциклопедический словарь
ТРАНСУРАНОВЫЕ ЭЛЕМЕНТЫ — хим. элементы с ат. номерами Z>92, расположенные в периодич. системе элементов за ураном. Т. э. испытывают радиоакт. распад. Из за относительно малого времени жизни они не сохранились в земной коре. Возраст Земли около 5 • 109 лет, а период… … Физическая энциклопедия
ТРАНСУРАНОВЫЕ ЭЛЕМЕНТЫ — химич. элементы с ат. номером Z>92, расположенные в периодич. системе элементов за ураном. Известно 15 Т. э. Из за относительно малого времени жизни Т. э. не сохранились в земной воре. Возраст Земли ок. 5•109 лет, а период полураспада T1/2 наиб.… … Физическая энциклопедия
Трансурановые элементы — Transuranium elements химические элементы с атомными номерами больше 92, члены актинидного ряда. В периодической системе элементов расположены после урана. Получены искусственным путем с помощью ядерных реакций, Периоды полураспада трансурановых… … Термины атомной энергетики
трансурановые элементы — Химические элементы с атомными номерами больше 92, члены актинидного ряда. В периодической системе элементов расположены после урана. Получены искусственным путем с помощью ядерных реакций, периоды полураспада трансурановых элементов меньше… … Справочник технического переводчика
ТРАНСУРАНОВЫЕ ЭЛЕМЕНТЫ — (трансураны, заурановые элементы) радиоактивные химические (см.), расположенные в Периодической системе элементов Д. И. Менделеева (см.) после урана и имеющие атомные номера больше 92. Большинство известных Т. э. (93 115) принадлежит к числу… … Большая политехническая энциклопедия
ТРАНСУРАНОВЫЕ ЭЛЕМЕНТЫ — ТРАНСУРАНОВЫЕ ЭЛЕМЕНТЫ, химические радиоактивные элементы, расположенные в периодической системе после урана, т.е. с атомного номера 93 и выше. Известно 17 трансурановых элементов, все они получены искусственно, в природе обнаружены только… … Современная энциклопедия
Трансурановые элементы — ТРАНСУРАНОВЫЕ ЭЛЕМЕНТЫ, химические радиоактивные элементы, расположенные в периодической системе после урана, т.е. с атомного номера 93 и выше. Известно 17 трансурановых элементов, все они получены искусственно, в природе обнаружены только… … Иллюстрированный энциклопедический словарь
трансурановые элементы — химические элементы, расположенные в периодической системе после урана, то есть с атомного номера Z≥93. Известно 17 трансурановых элементов. Все они синтезированы с помощью ядерных реакций (в природе обнаружены только микроколичества Np и Pu).… … Энциклопедический словарь
Трансурановые элементы — химические элементы, расположенные в периодической системе элементов (См. Периодическая система элементов) Д. И. Менделеева за Ураном, то есть с атомным номером Z ≥ 93. Известно 14 Т. э. Из за относительно высокой скорости их… … Большая советская энциклопедия
Что означает трансурановый элемент
В каждом кабинете химии, в каждой школе, в любой стране мира есть Периодическая таблица химических элементов. Раз в несколько лет эта химическая азбука, созданная русским химиком Дмитрием Менделеевым, пополняется новыми элементами-клеточками. Давайте разберёмся, что стоит за этими необычными изменениями в Периодической таблице.
Эта статья была опубликована в журнале OYLA №2(18). Оформить подписку на печатную и онлайн-версию можно здесь.
30 декабря 2015 года ИЮПАК официально признал открытие 113-го элемента и приоритет в этом учёных из RIKEN (институт физико-химических исследований). Таким образом, 113-й элемент стал первым, открытым в Японии и вообще в азиатской стране
Поводом для внимания к Периодической таблице стали не столь давние события, когда 28 ноября 2016 года объявили о появлении сразу четырёх (!) новых элементов. Конечно, они были известны и ранее, но вот имена собственные обрели только в конце прошлого года. Первенцем стал элемент нихоний (Nh) под номером 113, именовавшийся ранее унунтрием или эка-таллием. Имя он получил от японского «нихон», что означает «Страна восходящего солнца» и стал фактическим представителем этого государства в химической азбуке.
Кстати, а кто присваивает имена элементам? За это отвечает существующий уже почти сто лет Международный союз теоретической и прикладной химии или ИЮПАК (IUPAC — International Union of Pure and Applied Chemistry). Входящие в ИЮПАК солидные учёные с мировыми именами разрабатывают правила наименований химических соединений и элементов. Именно они выбрали для номера 113, синтезированного в японском институте РИКЕН, название нихоний. И клеточка 115, с расположенным в ней элементом, также получила название в честь географического объекта — московий (Mc). Московскую область отметили за расположенный на её территории наукоград Дубна, где находится Объединённый институт ядерных исследований — один из мировых центров «элементорождения». Ранее московий называли забавным словом унунпентий, а в некоторых случаях и эка-висмутом величали.
Американский штат Теннесси дал название 117 элементу, который ранее именовался унунсептий или эка-астат. Теперь это теннесин (Ts) и он отражает заслуги в исследованиях сверхтяжёлых элементов мирового масштаба Окриджской национальной лаборатории, Университета Вандербильта и Университета Теннесси в Ноксвилле. И, наконец, оганессон (Og), он же в прошлом унуноктий или эка-радон — элемент №118, названный в честь известного академика Юрия Оганесяна из дубнинского Объединённого института ядерных исследований. Это, кстати, второй в истории случай, когда элемент называют именем здравствующего учёного, первым стал в 1997 году Нобелевский лауреат из США Гленн Сиборг, который, собственно, и начал мировую трансурановую гонку.
Юрий Оганесян
Советский и российский учёный, специалист в области экспериментальной ядерной физики, научный руководитель лаборатории ядерных реакций им. Г. Н. Флёрова в Объединённом институте ядерных исследований в Дубне. Химический элемент оганесон назван в его честь
Гленн Теодор Сиборг
Эдвин Маттисон Макмиллан
Американский физик и химик, широко известный учёный своего времени. Внес значительный вклад в химию трансурановых элементов. Нобелевская премия по химии (1951) (вместе с Г. Сиборгом).
Элемент №92 — уран (U), своеобразный металл, делящий Периодическую таблицу на обычные и трансурановые элементы. Важно знать, что все «трансураны», начиная с №93, в природе практически отсутствуют и получать их приходится искусственно с помощью ядерных реакций. Первенцем подобных элементов стал нептуний (Np), синтезированный в 1940 году командой исследователей под руководством упомянутого Гленна Сиборга и Эдвина Макмиллана. Случилось это в США в национальной лаборатории имени Лоуренса в Беркли — первого центра синтеза новых элементов. Метод, применяемый для получения нептуния теоретически прост: необходимо просто бомбардировать уран нейтронами, один из которых превращается в ядре в протон, электрон и антинейтрино. Последние два долго не задерживаются и вылетают вон, а протон остаётся и увеличивает заряд ядра на единицу.
Так и получают новый элемент нептуний. Кстати, полезен он человечеству только тем, что из него синтезируют следующий «трансуран» №94 плутоний (Pu), наверное, самый зловещий элемент в истории. Именно на его основе изготавливают атомные бомбы, и сброшенная на японский Нагасаки 9 августа 1945 года была из их числа.
Из всех трансурановых элементов широкое применение получил лишь плутоний — он используется в космонавтике, в атомных реакторах, а также в качестве ключевого компонента в производстве ядерного оружия
Но есть у Pu (точнее, его изотопа-239) и мирная профессия в энергетике в качестве топлива атомных электростанций. Сугубо мирно применяется и элемент №95 америций (Am) в… детекторах дыма. Дело в том, что все трансурановые элементы радиоактивны и их излучение способно при определённых условиях создавать небольшой электрический ток. При попадании дыма на микроскопическое количество изотопа америция-241, ток в детекторе уменьшается и срабатывает аварийная сигнализация. Такая схема позволяет создавать чрезвычайно чувствительные приборы обнаружения задымления.
Законы природы таковы — ядро трансуранового элемента очень нестабильно и с повышением массы время его жизни, как правило, стремительно падает. Если у урана период полураспада (время, за которое распадается ровно половина атомов радиоактивного изотопа) порядка 700 млн лет, то 111‑й рентгений (Rg) аналогичный период проходит всего за 26 секунд. Поэтому, начиная с менделеевия (Md) под номером 101, трансурановые элементы не имеют значимого применения на практике. Их жизнь настолько коротка, что учёные порой едва успевают выявить характер их свойств.
Зачем же тогда нужна вся эта история с чрезвычайно дорогим синтезом? Неужели Германия, Россия, США и Япония тратят миллионы на удовлетворение пустого любопытства группы учёных? Во-первых, крайне важен ответ на вопрос: а есть предельный или конечный элемент и каковы будут его свойства? К примеру, крайний на данный момент 118‑й элемент оганессон по химическим свойствам очень похож на инертные газы, поэтому и суффикс «-он» получил по аналогии с неоном, криптоном… И учёные уверены, что это не предел и впереди элементы 119, 120, 121.
Во-вторых, синтез сверхтяжёлых элементов приводит к неожиданным открытиям. Оказывается, правило «чем тяжелее элемент, тем короче его жизнь» применимо до 113‑го элемента (нихоний, если кто забыл) включительно. А дальнейшее углубление открыло миру «островки стабильности» с ядрами-долгожителями, например, 114‑й флеровий имеет нетипично большой период полураспада — 2,7 секунды. Всё это даёт надежду, что в будущем получат сверхтяжёлые элементы с уникальными свойствами и с приемлемой длительностью существования.
Третьей причиной, почему нужно заниматься сложным синтезом элементов являются побочные эффекты физики высоких энергий. Загибайте пальцы: новые материалы, сверхчувствительные детекторы, явление сверхпроводимости, современная электроника, методы томографии — всё это так или иначе связано с фундаментальными исследованиями новых элементов.
И наконец, синтезировать новый элемент становится очень престижно для государства. Мировые лидеры в этом вопросе США и Россия, но, к примеру, Германия, присоединившаяся в 60‑х годах к трансурановой гонке, смогла получить целых шесть элементов — со 107‑го по 112‑й. А Япония позднее всех осознала необходимость подобных исследований и пока довольствуется одним местом в Периодической таблице. Но каждый новый элемент создаётся всё сложнее и дороже, поэтому и существуют так называемые научные коллаборации — объединение усилий нескольких институтов и даже стран для решения проблемы синтеза. Быть может, в будущем достижения физики высоких энергий станут заслугой всех стран мирового сообщества. И тогда, возможно, поводов для взаимных конфликтов станет меньше.
Что означает трансурановый элемент
Наука есть не что иное,
как отображение действительности
Химическим элементом называется совокупность атомов с одинаковыми зарядами атомных ядер и одинаковыми количествами электронов атомных оболочек. Химические элементы, существующие в природе, заканчиваются ураном U, зарядовое число (число единиц элементарного заряда в атомном ядре) которого равно Z = 92. Атомы с Z > 92 располагаются в периодической системе химических элементов за ураном. Поэтому они получили название трансурановых элементов.
Трансурановые элементы были синтезированы искусственно. Исключениями являются нептуний Np (Z = 93) и плутоний Pu (Z = 94), найденные в природе в чрезвычайно малых количествах в урановых рудах.
Для искусственного синтеза трансурановых элементов используются различные ядерные реакции. Сначала применялись реакции захвата нейтронов ядрами с дальнейшим β-распадом образовывавшихся нестабильных ядер.

Впервые такие реакции радиационного захвата нейтронов ядрами использовал Энрико Ферми (1901-1954) в 1934 г. для создания новых радиоактивных изотопов. Однако он не открыл новых трансурановых элементов, хотя был близок к такому открытию.
238 U + n → 239 U + γ,
239 U → 239 Np + ē+ ῡ,
где γ, ē и ῡ обозначают соответственно фотон, электрон и антинейтрино.
Период полураспада ядер 239 U равен t½= 23,5 минуты. Образовавшееся ядро 239 Np является радиоактивным, оно испытывает β-распад с t½ = 2,35 суток. Именно изучение периода полураспада позволило впервые идентифицировать этот изотоп нептуния, а уже потом были изучены его свойства.
Среди изотопов нептуния наибольшее время жизни имеет 237 Np, испытывающий α-распад с t½ = 2,14·10 6 лет.

Следующий трансурановый элемент — плутоний — открыла в 1940 г. группа физиков под руководством Гленна Теодора Сиборга (США) при наблюдении β-распада ядер нептуния
238 Np → 238 Pu + ē+ ῡ.
Ядра 238 Np распадаются с периодом полураспада t½ = 2,1 суток. Их обычно синтезируют в реакции взаимодействия ядер урана с дейтронами
238 U + d → 238 Np + 2n.
Изотоп 238 Pu является α-радиоактивным с периодом полураспада t½ = 86,4 лет. Очень важным изотопом является 239 Pu, который образуется при β-распаде нептуния
239 Np → 239 Pu + ē+ ῡ.
Этот изотоп плутония также радиоактивен. Большой период полураспада t½ = 2,43·10 4 лет позволяет использовать 239 Pu (который образуется в обычных ядерных реакторах в достаточном количестве) как топливо в специальных ядерных реакторах и как взрывчатое вещество в атомных бомбах. Наибольшее время жизни имеет α-радиоактивный изотоп 242 Pu: t½ = 3,8·10 5 лет.
По аналогии с ураном названия элементов нептуния и плутония происходят от названий планет Солнечной системы.
Дальнейший синтез элементов также осуществлялся с помощью реакций радиационного захвата нейтронов ядрами с последующим β-распадом образовавшихся нестабильных ядер. Таким путем были синтезированы ядра америция Am (Z = 95), кюрия Cm (Z = 96), берклия Bk (Z = 97) и калифорния Cf (Z = 98).

Названия элементов америция, берклия и калифорния связаны с географическими названиями, а название кюрия происходит от фамилии супругов Кюри (Curie). В символе Cm первая буква происходит от фамилии, а вторая — от имени Марии Склодовской-Кюри (1867-1934).
Однако дальнейший синтез элементов путем реакций радиационного захвата нейтронов ядрами с последующим β-распадом оказался невозможным, так как образующиеся ядра имеют очень малые времена жизни. Элементы эйнштейний Es (Z = 99) и фермий Fm (Z = 100) были обнаружены в продуктах термоядерного взрыва, проведенного на атолле Бикини в 1952 г.
Для дальнейшего синтеза трансурановых элементов начали применять реакции взаимодействия легких ядер, ускоренных до больших энергий, с тяжелыми ядрами.
Следующий элемент менделевий Md (Z =101) был открыт в 1955 г. в реакции
253 Es + α → 256 Md +n,
где α обозначает альфа-частицу.
Названия элементов Es, Fm и Md происходят от фамилий выдающихся учёных Альберта Эйнштейна, Энрико Ферми и Дмитрия Менделеева.

Альберт Эйнштейн (1879-1955)
Нобелий No (Z = 102) был открыт в 1957 г. при облучении ядер 244 Cm ионами углерода 13 С на циклотроне Института Нобеля в Стокгольме, откуда и происходит его название.
Лоуренсий Lr (Z = 103) синтезировали в 1961 г. в Калифорнийском университете. Свое название он получил в честь американского физика Эрнеста Лоуренса, который одним из первых начал создавать мощные ускорители заряженных частиц.
В 1968 г. в лаборатории Калифорнийского университета был синтезирован элемент резерфордий Rf (Z = 104), где ему дали название в честь выдающегося физика Эрнеста Резерфорда.
В 1968 г. в Лаборатории ядерных реакций (ЛЯР) в Объединенном институте ядерных исследований (ОИЯИ, Дубна, Россия) был синтезирован элемент дубний Db (Z = 105), название которого происходит от имени города, где он был открыт. Элемент с Z = 106 (1974 г., Дубна и независимо от них Калифорнийский университет) был назван сиборгием Sg в честь выдающегося американского физика Гленна Сиборга.

в лаборатории
207 Pb + 54 Cr → 259 Sg +2n.
Элементы с зарядовыми числами от Z = 107 до Z = 112 были открыты в Дармштадте (Германия) при исследовании ядерных реакций на ускорителе тяжелых ионов. Элемент с Z = 107 (1981 г.) получил название борий Bh в честь выдающегося датского физика Нильса Бора.
Элемент с Z = 108 (1984 г.) назвали хассий Hs, так как город Дармштадт расположен в земле Гессен, латинское название которой Hassia. Элемент с Z = 109 (1982 г.) имеет название мейтнерий Mt в честь выдающейся исследовательницы Лизе Мейтнер, которая более 30 лет работала в Германии с Отто Ганом, открывшим вместе с Фрицем Штрассманом деление ядер урана. Именно Лизе Мейтнер впервые объяснила эти эксперименты.
Элемент с Z = 110 (1994 г.) получил название дармштадтий Ds по имени города, где его впервые синтезировали. Элементу с Z = 111 (1994 г.) было присвоено название рентгений Rg в честь выдающегося немецкого физика Конрада Рентгена.


и Мстислав Келдыш
Элемент с Z = 112 (1996 г.) получил название коперникий Cn по имени великого польского ученого Николая Коперника, изменившего взгляды человечества на устройство Вселенной.
Элемент с Z = 113 был синтезирован в Японии (2004 г.). Он получил название нихоний Nh. Нихон — название Японии, которое означает страну восходящего Солнца. Это первый трансурановый элемент, открытый в Азии.
Элементы с зарядовыми числами от Z = 114 до Z = 118 были синтезированы в Дубне в совместных экспериментах российских учёных из ОИЯИ и американских учёных из Ливерморской национальной лаборатории США.
Элемент с Z = 114 (1998 г.) имеет название флеровий Fl в честь Георгия Николаевича Флерова, который на протяжении многих лет возглавлял ЛЯР ОИЯИ в Дубне.
Элемент с Z = 115 (2004 г.) получил название московий Mc, так как город Дубна расположен в Московской области. Элемент с Z = 116 (2000 г.) называется ливерморий Lv в знак того, что в его синтезе принимали участие учёные из Ливерморской национальной лаборатории (США).
Таким образом, к настоящему времени известно 26 трансурановых элементов с зарядовыми числами от Z = 93 до Z = 118. Работы по синтезу трансурановых элементов продолжаются. Поэтому есть надежда, что в ближайшие годы будет открыт ряд элементов с Z > 118.
Что означает трансурановый элемент
Самыми тяжелыми стабильными изотопами являются изотопы 204,206,207,208 Pb и 209 Bi, расположенные вблизи магических чисел Z = 82, N = 126. Все изотопы с Z > 93 являются радиоактивными (рис. 12.1). Среди этих изотопов относительно высокую распространенность на Земле имеют 232 Th (T1/2 = 1.4·10 10 лет) и 235 U (T1/2 = 4.468·10 9 лет), которые сохранились на Земле с момента образования Солнечной системы. Все химические элементы тяжелее урана получены на Земле искусственно в различных ядерных реакциях.
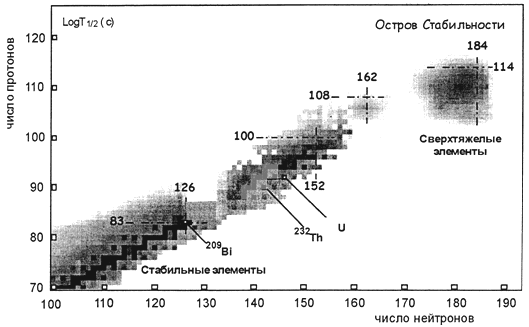
Рис. 12.1. N-Z-диаграмма области тяжелых ядер. Черные квадраты – изотопы стабильных элементов (наиболее тяжелый из них – висмут-209). Более светлым цветом показаны радиоактивные изотопы.
Химический элемент с атомным номером Z = 95 (америций) был получен в 1944 г. в результате реакции
Четвертый трансурановый элемент кюрий Cm ( Z = 96) также был получен в 1944 г. в результате реакции
239 Pu + 4 He → 242 Cm + n.
Элемент с порядковым номером Z = 97 был получен в 1949 г. и назван берклием Bk:
241 Am + 4 He → 243 Bk + 2n.
Химический элемент калифорний Cf (Z = 98) был получен в 1950 г. в реакции
242 Cm + 4 He → 245 Cf + n.
238 U + 12 C → 244 Cf + 6n,
238 U + 12 C → 246 Cf + 4n,
238 U + 14 N → 248 Cf + p + 3n.
Реакции, в которых впервые были получены трансурановые элементы
→ 287 115 + 4n, 287 115 → 283 113 + α
→ 289 114 + 3n
24 5 Cm + 48 Ca → 291 116 + 2n
24 5 Cm + 48 Ca → 290 116 + 3n
249 Bk + 48 Ca → 293 117 + 4n
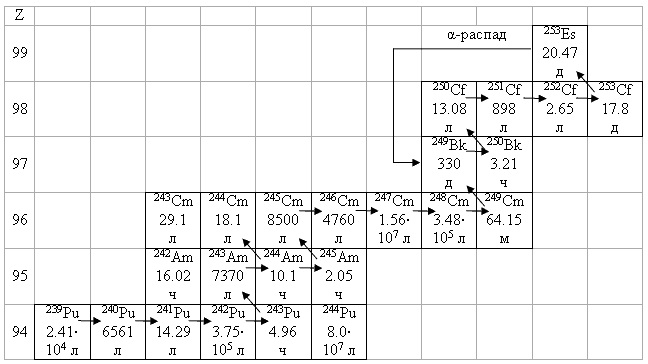
Рис. 12.2. Образование трансурановых элементов при облучении в реакторе нейтронами мишени 239 Pu. Для каждого изотопа приводится его период полураспада.
253 Es + 4 He → 246 Md + n.
Следующий этап в получении тяжелых ядер связан с использованием пучков ускоренных ионов углерода, азота и кислорода. Это позволило продвинуться к большим Z и получить изотопы трансурановых элементов вплоть до сиборгия (Z = 106). Использование в качестве налетающих частиц тяжелых изотопов Cr, Fe, Ni, Zn позволило вернуться к использованию более доступных мишеней из стабильных изотопов свинца и висмута. Так, элемент 102 получают как в реакции 242 Pu + 18 O, так и в реакции 208 Pb + 48 Ca.
Использование в качестве мишеней ядер, близких к магическим, имеет дополнительное преимущество, так как энергия реакции Q становится существенно более отрицательной, и энергия возбужденного составного ядра, образующегося в результате слияния исходных ядер, оказывается при этом более низкой, что приводит к испусканию меньшего количества нейтронов из составного ядра при его охлаждении. Кинетическая энергия налетающей частицы выбирается минимальной, вблизи высоты кулоновского барьера, чтобы преодолеть кулоновское взаимодействие сталкивающихся ядер (холодный синтез). Уменьшение величины энергии возбуждения ядра необходимо для уменьшения вероятности его распада в результате деления. Концепция холодного синтеза была впервые выдвинута Ю. Оганесяном и оказалась решающей при получении сверхтяжелых элементов.
Анализ цепочек распада трансфермиевых элементов показывает, что для большинства изотопов с Z > 100 наблюдается каскадный α-распад. При этом по мере увеличения Z увеличивается энергия
α-распада. Определение энергий последовательно испускаемых α частиц стало одним из основных методов идентификации трансфермиевых элементов.
Цепочки распадов трансурановых элементов
Анализ цепочек распада трансфермиевых элементов показывает, что для большинства ядер Z > 100 наблюдается каскадный α-распад. При этом по мере увеличения Z увеличивается энергия α-распада. Регистрация энергий последовательно испускаемых α-частиц является одним из основных методов идентификации трансфермиевых элементов.
Сверхтяжелые ядра
Ограничения на существование атомных ядер есть и со стороны сверхтяжелых элементов. Элементы с Z > 92 в естественных условиях не обнаружены. Расчеты по жидкокапельной модели предсказывают исчезновение барьера деления для ядер с Z2/A ≈ 46 (примерно 112 элемент). В проблеме синтеза сверхтяжелых ядер следует выделить два круга вопросов.
Так как образование сверхтяжелых ядер происходит в результате полного слияния ядра мишени и налетающей частицы необходимо создание теоретических моделей, описывающих динамику процесса слияния двух сталкивающихся ядер в компаунд-ядро.
Проблема синтеза сверхтяжелых элементов тесно связана с тем фактом, что ядра с Z,N = 8, 20, 28, 50, 82, N = 126 (магические числа) обладают повышенной стабильностью по отношению к различным модам радиоактивного распада. Это явление объясняется в рамках оболочечной модели − магические числа соответствуют заполненным оболочкам. Естественно возникает вопрос о существовании следующих магических чисел по Z и N. В случае, если они существуют в области N-Z-диаграммы атомных ядер N > 150, Z > 101, должны наблюдаться сверхтяжелые ядра, имеющие повышенные периоды полураспада, т.е. должен существовать Остров Стабильности. В работе [F.A. Gareev, B.N. Kalinkin, A. Sobiczewski Phys Lett 22 (1966), 500] на основе расчетов, выполненных с использованием потенциала Вудса-Саксона с учетом спин-орбитального взаимодействия, было показано, что повышение стабильности ядер следует ожидать для ядра с Z = 114, то есть следующая заполненная протонная оболочка соответствует Z = 114, заполненная нейтронная оболочка соответствует числу N
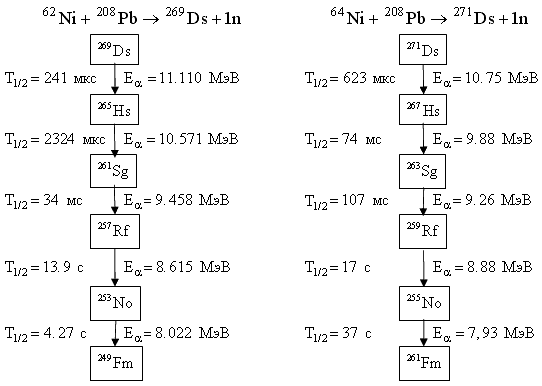
Рис. 12.3. Цепочки распадов изотопов Ds (Z = 110), Rg (Z = 111), Cn (Z = 112).
Новый этап в исследовании сверхтяжелых ядер начался в 1994 году, когда была существенно повышена эффективность регистрации и усовершенствована методика наблюдения сверхтяжелых ядер. Как результат были обнаружены изотопы Ds (Z = 110), Rg (Z = 111) и Cn (Z = 112) [S. Hofmann et al. Z. Phys A350, 1995, p.277; S. Hofmann et al. Z. Phys A350, 1995, p.281; S. Hofmann et al. Z. Phys A354, 1996, p.229].
Для получения сверхтяжелых ядер использовались ускоренные пучки 50 Ti, 51 V, 58 Fe, 62 Ni, 64 Ni, 70 Zn и 82 Se. В качестве мишеней применялись изотопы 208 Pb и 209 Bi. Различные изотопы 110 элемента были синтезированы в Лаборатории ядерных реакций им. Г.Н. Флерова с помощью реакции 244 Pu( 34 S,5n) 272 110 и в GSI (Дармштадт) в реакции 208 Pb( 62 Ni,n) 269 110. Изотопы 269 Ds, 271 Ds, 272 Rg и 277 Cn регистрировались по их цепочкам распада (рис. 12.3).
Большую роль в получении сверхтяжелых элементов играют теоретические модели, с помощью которых рассчитываются ожидаемые характеристики химических элементов, реакции, в которых они могут образовываться.
На основе различных теоретических моделей были рассчитаны распадные характеристики сверхтяжелых ядер. Результаты одного из таких расчетов показаны на рис. 12.4. Приведены периоды полураспада четно-четных сверхтяжелых ядер относительно спонтанного деления (а), α-распада (б), β-распада (в) и для всех возможных процессов распада (г). Наиболее устойчивым ядром по отношению к спонтанному делению (рис. 12.4а) является ядро с Z = 114 и N = 184. Для него период полураспада по отношению к спонтанному делению
10 16 лет. Для изотопов 114-го элемента, отличающихся от наиболее устойчивого на 6-8 нейтронов, периоды полураспада уменьшаются на
10-15 порядков. Периоды полураспада по отношению к α-распаду приведены на рис. 12.5б. Наиболее устойчивое ядро расположено в области Z = 114 и N = 184 (T 1/2 = 10 15 лет).
Стабильные по отношению к β-распаду ядра показаны на рис. 12.4в темными точками. На рис. 12.4г приведены полные периоды полураспада, которые для четно-четных ядер, расположенных внутри центрального контура, составляют
10 5 лет. Таким образом, после учета всех типов распада оказывается, что ядра в окрестности Z = 110 и N = 184 образуют «остров стабильности». Ядро 294 110 имеет период полураспада около 10 9 лет. Отличие величины Z от предсказываемого оболочечной моделью магического числа 114 связано с конкуренцией между делением (относительно которого ядро с Z = 114 наиболее стабильно) и α-распадом (относительно которого устойчивы ядра с меньшими Z). У нечетно-четных и четно-нечетных ядер периоды полураспада по отношению к
α-распаду и спонтанному делению увеличиваются, а по отношению к β-распаду уменьшаются. Следует отметить, что приведенные оценки сильно зависят от параметров, использованных в расчетах, и могут рассматриваться лишь как указания на возможность существования сверхтяжелых ядер, имеющих времена жизни достаточно большие для их экспериментального обнаружения.
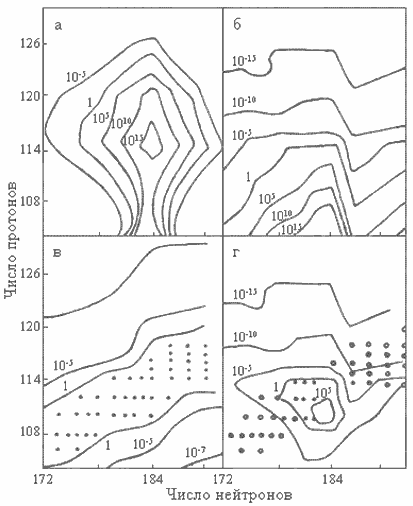
Рис. 12.4. Периоды полураспада, вычисленные для четно-четных сверхтяжелых ядер (числа обозначают периоды полураспада в годах):
а − относительно спонтанного деления, б − α-распада, в − е-захвата и β-распада, г − для всех процессов распада
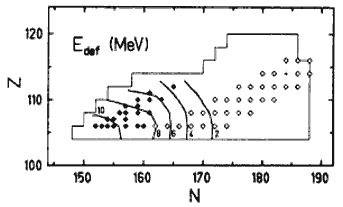 Рис. 12.5. Зависимость энергии равновесной деформации (указана в МэВ рядом с кривыми) от количества протонов и нейтронов. |
Результаты еще одного расчета равновесной формы сверхтяжелых ядер и их периодов полураспада показаны на рис. 12.5, 12.6 [R. Smolan’czuk Phys. Rev C56, 1997, p.812]. На рис. 12.5 показана зависимость энергии равновесной деформации от количества нейтронов и протонов для ядер с Z = 104-120. Энергия деформации определяется как разность энергий ядер в равновесной и сферической форме. Из этих данных видно, что в области Z = 114 и N = 184 должны располагаться ядра, имеющие в основном состоянии сферическую форму. Все обнаруженные на сегодня сверхтяжелые ядра (они показаны на рис. 12.5 темными ромбами) деформированы. Светлыми ромбами показаны ядра стабильные по отношению к β-распаду. Эти ядра должны распадаться в результате α-распада или деления. Основным каналом распада должен быть α-распад.
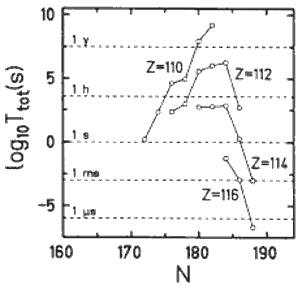 Рис. 12.6. Периоды полураспада для четно-четных β-стабильных изотопов. |
Периоды полураспада для четно-четных β-стабильных изотопов показаны на рис. 12.6. Согласно этим предсказаниям для большинства ядер ожидаются периоды полураспада гораздо большие, чем наблюдались для уже обнаруженных сверхтяжелых ядер (0.1–1 мс). Так например, для ядра 292 Ds предсказывается время жизни
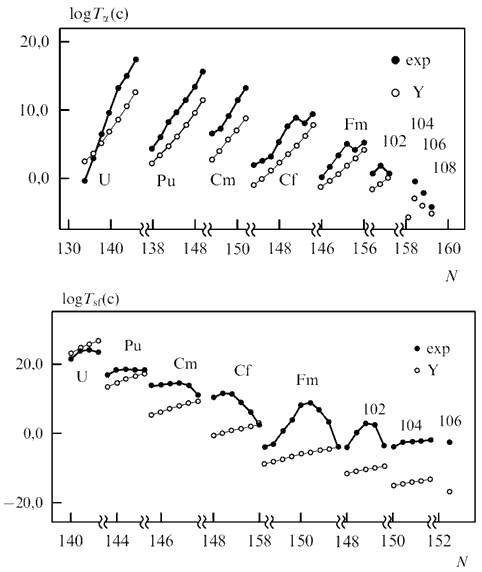
Рис. 12.7. Экспериментально измеренные (● exp) и теоретически рассчитанные (○ Y) периоды полураспада трансурановых элементов на основе модели жидкой капли без учета оболочечной структуры ядра. Верхний рисунок − периоды полураспада для α-распада, нижний рисунок − периоды полураспада для спонтанного деления.
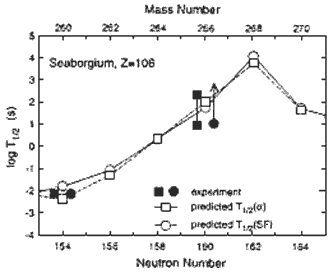 Рис. 12.8. Парциальные периоды полураспада по отношению к спонтанному делению и α-распаду. |
На рис. 12.8 показано измеренное время жизни изотопов сиборгия Sg (Z = 106) в сравнении с предсказаниями различных теоретических моделей [Z. Patyk et al. Nucl. Phys. A533, 1991, p.132; R. Smolanczuk et al. Phys. Rev. C52, 1995, p.1871]. Обращает на себя внимание уменьшение почти на порядок времени жизни изотопа с N = 164 по сравнению с временем жизни изотопа с N = 162.
Наибольшего приближения к острову стабильности можно достичь в реакции 76 Ge + 208 Pb. Сверхтяжелое почти сферическое ядро может образоваться в реакции слияния с последующим испусканием γ-квантов или одного нейтрона. Согласно оценкам образующееся ядро 284 114 должно распадаться с испусканием α-частиц с периодом полураспада
1 мс. Дополнительную информацию о заполненности оболочки в районе N = 162 можно получить, изучая α-распады ядер 271 Hs и 267 Sg. Для этих ядер предсказываются периоды полураспада 1 мин. и 1 час. Для ядер 263 Sg, 262 Bh, 205 Hs, 271,273 Ds ожидается проявление изомерии, причиной которой является заполнение подоболочек с j = 1/2 и j = 13/2 в районе N = 162 для ядер деформированных в основном состоянии.
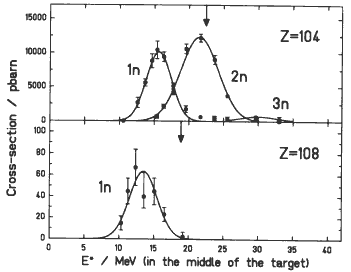 Рис. 12.9. Функции возбуждения реакции образования элементов Rf (Z = 104) и Hs (Z = 108) при слиянии налетающих ионов 50 Ti и 56 Fe с ядром мишенью 208 Pb. |
На рис. 12.9 показаны экспериментально измеренные функции возбуждения реакции образования элементов Rf (Z = 104) и Hs (Z = 108)для реакций слияния налетающих ионов 50 Ti и 56 Fe с ядром-мишенью 208 Pb.
Образовавшееся компаунд-ядро охлаждается испусканием одного или двух нейтронов. Информация о функциях возбуждения реакций слияния тяжелых ионов особенно важны для получения сверхтяжелых ядер. В реакции слияния тяжелых ионов необходимо точно сбалансировать действие кулоновских сил и сил поверхностного натяжения. Если энергия налетающего иона недостаточно большая, то расстояние минимального сближения будет недостаточно для слияния двойной ядерной системы. Если энергия налетающей частицы будет слишком большой, то образовавшаяся в результате система будет иметь большую энергию возбуждения и с большой вероятностью произойдет развал ее на фрагменты. Эффективно слияние происходит в довольно узком диапазоне энергий сталкивающих частиц.
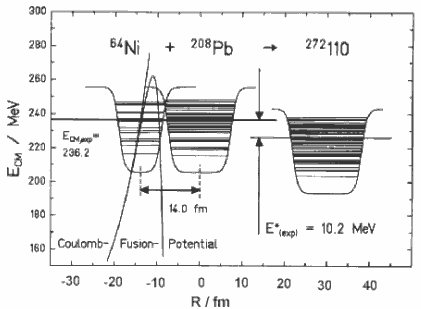
Рис.12.10. Схема потенциалов при слиянии 64 Ni и 208 Pb.
Реакции слияния с испусканием минимального числа нейтронов (1–2) представляют особый интерес, т.к. в синтезируемых сверхтяжелых ядрах желательно иметь максимально большое отношение N/Z. На рис. 12.10 показан потенциал слияния для ядер в реакции 64 Ni + 208 Pb → 272 Ds. Простейшие оценки показывают, что вероятность туннельного эффекта для слияния ядер составляет
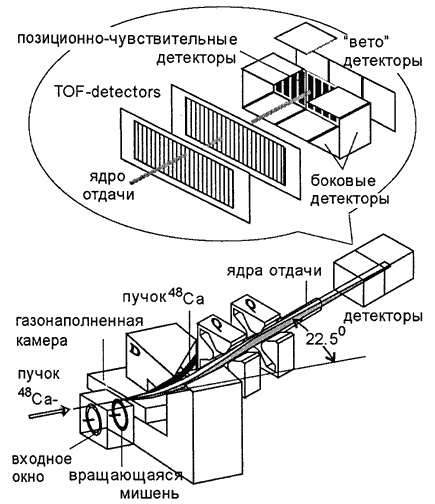
Рис. 12.11. Схематический вид сепаратора ядер отдачи, на котором проводятся эксперименты по синтезу сверхтяжелых элементов в Дубне.
Характеристики сверхтяжелых химических элементов Z = 110–118
На рис. 12.12 показаны все известные наиболее тяжелые изотопы с Z = 110–118, полученные в реакциях синтеза с указанием экспериментально измеренного периода полураспада. Здесь же показано теоретически предсказанное положение острова стабильности (Z = 114, N = 184).
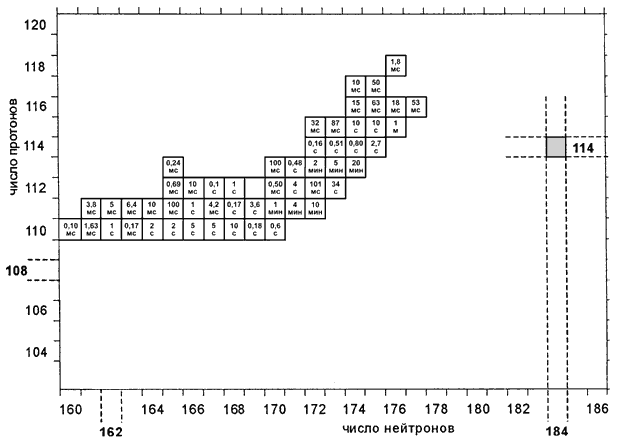
Рис. 12.12. N-Z-диаграмма элементов Z = 110–118.
Полученные результаты однозначно указывают на рост стабильности изотопов при приближении к дважды магическому ядру (Z = 114, N = 184). Добавление к ядрам с Z = 110 и 112 7–8 нейтронов увеличивает период полураспада от 2.8 ас (Ds-267) до ≈ 10 с (Ds-168, Ds 271). Период полураспада T1/2( 272 Rg, 273 Rg) ≈ 4–5 мс увеличивается до T1/2( 283 Rg) ≈ 10 мин. Наиболее тяжелые изотопы элементов Z = 110–112 содержат ≈ 170 нейтронов, что ещё далеко от магического числа N = 184. Все наиболее тяжелые изотопы с Z > 111 и N > 172 распадаются преимущественно в результате
α-распада, спонтанное деление – более редкий распад. Эти результаты находятся в хорошем согласии с теоретическими предсказаниями.
В Лаборатории ядерных реакций им. Г.Н. Флерова (Дубна) синтезирован элемент с Z = 114. Была использована реакция
Идентификация ядра 289 114 проводилась по цепочке α-распадов. Экспериментальная оценка периода полураспада изотопа 289 114
30 с. Полученный результат находится в хорошем согласии с ранее выполненными расчетами [Cherepanov E.A. Sub to Proc. Int VI Int. Conf on Dynamical Aspects on Nuclear Fission. Slovac Respublic. 1998].
При синтезе 114 элемента в реакции 48 Cu + 244 Pu максимальный выход изотопов с Z = 114 наблюдался в канале с испарением трех нейтронов. При этом энергии возбуждения составного ядра 289 114 была 35 МэВ.
Теоретически предсказываемая последовательность распадов, происходящих с ядром 296 116, образующемся в реакции 248 Cm + 48 Ca → 296 116, приведена на рис.12.13
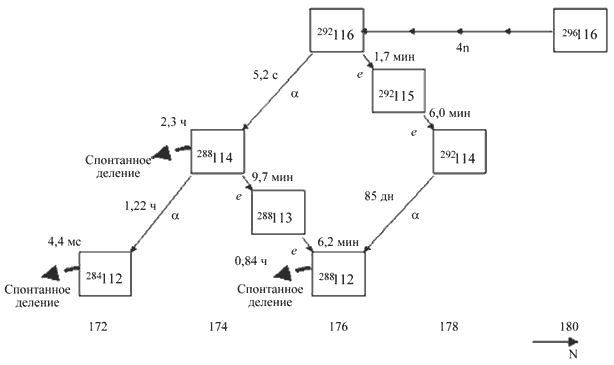
Рис. 12.13. Схема распада ядра 296 116.
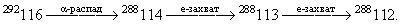
Конечное ядро 288 112, образующееся в результате обеих цепочек, имеет период полураспада около 1 часа и распадается в результате спонтанного деления. Примерно с 10%-ой вероятностью в результате α-распада изотопа 288 114 может образовываться изотоп 284 112. Приведенные выше периоды и каналы распада получены расчетным путем.
На рис. 12.14 приведена цепочка последовательных α-распадов изотопа 288 115, измеренная в экспериментах в Дубне. ER − энергия ядра отдачи, имплантированного в позиционно-чувствительный кремниевый детектор. Можно отметить хорошее совпадение в периодах полураспада и энергиях α-распадов в трёх экспериментах, что свидетельствует о надёжности метода идентификации сверхтяжелых элементов с помощью измерений спектров α-частиц.
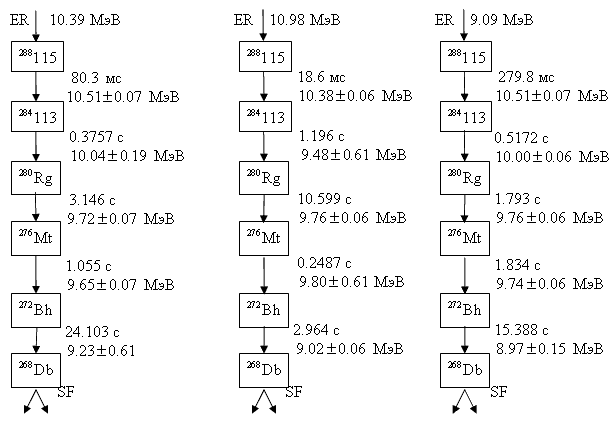
Рис. 12.14. Цепочка последовательных α-распадов изотопа 288 115, измеренная в экспериментах в Дубне.
Самый тяжелый, полученный в лабораторных условиях элемент с Z = 118, был синтезирован в реакции
48 Ca + 249 Cf → 294 118 + 3n.
При энергии ионов вблизи кулоновского барьера наблюдалось три случая образования 118 элемента. Ядра 294 118 имплантировались в кремниевый детектор и наблюдалась цепочка последовательных α-распадов. Сечение образования 118 элемента составляло
2 пикобарна. Период полураспада изотопа 293 118 равен 120 мс.
На рис. 12.15 показана теоретически рассчитанная цепочка последовательных α-распадов изотопа 293 118 и приведены периоды полураспада дочерних ядер, образующихся в результате α-распадов.
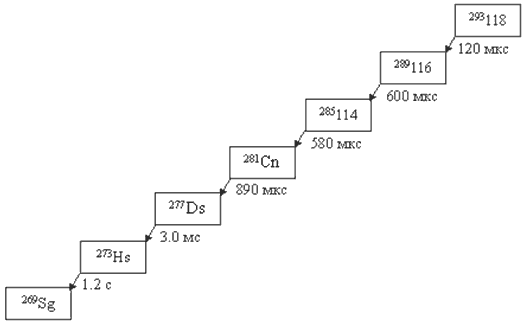
Рис. 12.15. Цепочка последовательных α-распадов изотопа 293 118.
Приведены средние времена жизни дочерних ядер, образующихся в результате α-распадов.
Анализируя различные возможности образования сверхтяжелых элементов в реакциях с тяжелыми ионами нужно учитывать следующие обстоятельства.
Весьма перспективным методом получения сверхтяжелых ядер являются реакции типа 238 U + 238 U, 238 U + 248 Cm, 238 U + 249 Cf, 238 U + 254 Es. На рис. 12.16 приведены оценочные сечения образования трансурановых элементов при облучении ускоренными ионами 238 U мишеней из 248 Cm, 249 Cf и 254 Es. В этих реакциях уже получены первые результаты по сечениям образования элементов с Z > 100. Для увеличения выходов исследуемых реакций толщины мишеней выбирались таким образом, чтобы продукты реакции оставались в мишени. После облучения из мишени сепарировались отдельные химические элементы. В полученных образцах в течение нескольких месяцев регистрировались продукты α-распада и осколки деления. Данные, полученные с помощью ускоренных ионов урана, ясно указывают на увеличение выхода тяжелых трансурановых элементов по сравнению с более легкими бомбардирующими ионами. Этот факт чрезвычайно важен для решения проблемы синтеза сверхтяжелых ядер. Несмотря на трудности работы с соответствующими мишенями прогнозы продвижения к большим Z выглядят довольно оптимистично.
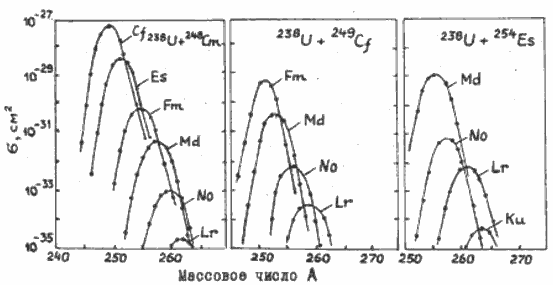
Рис. 12.16. Оценки сечений образования трансурановых элементов в реакциях 238 U с 248 Cm, 249 Cf и 254 Es
Продвижение в область сверхтяжелых ядер в последние годы оказалось ошеломляюще впечатляющим. Однако все попытки обнаружить Остров Стабильности пока не увенчались успехом. Поиск его интенсивно продолжается.
Оболочечная структура атомных ядер играет существенную роль в повышении стабильности сверхтяжелых ядер. Магические числа Z ≈ 114 и N ≈ 184, если они действительно существуют, могут привести к значительному повышению стабильности атомных ядер. Существенным является также то, что распад сверхтяжелых ядер будет происходить в результате α-распада, что важно для разработки экспериментальных методов детектирования и идентификации новых сверхтяжелых ядер.
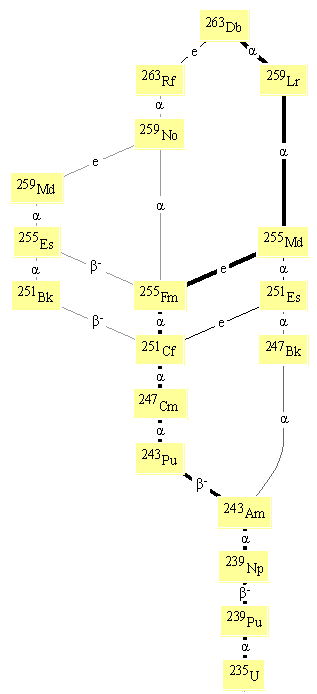
Распад изотопа 263 Db.
В результате цепочки последовательных распадов 263 Db образуется изотоп 235 U, имеющий период полураспада T1/2 = 7.04·10 8 лет. Из-за большого периода полураспада 235 U относят к стабильным изотопам. В естественной смеси изотопов урана изотоп 235 U составляет 0.7%. 235 U является родоначальником радиоактивного ряда A = 4n+3.
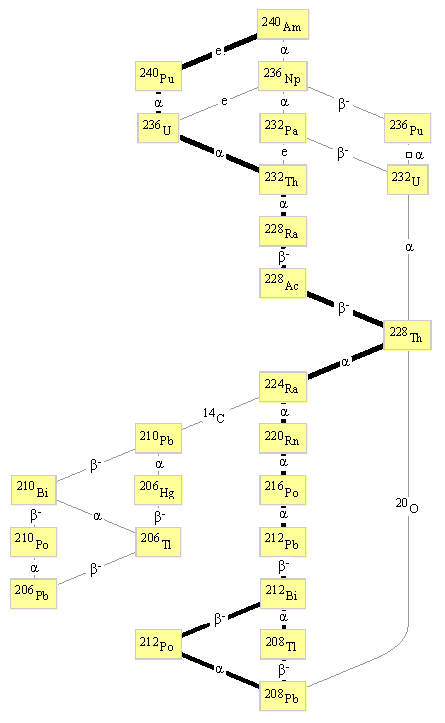
Распад изотопа 240Am.
Наряду с основными каналами распада тяжелых ядер − α-распадом и е-захватом в изотопе 238 Th наблюдается кластерный распад с испусканием 20 О, а в изотопе 224 Ra распад с испусканием кластера 14 С.
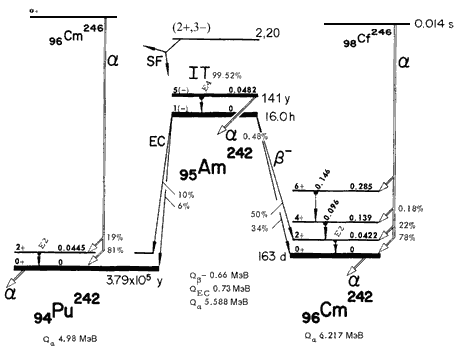
Распад ядер-изобар A = 242
Изотоп 242 Am имеет два изомерных состояния.
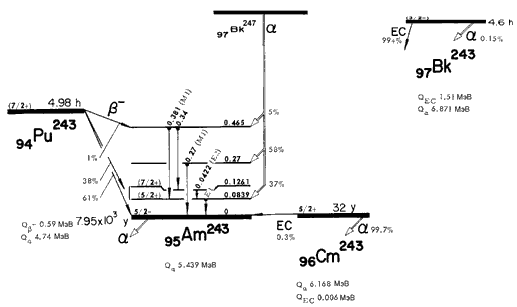
Распады ядер-изобар A = 243.
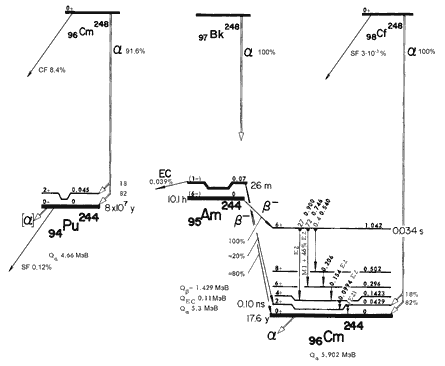
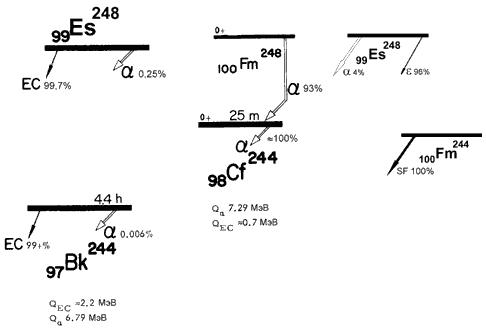
Распады ядер-изобар A = 244, A = 248.
Основными каналами распада ядер-изобар A = 244, A = 248 являются электронный захват и α-распад. При увеличении заряда ядра Z всё большую роль начинает играть спонтанное деление ( 244 Fm).