Что означает термодинамический процесс
Процессы в термодинамике
Вы будете перенаправлены на Автор24
В термодинамике выделяют несколько основных процессов. Термодинамическим процессом принято называть такое изменение общего состояния всей системы, когда в результате подобных трансформаций меняется полностью хотя бы один из ее основных параметров, его значение. Ими выступают:
Рисунок 1. Термодинамические процессы. Автор24 — интернет-биржа студенческих работ
Известно, что все термодинамические процессы имеют тесные связи друг с другом. При изменении хотя бы одного параметра может меняться в неизбежном режиме вся система. В общем смысле, любой термодинамический процесс можно представить в виде равновесной системы, которая балансирует на грани нарушения этого равновесия. Если вся система уже находится в равновесном состоянии, то это явление не предполагает наличия термодинамических процессов вовсе. В таких системах не фиксируются термодинамические процессы.
Хоть понятие равновесного состояния системы нельзя назвать четким, все же существуют некоторые законы его присутствия в реальном воплощении. Любые материальные вещи невозможно полностью изолировать от окружающего его мира, поэтому в любой реальной системе возможно протекание различных термодинамических процессов. Иногда подобные процессы протекают настолько слабо и медленно, что не всегда удается их зафиксировать в оптимальном выражении. Специалисты их устанавливают как цепь разнообразных равновесных состояний системы. Их еще могут называть равновесными процессами, а также квазистатическими процессами.
Круговыми процессами и циклическими процессами называют ряд последовательных повторяющихся изменений в системе. В итоге система после прохождения определенного отрезка пути возвращается в исходное состояние. Круговой и равновесный процесс возникает и изучается под видом прикладных приемов термодинамики физических явлений, а также они лежат в основании некоторых теоретических размышлений и выводов науки.
Готовые работы на аналогичную тему
Сегодня выделяют несколько основных термодинамических процессов:
Изобарный процесс
Рисунок 2. Изобарный процесс. Автор24 — интернет-биржа студенческих работ
Изобарный процесс – это такой термодинамический процесс, который может протекать при постоянном давлении. Подобный процесс осуществляется, например, когда помещается газ в плотный цилиндр, где есть подвижный поршневой крючок.
На поршень действует постоянная внешняя сила. Она достигается при подводе или отводе теплоты к объекту. При этом сама подвижная часть поршня способна менять свое местоположение при изменении параметров температуры. От этого зависит направление движения поршня. Согласно закону Гей-Люссака, объем газа в нем меняется, исходя из уравнения закона. Из этого следует, что занимаемый объем газа может быть прямо пропорционален определенной температуре воздействия. Внутренняя энергия газов изменяется под действием температурного режима извне. Этим правилом характеризуется весь изобарный процесс в термодинамике.
Изохорный процесс
Рисунок 3. Изохорный процесс. Автор24 — интернет-биржа студенческих работ
Изохорный процесс – термодинамический процесс, который заключается в протекании при постоянном объеме.
В качестве примера можно привести закрытый сосуд, куда помещен газ. При его нагревании возникают признаки изохорного процесса. При подводе особого температурного режима к изучаемому сосуду давление возрастает. Чем больше тепловой эффект, тем процесс становится более интенсивным. Подобные преобразования параметров газа в сосуде способен математическим методом описать закон Шарля.
Согласно его уравнению, давление газа на стенки сосуда будут прямо пропорциональными абсолютной температуре этого газа. Примечательно, что вся подведенная к сосуду теплота изменяет внутреннюю энергию газа, поэтому совершение работы не происходит изменение объема в сосуде при изохорном процессе равно нулевым значениям.
Адиабатный процесс
Рисунок 4. Адиабатный процесс. Автор24 — интернет-биржа студенческих работ
Изотермический процесс
Изотермический процесс – термодинамический процесс, который протекает при неизменной температуре. Его так же, как и адиабатный процесс осуществить с точностью очень сложно. Для этого необходимо соблюдение условий по расширению и сжатию рабочего газа при постоянной температуре. Также нужно, чтобы газы успевали обмениваться с окружающей средой без потери собственного температурного режима. Хорошо способен описать этот процесс закон Бойля-Мариотта.
Политропный процесс
Рисунок 5. Политропные процессы. Автор24 — интернет-биржа студенческих работ
Политропный процесс характеризуется иными свойствами термодинамических процессов. В отличие от вышеперечисленных процессов термодинамики политропный процесс предполагает возможность изменения любого параметра газа. В других процессах подобные параметры изменять нельзя. Иные термодинамические процессы принято считать частными случаями политропного процесса.
Если придавать известной формуле определенные значения показателю политропы, то в качестве результата получаем определенный термодинамический процесс. В зависимости от этих представлений приходит итог по изотермическому, адиабатному, изохорному или изобарному процессу.
Термодинамика
Лекция 1. Предмет технической термодинамики и ее методы
1. Предмет термодинамики
2. Основные параметры состояния тела
3. Понятие о термодинамическом процессе
4. Гомогенные и гетерогенные термодинамические системы
5. Термодинамическое равновесие
1. Предмет термодинамики
Термодинамика наука о превращениях различных видов энергии из одного в другой, и о наиболее общих макроскопических свойствах материи. Она изучает различные как физические, так и химические явления, обусловленные превращениями энергии. Применение закономерностей термодинамики позволяет анализировать свойства веществ, предсказывать их поведение в различных условиях. Термодинамика дает возможность исследовать различные процессы от простых в однородных средах до сложных с физическими и химическими превращениями, биологических и др.
Слово «термодинамика» происходит от греч. «therme» – тепло и «dynamis» – сила. Название науки возникло в период ее основания – в начале XIX в. В настоящее время слово «термодинамика» трактуют так: наука «о силах, связанных с теплотой».
Термодинамика основана на двух, экспериментально установленных законах (началах).
Первый закон (начало) является по существу законом преобразования и сохранения энергии применительно к процессам, изучаемым в термодинамике; невозможен процесс возникновения или исчезновения энергии.
Второй закон (начало) – определяет направление течения реальных (неравновесных) процессов; невозможен процесс, имеющий единственным своим результатом превращение теплоты в работу.
Термодинамический метод исследования основан на законах (началах) термодинамики и представляет собой их логическое и математическое развитие.
Объект исследования в термодинамике называют термодинамической системой или, в простом случае, термодинамическим телом. Одна из особенностей метода термодинамики состоит в том, что система (тело) противопоставляется всем другим телам, которые называют окружающей средой. Термодинамика построена дедуктивно: частные выводы получены из общих законов (начал).
Принято разделять термодинамику на физическую, или общую, химическую и техническую.
Физическая термодинамика разрабатывает метод термодинамики и применяет его для изучения фазовых превращений термоэлектрических и магнитных явлений, излучения, поверхностных явлений и т. п.
Химическая термодинамика изучает процессы с физическими и химическими превращениями с помощью метода термодинамики.
Техническая термодинамика устанавливает закономерности взаимного преобразования теплоты и работы, для чего изучает свойства газов и паров (рабочих тел) и процессы изменения их состояния; устанавливает взаимосвязь между тепловыми, механическими и химическими процессами, протекающими в тепловых двигателях и холодильных установках. Одна из основных ее задач – отыскание наиболее рациональных способов взаимного превращения теплоты, и работы.
Термодинамический процесс



Лекция 2
ПДК выбрососв АЭС 0,05 Зв/год для персонала0,005Зв/год для населения вблизи
Мы будем рассматривать только равновесные термодинамические процессы, протекающие в равновесных системах. Равновесным состояниемсистемы называется состояние, когда во всех точках системы давления и температуры одинаковы. Система, выведенная из состояния равновесия и предоставленная при постоянных параметрах окружающей среды самой себе, через некоторое время вновь придет в равновесное состояние, соответствующее этим параметрам. Процесс, проходящий через чередующиеся равновесные состояния системы называется равновесным процессом.
В противном случае система неравновесна. Все процессы, протекающие в реальном времени, как правило, неравновесны. Допущение о существовании равновесных систем основано на том, что любая система, выведенная из состояния равновесия и предоставленная при постоянных параметрах окружающей среды самой себе, через некоторое время вновь придет в равновесное состояние. Такое самопроизвольное (без внешнего воздействия) возвращение системы в состояние равновесия называется релаксацией, а промежуток времени, в течение которого реальная система возвращается в состояние равновесия, называется временем релаксации. Если реальный процесс протекает медленнее, чем идёт релаксация, то процесс является равновесным. Дли разных процессов и разных параметров время релаксации различно. Внутренними процессами, компенсирующими нарушение равновесия при изменение состояния тела и восстанавливающими термодинамическое равновесие, являются элементарные процессы обмена энергией при столкновении молекул.
Интересно отметить, что превращение энергии поступательного движения молекул в энергию вращательного движения и обратно при столкновении молекул происходит весьма быстро. Так, давление в объёме выравнивается со скоростью звука (более 340 м/с в воздухе при нормальных физических условиях). Температура – значительно медленнее. Связано это с тем, что превращение энергии поступательного или вращательного движения молекул в колебательное при росте температуры осуществляется сравнительно медленно. Вообще все процессы обмена энергии, в которых участвуют колебательные степени свободы движения молекул, требуют для своего осуществления сравнительно большого времени.
Рассмотрим, например, процесс сжатия газа в цилиндре. Если время смещения поршня от одного положения до другого существенно превышает время релаксации, то в процессе перемещения поршня давление и температура успеют выровняться по всему объему цилиндра. Это выравнивание обеспечивается непрерывным столкновением молекул, в результате чего подводимая от поршня к газу энергия достаточно быстро и равномерно распределяется между ними. Если последующие смещения поршня будут происходить аналогичным образом, то состояние системы в каждый момент времени будет практически равновесным.
Теоретически равновесный процесс можно осуществить только при бесконечно медленном изменении состояний системы и внешних условий. В этом смысле время как действующий физический фактор в равновесных процессах не применяется.
Уравнение состояния F (Р, v, Т) = 0 в трёхосной системе координат Р, v и Т представляют собой поверхность, называемую термодинамической поверхностью. Если рассечь эту поверхность (рис. 1.8) плоскостями параллельными осям координат, то получим кривые. Например, сечение плоскостью Т = const даёт линию изменения давления в зависимости от объёма в координатах Р и v, Описываемый процесс называется изотермным.
В термодинамике чаще всего применяют двухосную систему с координатами Р и v (рис. 1.9).
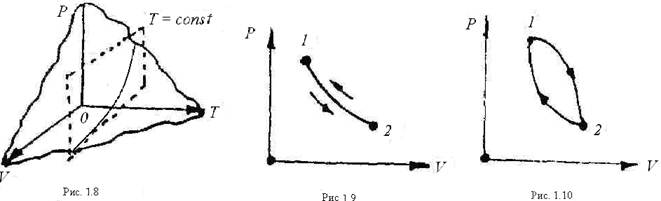 |
Процесс может быть прямым и обратным. Если система с параметрами Р1 и v1 (точка 1) переходит в состояние 2 с параметрами Р2 и v2, а затем возвращается в состояние 1, то такой процесс называется обратимым (рис. 1.9).Обратимым называется равновесный процесс, проходящий в прямом и обратном направлениях через ряд одинаковых состояний. В обратной последовательности состояний равновесного процесса рабочее тело и внешняя среда возвращаются в исходное состояние.
Процессы, не соответствующие этому условию, называются необратимыми. Все реальные процессы необратимы.
В начальном курсе термодинамики рассматриваются равновесные обратимые процессы, происходящие в закрытых (ΔМ = 0) системах:
1) изохорный, протекающий при неизменном объеме (v = const);
2) изобарный, протекающий при неизменном давлении (p = const);
3) изотермный, протекающий при неизменной температуре (Т = const);
4) адиабатный, совершающийся при отсутствии теплообмена (ΔQ =0);
5) политропный, обобщающий, процесс, частными случаями котоpoгo являются первые четыре процесса.
Особое значение имеют замкнутые процессы (или круговые). Это такие процессы, при которых система проходит ряд последовательных состояний, возвращаясь к первоначальному. Иначе такой процесс называется циклом (рис. 1.10).
2.1.Теплоёмкость идеальных газов
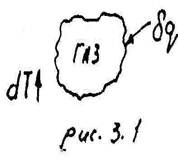
Отношение элементарного количества теплоты δQ, полученного телом при бесконечно малом изменении его состояния, к связанному с этим изменению температуры тела dT называется теплоёмкостью рабочего тела в данном процессе:
(Причина применения разных символов δ или d приэлементарных количествах теплоты и температуры будет объяснена ниже).
Изменение температуры тела при одном и том же количестве сообщаемой теплоты зависит от характера происходящего при этом процесса, поэтому теплоемкость является функцией процесса. Это означает, что одно и то же рабочее тело в зависимости от процесса требует для своего нагревания на 1 К различного количества теплоты. Численно величина с изменяется в пределах от + ∞ до — ∞. При этом разница является суммой разниц внутренней энергии и работ процессов.
—удельную массовую теплоёмкость с, отнесенную к 1 кг вещества, Дж/(кг-К);
—удельную мольную теплоёмкость сμ, отнесенную к одному киломолю вещества, Дж/(кмоль-К).
Массовая удельная теплоёмкость (с) равна:
Молярная теплоёмкость µс равна:.
Зависимость между удельными теплоёмкостями устанавливается очевидными соотношениями:
Здесь ρн — плотность газа при нормальных условиях, [кг / м 3 ].
Из уравнения (1): δqx = сх · dТ
можно найти количество тепла, сообщённого телу в течение процесса
Изохорная теплоёмкость
В термодинамических расчетах большое значение имеет теплоемкость при постоянном объеме
Она равна отношению количества теплоты δqv, подведенной к телу в процессе при постоянном объеме, к изменению температуры тела dТv;
— теплоемкость при постоянном давлении
| Теплоёмкость некоторых газов при температуре 0 0 С | |||
| Газ | Число степеней свободы | Мольная тепло- емкость, кДж/ (кмоль- К) | k=Cр / Cv |
| Гелий Не | 3 | 12,60 | 1,660 |
| Аргон Аr | 3 | 12,48 | 1,660 |
| Кислород О2 | 5 | 20,96 | 1,397 |
| Водород Н2 | 5 | 20,30 | 1,410 |
| Азот N2 | 5 | 20,80 | 1,400 |
| Метан СH4 | 6 | 26,42 | 1,315 |
| Аммиак NH3 | 6 | 26,67 | 1,313 |
| Диоксид угле- рода СО2 | 6 | 27,55 | 1,302 |
| Перегретый водяной пар Н2О | 6 | 1,30 |
Молекула одноатомного газа имеет три степени свободы соответственно трем составляющим в направлении координатных осей, на которые может быть разложено поступательное движение. Молекула двухатомного газа имеет пять степеней свободы, так как помимо поступательного движения она может вращаться около двух осей, перпендикулярных линии, соединяющей атомы. Молекула трехатомного и вообще многоатомного газа имеет шесть степеней свободы: три поступательных и три вращательных.
Результаты классической теории теплоемкости достаточно хорошо согласуются с экспериментальными данными в области комнатных температур, однако основной вывод о независимости от температуры эксперимент не подтверждает. Расхождения, особенно существенные в области низких и достаточно высоких температур, связаны с квантовым поведением молекул и находят объяснения в рамках квантовой теории теплоемкости.
С уменьшением температуры газа происходит «вымораживание» числа степеней свободы молекул. Так, для двухатомной молекулы происходит «вымораживание» вращательных степеней свободы и она вместо пяти имеет три степени свободы, а следовательно, и меньшую внутреннюю энергию и теплоемкость. С увеличением температуры у многоатомных молекул происходит возбуждение внутренних степеней свободы за счет возникновения колебательного движения атомов молекулы (молекула становится осциллятором). Это приводит к увеличению внутренней энергии, а следовательно, и теплоемкости с ростом температуры.
Выведем уравнение изохорной теплоёмкости. Первый закон термодинамики для равновесного процесса записывается так:
δq = du + p • dv (3)
Так как удельная внутренняя энергия u является полным дифференциалом, то можно её определить в зависимости от двух любых параметров, например от Т и v: и = f (T, v), тогда можно записать;
du = ( ∂u/∂T)v • dT + (∂u/∂υ)т • dυ (4)
Подставим значение du из (4) в уравнение'(3):
δq = (∂u/∂T)v · dT + (∂u/∂υ)т · dυ + p · dυ
δq = (∂u/∂T)v · dT + [p + (∂u/∂υ)т] · dυ (4′)
Так как в изохорном процессе υ = const, то dυ = 0. Тогда имеем:
а теплоёмкость в изохорном процессе равна:
Используя выражения (3), (5), (6) можно записать:
To есть в процессе при v = const, когда тело не совершает внешней работы вся теплота, подведённая к телу расходуется на изменение его удельной внутренней энергии.
Принимая сv = const, можно записать из (7):
q1-2, v = u2 – u1 = cv · (T2 – T1) (8)
Таким образом, изменение удельной внутренней энергии идеального газа равно произведению теплоёмкости сv при постоянном объеме, на разность температур тела.
Из уравнения (4′) при р = const имеем:
Учитывая выражение (9) можно записать:
Ср = (ди/ дТ)v + [ р + (ди / дυ)т ] • (дυ/dT)р
Используя уравнение (6 ’ ) запишем:
Для идеального газа. (дu / дv)T= 0, а так как R = р · v I T, то
дифференцируя его при р = const, имеем:
Подставляя (12) в (11) имеем окончательно:
Что означает термодинамический процесс
Понятие термодинамического прцесса характеризует термодинамическую систему с точки зрения ее энергетического взаимодействия с окружающей средой.
Термодинамическим процессом называется процесс изменения состояния термодинамического тела (системы), не находящегося в термодинамическом равновесии с внешней средой и не изолированный от нее. При этом наблюдается энергетическое взаимодействие между телом и окружающей средой, сопровождающееся изменением параметров тела.
Строго говоря, только для процессов, происходящих очень медленно, с малыми отклонениями промежуточных параметров (квазистатические равновесные процессы) можно воспользоваться уравнениями состояния, а сам процесс геометрически представить в виде непрерывной кривой на термодинамической поверхности. Графическое изображение действительных неравновесных процессов, протекающих с конечной скоростью, имеет условный характер. Понятие равновесности характеризует поведение параметров внутри и на границах тел при процессах, но не затрагивает превращения форм энергии и распределение ее в системе. Для характеристики процессов с точки зрения превращения и распределения энергии между всеми телами, участвующими в процессе, вводится понятие обратимости процессов.
Обратимыми называются процессы, которые могут быть проведены в прямом и обратном направлениях таким образом, что все тела, участвующие в процессе, проходят через одни и те же промежуточные равновесные состояния (но в обратной последовательности), а после проведения прямого и обратного процессов все тела системы возвращаются в первоначальное состояние, и, следовательно, распределение энергии между ними оказывается прежним.
Процессы, не отвечающие поставленным условиям, называются необратимыми.
Все неравновесные процессы необратимы. Так, при неравенстве давления в рабочем теле и внешнего давления, рабочее тело расширяется или сжимается, в результате возникают вихревые движения, которые со временем успокаиваются, а их энергия переходит в энергию теплового движения частиц. В этом случае наблюдается переход механической работы в теплоту, в результате чего для возврата системы в первоначальное состояние потребуется дополнительное количество механической работы.
При отсутствии термического равновесия процесс также необратим. Теплота самопроизвольно переходит от тела, более нагретого к телу менее нагретому, и обратный переход теплоты возможен только при наличии дополнительного источника теплоты.
Необратимость процессов подразделяется на:
— внешнюю необратимость, вызванную разностью температур при теплообмене между телами;
— внутреннюю необратимость, вызванную наличием трения. В прямом и обратном процессах в этом случае имеется работа, затрачиваемая на трение, она превращается в теплоту.
Всякая необратимость связана с уменьшением возможной работы системы, эта потеря является мерой необратимости процесса. Процессы с полной потерей возможной работы называются предельно необратимыми. Примерами предельно-необратимых процессов могут служить: расширение газа в вакуум, дросселирование газов и паров, рассеяние теплоты горячего тела в окружающую среду и т.п.
При термодинамических исследованиях процессов обычно не касаются внешней необратимости, обусловленной разностью температур при теплообмене, сами же процессы принимаются (естественно условно) внутренне равновесными. Такие процессы легко поддаются термодинамическому анализу, так как они могут изображаться графически в виде сплошных линий на диаграммах параметров состояния.
Термодинамика
Лекция 1. Предмет технической термодинамики и ее методы
1. Предмет термодинамики
2. Основные параметры состояния тела
3. Понятие о термодинамическом процессе
4. Гомогенные и гетерогенные термодинамические системы
5. Термодинамическое равновесие
1. Предмет термодинамики
Термодинамика наука о превращениях различных видов энергии из одного в другой, и о наиболее общих макроскопических свойствах материи. Она изучает различные как физические, так и химические явления, обусловленные превращениями энергии. Применение закономерностей термодинамики позволяет анализировать свойства веществ, предсказывать их поведение в различных условиях. Термодинамика дает возможность исследовать различные процессы от простых в однородных средах до сложных с физическими и химическими превращениями, биологических и др.
Слово «термодинамика» происходит от греч. «therme» – тепло и «dynamis» – сила. Название науки возникло в период ее основания – в начале XIX в. В настоящее время слово «термодинамика» трактуют так: наука «о силах, связанных с теплотой».
Термодинамика основана на двух, экспериментально установленных законах (началах).
Первый закон (начало) является по существу законом преобразования и сохранения энергии применительно к процессам, изучаемым в термодинамике; невозможен процесс возникновения или исчезновения энергии.
Второй закон (начало) – определяет направление течения реальных (неравновесных) процессов; невозможен процесс, имеющий единственным своим результатом превращение теплоты в работу.
Термодинамический метод исследования основан на законах (началах) термодинамики и представляет собой их логическое и математическое развитие.
Объект исследования в термодинамике называют термодинамической системой или, в простом случае, термодинамическим телом. Одна из особенностей метода термодинамики состоит в том, что система (тело) противопоставляется всем другим телам, которые называют окружающей средой. Термодинамика построена дедуктивно: частные выводы получены из общих законов (начал).
Принято разделять термодинамику на физическую, или общую, химическую и техническую.
Физическая термодинамика разрабатывает метод термодинамики и применяет его для изучения фазовых превращений термоэлектрических и магнитных явлений, излучения, поверхностных явлений и т. п.
Химическая термодинамика изучает процессы с физическими и химическими превращениями с помощью метода термодинамики.
Техническая термодинамика устанавливает закономерности взаимного преобразования теплоты и работы, для чего изучает свойства газов и паров (рабочих тел) и процессы изменения их состояния; устанавливает взаимосвязь между тепловыми, механическими и химическими процессами, протекающими в тепловых двигателях и холодильных установках. Одна из основных ее задач – отыскание наиболее рациональных способов взаимного превращения теплоты, и работы.



