Что означает таргетная терапия в онкологии
Таргетная терапия в онкологии
Рецензент материала
Профессор Капранов С.А. — Доктор медицинских наук, дважды Лауреат Государственных Премий Правительства Российской Федерации в области науки и техники, Лауреат Премии Ленинского Комсомола, автор более 350 научных работ по медицине, 7 монографий, и 10 патентов на изобретения по медицине, за 30 лет личного опыта провел более чем 10 000 различных эндоваскулярных операций
Использование таргетной терапии в онкологии – это инновационный подход, исследуемый и модифицируемый около полувека. Изначально не было понятия «таргетный», имелось слабое представление про рак, а сам эффект от лечения оценить было невозможно. Потом появились гормональные препараты и некоторое понимание механизмов точечного воздействия на клетки рака. В XXI веке таргетная терапия вошла в онкомедицину как действенный метод лечения, подкреплённый научной аргументацией.
Наряду с гормональным или химиотерапевтическим лечением данный вид терапии основан на приёме специальных медикаментозных препаратов. Ключевым отличием таргетного воздействия является то, что разрушительный эффект оказывается исключительно на злокачественные клетки. Также таргетная терапия может блокировать процессы канцерогенеза (размножения клеток рака). Рассмотрим особенности и возможные направления применения данного метода в онкологии.
Развитие таргетной терапии и преимущества метода
Рак – это бич современного общества, а потому процесс борьбы с онкологическими заболеваниями никогда не прекращается. Непосредственно при исследовании таргетного воздействия ищут новые комбинации препаратов и генерируют действующие вещества, находящие и разрушающие злокачественного образования. На сегодняшний день таргетная терапия осуществляется в следующих формах:
Однако полного разделения таргетного воздействия и химиотерапии на данный момент не произошло, т.к. новые препараты, используемые в борьбе с раком, всё также сочетаются с цитостатиками для усиления эффективности. Потому и полного отсутствия побочных эффектов, в частности, проявляющихся в клеточной биохимии, гарантировать нельзя.
Преимущества таргетной терапии
Принято сравнивать данный метод с другими терапевтическими подходами к борьбе с раком. Выделяют следующие преимущества от использования таргетных средств:
Назначение этого метода, как единственного способа лечения, либо в комплексе с химиотерапией, может произвести только специалист. Зачастую это делается на консилиуме при поддержке коллег, изучивших клиническую картину пациента.
Стоит отметить, что этот подход к борьбе с раковыми опухолями актуален практически для каждого пациента. Необходимо провести лишь специализированные исследования, которые позволят отобрать наиболее эффективные действующие вещества под каждый конкретный случай заболевания.
Разнообразие таргетных препаратов
Сегодня существует множество таргетных средств для осуществления точечного лечения различных форм рака. Некоторые активно используются в медицинской практике, другие же еще не связаны с онкологией, поскольку лишь тестируются или проходят клинические испытания. Исходя из эффекта, оказываемого в процессе лечения теми или иными таргетными средствами, все они делятся на следующие группы:
Конкретный способ борьбы с раком может определить исключительно лечащий врач, имеющий полное представление об особенностях развивающейся опухоли. Его рекомендации следует исполнять беспрекословно, избегая какого-либо самолечения. Любые народные средства или препараты, помогающие знакомым и родственникам, лишь отнимут время, которое может быть потрачено лечащим врачом с пользой.
Виды рака, поддающиеся таргетной терапии
Эффективность таргетного способа лечения можно оценить только после молекулярно-генетического анализа клеточной структуры рака. Цель исследования заключается в том, чтобы найти ту самую «мишень», на которую будут направлены применяемые препараты. Чаще всего таргетную терапию назначают на финальных стадиях развития рака с очевидной безрезультативностью других форм лечения и метастазированием. Рассмотрим виды заболеваний, поддающихся лечению препаратами таргетного типа.
При раке молочной железы
Прямое воздействие оказывается на гормональный рецептор, расположенный внутри железы. Тот, в свою очередь, функционирует в сочетании с половыми гормонами, находящимися в крови. Применяемый препарат подменяет гормон, таким образом рак уничтожается стандартным функционалом организма. Также возможна подмена половых гормонов в целях блокировки продуцирования веществ, необходимых клеткам рака.
При раке легкого
В данном случае таргетная терапия часто сочетается с химиотерапией, но может быть и одиночным методом. Суть таргетных препаратов заключается в том, чтобы заблокировать ангиогинез, исключить из работы органа мутантные белки, приводящие к тому, что клетки рака активно размножаются.
При колоректальном раке
При лечении формы рака, поражающей толстую и прямую кишку, применяются препараты, воздействующие на следующие элементы:
В зависимости от индивидуальных показаний лечение может осуществляться как в комплексе, так и по одному из направлений.
При раке почки
Опять же, когда раком поражаются почки, таргетные препараты нацелены на блокировку ангиогинеза, а также белков тирозинкиназы и mTOR.
Внимание! Это далеко не весь перечень опухолей, которые поддаются лечению посредством таргетной терапии. В сети Интернет вы можете найти обширный перечень таргетных препаратов, подходящих для каждого конкретного случая. Однако назначение на лечение может дать исключительно профильный специалист после тщательного осмотра, лабораторных исследований и составления оптимального плана приёма препаратов.
Возможные побочные эффекты таргетной терапии
Как уже было сказано, таргетная терапия отличается от химиотерапии тем, что оказывает минимум негативного воздействия на здоровые клетки организма. Если при лечении в комплексе с химиотерапией появление побочных эффектов очевидно, то самостоятельное применение таргетных препаратов вызывает иной спектр негативных проявлений.
Во избежание подобных эффектов, на определённое время лечение любой формы рака может быть приостановлено, либо специалист уменьшит дозировку, негативно влияющего на организм препарата. Также может последовать отказ от химиотерапии, как сопутствующего метода. Для улучшения самочувствия и восстановления пораженных побочными эффектами участков могут быть назначены сопроводительные препараты.
Чтобы можно было проконтролировать приём медикаментов, когда осуществляется лечение посредством таргетной терапии, пациент госпитализируется. Если выраженные побочные эффекты отсутствуют, а больной легко переносит все действующие вещества, то в дальнейшем лечебный процесс проводится амбулаторно.
Поддержка больных
Также при борьбе с раковыми заболеваниями одной из ключевых задач врача и самого пациента является формирование положительного психоэмоционального фона. Независимо от того, какой метод воздействия избран, будь то таргетная терапия или облучение раковых клеток, недопустимо настраиваться на отрицательный результат.
Квалифицированные специалисты способствуют улучшению настроения и общего самочувствия пациентов следующим образом:
При этом больной должен постоянно находиться в благоприятных условиях. Насколько бы эффективна ни была таргетная терапия – положительный настрой вносит весомый вклад в конечный результат лечебного процесса.
Реабилитационный процесс
Как такового, восстановления после таргетной терапии нет, поскольку она не имеет выраженного побочного действия, что было сказано ранее. Однако стоит помнить, что таргетная терапия неизменно связана с действующими веществами химиотерапевтического формата, а потому при восстановлении пациентов, прошедших комплекс приёма таких средств актуальны все рекомендации, касающиеся второго метода. Об этих и других нюансах лечебного процесса читайте в статьях нашего сайта.
Зачастую сразу после выписки пациенты могут приступать к рабочему процессу, если, конечно же, речь не идёт о финишных стадиях развития раковой опухоли. В таком случае таргетная терапия изначально направлена лишь на продление срока жизни и улучшение состояния пациента.
Обращение в Центр профессора Капранова
Предлагаем пройти обследование в Центре эндоваскулярной хирургии. Обращайтесь в наше учреждение в Москве, чтобы получить компетентную помощь от высококвалифицированных врачей различного профиля.
Основные преимущества обращения за помощью в Центр профессора Капранова:
Всё это вы можете получить, договорившись с нами о первом обследовании. Это можно сделать как по телефону из раздела «Контакты», так и лично, приехав по указанному адресу.
Важно! В нашем Центре любой лечебный процесс осуществляется с применением исключительно сертифицированных медпрепаратов. Каждое лекарственно средство закупается у надёжных поставщиков с обязательным предоставлением сертификата качества. Речь идёт только о проверенных препаратах, прошедших клинические испытания.
На сайте можно прочитать ряд статей, посвященных каждому заболеванию в рамках нашего профиля. Из этих материалов вы узнаете о способах борьбы с патологиями, опухолями и прочими заболеваниями. Пользовательские отзывы подробнее расскажут о наших технических возможностях и качественном уровне обслуживания в Центре. Оставьте и свой комментарий, можно и с конструктивной критикой, которая поможет нам улучшить сервис.
Ценовая политика предоставляемых услуг является конкурентной. Конечную стоимость обслуживания мы формируем на основании индивидуальных особенностей заболевания и личных потребностей пациента. Никогда не назначаются лишние процедуры или принудительные операции, если можно добиться положительного эффекта и без хирургического вмешательства. Будьте здоровы, а мы постараемся вам в этом помочь!
Таргетная терапия
Что такое таргетная терапия?
Таргетная терапия – это специальные лекарства, которые уничтожают определенные типы раковых клеток. Они воздействуют исключительно на вещества, благодаря которым некоторые виды онкологии растут и распространяются по организму.
Название метода происходит от английского слова «target» – цель или мишень. Именно так он и работает – точно против измененных тканей.
Чем таргетная терапия отличается от химиотерапии?
Подобные вещества, так же как и другие используемые для лечения рака лекарства, технически считаются химиотерапией, но принцип их действия отличается:
Как работает таргетная терапия?
Таргетные препараты предназначены для воздействия на определенные вещества в раковых клетках: избыток некоторых белков, а также соединения или изменения генов, которые отсутствуют в нормальных тканях.
Такие лекарства умеют:
Виды таргетной терапии
Существует несколько типов препаратов, каждый из которых выполняет определенную задачу.
Ингибиторы ангиогенеза: блокируют образование новых кровеносных сосудов, которые необходимы новообразованию для питания и быстрого роста – например, бевацизумаб, применяющийся при нескольких видах рака.
Моноклональные антитела: доставляют в опухолевую клетку молекулы, которые ее убивают. Одни их виды называют таргетной терапией, поскольку у них есть конкретная цель в онкологической клетке, которую они стремятся найти и атаковать. Другие действуют как иммунотерапия, стимулирующая иммунную систему и помогающая ей обнаруживать онкологию и бороться с ней. К таким лекарствам относят трастузумаб, работающий при некоторых типах новообразований молочной железы, и цетуксимаб, назначающийся пациентам с опухолями прямой кишки, легких, головы и шеи.
Ингибиторы протеасом: нарушают нормальную работу клеток, что приводит к их гибели. Их примером является бортезомиб, применяющийся при множественной миеломе – заболевании кроветворной системы.
Ингибиторы сигнальной трансдукции: блокируют активность молекул, передающих сигналы между клетками. Так работает препарат иматиниб, применяющийся при некоторых типах хронической лейкемии – поражении костного мозга, приводящем к образованию измененных клеток крови.
Высококвалифицированные специалисты Онкоцентра «Лапино-2» проводят любое противораковое лечение, включая таргетное – без очередей, задержек и потерь времени.
Как принимают таргетную терапию?
На сегодняшний день существует несколько форм, в которых выпускаются подобные препараты. Их можно принимать внутрь, как обычные таблетки, капсулы или сиропы, либо внутривенно.
Лекарства доставляют в организм через обычный катетер – тонкую мягкую пластиковую трубку в кровеносном сосуде, или центральный венозный, так называемый порт – устанавливаемое под кожу устройство. Они вводятся специалистом за несколько минут или часов.
Оральная таргетная терапия обычно принимается по четкому графику дома. Каждый пациент получает четкие инструкции о том, сколько, когда и как это нужно делать. Дозы средства рассчитываются таким образом, чтобы в организме постоянно присутствовало необходимое количество данных веществ, уничтожающих раковые клетки.
Любой малейший сбой или отклонение от схемы может повлиять на эффективность лечения.
О каждом пропуске или задержке в приеме препарата нужно сообщить врачу, который решит, как действовать в данной ситуации.
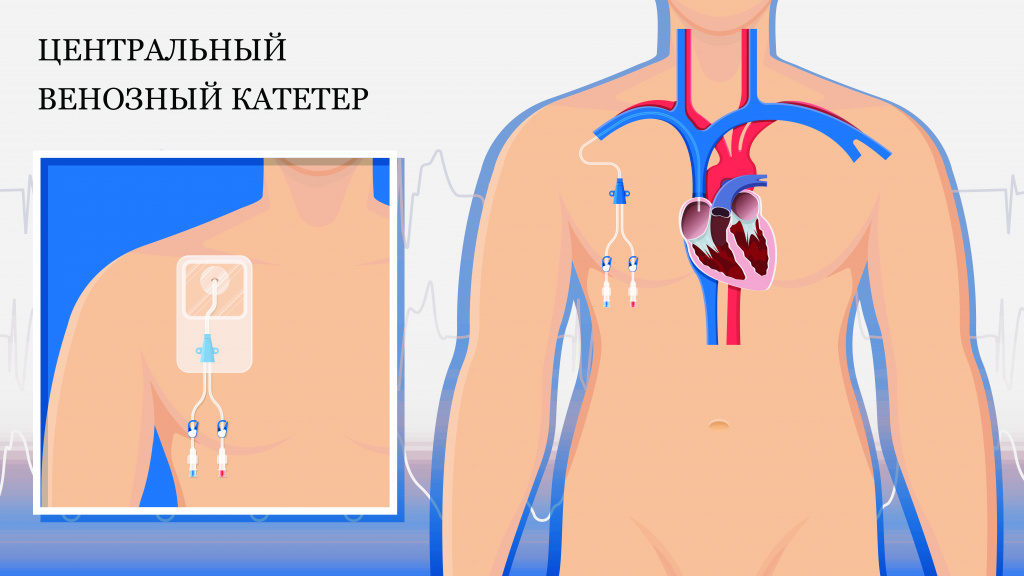
Порты для таргетной и химиотерапии
Центральный венозный катетер, или порт – удобное решение для онкобольных, которым нужно регулярно получать внутривенное лечение и сдавать кровь. С течением времени состояние их сосудов ухудшается из-за постоянных проколов, а попытки введения препаратов превращаются в пытку как для пациентов, так и для медицинского персонала.
Практически незаметное устройство, обычно устанавливаемое под кожу чуть ниже ключицы, эту проблему решает – его обладатели не испытывают проблем со сдачей анализов и доставкой в организм препаратов.
Преимуществ у портов много: они позволяют сократить количество уколов, избежать дискомфорта при проведении химио- или таргетной терапии, и уменьшить риски попадания препаратов на кожу, а значит и ее раздражения.
К их минусам можно отнести вероятность засорения катетера, появление в нем сгустков крови, его перекручивание либо смещение. Избежать неприятных последствий не сложно – достаточно строго следовать инструкциям по очистке, тщательно мыть руки, стараться избегать по нему ударов и не заниматься контактными видами спорта.
Побочные эффекты таргетной терапии
Несмотря на то, что таргетные препараты работают против раковых клеток и практически не повреждают здоровые, после их приема могут возникнуть побочные эффекты. Они встречаются не у всех пациентов и отличаются от «побочек» обычной химиотерапии, которая воздействует на все ткани тела.
Большая часть неприятных последствий проходит после окончания лечения, но поскольку многие вещества изобретены совсем недавно, долгосрочные последствия их приема еще изучены не полностью.
Проблемы с кожей
Самая распространенная из них – сыпь, обычно возникающая голове, лице, шее, груди и верхней части спины.
Чаще всего она начинается с покраснения и припухлостей на первых же неделях лечения, а примерно через месяц кожа покрывается корками, становится пересушенной и красной. У некоторых людей появляются круглые, плоские или выпуклые пятна или гнойные прыщи.
Сыпь вызывает зуд и жжение и нередко приводит к заметному изменению внешности, но обычно полностью проходит примерно через месяц после отмены таргетных препаратов.
Сухость, приводящая к ломкости, зуду, шелушению и даже трещинам – еще одна распространенная проблема, которая возникает практически у всех пациентов, получающих лечение на протяжении полугода.
Некоторые вещества могут вызвать покраснение и болезненность кутикулы, а также появление вокруг ногтей на руках и ногах отечных красных язв, которые нередко инфицируются.
Ладонно-подошвенный синдром – поражение кожи на ладонях и подошвах стоп, связан со многими препаратами для лечения рака, включая химио- и некоторые виды таргетной терапии. Его причина до сих пор точно не известна – возможно, все дело в повреждении крошечных кровеносных сосудов в конечностях или окружающих их тканей. Обычно он развивается в течение первых 2-6 недель лечения, а его первыми симптомами становятся повышенная чувствительность, покалывание или онемение. Затем пострадавшие области опухают, краснеют, как при солнечном ожоге, шелушатся, трескаются и покрываются волдырями.
Применение некоторых средств может привести к ухудшению качества волос – их сухости, ломкости, истончению и появлению залысин.
У части пациентов кожа или волосы темнеют или приобретают желтоватый оттенок.
Кроме того, возможно пересыхание, покраснение и ощущение жжения в области век и глаз.
При появлении сыпи или любых других проблем с кожей необходимо сразу же сообщить об этом врачу-онкологу, поскольку при отсутствии правильного лечения у пациента могут развиться инфекции, требующие отсрочки или даже прекращения терапии.
Другие побочные эффекты целевого лечения похожи на последствия стандартной «химии». К ним относят тошноту и рвоту, диарею или запоры, образование язв во рту, одышку – ощущение нехватки воздуха, кашель, усталость, головную боль, выпадение волос, повреждение печени, почек и щитовидной железы, а также аллергические реакции.
Таргетная терапия различных видов рака
Данные препараты подходят не для всех пациентов – они помогают только в том случае, если в раковых клетках человека присутствуют определенные изменения. Перед назначением лечения врачи проводят биопсию – изымают небольшую частичку новообразования и передают ее в лабораторию, где она тщательно исследуется. Если специалистам удается найти особенности опухоли, для которых уже созданы лекарства, их применяют – часто одновременно с химиотерапией или другими видами вмешательства.
Таргетная терапия рака гортани
Для лечения некоторых запущенных форм онкологии горла и гортани используется Цетуксимаб (Эрбитукс), блокирующий EGFR – белок, который помогает опухолевым клеткам быстро расти. Его можно комбинировать с лучевой или химиотерапией.
Таргетная терапия рака желчных протоков
На сегодняшний день при данном типе онкологии используется 2 типа препаратов:
Таргетная терапия немелкоклеточного рака легкого
Для пациентов с немелкоклеточной онкологией легких создано множество таргетных препаратов:
Таргетная терапия рака молочной железы
Примерно у 1 из 5 женщин с раком груди опухолевые клетки содержат на своей поверхности слишком много стимулирующего их рост белка – HER2. Эти HER2-положительные новообразования быстро развиваются и распространяются по организму. Для их лечения применяются:
Примерно 2 из 3 случаев рака молочной железы чувствительны к гормонам – веществам, которые создаются нашими железами, через кровоток попадают в органы и сообщают им, как действовать – работать или отдыхать, выделять что-то или поглощать. В таких ситуациях применяется гормональная терапия:
Олапариб (Линпарза) и Талазопариб (Талценна): блокируют белки PARP, необходимые для восстановления поврежденной ДНК, что часто приводит к гибели раковых клеток.
Сацитузумаб говитекан: моноклональное антитело, присоединенное к химиотерапевтическому препарату. Лекарство работает в случае избытка в опухоли белка Trop-2, помогающего ей быстро расти и распространяться по организму.
Таргетная терапия рака печени
Для пациентов с раком печени есть несколько типов таргетных препаратов:
Таргетная терапия рака пищевода
При лечении рака пищевода используется несколько типов таргетных препаратов.
Некоторые типы опухолей содержат слишком много белка HER2, который способствует быстрому росту онкологических клеток. Такие заболевания называются HER2-положительными. Против них можно применять:
Таргетная терапия рака поджелудочной железы
Для лечения онкологии поджелудочной железы используются:
Таргетная терапия рака почки
Врачи применяют 2 типа таргетных препаратов для лечения рака почки. Их назначают пациентам с запущенным заболеванием для снижения скорости разрастания опухоли или уменьшения ее размеров.
Таргетная терапия рака предстательной железы
При лечении онкологии простаты используются Рукабариб (Рубрака) и Олапариб (Линпарза) – так называемые ингибиторы PARP. Данные лекарства не позволяют восстанавливаться поврежденной ДНК в клетках новообразований, что приводит к их гибели.
Таргетная терапия саркомы матки
Пазопаниб (Вотриент): назначается при лейомиосаркоме – опасной для жизни опухоли гладкой мускулатуры матки, которая распространилась по организму или вернулась после проведенного лечения.
Таргетная терапия рака щитовидной железы
В случае папиллярного или фолликулярного рака щитовидной железы применяют 3 типа препаратов:
При медуллярном раке используются:
При анапластических новообразованиях применяются:
Таргетная терапия рака яичников
Пациенткам с онкологией яичников могут назначаться:
В Онкоцентре «Лапино-2» проводится не только инновационная таргетная терапия, но и любое другое противоопухолевое лечение всех типов онкологии самыми современными препаратами.
Таргетная терапия: принцип действия, показания и возможные осложнения
Что такое таргетная терапия?
Таргетная терапия – это новый современный вид лечения, который направлен на борьбу с опухолевыми клетками. Название методики произошло от английского слова «target», обозначающего «цель» или «мишень». Отличие этого вида лечения от химиотерапии состоит в том, что таргетные препараты действуют направленно на молекулы, участвующие в канцерогенезе, то есть, в процессе образования опухоли. А химиотерапия действует на все активно делящиеся клетки – и на опухолевые, и на нормальные. Поэтому при таргетной терапии здоровые ткани не повреждаются, что позволяет минимизировать побочные действия противоопухолевого лечения.
Первые таргетные препараты были разработаны в 80–90-х годах 20 века. Это антистероидные препараты: антиэстрогены и антиандрогены, то есть это гормональная терапия. Определить принадлежность таргетных препаратов можно по их названию: моноклональные антитела имеют окончание МАБ, малые молекулы ингибиторы киназ – ИБ.
Что такое моноклональные антитела?
Моноклональные антитела – это крупные белковые молекулы натурального происхождения. Они действуют на поверхности клеток, блокируя рецепторы к факторам роста. К ним относятся: трастузумаб, пертузумаб, цетуксимаб, панитумумаб, афлиберцепт, ритуксимаб. Это международные запатентованные названия препаратов. Они могут иметь торговые названия, которые присваиваются производителями, но если внимательно изучить упаковку, то можно найти их международные названия.
Что такое малые молекулы?
Малые молекулы – это полностью синтезированные химические вещества. Они способны проникать внутрь клетки и воздействовать на различные мишени, тем самым блокируя деление клетки. К ним относятся: афатиниб, иматиниб, гефитиниб, эрлотиниб, сунитиниб, лапатиниб, сорафениб, темсиролимус, эверолимус, пазопаниб, кризотиниб, дабрафениб.
Как применяется таргетная терапия?
Таргетная терапия может использоваться как самостоятельный метод лечения и в комбинации с химиотерапией, гормональной терапией или иммунной терапией. Моноклональные тела вводятся внутривенно один раз в 2–3 недели. Малые молекулы принимаются в виде таблетированных препаратов ежедневно. Прием таргетных препаратов может быть продолжительным – пока терапия действует, и нет прогрессирования заболевания.
Какие преимущества у таргетной терапии?
Достоинствами таргетной терапии являются:
Какие недостатки у таргетной терапии?
Процесс создания препаратов на основе моноклональных антител сложный и дорогостоящий. Предполагалось, что такой молекулярно нацеленный механизм действия поможет уменьшить сопутствующую побочную патологию. Однако достигнуть этого результата при помощи таргетной терапии удалось не полностью. Оказалось, что мишени, которые блокируются в опухолевых клетках, имеют и свое физиологическое назначение в нормальных клетках. Поэтому при их блокировке возникают побочные действия, которые ранее не были известны при проведении химиотерапии.
Зачем определять мутации генов при назначении тергетных препаратов?
Все изменения в опухолевых клетках, так или иначе, связаны с мутацией определенных генов. Сегодня изучено более десятка таких мутаций, что позволило разработать таргетные препараты, снижающие влияние этих факторов. При этом таргетная терапия должна быть подобрана, исходя из имеющейся у пациента той или иной мутации гена. Ведь при одном и том же заболевании возможен разный набор мутаций и потребуется назначение разных препаратов.
Чтобы таргетная терапия попала в цель – должна быть установлена мишень, поэтому для определения возможностей таргетной терапии назначается выполнение молекулярно-генетического или иммуногистохимического анализа. Задача этих исследований – выявление наиболее частых мутаций, которые могут послужить мишенью для таргетных препаратов. Если такие мутации обнаружены, то назначается таргетная терапия. Если никаких мутаций не выявлено, то будет назначаться другой вид противоопухолевого лечения. В некоторых случаях необходимо сочетать несколько видов противоопухолевого лечения.
Таргетная терапия при раке молочной железы
Для назначения гормональной терапии пациентам со злокачественными новообразованиями молочной железы рекомендуется выполнение иммуногистохимического исследования для определения рецепторов эстрогенов и прогестеронов. Определение экспрессии HER2 и введение препаратов трастузумаб, пертузумаб, лапатиниб. Также пациентам с заболеванием молочной железы рекомендуется проведение анализа крови на BRCA мутацию, для решения вопроса о назначении терапии препаратом олапариб. В зависимости от биологического вида опухоли лечение может быть разным.
Таргетная терапия при раке легкого
При раке легкого пациентам рекомендуется проведение молекулярно-генетического исследования для определения мутаций:
Назначение бевацизумаба и пембролизумаба не требует определение каких-либо мутаций. Бевацизумаб может назначаться пациентам только с аденокарциномой легкого, пембролизумаб только при неплоскоклеточном, немелкоклеточном раке легкого без активирующих мутаций.
Таргетная терапия при колоректальном раке
При опухолях кишечника необходимо выполнение молекулярно-генетического исследования для определения мутаций KRAS, NRAS, BRAF. В зависимости от наличия или отсутствия этих мутаций рекомендуется назначение препаратов цетуксимаб, панитумумаб, бевацизумаб и афлиберцепт. Выявление мутации BRAF дает возможность назначить дабрафениб и траметиниб.
Для назначения препаратов регорафениб и рамуцирумаб выявление мутаций не требуется. Однако они показаны только во второй и последующих линиях лечения. Также пациентам с заболеванием кишечника рекомендуется выполнение иммуногистохимического исследования для выявления микросателлитной нестабильности, которая позволяет назначить терапию препаратом пембролизумаб.
Таргетная терапия при опухолях головы и шеи
При опухолях головы и шеи возможно назначение такого препарата как цетуксимаб. В отличие от опухолей кишечника в данной ситуации пациентам не требуются исследования для выявления каких-либо мутаций. И этот препарат может назначаться одновременно с проведением лучевой терапии.
Таргетная терапия при раке яичника
Пациентам с заболеваниями яичников, особенно с рецидивирующими, назначается терапия препаратом бевацизумаб в комбинации с химиотерапией. Также возможно назначение в самостоятельном, поддерживающем режиме, независимо от каких-либо мутаций. Новым препаратом для лечения опухолей яичников является олапариб. Для его назначения необходимо выполнить анализ крови на BRCA мутацию.
Таргетная терапия при меланоме
При меланоме рекомендовано назначение молекулярно-генетического исследования на определение мутации BRAF V600E и назначение препаратов дабрафениб и вемурафениб. Ипилимумаб назначается во второй и последующих линиях терапии независимо от мутации BRAF.
Таргетная терапия при раке почки
Опухоли почки – это особенное заболевание, поскольку при его лечении используются только таргетные препараты. И проведение анализа на определение каких-либо мутаций не требуется. Всем пациентам с заболеванием почки возможно назначение таргетных препаратов.
Какие осложнения возможны при применении таргетной терапии?
Таргетные препараты работают более эффективно, чем химиотерапия. Но они все-таки могут влиять на работу нормальных клеток и, соответственно, вызывать побочные действия. Поэтому терапия таргетными препаратами должна проводиться под контролем врача-онколога.
Со стороны сердечнососудистой системы могут наблюдаться: повышение артериального давления, аритмия, тромбозы, инфаркт миокарда, миокардиты, периокардиты, кардимиопатия и сердечная недостаточность.
Со стороны дыхательной системы возможно появление инфильтратов в легких, интерстицального пневмонита, облитерирующего бронхиолита. В условиях нынешней эпидемиологической обстановки важно отличать осложнения таргетной терапии от возможных вирусных поражений легких.
Со стороны мочевыделительной системы возможно появление протеинурии, нефротического синдрома и почечной недостаточности.
Со стороны желудочно-кишечного тракта возможны диарея и перфорация кишечника.
Со стороны кожи частым побочным явлением становится сыпь.
Можно ли проводить таргетную терапии пожилым людям?
Пожилые люди часто подвергаются дискриминации в связи с возрастом. Многие исследования показали, что таргетная терапия показана данной группе пациентов, поскольку этот вид лечения менее токсичен, чем химиотерапия. Но необходимо учитывать сопутствующую патологию пациентов, поскольку ингибиторы антиогенеза могут вызвать тромбоз и гипертонию. Ингибиторы тирозинкиназы обладают более высокой частотой сердечной недостаточности, поэтому пациентам пожилого возраста необходим строгий мониторинг осложнений.
Но у пациентов пожилого возраста некоторые таргетные препараты имеют свои особенности. Например, афлиберцепт у пациентов старше 65 лет вызывает риск развития диареи, головокружений, астении, снижения массы тела и дегидратации. Гефитиниб у пациентов старше 55 лет повышает риск развития интерстициального поражения легких. У других таргетных препаратов не было выявлено никаких особенностей при применении у пациентов пожилого возраста.
Таким образом, можно сделать вывод, что таргетная терапия – это современный вид противоопухолевого лечения, который показан при разных локализациях опухолевого процесса, но для его назначения необходимо определение специальных рецепторов. Данный вид терапии позволяет добиться лучших результатов лечения и при этом снизить токсичность действия на весь организм в целом, тем самым улучшить качество жизни пациентов.
Список литературы: