Что означает формула hgo
Оксид ртути(II)
| Оксид ртути(II) | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Оксид ртути(II) |
| Химическая формула | HgO |
| Физические свойства | |
| Состояние (ст. усл.) | твёрдые кристаллы оранжевого/красного цвета |
| Отн. молек. масса | 216.5 а. е. м. |
| Молярная масса | 216.59 г/моль г/моль |
| Плотность | около 10 г/см³ |
| Термические свойства | |
| Температура разложения | 500 °C |
| Химические свойства | |
| Растворимость в воде | нерастворим г/100 мл |
| Классификация | |
| Рег. номер CAS | [21908-53-2] |
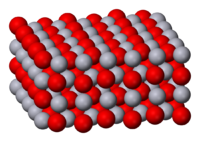
Оксид ртути(II) — бинарное соединение ртути и кислорода с формулой HgO. Это твёрдое непрочное при нормальных условиях вещество красного или оранжевого цвета является основным и важнейшим оксидом ртути и практически не встречается в природе, за исключением редкого минерала монтроидита.
Содержание
История
В 1774 году с помощью оксида ртути (II) Джозеф Пристли открыл новый химический элемент — кислород.
Получение
Красный оксид ртути получают нагреванием ртути до 350 °C или пиролизом нитрата ртути.

Жёлтый оксид получают осаждением солей ртути(II) щелочами, например:
Разница в цвете объясняется размером частиц, обе формы имеют одинаковую структуру — цепь линейных звеньев состава O-Hg-O соединённых под углом 108°. Размеры частиц жёлтого оксида ртути составляют до 4 мкм, красной — более 8 мкм.
Свойства
Жёлтый HgO является более химически активным, разлагается при температуре 332 o C, при нагревании краснеет. Красный HgO распадается при 500, а при нагревании обратимо меняет свой цвет на чёрный.
Растворяется в концентрированных растворах щелочей, при этом образуются гидроксокомплексы. Жёлтый HgO взаимодействует с NH3 с образованием основания Миллона:
Применяется для получения ртути, а также в некоторых видах гальванических элементов.
Обладает сильным токсическим действием.
Красная ртуть и HgO
В 90-е годы оксид ртути нередко выдавался за несуществующую красную ртуть, так как он действительно красного, скорее ярко-рыжего цвета и содержит ртуть. Во времена «краснортутной лихорадки» фиксировалось немало случаев хищения и продажи этого вещества под видом «красной ртути».
Оксид ртути II
| Оксид ртути II | |
|---|---|
 | |
| Систематическое наименование | Оксид ртути II |
| Хим. формула | HgO |
| Состояние | твёрдые кристаллы оранжевого/красного цвета |
| Молярная масса | 216.59 г/моль г/моль |
| Плотность | около 10 г/см³ |
| Температура | |
| • разложения | 500 °C |
| Энтальпия | |
| • образования | 90,458 кДж/моль |
| Растворимость | |
| • в воде | нерастворим |
| Рег. номер CAS | [21908-53-2] |
| PubChem | 30856 |
| Рег. номер EINECS | 244-654-7 |
| SMILES | |
| RTECS | OW8750000 |
| ChEBI | 81882 |
| Номер ООН | 1641 |
| Предельная концентрация | 0.0003 мг/м3 (в пересчёте на Hg) |
| ЛД50 | 18 мг/кг |
| Пиктограммы ECB |  |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
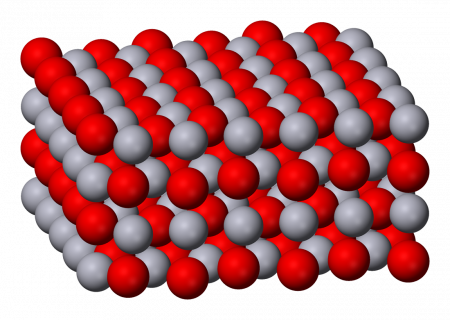
Оксид ртути II — бинарное соединение ртути и кислорода с формулой HgO. Это твёрдое непрочное при нормальных условиях вещество в зависимости от дисперсности красного или оранжевого (жёлтого) цвета является основным и важнейшим оксидом ртути и практически не встречается в природе, за исключением редкого минерала монтроидита. Очень ядовит.
Содержание
История
В 1774 году с помощью оксида ртути II Джозеф Пристли открыл новый химический элемент — кислород.
Получение
Красный оксид ртути получают нагреванием ртути до 300 °C или пиролизом нитрата ртути.
Жёлтый оксид получают осаждением солей ртути II щелочами, например:
HgS + 2 NaOH → HgO ↓ + Na2S + H2O
Разница в цвете объясняется размером частиц, обе формы имеют одинаковую структуру — цепь линейных звеньев состава O-Hg-O соединённых под углом 108°. Размеры частиц жёлтого оксида ртути составляют до 4 мкм, красной — более 8 мкм.
Свойства
Жёлтый HgO является более химически активным, разлагается при температуре 332 o C, при нагревании краснеет. Красный HgO распадается при 500, а при нагревании обратимо меняет свой цвет на чёрный.
Растворяется в концентрированных растворах щелочей, при этом образуются гидроксокомплексы. Жёлтый HgO взаимодействует с NH3 с образованием основания Миллона:
Применяется для получения ртути, а также в некоторых видах гальванических элементов.
Обладает сильным токсическим действием.
Токсикология
Красная ртуть и HgO
В 90-е годы оксид ртути нередко выдавался за несуществующую красную ртуть, так как он действительно красного, скорее ярко-рыжего цвета и содержит ртуть. Во времена «краснортутной лихорадки» фиксировалось немало случаев хищения и продажи этого вещества под видом «красной ртути».
Оксид ртути (II) красная модификация
Товар находится в неверной категории?
Нажмите на ссылку и мы подберем для товара правильную категорию.
Оксид ртути(II) — бинарное соединение ртути и кислорода с формулой HgO. Это твёрдое непрочное при нормальных условиях вещество в зависимости от дисперсности красного или оранжевого (жёлтого) цвета является основным и важнейшим оксидом ртути и практически не встречается в природе, за исключением редкого минерала монтроидита.
Получение
Красный оксид ртути получают нагреванием ртути до 300 °C или пиролизом нитрата ртути.
Жёлтый оксид получают осаждением солей ртути(II) щелочами, например:
Разница в цвете объясняется размером частиц, обе формы имеют одинаковую структуру — цепь линейных звеньев состава O-Hg-O соединённых под углом 108°. Размеры частиц жёлтого оксида ртути составляют до 4 мкм, красной — более 8 мкм.
Свойства
Жёлтый HgO является более химически активным, разлагается при температуре 332 o C, при нагревании краснеет. Красный HgO распадается при 500, а при нагревании обратимо меняет свой цвет на чёрный.
Растворяется в концентрированных растворах щелочей, при этом образуются гидроксокомплексы. Жёлтый HgO взаимодействует с NH3 с образованием основания Миллона:
Применяется для получения ртути, а также в некоторых видах гальванических элементов.
Обладает сильным токсическим действием.
Красная ртуть и HgO
В 90-е годы оксид ртути нередко выдавался за несуществующую красную ртуть, так как он действительно красного, скорее ярко-рыжего цвета и содержитртуть. Во времена «краснортутной лихорадки» фиксировалось немало случаев хищения и продажи этого вещества под видом «красной ртути».
Общие Физические свойства Термические свойства Химические свойства Классификация

















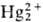 + 2Н2О (+1,065 В)
+ 2Н2О (+1,065 В)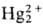 + 4Н2О (+1,279 В)
+ 4Н2О (+1,279 В)