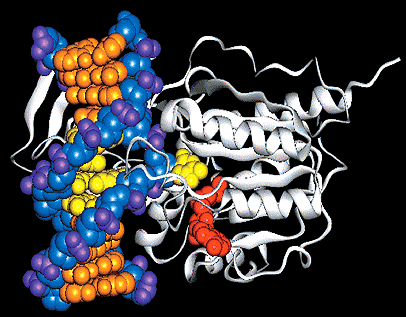Что относится к эпигенетическим структурам метильные группы
Старение и долголетие: эпигеном раскрывает тайны
Старение и долголетие: эпигеном раскрывает тайны
Детальное изучение эпигенома дает биологам возможность выбраться из тумана многочисленных теорий старения и более точно понять коренные причины этого явления, а также связанных с ним возрастных болезней.
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Эпигенетика — относительно недавно возникшая область науки. Предметом ее изучения являются устойчиво сохраняющиеся в ряду клеточных делений изменения активности генов, не связанные с изменением самой ДНК. Иными словами, за счет эпигенетических модификаций одни гены работают, а другие — молчат. Еще тридцать лет назад в научном сообществе многие из-за укоренившихся догм не хотели признавать важность эпигенетических процессов в биологическом мире. Сейчас к этой области знания приковано внимание множества лабораторий и институтов по всему миру, занимающихся в том числе и изучением природы старения. В геронтологии получило мощное развитие новое направление, связанное с описанием эпигенетических механизмов возрастных изменений.
Конкурс «био/мол/текст»-2015
Эта работа опубликована в номинации «Лучшая статья о механизмах старения и долголетия» конкурса «био/мол/текст»-2015.
Спонсором номинации «Лучшая статья о механизмах старения и долголетия» является фонд «Наука за продление жизни». Спонсором приза зрительских симпатий выступила фирма Helicon.
Спонсоры конкурса: лаборатория биотехнологических исследований 3D Bioprinting Solutions и студия научной графики, анимации и моделирования Visual Science.
Эпигенетика начинает поиск
Метилирование представляет собой способ регулирования активности генов путем присоединения к цитозиновым основаниям ДНК метильной группы (-СН3). Метилирование подавляет активность гена: синтез РНК (соответственно, и белка) по такой матрице становится невозможным. Это своего рода «заглушка», которую организм использует, инактивируя те или иные гены, работа которых в данный момент ему не нужна или может представлять опасность.
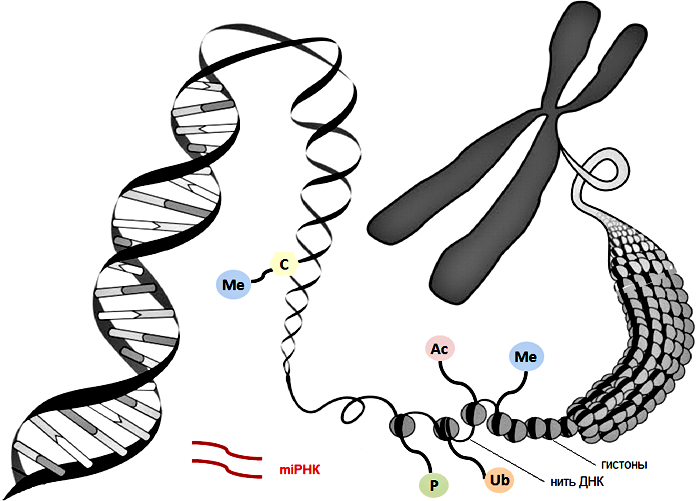
Еще одним важным механизмом эпигенетической регуляции является модификация гистонов, входящих в состав хроматина. Хроматин — это комплекс белков и нуклеотидов, обеспечивающий надежное хранение и нормальную работу ДНК. В наших клетках упаковка ДНК похожа на склад бижутерии. Иначе никак невозможно уложить спираль длиной два метра в одно маленькое клеточное ядро. Нить ДНК наматывается в полтора оборота на многочисленные «бусинки» из нескольких специальных белков, гистонов. Так формируются повторяющиеся структурные единицы эукариотического хроматина, называемые нуклеосомами. В каждой нуклеосоме содержится восемь молекул гистонов — по две молекулы каждого из четырех видов белков (H2A, H2B, H3, H4). Гистоны имеют «хвостики» — белковые «наросты», которые могут удлиняться или укорачиваться специальными ферментами. Длина такого «хвоста» напрямую влияет на активность генов, находящихся вблизи него.
Гистоновый «хвост» может подвергнуться процессу ацетилирования, то есть замене в нём атомов водорода на остаток уксусной кислоты. В результате этого связь гистонов с ДНК, основанная на притяжении разнозаряженных частиц, ослабится, гистон диссоциирует (отдалится от ДНК), и упаковка ДНК станет более «рыхлой» (менее плотной). Тогда белки-регуляторы смогут легче присоединяться к ДНК, и активность гена повысится. Эпигенетические процессы взаимосвязаны друг с другом: так, увеличение уровня метилирования ДНК обычно сопряжено со снижением уровня ацетилирования гистонов, и наоборот. Помимо ацетилирования существует множество других способов модификаций гистонов: метилирование, фосфорилирование, сумоилирование и так далее. Эти модификации могут как разрыхлять, так и «заматывать крепче» упаковку ДНК, что приводит к увеличению или уменьшению экспрессии генов соответственно.
Важные научные открытия, связанные с эпигенетикой, появляются практически ежегодно. И хотя ученые находятся в самом начале пути, полученные данные показывают исключительную ценность этого научного направления. Получив мировое признание, эпигенетика вскоре перешла из чисто научной области исследований в очень прикладную, когда выявилась ее тесная связь с развитием и старением. Не случайно одна из недавних статей в Nature вышла под названием «Эпигеномика начинает поиск» [7]. И этот поиск уже дает свои результаты.
Рисунок 1. Структура хроматина и эпигенетические механизмы воздействия на геном. Модификации гистонов: Ас, ацетилирование; Me, метилирование; Ub, убиквитинирование; P, фосфорилирование. Метилирование цитозина ДНК — Me
C. РНК-интерференция: miРНК, малые некодирующие РНК.
Метилирование и его связь со старением
В научных трудах по геронтологии часто встречается описание онтогенеза (индивидуального развития организма) лососевых рыб. И, как уже известно, молниеносно развивающееся сразу после нереста старение рыб этого вида сопровождается массивным деметилированием ДНК [8]. Установлено, что с возрастом происходит общее снижение уровня метилирования ДНК. В ДНК, которую брали у эмбрионов и новорождённых, присутствует наибольшее количество метилированных цитозиновых оснований. Получается, что некоторые гены, которые были «заглушены» и молчали в детском и молодом возрасте, к старости начинают проявлять активность. Другая, меньшая часть генов, напротив, с возрастом «замолкает», подвергшись метилированию. Последствия таких изменений генной активности сегодня еще не до конца изучены, но некоторые аспекты уже известны.
Насколько большим может быть влияние эпигенетики на продолжительность жизни, показали в своих работах ученые из Австралийского национального университета, Роберт Кухарски и его коллеги. В 2008 году Science опубликовал результаты их исследований о влиянии фермента ДНК-метилтрансферазы-3 (DNMT-3) на продолжительность пчелиной жизни [13]. Долгое время оставалось загадкой, каким образом из генетически совершенно одинаковых личинок появляются две разные касты пчел — рабочие и королевы (или матки).
Рисунок 2. Комплекс ДНК-метилтрансферазы с ДНК.
Если рабочие пчелы живут всего несколько недель, то матки — несколько лет. Такая огромная разница в длине жизненного пути генетически одинаковых организмов является следствием особого питания: тех личинок, которым суждено стать королевами, дольше кормят маточным молочком. Молекулярные механизмы этого явления стали понятны, когда Р. Кухарски и его команда искусственно уменьшили количество фермента DNMT-3 у личинок пчел. Этот фермент прикрепляет метильные группы к ДНК (рис. 2), подавляя экспрессию генов. Без DNMT-3 активность некоторых генов у личинок оказалась повышенной, и в итоге большинство из них превратилось в королев даже без кормления маточным молочком. Расшифровка пчелиного эпигенома подтвердила это предположение: в ДНК пчеломаток было найдено значительно меньше метильных групп, чем у рабочих пчел. Несколькими годами позже группа Р. Кухарски, проводя исследование уровня метилирования цитозина в нервной системе рабочих пчел и пчеломаток, нашла 561 ген со значительными различиями в метилировании между двумя пчелиными группами [14].
Конечно, не только особенности эпигенома влияют на срок жизни пчеломатки. Как сегодня известно, долгожительницу из королевы делает совокупность факторов: это и нужное соотношение полиненасыщенных и насыщенных жирных кислот, и уменьшенное содержание цитохрома с (который способен запускать процесс клеточной гибели, апоптоз), и повышенная антиоксидантная активность [15].
Как выяснилось, влияние эпигенома на продолжительность жизни чрезвычайно велико и у людей. Так, в 2013 году большая группа итальянских генетиков, возглавляемая Джованни Витале, опубликовала результаты работы, в ходе которой изучались возрастные изменения метилирования ДНК [16]. Объектами исследования стали две группы женщин-ровесниц, жительниц Северной Италии. В одной группе были собраны пожилые итальянки, имевшие матерей-долгожительниц и отцов, проживших не менее 77 лет. К другой группе отнесли итальянок, родители которых умерли, прожив около 70 лет (отцы — 67 лет, матери — 72 года). Распределив таким образом исследуемых, ученые поставили себе задачу сравнить, какие изменения на генном уровне могут лежать в основе долголетия. А также выяснить, существует ли явная преемственность в этом вопросе — передаются ли факторы долгожительства по наследству?
Результаты их работы превзошли все ожидания и показали следующее.
Снижение метилирования ДНК (гипометилирование), характерное для пожилого возраста, происходило гораздо быстрее у итальянок, чьи родители не дожили до 70 лет, чем у их сверстниц, имевших родителей-долгожителей. Исследователи обнаружили, что метилирование (а значит, и блокирование) элемента Alu было значительно выше у потомков долгожителей. Даже в старости люди, получившие в наследство от родителей хорошее здоровье, мало чем отличались на молекулярно-генетическом уровне от молодых людей. И такие потенциально опасные элементы генома, как ретротранспозоны, были у них надежно блокированы. Можно с большой долей уверенности говорить, что хорошее здоровье (как, впрочем, и плохое) передается по наследству.
Понимание природы эпигенетики показало, что родители ответственны за здоровье своих детей гораздо в большей степени, чем это считалось ранее. Совсем недавно было показано, что такая привычная сегодня вещь, как лишний вес будущих родителей, может самым негативным образом сказаться на их потомстве. Известный американский генетик Рэнди Джиртл и его коллеги из Университета Дьюка провели исследования ДНК лейкоцитов из пуповинной крови младенцев, родившихся в госпитале при их университете. По словам ученых, анализ зафиксировал существенное снижение уровня метилирования гена инсулиноподобного фактора роста 2 (IGF 2) у тех детей, чьи родители имели лишний вес: «Мы обнаружили у новорождённых, отцы которых страдали ожирением, значительное снижение метилирования IGF2 в ДНК, извлеченной из лейкоцитов пуповинной крови. Понижение уровня метилирования IGF2 связано с повышенным риском развития раковых заболеваний» [17].
Возрастные отклонения и эпигеном
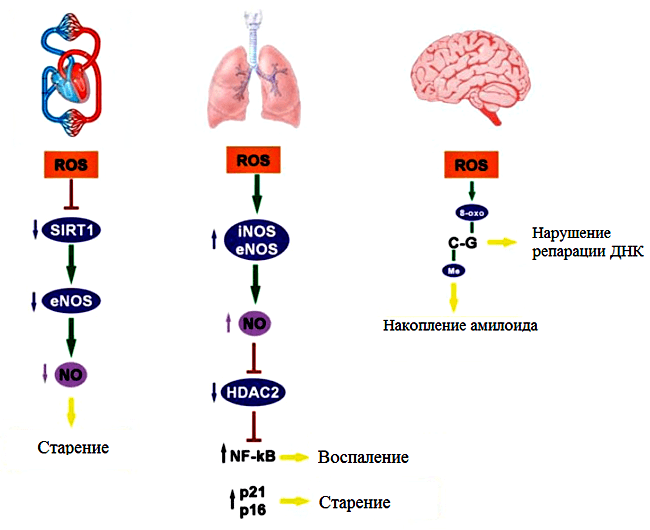
Еще в 1994 году Зигмунд Вейцман и его коллеги из Северо-Западного университета (Чикаго) обнаружили, что окисление свободными радикалами гуанина, обязательного «напарника» цитозина в двухцепочечной ДНК, влияет на метилирование. Окисленный продукт гуанина, 8-гидроксигуанин (8-OHdG), известный маркер окислительного повреждения ДНК, не только увеличивал частоту мутаций, но и препятствовал нормальному метилированию цитозина [21]. Оказалось, что эпигеном тесным образом связан с регулированием уровня АФК: общее возрастное уменьшение метилирования ДНК развивается параллельно с повышением уровня АФК и окислительным стрессом. И эти процессы связаны между собой. Так, возрастной окислительный стресс, вызванный повышенной продукцией АФК, достоверно снижает количество уже упоминавшихся сиртуинов, к которым сегодня приковано пристальное внимание геронтологов. Сиртуины представляют собой семейство консервативных (то есть встречающихся у всех живых организмов) белков, выполняющих одну из эпигенетических функций — деацетилирование гистонов. Многочисленные эксперименты показали благотворную роль сиртуинов в поддержании здоровья и увеличении продолжительности жизни. АФК же снижают уровень этих белков, сокращая тем самым срок жизни.
Если взять наугад любую патологию из длинного списка возрастных болезней (таких, как атеросклероз, болезнь Паркинсона, диабет или ревматоидный артрит), то совершенно точно обнаружится непосредственное участие эпигенома в их развитии. Этот вопрос сегодня хорошо изучен и уже ни у кого не вызывает сомнений. К примеру, у больных атеросклерозом обнаруживается повышенный уровень токсичного для артерий гомоцистеина. И причина этого — сбой в работе сложного биохимического процесса под названием фолатный цикл, который тесно связан с метилированием ДНК и эпигеномом.
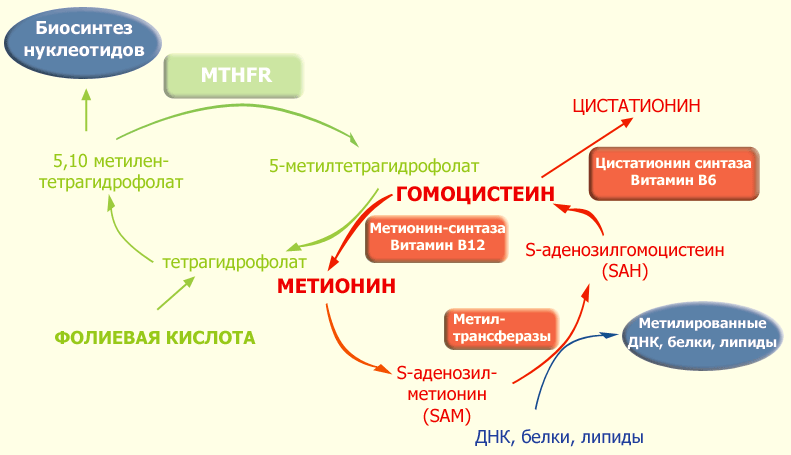
Фолатный цикл представляет собой каскад биохимических реакций, в котором задействовано большое количество ферментов (рис. 4). Для нормального протекания фолатного цикла необходимы витамины B9 (фолиевая кислота), В6 и В12. В этом цикле происходит перенос метильных групп, которые присоединяются к гомоцистеину, а избыток гомоцистеина превращается в метионин. Метионин переходит в свою активную форму, S-аденозилметионин (SАМ), который в клетке служит основным донором метильных групп, необходимых для синтеза и метилирования ДНК, РНК, белков и фосфолипидов [22].
Рисунок 4. Схема фолатного цикла. В реакции, катализируемой ферментом MTHFR, из тетрагидрофолата и серина образуется 5,10-метилентетрагидрофолат, который затем восстанавливается до 5-метилтетрагидрофолата. На следующем этапе метильная группа от 5-метилтетрагидрофолата переносится на гомоцистеин в реакции, катализируемой В12-зависимой метилтрансферазой. В результате реметилирования гомоцистеина образуется метионин. Данную реакцию катализирует цитоплазматический фермент метионинсинтаза (MTR). Для работы фермента необходим метилкобаламин, производное витамина В12. Метионинсинтаза обеспечивает преобразование гомоцистеина в метионин посредством реакции, в которой метилкобаламин выступает в роли промежуточного переносчика метильной группы. При этом происходит окисление кобаламина, и фермент MTR переходит в неактивное состояние
В фолатном цикле может произойти сбой по двум причинам: генетическим (из-за мутаций генов ферментов фолатного цикла) или алиментарным (из-за дефицита метионина, фолиевой кислоты и других витаминов группы В). Дефицит возникает, если в рационе недостает продуктов, богатых этими веществами, или если эти вещества плохо усваиваются — как правило, на фоне вредных привычек, приема лекарств, инфекций и др.
Нарушение фолатного цикла угрожает организму сразу тремя последствиями. Первое: низкий уровень одного из производных этого цикла, 5,10-метилентетрагидрофолата, приводит к разрывам в ДНК и нарушению процессов репарации [23]. Второе: возникает дефицит основного донора метильных групп, S-аденозилметионина (SAM), без которого невозможно производить метилирование ДНК. И третье последствие: нарушается метаболизм гомоцистеина, и его уровень в крови начинает расти. А далее токсичный для клеток гомоцистеин запускает цепную реакцию со множеством патологических ответвлений.
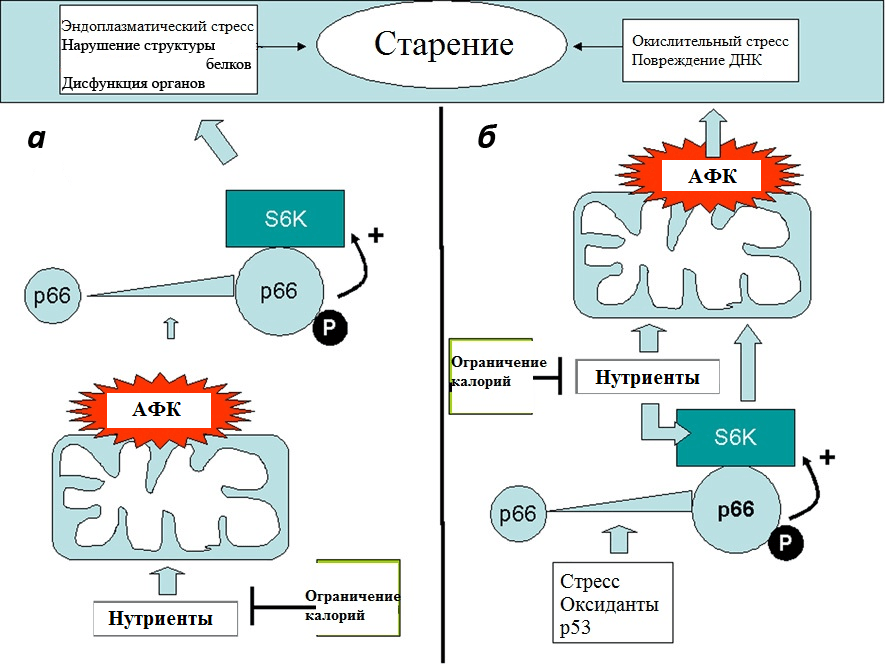
Итальянский исследователь Джовамбаттиста Пани связал возрастную активность p66 Shc и АФК с еще одним белком, вызывающим повышенный интерес у геронтологов, — mTOR (мишень рапамицина у млекопитающих), который регулирует в клетке процессы, связанные с развитием и клеточным ростом (рис. 5) [27]. По мнению одного из самых авторитетных исследователей mTOR, Михаила Благосклонного (Roswell Park Cancer Institute, США), этот белок занимает одно из центральных мест в процессах старения живых организмов, стимулируя развитие возрастных патологий, укорачивающих жизнь [28].
Рисунок 5. Две модели, показывающие, как p66 Shc может объединять АФК и mTOR/S6K-каскад в процессе старения. а — АФК активируют белок p66 Shc (или просто p66), который в свою очередь активирует рибосомную S6-киназу (S6K). АФК могут производиться в митохондриях в ответ на поступление питательных веществ (нутриентов), таким образом создавая альтернативный маршрут для детекции питательных веществ посредством S6K. б — Активированная p66 киназа S6K увеличивает образование АФК в митохондриях. В этом случае р66 может стимулироваться клеточным стрессом, белком р53 или экзогенными оксидантами. В обоих примерах воздействие р66 на старение тормозится ограничением калорий, что снижает поставку нутриентов. Активация p66 происходит в результате повышенной экспрессии (показана увеличенным значком) и фосфорилирования серина (буква «Р»). Оба изменения возникают в ответ на различные стрессы в клетках млекопитающих.
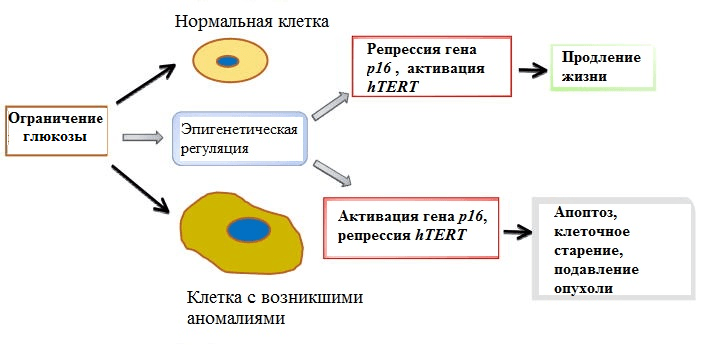
Сегодня большое внимание геронтологов приковано к механизмам благотворного воздействия на организм ограничения калорий. Как показали исследования, урезанный по калориям рацион может продлевать жизнь. Самый яркий и часто приводимый пример такого влияния — жители японского острова Окинава, которые при суточном рационе менее 2000 ккал уверенно держат первое место в мире по числу долгожителей. Суть этого феномена складывается из многих факторов, в том числе и из эпигенетических. Обнаружилось, что ограничение калорий меняет в позитивную сторону профиль метилирования ДНК: снижается метилирование генов — подавителей опухолевого роста, что ведет к их активации, и повышается метилирование онкогенов. Кроме этого, ограничение количества потребляемой глюкозы, которая дает немалую часть калорий, в эксперименте приводило к феномену расширения лимита Хейфлика — предела клеточного деления, лежащего в основе ограниченности срока жизни клетки (рис. 6). И опять это происходило вместе с изменениями эпигенома — изменениями в метилировании ДНК и модификациями гистонов, влияющими на активность ключевых генов — р16 и hTERT [30].
Рисунок 6. Влияние ограничения потребления глюкозы на продолжительность жизни. Ограничение поступления глюкозы может влиять на эпигенетическую регуляцию как в нормальных, так и в раковых клетках. В нормальных клетках это приводит к репрессии гена р16 и активации hTERT, что позволяет расширить лимит Хейфлика. Белок р16 замедляет процесс размножения клеток, ген hTERT кодирует фермент теломеразу, способный наращивать концевые участки ДНК, сокращающиеся при делении клеток, — теломеры. В предраковых клетках противоположные эффекты на p16 и hTERT приводят к апоптозу и гибели опасных клеток.
Эпигеном и теломеры
Еще один ассоциированный с возрастом процесс — укорочение теломер (повторяющихся последовательностей ДНК, стабилизирующих концевые участки хромосом, но уменьшающихся в длине при каждом клеточном делении) — также оказался тесно связанным с эпигеномом.
Очевидно, что гистоны хроматина играют очень важную роль в нормальной работе генома. И обнаруженное американскими исследователями возрастное снижение их синтеза, связанное с делением клетки и укорочением теломер, может приводить к дестабилизации генома. По предположению О`Салливана и его коллег, хронический стрессовый сигнал генерируется за счет сокращения теломер и приводит к снижению синтеза гистонов двух видов, H3 и H4. В свою очередь, это не позволяет точно восстановить ландшафт хроматина при следующем делении, и повреждение ДНК постепенно ограничивает жизнь клетки. Даже незначительные изменения в равновесии системы «ДНК — гистоны», по мнению ученых, могут нарушить синтез ДНК, архитектуру хроматина и жизнеспособность клеток.
Но, как оказалось, это не единственно возможная взаимосвязь теломер, старения и эпигенома. Не так давно проследили еще одну потенциальную связь. В.А. Галицкий и его коллеги из Института биохимии им. А.А. Палладина (Киев) описали возможность укорочения теломер на фоне возрастной геномной нестабильности. И вот как это может выглядеть.
По мнению украинских биохимиков, микроРНК в стволовых клетках поддерживают исходный профиль эпигенетических маркеров, что и лежит в основе уникальных качеств стволовых клеток (в первую очередь, их способности к долгой жизни). Но дифференцировка — превращение стволовых клеток в специализированные — требует репрессии генов некоторых микроРНК, чтобы те не мешали активности ряда нужных генов. В результате этого происходит возрастная потеря эпигенетических маркеров, снижается уровень метилирования ДНК. А это может приводить к дерепрессии «дремлющих» в ДНК ретротранспозонов и других мобильных элементов и, как следствие, к их перемещениям и повреждению ДНК. В ответ в клетке могут запуститься системы репарации ДНК, провоцирующие несанкционированные рекомбинации в участках теломер (так называемых теломерных кэпах). И по этой причине теломеры будут терять свою длину [33]. А укорочение теломер, как мы знаем, выступает одним из признанных маркеров старения организма.
Этот процесс на примере профориентации клеток крови прекрасно проиллюстрирован (в прямом смысле) в комиксе «Кем быть? Как гемопоэтическая стволовая клетка выбирает профессию» [34]. — Ред.
Заключение. «Эпигенетический дрейф»
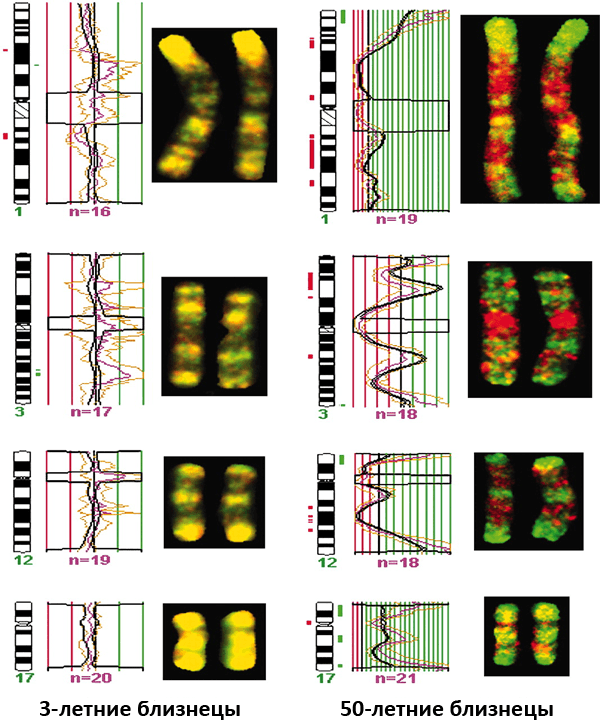
Насколько сильно меняется эпигеном с возрастом в зависимости от внешних факторов, наглядно показали исследования ДНК близнецов, выполненные испанскими учеными, Марио Фрага и его коллегами. Изучая монозиготных (однояйцевых) близнецов, они определили, что близнецы в возрасте трех лет идентичны не только генетически, но и эпигенетически [35]. А вот у 50-летних — по-прежнему одинаковых генетически — людей возникают существенные эпигенетические различия (рис. 7). Причем тем больше, чем внушительнее географическая дистанция между местами их проживания и, следовательно, разница в условиях проживания. Это может говорить о том, что подобные различия возникают не случайно, а зависят от условий, в которых живут люди.
Рисунок 7. Разница в метилировании ДНК близнецов в возрасте трех и 50 лет. Для того чтобы определить эпигенетические различия между близнецами, исследователи разработали оригинальную методику окраски одинаковых участков (локусов) гомологичных хромосом. В случае одинаковой экспрессии эти локусы окрашивались в желтый цвет, если были гипометилированы — в красный, а если гиперметилированы — в зеленый. Так вот, если у 3-летних близнецов хромосомы были окрашены практически полностью в желтый цвет, то у 50-летних явно доминировали зеленый и красный.
Результаты всех этих исследований позволили немецкому генетику Акселю Шумахеру разработать концепцию «эпигенетического дрейфа» — постепенного изменения с возрастом профиля метилирования ДНК [36]. Согласно концепции, возрастзависимый «эпигенетический дрейф» является естественным процессом, наблюдающимся у всех, даже полностью здоровых людей. Но у тех, кто подвергается сильному влиянию окружающей среды, вредных привычек, стрессов, неправильного питания, дрейф может «давать крен» в сторону неблагоприятных профилей, негативно меняя работу генома.
О природе различных, не только эпигенетических, возрастных изменений в клетках и возможных путях их преодоления образно рассказывает статья «Зачем клетки стареют» [37]. — Ред.
После всех проведенных исследований ученые могут уверенно говорить, что основу долголетия и хорошего здоровья вместе с другими факторами во многом определяет именно состояние эпигенома. А оно складывается из двух составляющих: из того, что мы получили в наследство от своих родителей, и из привычек, которые мы выработали в нашей жизни. Как сказал один из основоположников эпигенетики, профессор МГУ Б.Ф. Ванюшин, «нет никакого сомнения в том, что метилирование ДНК и модификации гистонов, а также избирательный сайленсинг генов малыми РНК играют очень важную роль в жизни клетки и организма, поэтому дальнейшие исчерпывающие исследования в этой захватывающей области знаний — очень важная и плодотворная задача нашего века» [38]. И с этим трудно поспорить. Остается ждать новых открытий, которые подарит нам область знаний, стремительно ворвавшаяся в нашу жизнь, — наука ЭПИГЕНЕТИКА.
Эпигеном: параллельная реальность внутри клетки
Кадр из видео «Мир эпигенетики», иллюстрированного пятиминутного рассказа «как будто для детей» об эпигеноме как источнике изменчивости
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Что представляет собой эпигеном, какова его роль в жизни клетки и чем он выступает по отношению к геному? Второстепенным дополнением, неким приложением или же загадочной, малоизученной системой, управляющей генетическими процессами? В последние годы наука находит всё новые определения этому термину. Предрасположенность к наследственным болезням, генетическая стабильность, адаптация, реакция на стрессовые факторы, темпы развития и старения клеток — во всём этом задействована «структура» под названием эпигеном. Изучение эпигенетических закономерностей открывает для биологии двери в лабиринты познания, где можно найти ответы на многие неразрешимые вопросы современной науки.
Конкурс «био/мол/текст»-2016
Эта работа опубликована в номинации «Своя работа» конкурса «био/мол/текст»-2016.
Генеральным спонсором конкурса, согласно нашему краудфандингу, стал предприниматель Константин Синюшин, за что ему огромный человеческий респект!
Спонсором приза зрительских симпатий выступила фирма «Атлас».
Младшая сестра генетики
Чтобы понять, что такое эпигеном и эпигенетика, сначала нужно прояснить, что такое геном и генетика. Геном — это совокупность генов того или иного организма. Генетика — наука, изучающая механизмы реализации генетической информации и передачи генов потомству. Соответственно, эпигеном — совокупность специфических меток, определяющих активность генов, но не затрагивающих первичную структуру ДНК. Эпигеном (приставка «эпи-» в переводе с греческого означает «над») представляет собой своеобразный регуляторный слой, расположенный как бы «над» геномом клетки. Условно говоря, эпигеном раздает команды, какие гены должны работать (экспрессироваться), а какие — отдыхать (или «молчать», то есть находиться в состоянии сайленсинга). Эпигенетика — научное направление, изучающее эпигенетические модификации генома, пути реализации состояний генов, их передачу в клеточных генерациях и механизмы регуляции наследственной информации (без изменения нуклеотидной последовательности) в ответ на действие внешних факторов [1].
Со времени первых открытий в области генетики и до недавних пор в науке прочно укоренилось представление о том, что структура ДНК — это единственный носитель наследственной информации. Благодаря крупномасштабным расшифровкам геномов, в том числе человеческого [2], была раскрыта природа гена и мутаций — нарушений генетической записи, — поняты принципы организации ДНК, изучены последовательности нуклеотидов, обусловливающие наследственные патологии. Было установлено, что генетическая информация человека хранится в 23 парах хромосом, содержащих 20–25 тысяч генов (оказалось, что точно определить их количество тоже не очень-то просто [3]), или три миллиарда пар нуклеотидов, несущих азотистые основания преимущественно четырех типов: аденин, тимин, гуанин, цитозин (сокращенно — А, Т, Г, Ц). Однако роль внешних факторов в механизмах реализации генетической информации была сведена к минимуму. Проще говоря, ученые считали: что записано в генόм, того не вырубишь топором [4].
Действительно, ДНК — это основа основ большинства жизненных форм. В ее структуре записано всё о живом организме, начиная с его видовых характеристик, морфологических параметров, предрасположенностей к болезням, заканчивая типом высшей нервной деятельности, поведенческими особенностями и наклонностями. Но было бы неправильно воспринимать геном как некий фатум, которым заранее предопределена жизнь индивида. Не всем генетическим «предсказаниям» суждено сбыться: некоторые из них еще не раз будут переписаны в течение онтогенеза (индивидуального развития организма).
Со временем ученые пришли к выводу, что активность многих генов непостоянна: они включаются (экспрессируются) и выключаются (репрессируются) в зависимости от воздействия внешних факторов. Это изменение активности генов, не затрагивающее первичную структуру ДНК, но влияющее на проявление тех или иных свойств и признаков, и составило предмет изучения эпигенетики.
Эпигенетика — сравнительно молодое направление науки. Впервые этот термин в 1942 году употребил английский ученый Конрад Уоддингтон. Изучая ряд закономерностей, научное сообщество пришло к выводу, что функции живого организма не обусловлены одной только закодированной в генах информацией, а во многом служат ответом на сигналы из окружающей среды. То, как происходит эпигенетически обусловленное включение и выключение определенных генов, стало одним из важных открытий современности, за что в 2006 году американским исследователям присудили Нобелевскую премию [10].
Классическая менделевская генетика опирается на то, что в основе изменений фенотипических признаков лежат мутации ДНК, то есть механические — случайные или индуцированные — изменения структуры наследственной информации. Эпигенетика опирается на варианты нормы, представленные модификациями. Каждое из нарушений эпигенома имеет не меньшее значение, чем генетические нарушения, и выступает эпигенетическим эквивалентом генетической мутации. Однако, несмотря на всю свою значимость, эпигенетика всё равно остается вторичной по отношению к генетике, ее младшей сестрой, ответвлением, а не самостоятельной наукой. Поскольку основным носителем наследственной информации является геном, эпигенетические механизмы могут только управлять работой тех или иных генов, исходя из имеющегося в наличии материала. Эпигеном служит механизмом контроля реализации генетической информации, что осуществляется посредством модификаций отдельных нуклеотидов. Проще говоря, не все гены, которые у нас есть, работают. Одни гены проявляют активность в одной клетке и неактивны в другой, и наоборот. Существуют некие регуляторные элементы, управляющие активностью генов. По современным представлениям, к таким элементам относятся: метилирование ДНК, гистоновые модификации, ацетилирование, фосфорилирование, гликозилирование, разнообразные микроРНК и другие структуры/процессы, «дирижирующие» нашим геномом [10], [11].
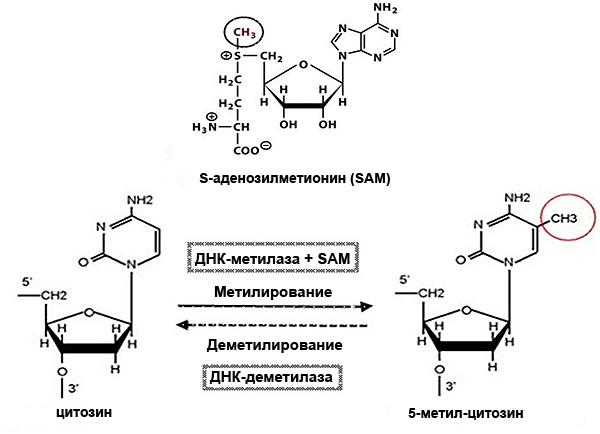
Рассмотрим самую известную и самую важную модификацию — метилирование ДНК. Это единственная химическая модификация ДНК, задействованная во многих генетических процессах у эукариот. Метилирование — добавление СН3-группы к цитозину ферментами ДНК-метилтрансферазами (рис. 1), что приводит к инактивации целого гена, в состав которого входит этот модифицированный нуклеотид.
Метилцитозин, немало удививший исследователей туберкулезной бациллы еще век назад, иногда называют пятым основанием ДНК, а недавно ученому миру явилось и шестое: «Шестое ДНК-основание: от открытия до признания» [12]. — Ред.
Рисунок 1. Модификация цитозина в 5-метилцитозин с участием ДНК-метилаз и S-аденозилметионина
Что же происходит, когда к цитозину, входящему в состав того или иного гена, присоединяется метильная группа? Оказывается, такая модификация провоцирует присоединение белков, изменяющих состояние хроматина. Чаще всего эпигенетическая регуляция осуществляется именно путем дифференциального метилирования цитозина в специфических участках генома. Формально ген никуда не девается, он продолжает находиться на своем месте, но никак себя не проявляет. Ген словно выключен, он не может производить продукт. В таком выключенном состоянии ген способен наследоваться. Передача потомству признаков, приобретенных организмами в течение жизни, в том числе посредством метилирования, называется эпигенетической наследственностью. Это наследование сохраняется у нескольких клеточных поколений или нескольких поколений живых существ.
Но всегда ли плохо то, что гены выключаются? Если представить, к примеру, что путем такой нехитрой модификации происходит выключение каких-либо вредоносных генов, вызывающих развитие патологий, наследственных аномалий или онкотрансформацию клеток, это же будет хорошо. Однако эпигеном может и навредить организму, инактивируя нужные гены. Еще до конца не изучено, как поддерживаются и воспроизводятся те или иные эпигенетические состояния [1].
Как уже упоминалось, метилирование ДНК влияет на многие генетические процессы у эукариот. Оно контролирует экспрессию генов, задействовано в пререкомбинационных событиях (предшествующих рекомбинации — процессу перераспределения генов между участками хромосом), выполняет функцию защиты от встраивания экзогенных нуклеотидных последовательностей, ограничивает перемещение транспозонов (особых участков ДНК, способных передвигаться по геному). Метилирование связано в основном с репрессией генов, инактивацией чужеродных последовательностей, регулировкой развития и организации генома. Регуляторные эпигенетические механизмы могут вызывать перемены в генетической активности. Метилирование цитозина в ДНК эукариот относится к ключевым факторам их развития. Оно оказывает влияние на структурно-функциональную организацию генома, принимая участие в регуляции конформационных изменений хроматина, что способствует изменениям в соответствующих локусах (местах локализации гена на хромосоме). ДНК в разных типах клеток организма метилирована по-разному. Это связано с расхождениями в выполняемых функциях, степени дифференцировки клеток и свойственной им экспрессии генов [13–15].
Различные эпигеномы как разные варианты реализации наследственной информации представляют собой своего рода набор параллельных реальностей, существующих в каждой клетке нашего организма. От того, какой ген заблокирован или разблокирован, зависит проявление того или иного фенотипического признака, а также скорость старения [16] и способность взаимодействовать с окружающей средой. Является ли это включение-выключение случайным или запрограммированным процессом и как связаны между собой различные «миры» эпигеномов, пока известно мало. Но сам факт того, что наука уже вплотную подошла к таким вопросам, не может оставаться без внимания.
На страже спокойствия генома. Метилирование как защитный механизм
Метилирование как функция защиты генетического материала от встраивания вирусных и других чужеродных нуклеотидных последовательностей встречается даже у таких примитивных живых организмов, как бактерии. Осуществляется это за счет системы рестрикции-модификации. Чужеродная ДНК, попав в бактерию, расщепляется рестриктазами (специальными ферментами, разрезающими ДНК в определенных участках). Однако те же самые последовательности собственной ДНК бактерии защищены от расщепления метильными метками [17].
Считается, что метилирование в качестве механизма, предотвращающего проникновение в геном чужеродных последовательностей, сохраняется и у более сложных организмов. Оно подавляет распространение вирусных генов, тандемных повторов (бессмысленных последовательностей ДНК) и транспозонов. Больше всего таких модификаций наблюдается в некодирующих районах ДНК. Метилирование репрессирует «ненужные» гены путем добавления метильной группы к цитозиновым остаткам в составе этих последовательностей. У млекопитающих, в частности человека, метилирование повторяющихся участков играет важную роль в стабилизации ДНК. В свою очередь, если повторяющиеся участки деметилируются (теряют метильные метки), они становятся мутагенными и вызывают геномную нестабильность — хромосомные аномалии, каскад апоптозных реакций, онкотрансформацию клетки. Метилирование обеспечивает целостность генома, а также стабилизирует двойную спираль ДНК за счет усиления связи с комплементарным гуанином [4], [18], [19].
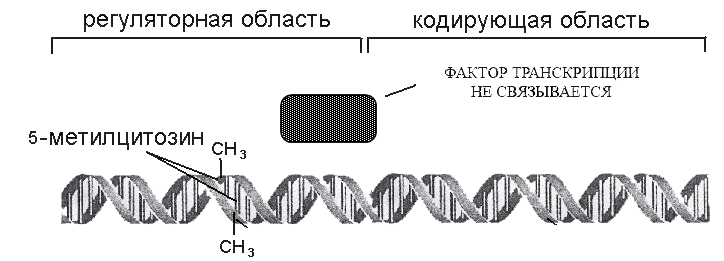
Процессы метилирования и деметилирования ДНК эукариот принимают участие в регуляции экспрессии генов в ходе роста, дифференцировки, старения клеток и их реакций на повреждающие воздействия [19], [20]. Негативные факторы способны переключать программы функционирования генов. В частности, метилирование задействовано в регуляции экспрессии генов в ответ на биотические (вирусные, грибковые, бактериальные инфекции) и абиотические (температура, радиация, УФ-излучение) стрессы [21–23]. К примеру, при действии радиационного стресса уровень метилирования генома снижается, вследствие чего активируется транскрипция транспозонов, избыток которых может вызывать генетическую нестабильность, хромосомные аномалии и другие повреждения ДНК. Однако в ответ на увеличение транскрипционной активности происходит обратная реакция: запускаются защитные процессы метилирования транспозонных промоторов — регуляторных участков, обеспечивающих транскрипцию (рис. 2). Таким образом, радиация провоцирует повышение уровня метилирования ДНК, что может быть проявлением защитной реакции — ответа генома на усиление транспозонной активности. То есть, с одной стороны, стресс активирует мобильные элементы и увеличивает их вредное действие, с другой — это ведет к запуску эпигенетического «молчания» транспозонов и стабилизации хромосом. Также в пользу того, что метилирование ДНК участвует в защите генома, поддерживая его постоянство в изменяющихся условиях, говорит и тот факт, что искусственное снижение метилирования вызывает увеличение транспозонной активности и количества хромосомных перестроек [13], [24].
Рисунок 2. Метильные группы в регуляторной области гена препятствуют транскрипции. Механизм — прямое ингибирование.
Согласно данным, полученным на животных, радиация способствует подавлению тотального метилирования в непосредственно облученных тканях, а также в тканях-«свидетелях». До недавнего времени считалось, что биологические последствия ионизирующего облучения связаны с прямыми повреждениями ДНК. Но сегодня эта концепция дополнена. Было обнаружено, что облученные клетки провоцируют повышение уровня генных мутаций и хромосомных аберраций (нарушений структуры хромосом) в соседних клетках, которые не подвергались действию радиации. То есть молекулярные и клеточные эффекты в них обусловлены не самόй ионизирующей радиацией, а сигналом повреждения из облученных клеток. Эти реакции называются эффектом свидетеля. Они хорошо изучены на культурах клеток. Предполагается, что облученные клетки выделяют эпигенетические сигнальные факторы, которые и в необлученных соседках вызывают аналогичные изменения. Природа этих факторов и точный механизм «эффекта свидетеля» еще довольно слабо исследованы [25].
Если провести аналогию между геномом и человеческим обществом, то транспозоны можно было бы сравнить с антисоциальными элементами или просто нарушителями общественного порядка. В зависимости от размеров и мест локализации транспозоны могут быть как мелкими хулиганами, так и опасными преступниками, сеющими хромосомный беспорядок. Метилирование в таком случае считалось бы внутригеномной полицейской службой, поскольку именно оно выступает основным механизмом, предотвращающим разгул транспозонного «бандитизма» в ДНК. Навешивание метильных меток на потенциально опасные генетические последовательности изолирует их от общества, обеспечивает стабильность и порядок, позволяя добропорядочным генам спокойно трудиться на благо клетки и организма.
Старость — не радость, а эпигенетическая программа
Эпигеном — пластичная система, функционирующая в соответствии с программой развития и реагирующая на воздействие внешних факторов. Считается, что существует эпигенетически обусловленный каскад изменений, охватывающих процессы старения и реакции на стрессовые факторы [26–28]. Поэтому одним из важных направлений современных исследований является выяснение роли метилирования цитозина в регуляции экспрессии генов в механизмах стрессового ответа и возрастной деградации. Понимание аспектов эпигенетического контроля старения поможет прояснить, что служит отправной точкой этого процесса.
При старении наблюдается уменьшение числа генов, «работающих» в молодости, и активация генов, которые «спали», пока организм был полон бодрости и здоровья, но «проснулись» на этапе его одряхления. Потеря функциональной активности генов, нарушение проницаемости мембран, увеличение количества неактивного хроматина, возрастание частоты хромосомных аберраций, изменение паттернов (шаблонов) метилирования тотальной ДНК и отдельных генов — всё это составляет многокомпонентный детерминированный процесс старения. И хотя пока не найдены группы генов, запускающие каскад молекулярных событий в стареющей клетке, осуществление программы старения в последнее время часто связывают с эпигенетическими механизмами (рис. 3).
По некоторым предположениям, метилирование ДНК запрограммировано и играет ключевую роль в реализации процесса возрастной гибели клеток. Концепция запрограммированной гибели клеток в ходе старения объясняется активацией эпигенетических механизмов на фоне снижения эффективности репарационных (ремонтных) систем. Согласно одной из гипотез, апоптоз (программируемая клеточная гибель) связан с активацией определенных «генов старения», которые запускают деградационные процессы в клетке. Это происходит путем снижения уровня метилирования ДНК, что наблюдается в процессе старения дифференцированных клеток и сопровождается дерепрессией хроматина. В итоге активируются дремлющие транспозоны, склонные ввергать клетку в состояние генетического хаоса. Возрастная потеря метильных меток ускоряет клеточную гибель, в ткани меняется цитокиновый фон, что может подталкивать к гибели соседние клетки. Таким образом, старение чем-то сродни медленным инфекциям. И даже иногда к ним приравнивается: некоторые биологи допускают возможность миграции «освобожденных» транспозонов в другие клетки [1], [29–32].
Рисунок 3. Эпигенетика отсчитывает часы жизни. Подробно о «часах жизни» и их разновидностях рассказано в статьях [16], [33], [34].
Возрастное снижение метилирования было доказано на примере горбуши в середине ХХ столетия [35]. Позже это подтвердилось и в отношении других организмов. Также было установлено, что искусственное деметилирование ведет к преждевременному старению животных. Идея о том, что старение и уменьшение метилирования взаимосвязаны, стала новым словом в эпигенетике. Кроме того, снижение метилирования в ходе старения ведет к конформационным изменениям хроматина, что повышает доступность ДНК для нуклеаз (ферментов-разрушителей) и нарушает целостность макромолекул стареющей клетки. При ослаблении метилирования ДНК становится более чувствительной к действию вредных факторов, эндогенных ферментов, транспозонов [26], [36]. Стабильность генома у организмов с более «молчаливыми» транспозонами выше, что делает их устойчивыми к повреждающим факторам среды и обеспечивает им бόльшую продолжительность жизни в сравнении с организмами, чей уровень репрессии мобильных генетических элементов низок. Полагают, что восстановление в стареющей клетке эпигенетических маркеров, свойственных молодой клетке, может привести к необходимой репрессии транспозонов, стабилизации генома и замедлению темпов старения [37], [38].
С возрастом снижается экспрессия генов поддержания клеточного равновесия, в результате чего начинается свойственная старению деградация тканей и органов. Происходит увеличение числа разрывов в ДНК и сшивок ДНК с белком, снижаются активности ферментов поддержания структуры хромосом и количество 5-метилцитозина, накапливаются структурные дефекты. Процесс старения сопровождается транскрипцией определенных генов и синтезом ряда белков. Этот каскад сурово скоординированных событий подчинен некой программе. Переход к каждой новой стадии онтогенеза (индивидуального развития) характеризуется изменениями эпигенетического статуса, который обеспечивает активацию или репрессию специфического набора генов. С помощью воздействия на эпигеном можно некоторым образом корректировать генетическую программу развития живых организмов [36], [39–41].
Все перечисленные процессы действуют в направлении ухудшения состояния и функционирования генетического аппарата. А реализуются они под действием внешних и внутренних факторов. Старение — это результат изменения надгеномных процессов, которые на определенном этапе онтогенеза запускают деструктивные механизмы по двум направлениям. С одной стороны, происходит индукция генетической программы деградации структур и функций, которая репрессирует гены поддержки клеточного гомеостаза и активирует гены, отвечающие за реакции распада. С другой стороны, запускается механизм ослабления деятельности защитных систем, что делает клетку восприимчивой к повреждающему действию стрессовых факторов. Несмотря на эффективную репарационную машину, в структуре ДНК с возрастом накапливаются разрывы и другие дефекты, всё меньше и меньше индуцируются защитные белки теплового шока, в делящихся клетках сильно сокращается длина теломер (защитных концевых участков хромосом). Всё это — элементы единого многосложного процесса надгеномной регуляции процессов старения. Согласно некоторым гипотезам, множественность механизмов старения эукариот может быть обусловлена тем, что природа страхуется от появления долгоживущих видов и особей [42], [43].
Всей этой котовасии со старением и даже нестарением «Биомолекула» посвятила целый уникальный спецпроект. Из материалов которого, в общем-то, не следует, что старение — это злой умысел Природы. Например, можно обратиться к статьям: «Старческие капризы природы: почему люди прекращают стареть, а мыши не успевают жить» [44], «Нутригеномика: питание vs. заболевания» [45], «Сон и старение I: „Часы в мозге“ и влияние генов на ритм жизни» [46] — и далее проследовать по ссылкам на другие, не менее интересные странички проекта. — Ред.
Метки смерти на генах. Метилирование и онкогенез
Недостаточное метилирование (гипометилирование) генома было одним из первых выявленных эпигенетических маркеров онкозаболеваний. Гипометилирование ведет к активации генов, которые в норме должны молчать. В случае опухолей это индивидуальные онкогены, пребывающие в здоровой клетке в метилированном (неактивном) состоянии. Понижение тотального уровня метилирования генома выражается в снятии естественных репрессивных меток с онкогенов, что вызывает каскад разрушительных событий. Попутно гипометилирование больших участков генома активирует транспозоны, за счет чего увеличивается хромосомная нестабильность и растет число аномалий. Эти два процесса ставят клетку на путь онкологической трансформации. Во многих лабораториях именно тотальное гипометилирование ДНК диагностируется как основной признак раковых клеток [15], [47], [48].
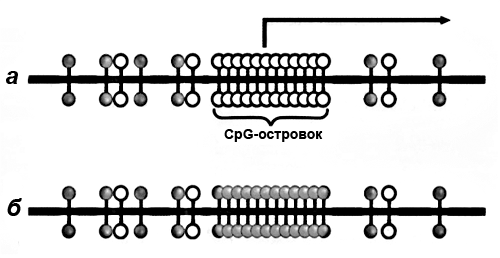
Вместе с тем, онкогенез сопровождается и гиперметилированием (избыточным метилированием) CpG-островков в области промоторов генов (рис. 4). В норме 90% CpG-островков не метилированы, то есть транскрипционно активны. Метилирование в этих участках чревато фатальными последствиями, поскольку вызывает «выключение» генов — супрессоров (подавителей) опухолей. Гены-онкосупрессоры, противостоящие онкологическому процессу, перестают работать, что дает зеленую улицу раковой трансформации, вызывает бесконтрольное деление клеток опухоли. Одним из лабораторных маркеров диагностики рака на ранних стадиях выступает повышенное метилирование CpG-островков генов — супрессоров опухолей [49], [50].
Рисунок 4. CpG-островок промоторной области гена. а — Транскрипционно активный (неметилированный) островок. б — Сайленсированный (метилированный) островок.
Как видим, рак не обходится без эпигенетических событий. Как недостаток метилирования, так и его избыток в равной мере способствуют раковому перерождению здоровой клетки. Нарушенное метилирование ведет к аномалиям развития и опухолеобразованию. Как тут не вспомнить о том, что всё хорошо в меру. Онкогенез — это многофакторный и многоэтапный процесс, включающий в себя как активацию онкогенов, так и молчание генов-онкосупрессоров. Каждое из этих нарушений эпигенома для опухолевой прогрессии имеет не меньшее значение, чем генетические нарушения, то есть служит эпигенетическим эквивалентом генетической мутации [50]. Изменение нормальных паттернов (шаблонов) метилирования ДНК неизбежно ведет к отрицательным последствиям. А сохранение здорового статуса метилирования генома является основным условием нормального развития организма.
Выходит, что рак — это не только генетически обусловленное заболевание, как считалось раньше, а заболевание, в основе которого лежит ряд еще во многом не изученных эпигенетических изменений. При этом нельзя считать, что неправильное метилирование — всего лишь маркер онкозаболевания; зачастую оно выступает причиной последнего. Так, например:
Здесь стоит отметить, что активация гена, наступающая вследствие деметилирования определенных сайтов, может происходить только в том случае, если в клетке присутствует специфический транскрипционный фактор. Этим объясняется ограниченное количество генов, активированных в опухолях посредством гипометилирования [50].
Однако нельзя забывать, что недостаток метилирования ДНК так же опасен, как и его избыток, и так же служит причиной ряда онкопатологий. К примеру, при хроническом лимфолейкозе наблюдается тотальное деметилирование ДНК в раковых клетках на фоне высокой ДНК-метилтрансферазной активности. Тотальное снятие метильных меток оказывает значительное дестабилизирующее действие на геном эукариот, меняет структуру хроматина, степень его конденсации, время репликации, что может вызывать нарушения экспрессии различных генов [15], [54].
Вместе с тем не менее опасна и спонтанная потеря сайтов метилирования. Спонтанное дезаминирование (потеря аминогрупп) 5-метилцитозина приводит к возникновению остатка тимина и образованию неканонической пары оснований Г:Т, которая становится мишенью для системы репарации. Репаративные ферменты удаляют тимин из этой пары и восстанавливают исходную последовательность Г:Ц, однако иногда возникают мутации, выражающиеся в замене пары Г:Ц на А:Т. Именно нестабильность 5-метилцитозина и спонтанные замены Г:Ц на А:Т привели в ходе эволюции к низкому уровню CpG-динуклеотидов в геноме млекопитающих. Таким образом, спонтанный мутагенез, происходящий в животной клетке при отсутствии экзогенных и эндогенных агентов, нарушает структуру многих генов, в том числе и онкосупрессоров. Этот механизм играет не последнюю роль в процессах онкологической трансформации [55].
Помимо аберрантного метилирования промоторов генов-онкосупрессоров, в опухолевых клетках обнаруживается и нестабильность микросателлитов (коротких тандемных повторов ДНК), при которой микросателлитные маркеры представлены одновременно многими разными аллелями, дополнительными к двум родительским [52], [56]. Сателлитные ДНК в геноме человека в норме высоко метилированы. В процессе опухолеобразования наблюдается микросателлитная нестабильность, резкое гипер- или гипометилирование (в зависимости от вида опухоли). В качестве примера здесь можно упомянуть ген MLH1, продукт которого участвует в репарации ошибок спаривания нуклеотидов. Гиперметилирование промотора этого гена и микросателлитная нестабильность ассоциированы с опухолями желудочно-кишечного тракта и некоторых других органов [52].Изменчивость микросателлитных последовательностей по-разному проявляется на разных стадиях развития и зависит от состояния дифференцировки и типа ткани [57].
Однако не все гены задействованы в эпигенетических событиях канцерогенеза. Ген белка р53 не содержит в своей промоторной области CpG-островков и не поддается метилированию. Нарушение функций р53 наблюдаются во многих случаях рака, но инактивация его гена обусловлена не эпигенетическими, а генетическими механизмами. В кодирующей части гена присутствуют одиночные метилированные CpG-динуклеотиды, которые в силу спонтанного дезаминирования 5-метилцитозина мутируют с заменой комплементарных пар [50], [52].
Кстати, подобные таблетки фармкомпании уже производят, да и природа не отстает: вещества — модификаторы эпигенома обнаружены в растительных продуктах, особо почитаемых приверженцами здорового питания: «Пилюли для эпигенома» [59]. Только вот к природным «технологиям» есть небольшая (для всех, кроме фармацевтов, Эркюля Пуаро и детектива Монка) претензия: беспорядочно там всё как-то. — Ред.
Перспективы изучения эпигенома
Общая черта, присущая как метилированию, так и мутациям — это наследуемость, хотя в отличие от большинства мутаций метилирование — процесс обратимый. Контроль модификации ДНК интересен прежде всего для биотехнологической отрасли. Воздействуя на эпигеном, можно не только вылечить ряд заболеваний, но и добиться промышленной выгоды. К примеру, направленная регуляция экспрессии генов у растений способна увеличить их продуктивность. Замечено, что в результате обработки 5-азацитидином наблюдается увеличение белка в зерновках пшеницы за счет активации генов запасных белков. Причем индуцированные химическим агентом признаки сохраняются в течение трех поколений. Какие механизмы отвечают за возвращение к исходному паттерну метилирования, соответственно, и к исходному фенотипу — пока неизвестно [60], [61].
Как отмечалось выше, эпигеном — система пластичная, что позволяет в перспективе подобраться к рычагам управления эпигенетическими модификациями, минимизировать действие неблагоприятных факторов и обеспечить оптимальные условия для существования клетки. Ключ к разгадке наследственных патологий, продлению жизни, управлению полезными свойствами живых организмов — всё это сулит эпигенетика. Уже сегодня можно без преувеличения сказать, что открытия в области эпигенетики в скором времени поднимут биологическую науку на качественно новый уровень развития, и это кардинальным образом изменит саму человеческую цивилизацию.