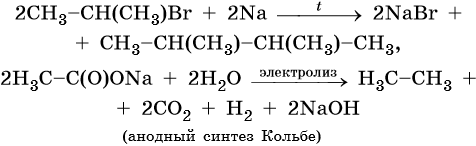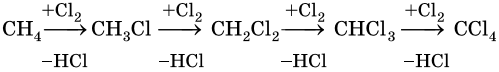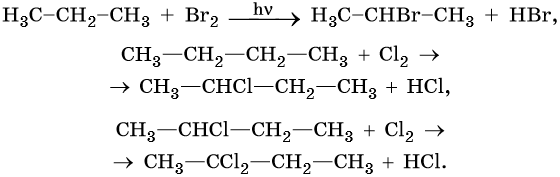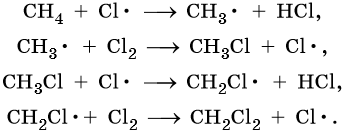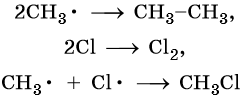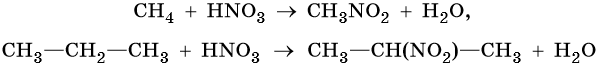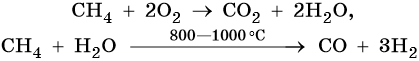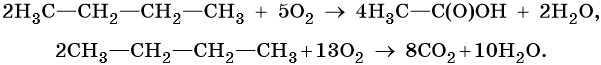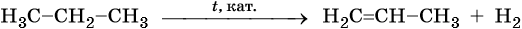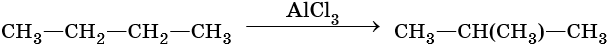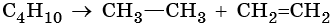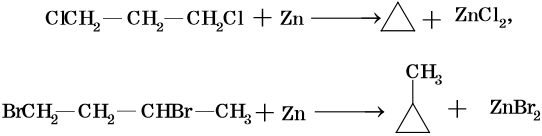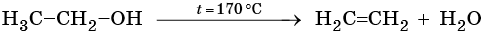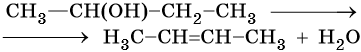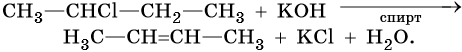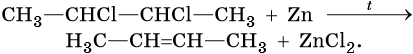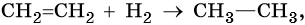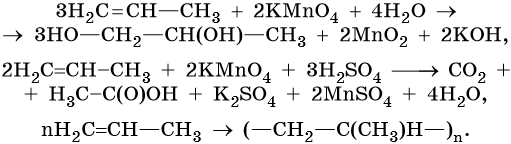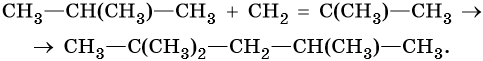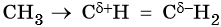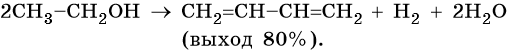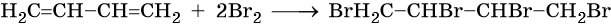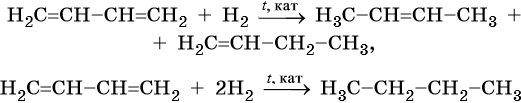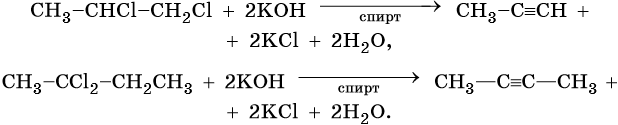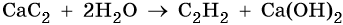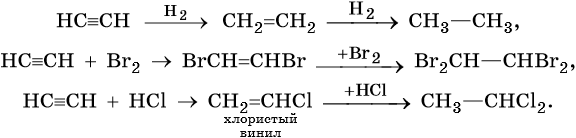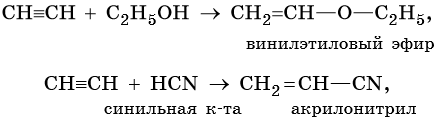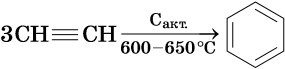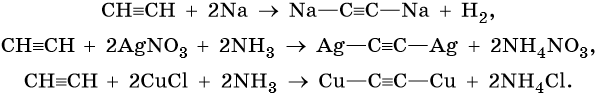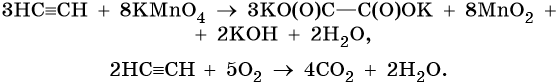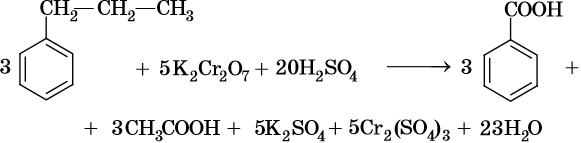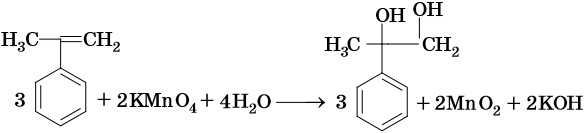Что относится к алкенам
Алкены — номенклатура, получение, характерные химические свойства
К непредельным относят углеводороды, содержащие в молекулах кратные связи между атомами углерода. Непредельными являются алкены, алкины, алкадиены (полиены). Непредельным характером обладают также циклические углеводороды, содержащие двойную связь в цикле (циклоалкены), а также циклоалканы с небольшим числом атомов углерода в цикле (три или четыре атома). Свойство «непредельности» связано со способностью этих веществ вступать в реакции присоединения, прежде всего водорода, с образованием предельных, или насыщенных углеводородов — алканов.
Строение алкенов
Образование двойной связи в алкенах
Гомологический ряд этена
Неразветвленные алкены составляют гомологи- ческий ряд этена (этилена): С2Н4 — этен, С3Н6 — пропен, С4Н8 — бутен, С5Н10 — пентен, С6Н12 — гексен, С7Н14 — гептен и т.д.
Изомерия алкенов
Для алкенов характерна структурная изомерия. Структурные изомеры отличаются друг от друга строением углеродного скелета. Простейший алкен, для которого характерны структурные изомеры, — это бутен:

Особым видом структурной изомерии является изомерия положения двойной связи:
Алкены изомерны циклоалканам (межклассовая изомерия), например:
Вокруг одинарной углерод-углеродной связи возможно практически свободное вращение атомов углерода, поэтому молекулы алканов могут приобретать самую разнообразную форму. Вращение вокруг двойной связи невозможно, что приводит к появлению у алкенов еще одного вида изомерии — геометрической, или цис- и транс-изомерии.
Номенклатура алкенов
1. Выбор главной цепи. Образование названия углеводорода начинается с определения главной цепи — самой длинной цепочки атомов углерода в молекуле. В случае алкенов главная цепь должна содержать двойную связь.
2. Нумерация атомов главной цепи. Нумерация атомов главной цепи начинается с того конца, к которому ближе находится двойная связь.
Например,правильное название соединения:
Если по положению двойной связи нельзя определить начало нумерации атомов в цепи, то его определяет положение заместителей так же, как для предельных углеводородов.
3. Формирование названия. В конце названия указывают номер атома углерода, у которого начинается двойная связь, и суффикс -ен, обозначающий принадлежность соединения к классу алкенов. Например:
Физические свойства алкенов
Первые три представителя гомологического ряда алкенов — газы; вещества состава С5Н10 — С16Н32 — жидкости; высшие алкены — твердые вещества.
Температуры кипения и плавления закономерно повышаются при увеличении молекулярной массы соединений.
Химические свойства алкенов
Реакции присоединения. Напомним, что отличительной чертой представителей непредельных углеводородов — алкенов является способность вступать в реакции присоединения. Большинство этих реакций протекает по механизму электрофильного присоединения.
1. Гидрирование алкенов. Алкены способны присоединять водород в присутствии катализаторов гидрирования, металлов — платины, палладия, никеля:
Эта реакция протекает при атмосферном и повышенном давлении и не требует высокой температуры, т. к. является экзотермической. При повышении температуры на тех же катализаторах может пойти обратная реакция — дегидрирование.
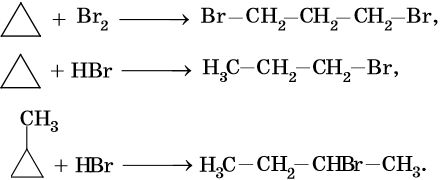
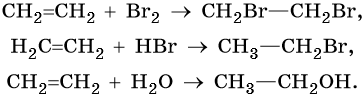
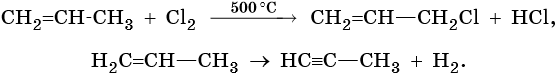
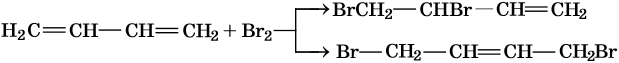
2. Галогенирование (присоединение галогенов). Взаимодействие алкена с бромной водой или раствором брома в органическом растворителе (СС14) приводит к быстрому обесцвечиванию этих растворов в результате присоединения молекулы галогена к алкену и образования дигалогеналканов.
3. Гидрогалогенирование (присоединение галогеноводорода).

Эта реакция подчиняется правилу Марковникова:
При присоединении галогеноводорода к алкену водород присоединяется к более гидрированному атому углерода, т. е. атому, при котором находится больше атомов водорода, а галоген — к менее гидрированному.

4. Гидратация (присоединение воды). Гидратация алкенов приводит к образованию спиртов. Например, присоединение воды к этену лежит в основе одного из промышленных способов получения этилового спирта.
Эта реакция протекает также в соответствии с правилом Марковникова — катион водорода присоединяется к более гидрированному атому углерода, а гидроксогруппа — к менее гидрированному.
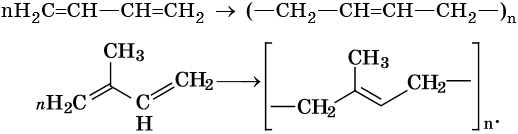
5. Полимеризация. Особым случаем присоединения является реакция полимеризации алкенов:

Эта реакция присоединения протекает по свободнорадикальному механизму.
Реакции окисления.
1. Горение. Как и любые органические соединения, алкены горят в кислороде с образованием СО2 и Н2О:

2. Окисление в растворах. В отличие от алканов алкены легко окисляются под действием растворов перманганата калия. В нейтральных или щелочных растворах происходит окисление алкенов до диолов (двухатомных спиртов), причем гидроксильные группы присоединяются к тем атомам, между которыми до окисления существовала двойная связь:
Алкены
Соединения, имеющие двойные и тройные связи, называют ненасыщенными, непредельными. Алкены (или олефины) — ненасыщенные углеводороды, содержащие одну двойную связь.
Физические свойства алкенов
В гомологическом ряду этилена первые три члена — газообразные вещества, начиная с пентена — жидкости, высшие гомологи — твердые кристаллические тела. Физические свойства алкенов в основном сходны со свойствами соответствующих алканов, однако низшие гомологи этилена образуют более плотно упакованные молекулярные кристаллические решетки (из-за плоского строения участка двойной связи), что объясняет их более высокую относительную плотность по сравнению с соответствующими алканами. Чем выше молекулярная масса, тем меньше это различие.
Физические свойства некоторых алкенов (таблица 10-1)
Этилен
Пропилен
Бутен-1
Изобутен
Пентен -1
Пентен-2 (цис-)
Октадецен
Строение алкенов
Появление π-связи в алкенах самым существенным образом меняет их строение и свойства по сравнению с алканами. Структурная изомерия алкенов значительно разнообразнее, чем у алканов, что связано со структурой углеродного скелета и положением двойной связи. Например, алкенам состава С5 H 10 соответствуют структурные изомеры:
Варьирование двух признаков приводит к значительному увеличению числа структурных изомеров по сравнению с алканами. Невозможность в нормальных условиях свободного вращения вокруг двойной связи, как отмечалось ранее, приводит к появлению у алкенов геометрической (цис-, транс-) изомерии (см. раздел 3.2.1)
Геометрические изомеры, подобно структурным, отличаются как физическими, так и химическими свойствами. Сравните, например, свойства цис-, транс-бутенов-2, фумаровой и малеиновой кислот, являющихся геометрическими изомерами по отношению друг к другу (табл. 10-2)
Пространственные конформационные изомеры алкенов, как и в случае алканов, в нормальных условиях не могут быть выделены в индивидуальном виде.
Разнообразие типов связей в алкенах значительно выше, чем в алканах, как по способам образования, так и по физическим характеристикам (энергии, длине и т. д.). Например, в молекуле бутена-2 имеются связи:
Химические свойства алкенов
Разрыв С-Сπ связи приводит к реакциям присоединения, а Сα-Н ;— замещения, то есть наиболее характерными для алкенов являются реакции именно этих типов.
Реакции присоединения
По этим причинам следует ожидать, что С—Сπ связь легче подвергается воздействию частиц с недостаточной электронной плотностью, принимающих электроны, то есть электрофилов (кислот Льюиса), радикалов, карбенов. Таким образом, наиболее типичными для алкенов являются реакции электрофильного и радикального присоединения. Процесс присоединения (механизм) может осуществляться двояким образом:
· синхронный, одностадийный механизм требует строгой ориентации четырех атомов друг относительно друга;
· асинхронный, многостадийный механизм не требует строгой ориентации двух молекул друг относительно друга.
Читайте также:
Практическое значение алкенов
Практическое значение алкенов связано с тремя основными обстоятельствами.
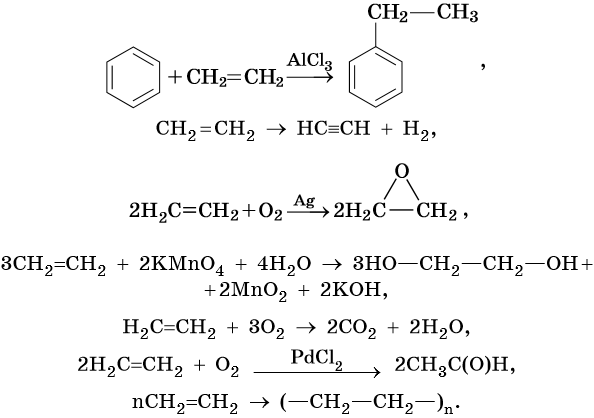
Во-первых, повышенная реакционная способность алкенов, как это было показано выше, позволяет использовать их в качестве исходных продуктов для получения самых разнообразных, необходимых в жизнедеятельности человека продуктов:
то есть в качестве сырья для промышленности тонкого и основного органического синтеза.
Переход химической промышленности на алкан-алкеновое сырье продуктов переработки нефти, как более экономичное энергетически, в 50-60-е годы XX столетия позволил передовым развитым странам мира совершить технологическую революцию.
Во-вторых, алкенами являются многие природные соединения растительного и животного происхождения, играющие важную биологическую роль (см. Феромоны). Отметим некоторые из них. Например, в состав растительных жиров входят ненасыщенные и полиненасыщенные кислоты (подробнее об их составе, свойствах, биологическом значении см. главу XXI).
В-третьих, алкены являются исходным сырьем для получения полиолефинов. Это одна из важнейших областей применения алкенов. Значение и масштабы мирового производства полиолефинов прерывно растут. По этим причинам реакции полимеризации аланов заслуживают отдельного рассмотрения.
Экологическое послесловие
Загрязнение атмосферы, почв, водоемов и подземных вод алкенами и способы борьбы с этим аналогичны описанным выше для алканов.
Заслуживает отдельного рассмотрения наиболее широкая область применения алкенов — производство высокомолекулярных соединений (ВМС), которая имеет два аспекта: собственно производство и утилизация использованных изделий из ВМС.
Производство ВМС, особенно крупное, является, несомненно, «грязным». Основные загрязнения связаны с выбросом в атмосферу легколетучих неорганических и органических соединений, таких, как хлористый водород, фтористый водород, хлор, фтор, аммиак, синильная кислота, этилен, пропилен, бутилены, хлористый винил и др., которые, являясь ядовитыми, губительно сказываются на человеке, растительном и животном мире на значительных территориях вокруг такого производства.
Не менее острой для таких заводов является проблема утилизации промышленных стоков. Известные решения проблемы очистки таких стоков значительно удорожают строительство, и зачастую ее решают закачкой стоков в подземные горизонты. Однако загрязнение подземных вод приводит к загрязнению питьевой воды и воды для хозяйственных нужд.
Именно таким бумерангом обернулось для города Томска строительство химического комбината по производству полиэтилена и других органических продуктов.
В связи с этим понятно желание развитых стран размещать «грязные» крупнотоннажные производства за пределами своих границ. Проект строительства целого ряда крупных заводов по производству ВМС на территории Тюменской области в Российской Федерации — из этого ряда. Очевидна необходимость в таких случаях тщательной экологической экспертизы проектов, особенно технологий утилизации промышленных стоков.
Вторая проблема, связанная с утилизацией использованных изделий из ВМС, становится все более актуальной в связи с резким расширением применения человеком пластических масс и синтетических волокон во второй половине XX века. Масштабы этого явления хорошо известны жителям морских побережий, даже таких отдаленных, как Курильские острова, полярные районы Сибири, Дальнего Востока.
Острота проблемы связана с тем, что изделия из ВМС являются долговечными, слабо подвергаются разрушению кислородом и биодеградации.
В настоящее время используют в основном два варианта утилизации изделий из ВМС:
Оба метода имеют свои ограничения. К сожалению, не все ВМС могут быть подвергнуты вторичной переработке, а массовый сбор использованных изделий из ВМС трудно организовать как по экономическим соображениям, так и в связи с недостаточной экологической культурой населения.
Сжигание изделий из ВМС также имеет свои отрицательные моменты, связанные с выделением диоксида углерода и деполимеризацией, образованием при воздействии высоких температур первичных и вторичных токсичных продуктов, таких, как хлористый водород, фтористый водород, аммиак, оксиды азота, серы, хлористый винил, стирол, диоксин и др.
По этим причинам актуальной становится проблема получения ВМС и изделий из них нового поколения с заданным сроком эксплуатации, подверженных биодеградации.
Алкины
Номенклатура и изомерия алкинов
Названия алкинов формируются путем добавления суффикса «ин» к названию алкана с соответствующим числом: этин, пропин, бутин и т.д.
При составлении названия алкина важно учесть, что главная цепь атомов углерода должна обязательно содержать тройную связь. Нумерация атомов углерода в ней начинается с того края, к которому ближе тройная связь. В конце названия указывают атом углерода у которых начинается тройная связь.
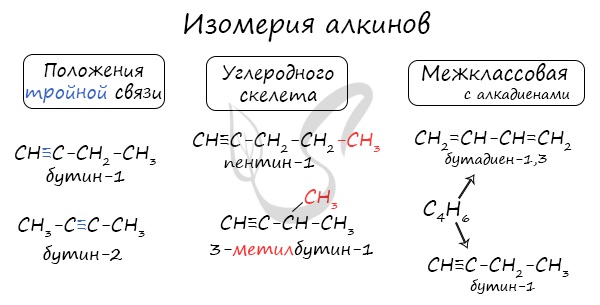
Для алкинов характерна изомерия углеродного скелета, положения тройной связи, межклассовая изомерия с алкадиенами.
Пространственная геометрическая изомерия для них невозможна, ввиду того, что каждый атом углерода, прилежащий к тройной связи, соединен только с одним единственным заместителем.
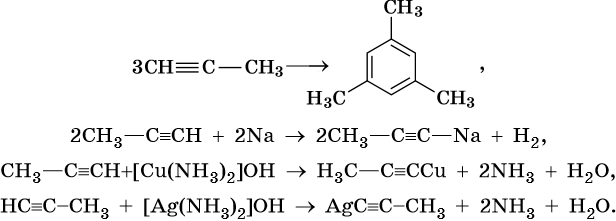
Получение алкинов
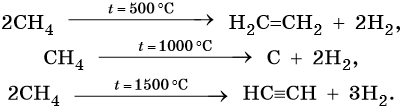
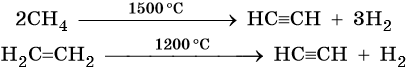
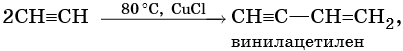
При нагревании метана до 1200-1500 °C происходит димеризация молекул метана, в ходе чего отщепляется водород.
Осуществляется напрямую, из простых веществ. Протекает на вольтовой (электрической) дуге, в атмосфере водорода.
2C + H2 → (t, вольтова дуга) CH≡CH
В результате разложения карбида кальция образуется ацетилен и гидроксид кальция II.
Получение гомологов ацетилена возможно в реакциях дегидрогалогенирования дигалогеналканов, в которых атомы галогена расположены у одного атома углерода или у двух соседних атомов.
Химические свойства алкинов
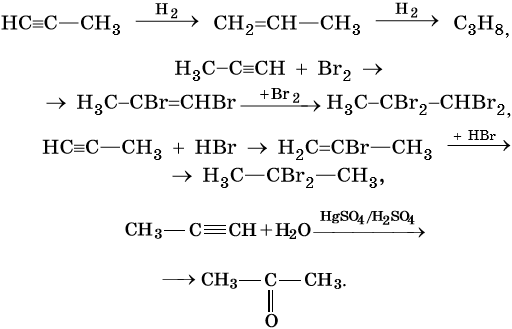
Водород присоединяется к атомам углерода, образующим тройную связь. Пи-связи (π-связи) рвутся, остается единичная сигма-связь (σ-связь).
CH≡C-CH3 + H2 → (t, Ni) CH2=CH-CH3 (в реакции участвует 1 моль водорода)
CH≡CH + 2H2 → (t, Ni) CH3-CH3 (в реакции участвует 2 моль водорода)
Реакция с бромной водой является качественной для непредельных соединений, содержащих двойные (и тройные) связи. В ходе такой реакции бромная вода обесцвечивается, что указывает на присоединение его по кратным связям к органическому веществу.
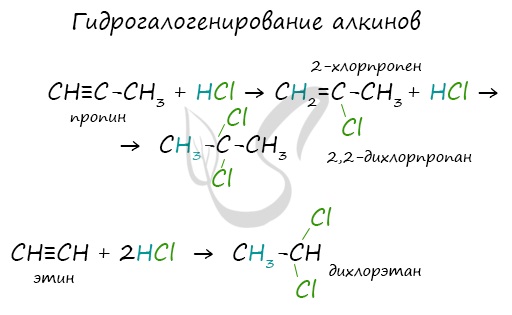
Алкины вступают в реакции гидрогалогенирования, протекающие по типу присоединения.
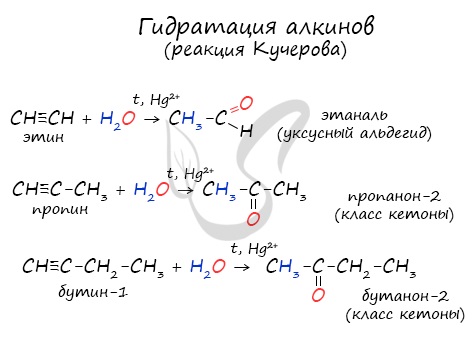
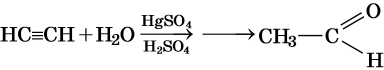
Только в реакции с ацетиленом образуется уксусный альдегид. Во всех остальных реакциях (с гомологами ацетилена) образуются кетоны.
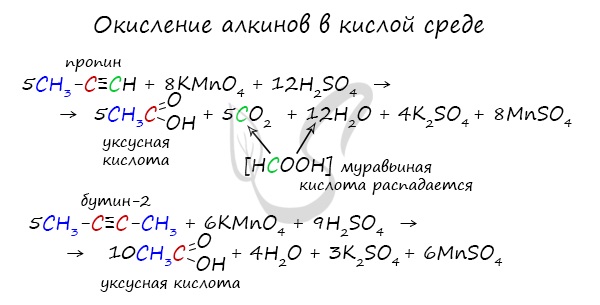
Так, при окислении пропина, образуется уксусная кислота и муравьиная кислота, окисляющаяся до угольной кислоты, которая распадается на углекислый газ и воду.
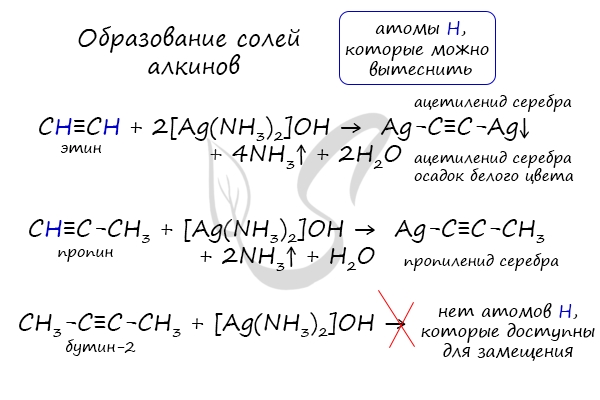
В случае если тройная связь прилежит к краевому атому углерода, то имеющийся у данного атома водород может быть замещен атомом металла. Если тройная связь спрятана внутри молекулы, то образование солей невозможно.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Углеводороды
Углеводородами называют органические вещества, состоящие только из углерода и водорода. По составу их классифицируют на насыщенные и ненасыщенные, по строению — на алифатические, циклические и ароматические.
Алканами называют предельные алифатические углеводороды, отвечающие общей формуле CnH2n+2, в молекулах которых атомы углерода связаны между собой простой (одинарной) σ-связью.
Для алканов характерна изомерия углеродного скелета.
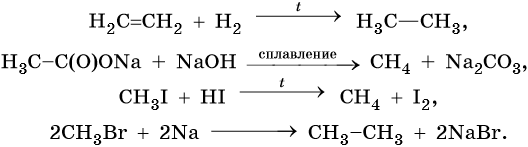
Способы получения алканов. Как правило, алканы получают из природного сырья, однако известно большое число синтетических методов их получения. Это реакции гидрирования алкенов и алкинов, декарбоксилирование натриевых или калиевых солей карбоновых кислот, восстановление йодалканов йодоводородом, реакция Вюрца:
Для алканов характерны реакции замещения, которые идут при нагревании или УФ-облучении. При этом происходит разрыв связи C—H с последующей заменой атома водорода на другой атом или группу атомов или же разрыв молекулы по связи C—С.
Большинство реакций алканов протекают по механизму радикального замещения SR. В этих реакциях реакционная способность атомов водорода убывает в ряду: третичные > вторичные > первичные.
Ниже приведены уравнения химических реакций, характерных для алканов.
1. Галогенирование:
Реакция идет на свету или при температуре 250— 400 °С.
Реакционная способность галогенов в этой реакции уменьшается в ряду F2 > Cl2 > Br2 > I2.
Реакции замещения в алканах протекают по радикальному механизму. При этом легче всего происходит замещение атома водорода, связанного с третичным углеродным атомом, затем — со вторичным и наконец — с первичным. Это объясняют значением энергии связей C–H, имеющих величину для первичной около 419 кДж/моль, вторичной — 393,6 кДж/моль и третичной — 372,6 кДж/ моль.
Наиболее широко известны реакции галогенирования алканов. Эти реакции идут на свету или при нагревании в присутствии инициаторов радикальных реакций. Рассмотрим механизм реакции на примере хлорирования метана.
На первой стадии этой реакции происходит распад молекулы хлора на два свободных радикала:
Cl:Cl → 2Cl• — зарождение, или инициирование цепи. Затем начинается рост цепи, связанный с взаимодействием свободного радикала с молекулой метана, что приводит к образованию новых радикалов:
Реакция заканчивается обрывом цепи, который наступает в результате взаимодействия между собой свободных радикалов:
Механизм реакции галогенирования был установлен академиком Н.Н. Семеновым.
2. Нитрование:
3. Термические превращения:
4. Окисление:
Каталитическое окисление бутана приводит к уксусной кислоте, а горение в кислороде — к углекислому газу и воде:
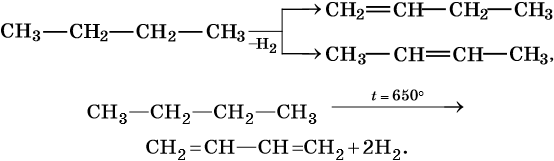
5. Дегидрирование:
Реакции дегидрирования (отщепления водорода) протекают по разным направлениям:
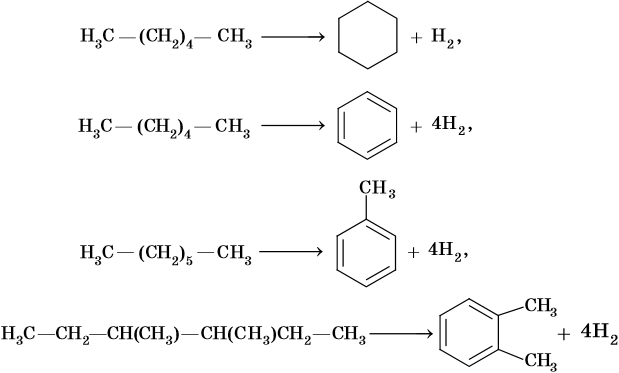
Реакции циклизации и ароматизации:
Последние две реакции идут при температурах 450–500 °С с использованием в качестве катализаторов оксидов хрома или алюминия.
Алициклическими называют углеводороды, которые содержат один или несколько циклов неароматического характера. По своим свойствам они схожи с соответствующими соединениями алифатического ряда. Термин «алициклические» означает «алифатические циклические» углеводороды. Несмотря на большое сходство между алифатическими и алициклическими соединениями, у последних имеются некоторые специфические свойства, обусловленные их циклической структурой. Общая формула гомологического ряда циклоалканов CnH2n.
Иногда циклоалканы называют нафтенами, т. к. производные циклопентана и циклогексана содержатся в некоторых сортах нефти.
Для гомологов и производных циклоалканов возможны следующие виды изомерии: изомерия, связанная с размером цикла, например, циклобутан является изомером метилциклопропана; изомерия положений заместителей в цикле; изомерия боковых цепей.
Циклопентан, циклогексан и их производные широко распространены в природе и составляют основную часть некоторых сортов нефти.
Низшие циклы синтезируют циклизацией дигалоидпроизводных, например:
Циклобутан и циклопентан получают циклизацией 1,4-дибромбутана и 1,5-дибромпентана под действием амальгамы лития. Циклогексан и его производные получают из нефти или гидрированием бензола и его производных.
Химические свойства циклоалканов во многом определяются размерами цикла. Наибольшей химической стойкостью обладают пяти- и шестичленные циклы. Циклопропан склонен к многочисленным реакциям раскрытия цикла.
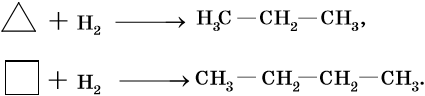
Гидрирование циклопропана и циклобутана идет над никелевым катализатором при температуре 80 и 120 °С соответственно. При этом образуются пропан и бутан.
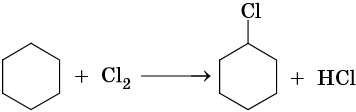
Циклопропановый цикл легко раскрывают при бромировании или гидробромировании, например:
В аналогичных условиях углеводороды от циклобутана до циклогексана вступают в реакции замещения:
Циклопропан используют в качестве анестезирующего средства. Циклогексан используют как растворитель. Окислением циклогексана получают циклогексанол C6H11OH, циклогексанон C6H10O и адиптиновую кислоту HOOC(CH2)4COOH. Циклогексанон является промежуточным продуктом при получении полиамидного волокна — капрона.
Алкенами, или олефинами, называют алифатические непредельные углеводороды, молекулы которых отвечают общей формуле CnH2n и имеют в своем составе одну двойную связь C=C. Родоначальником этого класса органических соединений является этилен CH2=CH2. Для алкенов характерна изомерия углеродного скелета, изомерия положения кратной связи, геометрическая изомерия, а также межклассовая изомерия с циклоалканами.
Способы получения алкенов. Этилен, пропилен и бутилены выделяют из газов нефтепереработки, образующихся при термическом крекинге. Алкены также образуются в большом количестве при пиролизе нефти.
Промышленным способом получения алкенов является дегидрирование алканов на катализаторе (K2O—Cr2O3—Al2O3), при температуре 560—620 °C из н-бутана образуются изомерные бутены. Еще легче этот процесс идет в случае изобутана:
Алкены получают дегидратацией спиртов при катализе серной или фосфорной кислотами, оксидом алюминия или хлоридом цинка:
При дегидратации спиртов атом водорода наиболее легко отщепляется от наименее гидрогенизированного атома углерода (правило Зайцева):
Алкены образуются при действии на галоидные алкилы спиртовой или измельченной твердой щелочи. Эта реакция дегидрогалогенирования также идет по правилу Зайцева:
Алкены можно получить обработкой цинковым или магниевым порошком вицинальных дигалоидалканов:
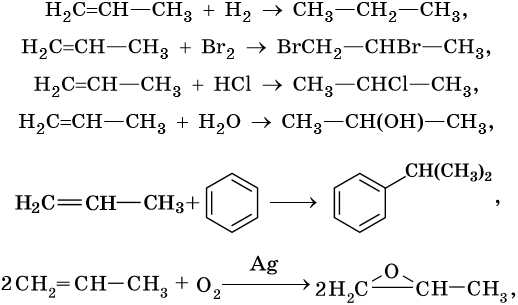
Алкены вступают в реакции соединения по двойной связи. Они протекают по механизму электрофильного присоединения, или AE. Присоединение галогеноводородов и воды к несимметричным алкенам идет по правилу Марковникова: атом водорода присоединяется к наиболее гидрогенизированному, т. е. связанному с наибольшим числом водородных атомов, атому углерода. По легкости присоединения к алкенам галогеноводороды можно расположить в ряд: HI > HBr > HCl > HF.
Ниже приведены реакции алкенов на примере этена и пропена:
Реакция гидратации катализируется кислотами.
Реакция алкилирования протекает между алканами и алкенами в присутствии катализаторов:
Кроме реакций соединения для алкенов возможны отдельные реакции замещения, которые протекают по радикальному механизму, а также реакции разложения:
C позиции электронной теории правило Марковникова объясняют так: под действием метильного радикала в молекуле пропилена происходит перераспределение электронной плотности электронного облака π-связи в сторону крайнего ненасыщенного атома углерода, в результате чего на атомах углерода, связанных двойной связью, возникают частичные заряды:
При взаимодействии такой молекулы с галогенводородом присоединение положительно заряженного иона водорода идет по атому углерода с частичным отрицательным зарядом, а отрицательно заряженного галогенидиона — по атому углерода с частичным положительным зарядом.
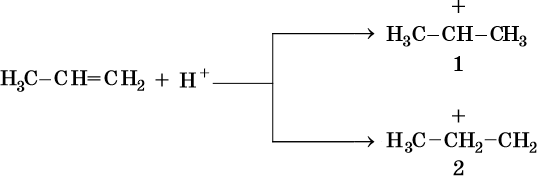
Другое объяснение правила Марковникова следующее. В результате электрофильного присоединения возможно образование двух различных карбокатионов: из-за положительного индуктивного эффекта двух метильных групп карбокатион 1 более стабилен, чем карбокатион 2.
Таким образом, реакции электрофильного присоединения по двойной связи идут в направлении образования наиболее устойчивого промежуточного карбокатиона.
Существуют исключения из правила Марковникова. Это присоединение бромоводорода к алкенам в присутствии органических пероксидов или кислорода. В этом случае из пропена и бромоводорода образуется 1-бромпропан (перекисный эффект Хараша). Подчеркнем особо: перекисный эффект имеет место только в случае реакции алкенов с бромоводородом. При присоединении к алкенам HCl, H2O, HI пероксиды не влияют на направление реакции, и она идет по правилу Марковникова.
Диеновыми углеводородами называют класс химических соединений, молекулы которых отвечают общей формуле CnH2n–2 и содержат в своем составе две двойные углерод-углеродные связи. Для диенов характерна изомерия углеродного скелета, изомерия положения кратных связей, геометрическая изомерия, а также межклассовая изомерия с ацетиленовыми углеводородами.
Способы получения диенов. Дивинил и изопрен выделяют из продуктов пиролиза нефти. Основным промышленным способом получения бутадиена-1,3 является дегидрирование бутан-бутеновой смеси над катализатором, состоящим из окиси хрома, нанесенной на окись алюминия.
Метод получения дивинила по С.В. Лебедеву заключается в дегидрировании-дегидратации этилового спирта над катализатором MoO — ZnO при 450 °С.
Диены, у которых двойные связи разделены более чем одной одинарной связью, в химическом отношении ведут себя подобно алкенам.
Диены, у которых двойные связи разделены одной простой связью, называют конъюгированными или сопряженными диенами. Эти соединения обладают специфическими химическими свойствами и имеют важное практическое значение.
Своеобразные химические свойства диенов проявляются в реакциях присоединения, которые идут не только по одной или двум отдельным двойным связям (1,2-присоединение), но и по противоположным концам молекулы (1,4-присоединение). Выход продуктов 1,2- или 1,4-присоединения определяется характером реагента и условиями реакции.
При низких температурах преобладают продукты 1,2-присоединения, при повышенных — 1,4-присоединения.
Полное бромирование бутадиена-1,3 приведет к 1,2,3,4-тетрабромбутану:
Неполное гидрирование диенов приводит к смеси алкенов, а при полном образуются алканы:
Окисление сопряженных диенов, в зависимости от используемого окислителя и условий проведения реакции, может протекать с образованием различных кислородсодержащих соединений. При частичном окислении в нейтральной среде образуется щавелевая кислота, а действие перманганата калия в кислой среде при нагревании приведет к полному окислению диена до углекислого газа и воды.
Ацетиленовыми углеводородами, или алкинами, называют класс органических соединений, которые соответствуют общей формуле CnH2n–2 и содержат в молекуле одну тройную связь. Родоначальником этого класса соединений является ацетилен, или этин, — HC≡CH. Для ацетиленовых углеводородов характерна изомерия углеродной цепи, изомерия положения кратной связи и межклассовая изомерия с диеновыми углеводородами.
Общим методом получения алкинов является реакция спиртовых растворов щелочи с дигалоидалканами, содержащими два атома галогена при одном атоме углерода или двух соседних атомах углерода:
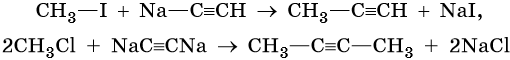
Производные ацетилена можно получить, действуя на его металлические производные галоидными алкилами:
Ацетилен получают действием воды на карбид кальция:
Кроме того, ацетилен получают термолизом метана и дегидрированием этилена:
Для алкинов характерны реакции соединения и некоторые реакции замещения, которые приведены ниже на примере ацетилена и пропина. Катализаторами для реакций гидрирования алкинов являются Pd или PbO. Следует отметить, что реакции галогенирования и гидрогалогенирования алкинов идут медленнее, чем с алкенами.
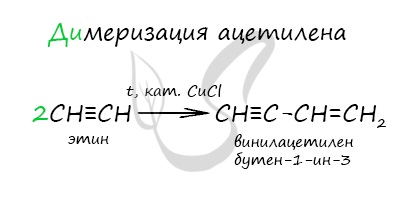
Реакции ди- и тримеризации:
Ароматическими углеводородами, или аренами, называют класс химических соединений, который отвечает общей формуле CnH2n–6 и имеет в своем составе устойчивую циклическую группировку (бензольное кольцо), обладающую особыми химическими свойствами.
Получение ароматических углеводородов. Основным природным источником ароматических углеводородов является нефть. Для получения гомологов бензола разработаны многочисленные синтетические методы.
Некоторые сорта нефти содержат достаточное количество ароматических углеводородов, которые выделяют простой перегонкой, пиролизом или каталитическим крекингом.
Синтетические методы — это ароматизация алканов, алкилирование бензола и т.д.
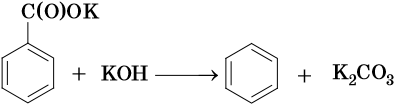
Так, например, бензол можно получить реакцией декарбоксилирования бензоата натрия или калия:
Для ароматических углеводородов наиболее характерны реакции замещения и некоторые реакции присоединения.
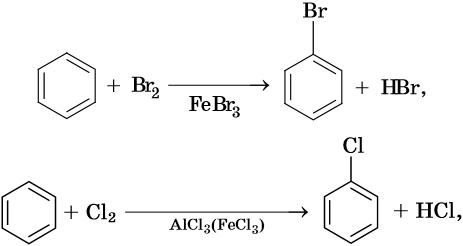
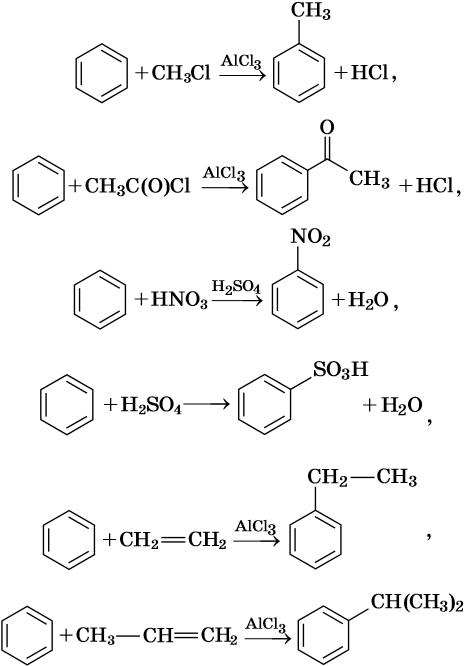
Как правило, все реакции замещения в ароматических соединениях протекают по электрофильному механизму SE. К таким реакциям относятся реакции алкилирования, галогенирования, нитрования, сульфирования, ацилирования и другие. Характерные химические свойства бензола:
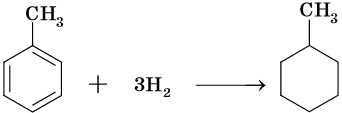
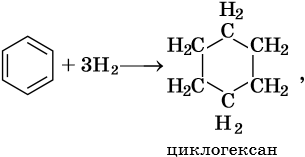
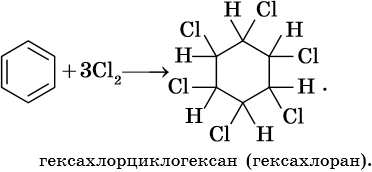
Гидрирование бензола до циклогексана идет при повышенной температуре, в присутствие катализатора (никель, платина), а хлорирование до гексахлорциклогексана — в газовой фазе под ультрафиолетовым излучением.
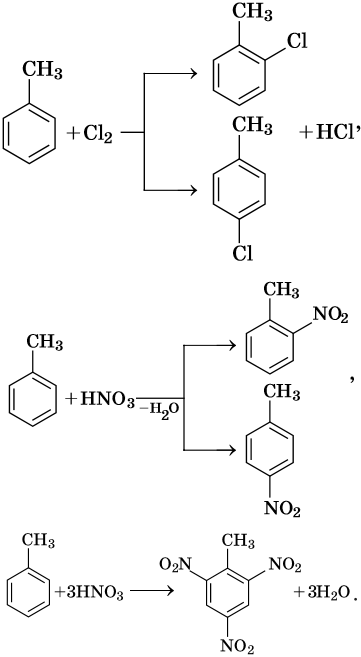
В молекуле толуола проявляется взаимное влияние метильного радикала на ароматическое ядро и ароматического ядра на метильный радикал. Толуол вступает в реакции замещения легче, чем бензол. При этом метильная группа ориентирует вхождение заместителей в орто— и пара-положения:
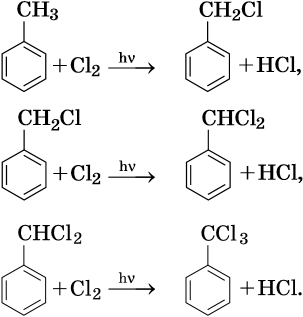
Галогенирование атомов водорода боковой цепи:
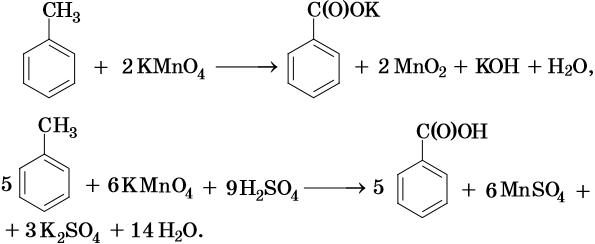
Окисление метильного радикала сильными окислителями, в зависимости от среды реакции, идет по разным направлениям:
В ходе реакций окисления алкилбензолов происходит окисление боковой цепи, а бензольное кольцо изменений не претерпевает:
Исключением являются третбутильные группы, связанные с бензольным кольцом — бензольное кольцо окисляется легче, чем эти группы.
При окислении жирноароматических соединений, содержащих ненасыщенные радикалы, соблюдаются общие закономерности, например:
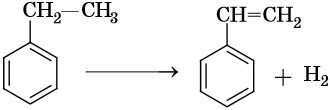
Этилбензол вступает в реакцию дегидрирования с образованием стирола:
Реакция протекает с высоким (92%) выходом при катализе оксидом цинка при температуре 600–650 °С.
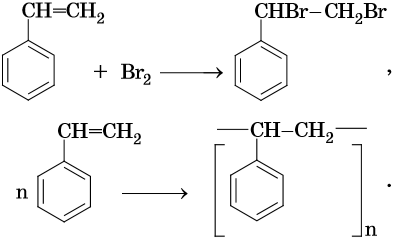
Стирол легко вступает в реакции по двойной связи и в реакции полимеризации и сополимеризации:
Свойства бутадиен-стирольных каучуков зависят от их состава. На их основе изготавливают шины и другие резинотехнические изделия.