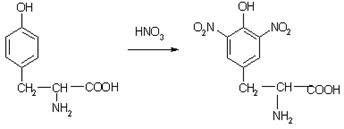
Что открывает ксантопротеиновая реакция
ЦВЕТНЫЕ И ИМЕННЫЕ КАЧЕСТВЕННЫЕ РЕАКЦИИ НА БЕЛКИ
История химии в школьном курсе
РЕАКЦИЯ ПИОТРОВСКОГО (БИУРЕТОВАЯ РЕАКЦИЯ)
В белках аминокислоты связаны друг с другом по типу полипептидов и дикетопиперазинов. Образование полипептидов из аминокислот происходит путем отщепления молекулы воды от аминогруппы одной молекулы аминокислоты и карбоксильной группы другой молекулы:
Образующаяся группа –С(О)–NН– называется пептидной группой, связь С–N, соединяющая остатки млекул аминокислот, – пептидной связью.
При взаимодействии дипептида с новой молекулой аминокислоты получается трипептид и т. д.
Дикетопиперазины образуются при взаимодействии двух молекул аминокислот с отщеплением двух молекул воды:
Дикетопиперазины были выделены из белков Н.Д.Зелинским и В.С.Садиковым в 1923 г.
Наличие в белке повторяющихся пептидных групп подтверждается тем, что белки дают фиолетовое окрашивание при действии небольшого количества раствора медного купороса в присутствии щелочи (биуретовая реакция).
Реакция идет по схеме:
Это реакция на цистеин и цистин. При щелочном гидролизе «слабосвязанная сера» в цистеине и цистине достаточно легко отщепляется, в результате чего образуется сероводород, который, реагируя со щелочью, дает сульфиды натрия или калия. При добавлении ацетата свинца(II) образуется осадок сульфида свинца(II) серо-черного цвета.
Описание опыта. В пробирку наливают 1 мл раствора цистина, прибавляют 0,5 мл 20%-го раствора гидроксида натрия. Смесь нагревают до кипения, а затем добавляют 0,5 мл раствора ацетата свинца(II). Наблюдается выпадение серо-черного осадка сульфида свинца(II):
Описание опыта. В пробирку наливают 5 капель 1%-го раствора глицина и прибавляют 1 каплю индикатора метилового красного. Раствор окрашивается в желтый цвет (нейтральная среда). К полученной смеси добавляют равный объем 40%-го раствора формальдегида (формалин). Появляется красное окрашивание (кислая среда):
Это реакция на аминокислоту глицин.
В таких солях ион меди координационными связями соединен с аминогруппами.
Описание опыта. В пробирку наливают 3 мл 3%-го раствора сульфата меди(II), добавляют несколько капель 10%-го раствора гидроксида натрия до образования голубого осадка. К полученному осадку гидроксида меди(II) приливают 0,5 мл концентрированного раствора глицина. При этом образуется темно-синий раствор глицината меди:
Описание опыта. В пробирку наливают 1 мл раствора тирозина и добавляют 0,5 мл концентрированной азотной кислоты. Смесь нагревают до появления желтой окраски. После охлаждения добавляют 1–2 мл 20%-го раствора гидроксида натрия до появления оранжевой окраски раствора:
Описание опыта. В пробирку наливают около
0,5 мл раствора уксуснокислого свинца и прибавляют раствор едкого кали до растворения образовавшегося осадка гидроксида свинца. В другую пробирку наливают
Триптофан, реагируя в кислой среде с альдегидами, образует окрашенные продукты конденсации. Например, с глиоксиловой кислотой (являющейся примесью к концентрированной уксусной кислоте) реакция протекает по уравнению:
По аналогичной схеме протекает и реакция триптофана с формальдегидом.
В ходе проведенного исследования мы выявили по литературным источникам имеющуюся информацию о цветных качественных реакциях на белковые аминокислоты; выполнили ряд перечисленных реакций и составили базу данных. Эта база может быть использована в школьной практике как в теоретическом плане, так и в практическом, т. к. мы приводим краткие, но подробные описания выполнения всех опытов.
Из предложенных 18 качественных реакций каждая практически осуществима в школьном курсе химии и имеет важное практическое значение. Сопровождение реакций химическими уравнениями конкретизирует и углубляет знания по биологической и органической химии, особенно знания учащихся специализированных биологических и химических классов.
Использованная литература
Ермаков А.Н., Арасимович В.В., Смирнова-Иконникова М.И., Мирри И.К. Методы биохимического исследования растений. М.,1952, 520 с.
Полянская А.С., Шевелева А.О. Методическая разработка по лабораторным работам: «Аминокислоты» и «Белки». Л., 1976, 37 с.
Пустовалова Л.М. Практикум по биохимии. 1999, 541 с.
Руководство к практическим занятиям по органической химии. Под ред. В.М.Родионова. М., 1954, 111 с.
Соловьев Н.А. Лабораторные работы по биологической химии. Методическая разработка. СПб., 1996, 70 с.
Филиппович Ю.Б., Егорова Т.А., Севастьянова Г.А. Практикум по общей биохимии. М., 1982, 311 с.
З.Саитов, С.В.Телешов, Б.Харитонцев,
секция «Юный химик» РХО им. Д.И.Менделеева (г. Тобольск)
КСАНТОПРОТЕИНОВАЯ РЕАКЦИЯ



Ксантопротеиновая реакция открывает наличие в белках циклических аминокислот – триптофана, фенилаланина, тирозина, содержащих в своем составе ароматическое ядро.
Реакция носит название от греч. слова Xanthos – желтый. Ряд белков при добавлении к ним концентрированной азотной кислоты при нагревании дают желтое окрашивание, которое может переходить в оранжевое в щелочной среде.
Реакция вызвана нитрованием бензольного ядра указанных циклических аминокислот и образованием нитросоединений желтого цвета.
Тирозин Динитротирозин (желт.цв.)
При подщелачивании возникает хиноидная структура, окрашенная в оранжевый цвет.
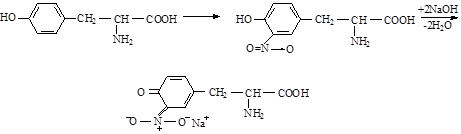
Аналогично протекает реакция нитрования триптофана.
Ксантопротеиновую реакцию дают почти все белки. Ксантопротеиновая реакция обуславливает появление желтого окрашивания при попадании концентрированной азотной кислоты на кожу, ногти. Эту реакцию могут давать и более простые ароматические соединения (например, фенолы).
Исключение составляют клупеин и сальмин (из группы протаминов) и желатина, в молекуле которых почти полностью отсутствуют ароматические аминокислоты.
Ход работы: К раствору белка 1 мл прилить 5-6 капель концентрированной азотной кислоты, белок выпадает в осадок. При подогревании (осторожно) раствор окрашивается в желтый цвет. После охлаждения в пробирку наливают по каплям 10% раствор едкого натра до появления оранжевого окрашивания вследствие образования натриевой соли динитротирозина.
КСАНТОПРОТЕИНОВАЯ РЕАКЦИЯ
Смотреть что такое «КСАНТОПРОТЕИНОВАЯ РЕАКЦИЯ» в других словарях:
ксантопротеиновая реакция — ksantoproteininė reakcija statusas T sritis chemija apibrėžtis Spalvinė baltymų reakcija su HNO₃. atitikmenys: angl. xanthoproteic reaction rus. ксантопротеиновая реакция … Chemijos terminų aiškinamasis žodynas
Ксантопротеиновая реакция — цветная качественная реакция (появление жёлтого окрашивания), которую дают растворы белка при кипячении с концентрированной азотной кислотой. После добавления концентрированной щёлочи жёлтое окрашивание переходит в оранжевое. Реакция… … Большая советская энциклопедия
ксантопротеиновая реакция — метод определения циклических аминокислот, основанный на способности тирозина, триптофана и фенилаланина давать желтое окрашивание при нагревании с концентрированной азотной кислотой; используется также для обнаружения белка … Большой медицинский словарь
КСАНТОПРОТЕИНОВАЯ ПРОБА — КСАНТОПРОТЕИНОВАЯ ПРОБА, или реакция Мульдера (Mulder), цветная реакция на белки, обусловленная присутствием в них ароматических (гл. обр. тирозин) и нек рых гетероциклических (триптофан) групп. К испытуемому веществу прибавляют концентрированной … Большая медицинская энциклопедия
ГИСТОЛОГИЧЕСКАЯ ТЕХНИКА — ГИСТОЛОГИЧЕСКАЯ ТЕХНИКА. Содержание: Методика гистологич. исследований. 242 Теоретические основы Г. т. 246 Гистохимия. 253 Краски, употребляемые в Г. т. 258 Гистологическая техник а техника изучения… … Большая медицинская энциклопедия
Мандаринаж — I см. также Печатание тканей. II Этим именем называется прием окрашивания шелка и шерсти в очень прочный и красивый желтый цвет нагреванием с азотной кислотой. В данном случае утилизируется характерная для всех протеиновых веществ так называемая… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Шерсть* — (сельскохоз.) Ш. в общежитии называется связное собрание тонких, мягких, извитых волокон. В таком смысле говорится как о растительной, так и животной Ш. Ниже будет рассмотрена только животная Ш. и главным образом Ш. овечья. Под Ш. овцы понимают… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Шерсть — (сельскохоз.) Ш. в общежитии называется связное собрание тонких, мягких, извитых волокон. В таком смысле говорится как о растительной, так и животной Ш. Ниже будет рассмотрена только животная Ш. и главным образом Ш. овечья. Под Ш. овцы понимают… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
АЗОТНАЯ КИСЛОТА — АЗОТНАЯ КИСЛОТА, или крепкая водка, HNOj, в виде аммониевых, щелочных и щелочно земельных солей, называемых селитрами, встречается повсеместно в почве; известны (единственные) залежи селитры в Чили. А. к. получена Гебером в VIII в.; состав А. к.… … Большая медицинская энциклопедия
Лабораторная работа №1
Лабораторная работа №1
ХИМИЯ ПРОСТЫХ БЕЛКОВ.
ЦВЕТНЫЕ РЕАКЦИИ НА БЕЛКИ И АМИНОКИСЛОТЫ
Белки представляют собой высокомолекулярные полимерные органические соединения, построенные из остатков различных α-аминокислот, соединенных ковалентной пептидной связью.
Присутствие белка в растворах можно обнаружить с помощью цветных реакций, обусловленных наличием в белке аминокислот, их специфических групп и пептидных связей. Существуют универсальные цветные реакции, т. е. на все белки (биуретовая и нингидриновая), и специфические, т. е. на определенные аминокислоты (ксантопротеиновая, Миллона, Фоля и др.).
На основании некоторых цветных реакций разработаны методы количественного определения белков и аминокислот, которые широко используются в биохимических лабораториях.
Цель: Ознакомиться с универсальными цветными реакциями на белки и специфическими реакциями на отдельные аминокислоты, содержащиеся в белковых растворах.
Работа 1. Биуретовая реакция на пептидную связь (Пиотровского)
Биуретовая реакция обусловлена наличием в белке пептидных связей, которые в щелочной среде образуют с сернокислой медью комплексы фиолетового цвета с красным или синим оттенком. Группа, образующая пептидную связь, в щелочной среде присутствует в своей таутомерной енольной форме:
При избытке щелочи происходит диссоциация ОН-группы, появляется отрицательный заряд, с помощью которого кислород взаимодействует с медью. Возникает солеобразная связь. Кроме того, медь образует дополнительные координационные связи с атомами азота, участвующими в пептидной связи, путем использования их электронных пар. Возникающий таким образом комплекс очень стабилен. Интенсивность окраски комплекса зависит от концентрации белка и количества медной соли в растворе.
Исследуемый материал: раствор яичного белка, раствор растительного белка, 1% раствор желатина.
Реактивы: 10% раствор NaOH, 1% раствор CuSO4.
Оборудование: пробирки, капельницы.
Ход работы. К 5 каплям водного раствора белка добавляют 5 капель 10% раствора NaOH и 2 капли 1% раствора CuSO4. Содержимое перемешивают. Оно приобретает сине-фиолетовый цвет. Нельзя добавлять избыток CuSO4, так как синий осадок маскирует характерное фиолетовое окрашивание биуретового комплекса.
Работа 2. Нингидриновая реакция на α-аминокислоты
Белки, полипептиды и свободные α-аминокислоты дают синее или фиолетовое окрашивание с нингидрином. При нагревании белка с водным раствором нингидрина аминокислоты окисляются и распадаются, образуя СО2, NH3 и соответствующий альдегид. Нингидрин, являясь сильным окислителем, вызывает окислительное дезаминирование α-аминокислоты, приводящее к образованию аммиака, двуокиси углерода, соответствующего альдегида и восстановленной формы нингидрина. Нингидрин восстанавливается и связывается со второй молекулой нингидрина посредством молекулы аммиака, образуя продукты конденсации, окрашенные в синий, фиолетовый, красный, а в случае пролина – в желтый цвет.
Опыт № 2. Ксантопротеиновая реакция
Реакция получила название ксантопротеиновой от греческого хаnthos − желтый. Реакция обеспечивает появление желтого окрашивания при попадании концентрированной озотной кислоты на кожу, ногти и т.п. Такую реакцию дают и более простые ароматические соединения, например фенолы. Желатин и др. протеины дают отрицательную реакцию, т. к. в них отсутствуют ароматические аминокислоты.
Таким образом, ксантопротеиновая реакция доказывает присутствие в белковых биополимерах ароматических аминокислот: триптофана, фенилаланина, тирозина:






 |
 |
 |








пропионовая кислота) пропионовая кислота)

 |


При обработке раствора белка концентрированной азотной кислотой появляется желтое окрашивание (нитрование), которое при добавлении щелочи переходит в оранжевое.
Химизм реакции нитрования с образованием нитросоединений следующий:


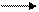








 |
 |


Тирозин Динитротирозин (желтого цвета)
В щелочной среде нитропроизводные аминокислот образуют соли хиноидной структуры, окрашенные в оранжевый цвет.
Задания: 1. Написать уравнение реакции взаимодействия тирозина с концентрированной азотной кислотой.
2. Указать, какие α-аминокислоты будут давать подобную реакцию.
Опыт № 3. Реакция на аминокислоты, содержащие слабосвязанную серу (Фоля)
Сульфогидридные группы SH в белке или пептиде подвергаются щелочному гидролизу, в результате которого происходит отщепление серы в виде нерастворимого сульфида свинца, который имеет черный цвет.





плюмбит натрия черный осадок
Метионин (СН3SСН2СН2СН(NH)2CООН, α-аминометилмеркапто- масляная кислота) хотя и является аминокислотой, содержащей серу, в отличие от цистина, этой реакции не дает, т. к. сера в нем связана прочно.
Порядок выполнения работы
В две пробирки наливают по 10 капель раствора ацетата свинца и по каплям в каждую из них прибавляют раствор гидроксида натрия до растворения первоначально образовавшегося осадка. В одну пробирку добавляют небольшой кусочек шкурки без волос (0,5 см), в другую − немного волос меха. Смеси кипятят 1−2 мин и наблюдают за изменением их цвета и выпадением черного осадка РdS в пробирке с волосом меха. Сделайте вывод.
То же самое проделайте с кусочком шерстяной ткани светлого тона.
Оформление лабораторной работы
При проведении цветных реакций на белковые биополимеры и составляющие их аминокислоты необходимо составить следующую таблицу (табл. 3).
Цветные реакции на белковый биополимер и аминокислоты
| Название реакции | Применяемые реактивы | Характеристика окрашивания | Что открывает данная реакция, ее механизм |
| Биуретовая и т. д. |
После каждой реакции сделать вывод о ее специфичности для исследуемого вещества в присутствии соответствующих функциональных групп.
Задание. Указать, какие α-аминокислоты в составе белка можно открыть данной качественной реакцией.
Контрольные вопросы
1. Дайте определение белков и пептидной связи в них.
2. Чем по белковому составу отличается белок шерсти кератин от белка кожи коллагена?
3. Что такое биополимер? Какие известные биополимеры Вы знаете?
4. Что такое денатурация белков? Назовите денатурирующие факторы.
5. Напишите схемы реакций взаимодействия фенилаланина, серина, глицина с сульфатом меди (II) в щелочной среде, этиловым спиртом в кислой среде, формальдегидом.
6. Приведите синтез дипептидов Ала-Гли, Вал-Лей, Иле-Три.
ТЕМА 26 БЕЛКИ КОЖИ, ШЕРСТИ И ШЕЛКА
Белки (протеины) – высокомолекулярные природные органические соединения, построенные из остатков α-аминокислот, связанных амидными (пептидными) связями соединения.
Белки не устойчивы к различным воздействиям. Различают белок нативный (т. е. содержащийся в живом организме) и измененный белок (в выделенном состоянии).
Независимо от источника происхождения белки содержат С, О, Н, N, незначительное количество S, иногда в их состав входят P, Fe, Cu, J, Zn, Br, Mn, Ca и др.
Обычно М колеблется в пределах от 5000–7000000 у.е. Белки ограничено растворимы в воде.
В состав шкуры входит вода (50–70 %), минеральные вещества (0,35–0,50 %), жиры, углеводы, азотсодержащие соединения и белки.
Важнейшими белками являются биополимерные волокнистые белки – коллаген, кератин, эластин, ретикулин. Кроме того в шкуре содержатся глобулярные белки – альбумины, глобулины и сложные белки. Средний белковый состав шкуры, процент от массы сухой дермы (без волосяного кератинового белка): коллаген – 64–80; эластин – 0,3–1,0; альбумин – 1,0–3,5; глобулин – 1,0–3,2; сложные белки – 0,5–3,5.
Волокнистый коллаген дермы шкур составляет соединительную ткань. Основные его свойства: сопротивление изменению длины, химическая инертность, при нагревании с водой расщепляется в желатин.
Характеристики очищенного коллагена представлена в табл. 4.
Характеристики очищенного коллагена
| Показатель | Значение |
| рН водного экстракта | 6,0–7,0 |
| Изоэлектрическая точка (рН) | 6,0–7,5 |
| Содержание золы, % | менее 0,1 |
| Содержание амидного азота, % от общего количества азота | около 3,8 |
Элементарный состав коллагена представлен в табл. 5.
| Атом | Содержание, % |
| Углерод | 50,2–51,5 |
| Азот | 17,0–18,1 |
| Водород | 6,4–6,5 |
| Кислород | 25,1–26,1 |
| Сера | 0,1–0,3 |
Аминокислотный состав коллагена представлен в табл. 6.
Аминокислотный состав коллагена
| Аминокислоты | Содержание г/100 сухого биополимера | Аминокислоты | Содержание г/100 сухого биополимера |
| Глицин | 26,57 | Лизин | 3,96 |
| Аланин | 10,32 | Оксилизин | 1,15 |
| Валин | 2,46 | Гистидин | 0,7 |
| Лейцин | 3,73 | Серин | 4,27 |
| Изолейцин | 1,88 | Треонин | 2,26 |
| Пролин | 14,42 | Цистин | — |
| Оксиглорин | 12,83 | Метионин | 0,97 |
| Аспарагиновая кислота | 6,95 | Фенинлаланин | 2,35 |
| Глутаминовая кислота | 11,16 | Тирозин | 0,99 |
| Аргинин | 8,22 | Триптофан | — |
Первичная структура коллагена – полипептидная цепь из 18 α-аминокислот, из них на долю глицина приходится 32,9 %, доля остальных аминокислотных остатков составляет от 0,4–13,3 %.
Все аминокислотные остатки имеют одинаковую протяжность вдоль полипептидной цепи, масса же их значительно различается в связи с различием боковых цепей.
В коллагене имеются четыре структуры возрастающей степени сложности и разных уровней организации. Структуру коллагена подразделяют на первичную, вторичную, третичную и четвертичную.
Коллаген содержит 50–80 % воды от его массы. Вода гидратационная, связана межмолекулярными силами. Гидроксильные группы коллагена присоединяют до 2–3 молекул воды, карбоксильные – 3–4, аминогруппы – 1–2. Вода набухания составляет 230–350 % от веса сухого коллагена. Фибриллы набухают, укорачиваются.
Температура сваривания ≈ 65 °С. В результате сваривания химический состав коллагена остается прежним, но в структуре происходят изменения − укорачивание пучков фибрилл, обезвоживание, разрыв ММС. Сухой коллаген способен свариваться, т. е. сверхсокращаться (t = 120 °С).
В растворах сильных кислот и щелочей коллаген сильно набухает. Затем идет разрушение поперечных меж- и внутримолекулярных связей, иногда идет деполимеризация. При облучении γ-лучами происходит структурирование коллагена, а затем его деструктурирование.
Эластин – основной белок эластиновых волокон соединительной ткани, его всего
1 % от массы коллагена. Основное его свойство – высокая эластичность. Он состоит из 15 аминокислот, где до 90 % –остатки от неполярных аминокислот (с неполярными боковыми цепями). Структура эластина аморфна. Его высокая эластичность связана с конформацией его цепей и их беспорядочным расположением.
Длинные молекулярные цепи связаны редкими ММС. Поперечных связей очень мало. Эластичность и его стабильность объясняются свертыванием его спиральных цепей путем их стяжения, при этом получается сетчатая структура с низкой степенью упорядоченности.
По свойствам эластин значительно отличается от коллагена. Он устойчив к действию горячей воды, не образует клея, более устойчив к действию кислот, щелочей, ферментов. При длительном (40 час) кипячении в большом количестве 40 %-го раствора мочевины эластин полностью растворяется.
Ретикулин – основная составная часть ретикулиновых волокон, встречающихся в соединительных тканях в виде сетки из очень тонких фибрилл. В шкуре его очень мало.
Ретикулин– аргирофильный белок (окрашивающий серебром). В ретикулине 50 % углеводов и липидов (от 10–20 %). Углеводы представлены глюкозой, галактозой, маннозой и фукозой.
Ретикулин отличается от коллагена, главным образом, количественным остатком. Он содержит меньше азота и больше серы по сравнению с коллагеном. Ретикулин состоит из 20 тех же аминокислот, что и коллаген, но в другом количественном соотношении.
В отличие от эластина ретикулин содержит больше полярных кислот. Он состоит из фибрилл. По строению сходен с коллагеном. Ретикулин очень устойчив к действию горячей воды, растворов кислот и щелочей и некоторых ферментов. Сульфид натрия вызывает значительные изменения в ретикулине.
В шкуре кроме коллагена, эластина, ретикулина содержатся еще глобулярные белки: альбумины – 1–3,5 %, глобулины – 1–3,2 % и сложные белки – 0,5–3,5 %.
Альбумины содержатся в межволоконном веществе. Состав их мало изучен. Характерная особенность – содержат серу. Они растворимы в воде, при нагревании коагулируют. При отмоке почти полностью удаляются.
Глобулины содержатся там же, где альбумины, они всегда вместе. Состав мало изучен. М ≈ 150000–170000. Глобулины в воде не растворяются, но растворяются в растворах нейтральных солей, слабых растворах кислот и щелочей. При нагревании они осаждаются лучше, чем альбумины. Они удаляются из шкуры еще при их консервировании.
Гликопротеидыэкстрагируют полунасыщенным раствором Ca(OH)2. Комплексы белков с мукополисахаридами – мукоиды входят в состав межволоконного вещества (50–85 % углеводов).
Фосфоропротеиды находятсяв толще шкуры, в подкожной клетчатке, растворимы в слабых щелочах.
Липопротеиды и хромопротеиды входят в состав подкожной клетчатки.
Кератин входит в состав рогов. Отсюда и его название «keras», что по-гречески – «рог». Кератин отличается от других белков содержанием большого количества цистина, а следовательно, серы. Чем меньше в кератине цистина, тем он мягче, его М = 60000–650000.
Кератин содержит в своем составе 20 аминокислотных остатков.
Волокна шерсти обладают фрикционными свойствами. Максимальное трение наблюдается при движении в направлении от корневого к верхушечному концу.
Волокна волос обладают способностью к свойлачиванию. Волокна шерсти можно растянуть при повышении температуры и влажности на 100 % (переход α-формы в β-), а в сухом состоянии – на 30 %.
На прочность сильно влияет длина главных молекулярных цепей. Прочность волокон кератина в мокром состоянии снижается почти пропорционально уменьшению содержания цистина. Прочность сухих волос значительно больше, чем мокрых. Кератин более устойчив к действию кислот, чем щелочей.
Волокна шерсти очень хорошо поглощают воду. Гидратация и набухание происходят внутри волокна. Многие реагенты вызывают разрушение дисульфидных связей: вода, кислоты, щелочи, окислители, восстановители, формальдегид, соли металлов, красители, ферменты.
Волокна шерсти в сухом состоянии более прочны, т. к. вода вызывает набухание и изменение межмолекулярных сил. При сухом нагревании волос менее подвержен изменениям, чем при нагревании в воде. При t°= 120 °в течение 24 часов он сохраняет все свои химические и физические свойства. При t°> 160 °происходит переход от α- в β-форму. При t°= 180–200 °резко снижается прочность.