Что открыл томсон в химии
Джозеф Томсон Биография и вклад в науку и химию
Джозеф Джон Томсон Он был выдающимся химиком для различных вкладов, таких как открытие электрона, его атомная модель, открытие изотопов или эксперимент с катодными лучами.
Он родился в Cheetam Hill, округ Манчестер, Англия, 18 декабря 1856 года. Также известен как «J.J.» Томсон, он изучал инженерию в Оуэнс-колледже, в настоящее время является частью Манчестерского университета, а затем и математику в Кембридже.
В 1890 году Дж. Дж. Томсон женился на Розе Элизабет Пейджет, дочери врача сэра Эдварда Джорджа Пейджета, с которым у меня было двое детей: девочка по имени Джоан Пейджет Томсон и мальчик Джордж Пейджет Томсон.
Последний станет известным ученым, получив в 1937 году Нобелевскую премию по физике за работу с электронами..
С юных лет Томсон сосредоточил свои исследования на структуре атомов, открыв, таким образом, существование электронов и изотопов среди многих других вкладов..
В 1906 году Томсон получил Нобелевскую премию по физике «в знак признания большой заслуги его теоретических и экспериментальных исследований в области проводимости электричества через газы», а также многие другие награды за свою работу. (1)
В 1908 году он был посвящен в рыцари британской короной и служил почетным профессором физики в Кембридже и в Королевском институте в Лондоне..
Он умер 30 августа 1940 года в возрасте 83 лет в городе Кембридж, Великобритания. Физик был похоронен в аббатстве Вестминстер, недалеко от гробницы сэра Исаака Ньютона. (2)
Основные вклады Томсона в науку
Открытие электрона
В 1897 году J.J. Томсон обнаружил новую частицу легче водорода, которая была крещена «электроном».
Водород считался единицей измерения атомного веса. До этого атом был наименьшим делением материи.
В этом смысле Томсон был первым, кто открыл отрицательно заряженные корпускулярные субатомные частицы..
Атомная модель Томсона
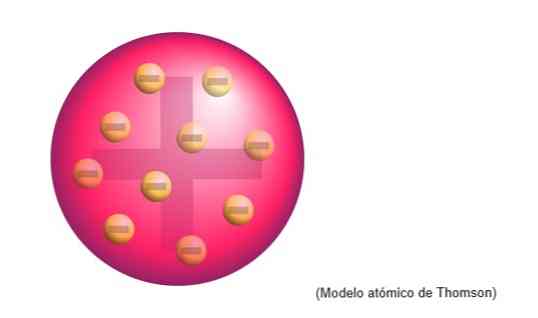
Атомная модель Томсона была структурой, которую английский физик приписал атомам. Для ученого атомы были сферой положительного заряда.
Там были погружены отрицательно заряженные электроны, равномерно распределенные по этому положительно заряженному облаку, нейтрализуя положительный заряд массы атома.
Эта новая модель заменяет модель, разработанную Далтоном, и позже она будет опровергнута Резерфордом, учеником Томсона в Кавендишских лабораториях Кембриджа..
Разделение атомов
Томсон использовал положительные или анодные лучи для разделения атомов разной массы. Этот метод позволил ему рассчитать электричество, переносимое каждым атомом, и количество молекул на кубический сантиметр..
Будучи способным делить атомы различной массы и заряда, физик обнаружил существование изотопов. Таким образом, благодаря изучению положительных лучей, он сделал большой шаг вперед в направлении масс-спектрометрии..
Открытие изотопов
Джей-Джей Томсон обнаружил, что ионы неона имеют разные массы, то есть разные атомные массы. Так Томсон показал, что у неона есть два подтипа изотопов: неон-20 и неон-22..
Изотопы, изученные по сей день, являются атомами одного и того же элемента, но их ядра имеют разные массовые числа, так как они состоят из разных количеств нейтронов в их центре.
Эксперименты с катодными лучами
Когда отрицательный электрод, или также называемый катодом, нагревается, он излучает излучение, направленное к положительному электроду или аноду, по прямой линии, если на этом пути нет магнитного поля..
Если стенки стекла трубки покрыты люминесцентным материалом, попадание катодов в этот слой создает проекцию света.
Томсон изучил поведение катодных лучей и пришел к выводу, что лучи распространяются по прямой линии..
Также, что эти лучи могли отклоняться от их траектории присутствием магнита, то есть магнитного поля. Кроме того, лучи могли перемещать лопасти с силой массы циркулирующих электронов, демонстрируя тем самым, что электроны имели массу.
Джей-Джей Томсон экспериментировал с изменением газа внутри электронно-лучевой трубки, но поведение электронов не менялось. Также катодные лучи согревали предметы, попавшие между электродами.
В заключение Томсон показал, что катодные лучи оказывают световое, механическое, химическое и тепловое воздействие..
Катодно-лучевые трубки и их световые свойства были трансцендентными для более позднего изобретения лампового телевидения (CTR) и видеокамер..
Масс-спектрометр
Джей-Джей Томсон создал первый подход к масс-спектрометр. Этот инструмент позволил ученому изучить отношение массы к заряду электронно-лучевых трубок и измерить, насколько они отклоняются под воздействием магнитного поля и количества энергии, которую они несут..
В результате этого исследования он пришел к выводу, что катодные лучи состоят из отрицательно заряженных корпускул, которые находятся внутри атомов, таким образом, постулируя делимость атома и порождая фигуру электрона..
Аналогичным образом, достижения в области масс-спектрометрии продолжались до сегодняшнего дня, развиваясь различными способами для отделения электронов от атомов..
Кроме того, Томсон первым предложил первый волновод в 1893 году. Этот эксперимент состоял в распространении электромагнитных волн в контролируемой цилиндрической полости, который был впервые проведен в 1897 году лордом Рэлеем, еще одной Нобелевской премией по физике..
Волноводы будут широко использоваться в будущем, даже сегодня, для передачи данных и волоконной оптики..
Наследие Томсона
Томсон (Th) был создан как единица измерения масс-нагрузки в масс-спектрометрии, предложенная химиками Куксом и Роквудом в честь Томсона..
Эта методика позволяет определить распределение молекул вещества по его массе и, распознавая его, которые присутствуют в образце вещества.
Джозеф Джон Томсон
английский физик, открывший электрон, Нобелевский лауреат

Джозеф Томсон был одним из ярчайших физиков-классиков, ему принадлежит колоссальная роль в формировании большой международной школы физиков. За научные заслуги он был награжден медалями Франклина, Фарадея, Юза, Копли и другими наградами. В 1908 году ему было пожаловано дворянство, он являлся членом Академий наук многих стран.
Джозеф Джон Томсон (англ. Joseph John Thomson) родился 18 декабря 1856 года в пригороде Манчестера Читем-Хилле. В возрасте 14 лет его определили в Оуэнс-колледж (ныне Манчестерский университет), а затем он продолжил образование в Тринити-колледже Кембриджского университета. Именно тогда Томсон увлекся физикой и математикой, а важную роль в его карьере сыграли курсы экспериментальной физики при колледже.
В 1880 году он окончил обучение, получив степень бакалавра по математике, и уже на следующий год был избран членом ученого совета Тринити-колледжа и начал работать в Кавендишской лаборатории в Кембридже. Первая статья Томсона, опубликованная в 1880 году, была посвящена электромагнитной теории света. В следующем году появились еще две работы.
Научные успехи Джозефа были высоко оценены руководителем лаборатории Кавендиша Рэлеем. Уходя в 1884 году с поста директора, он рекомендовал своим преемником Томсона, который с этого времени стал руководителем Кавендишской лаборатории и одновременно был профессором Кембриджского университета и Королевского института в Лондоне.
Наибольшую известность Томсону принесли его исследования, связанные с открытием электрона в 1897 году. Занимаясь изучением прохождения электрического тока через разреженные газы, он не только открыл электрон, но и определил его заряд, а также впервые измерил отношение заряда электрона к массе, разработал теорию движения электрона в магнитном и электрическом полях. За открытие электрона Томсон в 1906 году был удостоен Нобелевской премии по физике.
Томсон – один из основоположников классической электронной теории металлов. Им получено выражение для эффективного сечения рассеяния электромагнитных волн свободными электронами (формула Томсона). Эта формула и поныне играет видную роль в физике элементарных частиц. Важна роль ученого в открытии фотоэффекта и термоэлектронной эмиссии, а его исследования «каналовых» лучей легли в основу масс-спектрометрии.
Томсон дал объяснение непрерывного спектра рентгеновского излучения, установил природу положительных ионов, разработал так называемый метод парабол для измерения отношения заряда частицы к ее массе, который сыграл большую роль в исследовании изотопов.
В 1918 году Джозеф вышел в Кавендише в отставку, передав лабораторию своему ученику Э.Резерфорду, и возглавил Тринити-колледж в Кембридже.
Большое значение имела не только научная, но и организационная деятельность Томсона. Кавендишская лаборатория за время, когда он ее возглавлял, превратилась в ведущий исследовательский физический центр и стала научной школой для многих физиков-экспериментаторов. Там под его руководством работали крупнейшие ученые – Э.Резерфорд, Ч.Вильсон, Ф.Астон, У.Ричардсон, Ч.Баркла, П.Ланжевен, Д.Тейлор, Э.Эпплтон и другие.
Томсон был женат на Розе Пейджет, у них были сын и дочь. Сын Томсона Джордж Пейджт также со временем стал Нобелевским лауреатом по физике (в 1937 году за экспериментальное открытие дифракции электронов на кристаллах).
Умер Джозеф Джон Томсон 30 августа 1940 года в Кембридже, был похоронен в Вестминстерском аббатстве в Лондоне.
Джозеф Томсон: биография и вклад в науку и химию
Содержание:
Джозеф Джон Томсон Он был выдающимся химиком, внесшим различные вклады, такие как открытие электрона, его атомной модели, открытие изотопов или эксперимент с катодными лучами.
В 1890 году Дж. Дж. Томсон женился на Роуз Элизабет Пэджет, дочери врача сэра Эдварда Джорджа Пэджета, от которой у него было двое детей: девочка по имени Джоан Пэджет Томсон и мальчик Джордж Пэджет Томсон.
Последний стал известным ученым, получив в 1937 году Нобелевскую премию по физике за свои работы с электронами.
С юных лет Томсон сосредоточил свои исследования на структуре атомов, открыв, таким образом, существование электронов и изотопов, среди многих других вкладов.
В 1906 году Томсон получил Нобелевскую премию по физике «в знак признания огромной заслуги его теоретических и экспериментальных исследований по проводимости электричества через газы», среди многих других наград за свою работу. (1)
В 1908 году он был посвящен в рыцари британской короны и был почетным профессором физики в Кембридже и Королевском институте в Лондоне.
Он умер 30 августа 1940 года в возрасте 83 лет в городе Кембридж, Соединенное Королевство. Похоронен физик в Вестминстерском аббатстве, недалеко от могилы сэра Исаака Ньютона. (2)
Основной вклад Томсона в науку
Открытие электрона
В 1897 году Дж. Дж. Томсон открыл новую частицу легче водорода, которую назвали «электроном».
Водород считался единицей измерения атомного веса. До этого момента атом был самым маленьким делением материи.
В этом смысле Томсон первым открыл отрицательно заряженные корпускулярные субатомные частицы.
Атомная модель Томсона
Атомная модель Томсона была структурой, которую английский физик приписал атомам. Для ученого атомы были сферой положительного заряда.
Там электроны с отрицательным зарядом, равномерно распределенные на облаке положительного заряда, были встроены, то есть нейтрализовали положительный заряд массы атома.
Эта новая модель заменяет модель, разработанную Далтоном, и позже будет опровергнута Резерфордом, учеником Томсона из Кавендишских лабораторий в Кембридже.
Разделение атома
Томсон использовал положительные или анодные лучи для разделения атомов разной массы. Этот метод позволил ему рассчитать электричество, переносимое каждым атомом, и количество молекул на кубический сантиметр.
Имея возможность разделять атомы разной массы и заряда, физик обнаружил существование изотопов. Таким же образом, изучая положительные лучи, он сделал большой шаг вперед в масс-спектрометрии.
Открытие изотопов
J.J. Томсон обнаружил, что ионы неона имеют разную массу, то есть разную атомную массу. Так Томсон показал, что у неона есть два подтипа изотопов: неон-20 и неон-22.
Изотопы, изучаемые по сей день, представляют собой атомы одного и того же элемента, но их ядра имеют разные массовые числа, поскольку они состоят из разного количества нейтронов в своем центре.
Электронно-лучевые эксперименты
Когда отрицательный электрод, или также называемый катодом, нагревается, он испускает излучение, которое направлено к положительному электроду или аноду по прямой линии, если на этом пути нет магнитного поля.
Если стеклянные стенки трубки покрыты флуоресцентным материалом, удары катодов об этот слой создают проекцию света.
Томсон изучил поведение катодных лучей и пришел к выводу, что лучи движутся по прямым линиям.
Кроме того, эти лучи могут отклоняться с их пути из-за наличия магнита, то есть магнитного поля. Кроме того, лучи могли перемещать лопасти с силой массы циркулирующих электронов, тем самым демонстрируя, что электроны имеют массу.
J.J. Томсон экспериментировал с изменением содержания газа в электронно-лучевой трубке, но не менял поведение электронов. Также катодные лучи нагревали предметы, которые попадали между электродами.
В заключение Томсон показал, что катодные лучи обладают световыми, механическими, химическими и тепловыми эффектами.
Электронно-лучевые трубки и их световые свойства сыграли решающую роль в последующем изобретении трубочного телевидения (CTR) и видеокамер.
Масс-спектрометр
J.J. Томсон создал первый подход к Масс-спектрометр. Этот инструмент позволил ученому изучить соотношение массы / заряда электронно-лучевых трубок и измерить, насколько они отклоняются под действием магнитного поля и количество энергии, которое они переносят.
В ходе этого исследования он пришел к выводу, что катодные лучи состоят из отрицательно заряженных частиц, находящихся внутри атомов, тем самым постулируя делимость атома и создавая фигуру электрона.
Кроме того, достижения в масс-спектрометрии продолжаются и по сей день, развиваясь в различные методы отделения электронов от атомов.
Более того, Томсон был первым, кто предложил первый волновод в 1893 году. Этот эксперимент заключался в распространении электромагнитных волн внутри контролируемой цилиндрической полости, который был впервые проведен в 1897 году лордом Рэлеем, другим лауреатом Нобелевской премии по физике.
Волноводы будут широко использоваться в будущем, даже сегодня с передачей данных и волоконной оптикой.
Наследие Томсона
Томсон (Th) был установлен как единица измерения массового заряда в масс-спектрометрии, предложенная химиками Куком и Роквудом в честь Томсона.
Этот метод позволяет определить распределение молекул вещества по их массе и по этому распознать, какие из них присутствуют в образце вещества.
Формула Томсона (Th):
Выдающиеся работы
Ссылки
Саркодинос: характеристики и классификация
51 лучшая экологическая фраза (короткометражка)
Открытие электрона
На протяжении всей второй половины XIX века физики активно изучали феномен катодных лучей. Простейший аппарат, в котором они наблюдались, представлял собой герметичную стеклянную трубку, заполненную разреженным газом, в которую с двух сторон было впаяно по электроду: с одной стороны катод, подключавшийся к отрицательному полюсу электрической батареи; с другой — анод, подключавшийся к положительному полюсу. При подаче на катодно-анодную пару высокого напряжения разреженный газ в трубке начинал светиться, причем при низких напряжениях свечение наблюдалось лишь в области катода, а при повышении напряжения — внутри всей трубки; однако при откачивании газа из трубки, начиная с какого-то момента, свечение исчезало уже в области катода, сохраняясь около анода. Это свечение ученые и приписали катодным лучам.
К концу 1880-х годов дискуссия о природе катодных лучей приняла острый полемический характер. Подавляющее большинство видных ученых немецкой школы придерживалось мнения, что катодные лучи представляют собой, подобно свету, волновые возмущения невидимого эфира. В Англии же придерживались мнения, что катодные лучи состоят из ионизированных молекул или атомов самого газа. У каждой стороны имелись веские доказательства в пользу своей гипотезы. Сторонники молекулярной гипотезы справедливо указывали на тот факт, что катодные лучи отклоняются под воздействием магнитного поля, в то время как на световые лучи магнитное поле никак не воздействует. Следовательно, они состоят из заряженных частиц. С другой стороны, сторонники корпускулярной гипотезы никак не могли объяснить ряда явлений, в частности обнаруженного в 1892 году эффекта практически беспрепятственного прохождения катодных лучей через тонкую алюминиевую фольгу.
Наконец в 1897 году молодой английский физик Дж. Дж. Томсон положил конец этим спорам раз и навсегда, а заодно прославился в веках как первооткрыватель электрона. В своем опыте Томсон использовал усовершенствованную катодно-лучевую трубку, конструкция которой была дополнена электрическими катушками, создававшими (согласно закону Ампера) внутри трубки магнитное поле, и набором параллельных электрических конденсаторных пластин, создававших внутри трубки электрическое поле. Благодаря этому появилась возможность исследовать поведение катодных лучей под воздействием и магнитного, и электрического поля.
Используя трубку новой конструкции, Томсон последовательно показал, что: (1) катодные лучи отклоняются в магнитном поле в отсутствие электрического; (2) катодные лучи отклоняются в электрическом поле в отсутствие магнитного; и (3) при одновременном действии электрического и магнитного полей сбалансированной интенсивности, ориентированных в направлениях, вызывающих по отдельности отклонения в противоположные стороны, катодные лучи распространяются прямолинейно, то есть действие двух полей взаимно уравновешивается.
Томсон выяснил, что соотношение между электрическим и магнитным полями, при котором их действие уравновешивается, зависит от скорости, с которой движутся частицы. Проведя ряд измерений, Томсон смог определить скорость движения катодных лучей. Оказалось, что они движутся значительно медленнее скорости света, из чего следовало, что катодные лучи могут быть только частицами, поскольку любое электромагнитное излучение, включая сам свет, распространяется со скоростью света (см. Спектр электромагнитного излучения). Эти неизвестные частицы. Томсон назвал «корпускулами», но вскоре они стали называться «электронами».
Сразу же стало ясно, что электроны обязаны существовать в составе атомов — иначе, откуда бы они взялись? 30 апреля 1897 года — дата доклада Томсоном полученных им результатов на заседании Лондонского королевского общества — считается днем рождения электрона. И в этот день отошло в прошлое представление о «неделимости» атомов (см. Атомная теория строения вещества). Вкупе с последовавшим через десять с небольшим лет открытием атомного ядра (см. Опыт Резерфорда) открытие электрона заложило основу современной модели атома.
Описанные выше «катодные», а точнее, электронно-лучевые трубки стали простейшими предшественницами современных телевизионных кинескопов и компьютерных мониторов, в которых строго контролируемые количества электронов выбиваются с поверхности раскаленного катода, под воздействием переменных магнитных полей отклоняются под строго заданными углами и бомбардируют фосфоресцирующие ячейки экранов, образуя на них четкое изображение, возникающее в результате фотоэлектрического эффекта, открытие которого также было бы невозможным без нашего знания истинной природы катодных лучей.
Открытие электрона
Датой открытия электрона считается 1897 год, когда Томсоном был поставлен эксперимент по изучению катодных лучей. Первые снимки треков отдельных электронов были получены Чарльзом Вильсоном при помощи созданной им туманной камеры.
Содержание
Предпосылки открытия, гипотезы
В 1749 году Бенджамин Франклин высказал гипотезу, что электричество представляет собой своеобразную материальную субстанцию. Центральную роль электрической материи он отводил представлению об атомистическом строении электрического флюида. В работах Франклина впервые появляются термины: заряд, разряд, положительный заряд, отрицательный заряд, конденсатор, батарея, частицы электричества.
Иоганн Риттер в 1801 году высказал мысль о дискретной, зернистой структуре электричества.
Вильгельм Вебер в своих работах с 1846 года вводит понятие атома электричества и гипотезу, что его движением вокруг материального ядра можно объяснить тепловые и световые явления.
Майкл Фарадей ввел термин «ион» для носителей электричества в электролите и предположил, что ион обладает неизменным зарядом. Г. Гельмгольц в 1881 году показал, что концепция Фарадея должна быть согласована с уравнениями Максвелла. Джордж Стоней в 1881 году впервые рассчитал заряд одновалентного иона при электролизе, а в 1891 году, в одной из теоретических работ Стоней предложил термин «электрон» для обозначения электрического заряда одновалентного иона при электролизе.
Катодные лучи
Катодные лучи открыты в 1859 году Юлиусом Плюккером, название дано Эйгеном Гольдштейном, который высказал волновую гипотезу: катодные лучи представляют собой процесс в эфире. Английский физик Уильям Крукс высказал идею, что катодные лучи это потоки частичек вещества. В 1895 году французский физик Жан Перрен экспериментально доказал, что катодные лучи — это поток отрицательно заряженных частиц, которые движутся прямолинейно, но могут отклоняться магнитным полем.
Бета-лучи
В то же время Анри Беккерель исследовал естественную радиацию и в 1900 году показал, что лучи, испускаемые радием, которые Эрнст Резерфорд назвал бета-лучами, имеют такой же удельный заряд, что и катодные лучи.
Опыт Томсона
С 1895 года Джозеф Джон Томсон в Кавендишской лаборатории Кембриджского университета начинает методическое количественное изучение отклонения катодных лучей в электрических и магнитных полях. Итоги этой работы были опубликованы в 1897 г. в октябрьском номере журнала «Philosophical Magazine». В своем опыте Томсон доказал, что все частицы, образующие катодные лучи, тождественны друг другу и входят в состав вещества. Суть опытов и гипотезу о существовании материи в состоянии ещё более тонкого дробления, чем атомы, Томсон изложил на вечернем заседании Королевского общества 29 апреля 1897 г. Извлечение из этого сообщения было опубликовано в «Electrican» 21 мая 1897 г. За это открытие Томсон в 1906 году получил Нобелевскую премию по физике.
Примечания
Источники
Полезное
Смотреть что такое «Открытие электрона» в других словарях:
АТОМА СТРОЕНИЕ — раздел физики, изучающий внутреннее устройство атомов. Атомы, первоначально считавшиеся неделимыми, представляют собой сложные системы. Они имеют массивное ядро, состоящее из протонов и нейтронов, вокруг которого в пустом пространстве движутся… … Энциклопедия Кольера
Электрон — У этого термина существуют и другие значения, см. Электрон (значения). Электрон Символ Масса 9,10938291(40)·10−31кг[1], 0,510998928(11) МэВ … Википедия
МАТЕРИАЛИЗМ — (от лат. materialis вещественный) многозначная идея, которой чаще всего придается один или некоторые из следующих смыслов. 1. Утверждение относительно существования или реальности: только материя существует или является реальной; материя является … Философская энциклопедия
История физики — История науки … Википедия
НАУКА — особый вид познавательной деятельности, направленный на выработку объективных, системно организованных и обоснованных знаний о мире. Взаимодействует с др. видами познавательной деятельности: обыденным, художественным, религиозным, мифологическим … Философская энциклопедия
Негатрон (физика) — Электрон Символ Масса 9,10938215(45)×10−31кг, 0,510998910(13) МэВ/c2 Античастица позитрон Классы фермион, лептон … Википедия
Электрон (квазичастица) — Электрон Символ Масса 9,10938215(45)×10−31кг, 0,510998910(13) МэВ/c2 Античастица позитрон Классы фермион, лептон … Википедия
Электрон (физич.) — Электрон Символ Масса 9,10938215(45)×10−31кг, 0,510998910(13) МэВ/c2 Античастица позитрон Классы фермион, лептон … Википедия
Электрон (частица) — Электрон Символ Масса 9,10938215(45)×10−31кг, 0,510998910(13) МэВ/c2 Античастица позитрон Классы фермион, лептон … Википедия
Электроны — Электрон Символ Масса 9,10938215(45)×10−31кг, 0,510998910(13) МэВ/c2 Античастица позитрон Классы фермион, лептон … Википедия