Что осуществляет транспорт кислорода в крови
Что осуществляет транспорт кислорода в крови
Кровообращение выполняет одну из важнейших функций переноса кислорода от легких к тканям, а углекислого газа — от тканей к легким. Потребление кислорода клетками тканей может изменяться в значительных пределах, например при переходе от состояния покоя к физической нагрузке и наоборот. В связи с этим кровь должна обладать большими резервами, необходимыми для увеличения ее способности переносить кислород от легких к тканям, а углекислый газ в обратном направлении.
Транспорт кислорода.
При 37 С растворимость 02 в жидкости составляет 0,225 мл • л-1 • кПа-1 (0,03 мл/л/мм рт. ст.). В условиях нормального парциального давления кислорода в альвеолярном воздухе, т. е. 13,3 кПа или 100 мм рт.ст., 1 л плазмы крови может переносить только 3 мл 02, что недостаточно для жизнедеятельности организма в целом. В покое в организме человека за минуту потребляется примерно 250 мл кислорода. Чтобы тканям получить такое количество кислорода в физически растворенном состоянии, сердце должно перекачивать за минуту огромное количество крови. В эволюции живых существ проблема транспорта кислорода была более эффективно решена за счет обратимой химической реакции с гемоглобином эритроцитов. Кислород переносится кровью от легких к тканям организма молекулами гемоглобина, которые содержатся в эритроцитах.
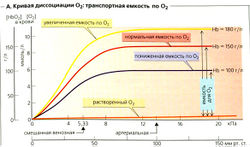
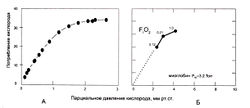
Гемоглобин способен захватывать кислород из альвеолярного воздуха (соединение называется ок-сигемоглобином) и освобождать необходимое количество кислорода в тканях. Особенностью химической реакции кислорода с гемоглобином является то, что количество связанного кислорода ограничено количеством молекул гемоглобина в эритроцитах крови. Молекула гемоглобина имеет 4 места связывания с кислородом, которые взаимодействуют таким образом, что зависимость между парциальным давлением кислорода и количеством переносимого кислорода с кровью имеет S-образную форму, которая носит название кривой насыщения или диссоциации оксигемоглобина (рис. 10.18). При парциальном давлении кислорода 10 мм рт. ст. насыщение гемоглобина кислородом составляет примерно 10 %, а при Р02 30 мм рт. ст. — 50—60 %. При дальнейшем увеличении парциального давления кислорода от 40 мм рт. ст. до 60 мм рт. ст. происходит уменьшение крутизны кривой диссоциации оксигемоглобина и процент его насыщения кислородом возрастает в диапазоне от 70—75 до 90 % соответственно. Затем кривая диссоциации оксигемоглобина начинает занимать практически горизонтальное положение, поскольку увеличение парциального давления кислорода с 60 до 80 мм рт. ст. вызывает прирост насыщения гемоглобина кислородом на 6 %. В диапазоне от 80 до 100 мм рт. ст. процент образования оксигемоглобина составляет порядка 2. В результате кривая диссоциации оксигемоглобина переходит в горизонтальную линию и процент насыщения гемоглобина кислородом достигает предела, т. е. 100. Насыщение гемоглобина кислородом под влиянием Р02 характеризует своеобразный молекулярный «аппетит» этого соединения к кислороду.
Значительная крутизна кривой насыщения гемоглобина кислородом в диапазоне парциального давления от 20 до 40 мм рт. ст. способствует тому, что в ткани организма значительное количество кислорода может диффундировать из крови в условиях фадиента его парциального давления между кровью и клетками тканей (не менее 20 мм рт. ст.). Незначительный процент насыщения гемоглобина кислородом в диапазоне его парциального давления от 80 до 100 мм рт. ст. способствует тому, что человек без риска снижения насыщения артериальной крови кислородом может перемещаться в диапазоне высот над уровнем моря до 2000 м.
Общие запасы кислорода в организме обусловлены его количеством, находящимся в связанном состоянии с ионами Fe2+ в составе органических молекул гемоглобина эритроцитов и миоглобина мышечных клеток.
Один грамм гемоглобина связывает 1,34 мл 02. Поэтому в норме при концентрации гемоглобина 150 г/л каждые 100 мл крови могут переносить 20,0 мл 02.
Количество 02, которое может связаться с гемоглобином эритроцитов крови при насыщении 100 % его количества, называется кислородной емкостью гемоглобина. Другим показателем дыхательной функции крови является содержание 02 в крови (кислородная емкость крови), которое отражает его истинное количество, как связанного с гемоглобином, так и физически растворенного в плазме. Поскольку в норме артериальная кровь насыщена кислородом на 97 %, то в 100 мл артериальной крови содержится примерно 19,4 мл 02.
Транспорт кислорода
Содержание
Связывание и транспорт кислорода в крови [ править | править код ]
При насыщении кислородом 1 моль тетрамерного НЬ соединяется с 4 молекулами O2, т. е. 64 500 г НЬ соединяется с 4 • 22,4 л O2. Таким образом, 1 г НЬ теоретически может транспортировать in vivo 1,39 мл O2, или 1,35 мл (число Хюфнера). Общая концентрация НЬ в крови ([Hb]total) в среднем составляет 150 г/л (с. 94), что соответствует максимальной концентрации O2 9,1 ммоль/л или 0,203 л O2А1 крови. Транспортная емкость крови по кислороду является функцией [Hb]tote/(A).
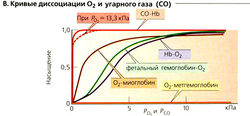
Миоглобин представляет собой Fe(II)-содержащий мышечный белок, который служит для кратковременного запасания O2. Поскольку это мономер (нет положительной кооперативное™), его кривая диссоциации O2 при низких PO2 гораздо круче, чем аналогичная кривая для НЬ (В). Кривая диссоциации O2 фетального гемоглобина (2а + 2у = HbF) также достаточно крутая, и в пупочной вене эмбриона могут быть достигнуты Яд2 от 45 до 70%, несмотря на низкое давление PO2 (3-4 кПа или 22-30 мм рт. ст.) в материнской плацентарной крови. Это существенно, поскольку у эмбриона концентрация [Нb]total =180 г/л. Кривая диссоциации монооксида углерода (СО) имеет очень крутой наклон. Таким образом, даже незначительные количества СО во вдыхаемом воздухе вызывают диссоциацию O2 из НЬ. Это может привести к отравлению СО (В). Метгемоглобин Met-Hb (обычно 1% от НЫ образуется из гемоглобина при окислении Fe(ll) в Fe(lll) либо спонтанно, либо под действием эндогенных оксидантов. Met-Hb не может присоединять O2 (В). Редуктаза метгемоглобина восстанавливает Fe(lll) из Met-Hb в Fe(ll); дефицит этого фермента может вызывать метгемоглобинемию, приводя к неонатальной аноксии.
Транспортная система крови [ править | править код ]
Напротив, существуют данные о том, что снижение концентрации гемоглобина до нормального уровня (140 г/л, изоволюмические условия) у акклиматизированных к высокогорью (9 недель; 5260 м над ур. моря) физически активных людей не приводит к увеличению максимального СВ и максимального УО, как в гипоксических, так и в нормоксических условиях. Это свидетельствует о незначительной роли изменений концентрации гемоглобина и вязкости крови как факторов, определяющих показатели центральной гемодинамики.
В исследовании, выполненном с участием высококвалифицированных бегунов, также было показано, что аутогемотрансфузия, приводящая к увеличению гематокрита с 46 до 51%, приводит к увеличению СВ за счет увеличения УО. При этом аутогемотрансфузия не оказывает влияния на максимальное артериальное давление и электрокардиографические показатели. Это свидетельствует о том, что эритроцитомия не оказывает отрицательного действия на работу сердца при максимальной нагрузке.
Косвенно отсутствие отрицательного влияния физиологического увеличения концентрации эритроцитов и величины гематокрита подтверждается широким распространением кровяного допинга в спорте.
Сердце и доставка кислорода к мышцам [ править | править код ]
Как отмечалось выше, интегральным показателем, характеризующим производительность сердца, является максимальный СВ. Поскольку максимальная частота сердечных сокращений (ЧСС) у тренированных людей не отличается от этого показателя обычных людей, различие в величине сердечного выброса у двух контингентов определяется различием в УО сердца. УО сердца зависит от величины венозного возврата, объема камер сердца, силы, развиваемой миокардом, и сопротивления на выходе, которое определяется диаметром и эластичностью аорты и частично общим периферическим сопротивлением. У высококвалифицированных спортсменов, тренирующих выносливость, максимальный УО и СВ практически в два раза больше, чем у обычных людей, и достигают 200 мл и 40 л/мин, соответственно. По данным многочисленных исследований, СВ, размеры сердца и масса левого желудочка (расчетный показатель) связаны с величиной МПК и со спортивным результатом в видах спорта, требующих проявления выносливости.
В настоящее время основным методом измерения размеров сердца в покое является ультразвуковое исследование. Для измерения УО во время работы, в том числе и максимальной, наиболее надежными методами являются прямой метод по Фику и измерение УО с помощью дыхания газовой смесью, содержащей растворимый газ в закрытом или открытом дыхательном контуре.
У нетренированного человека УО растет при увеличении мощности вплоть до ЧСС 140—145 уд./мин. При дальнейшем увеличении мощности УО выходит на плато и начинает снижаться при достижении максимальной аэробной мощности (мощность на уровне МПК). Выход на плато и снижение УО связывают с дефектом диастолы, а также с неадекватным венозным возвратом (механизм ФранкаСтарлинга). Дефект диастолы может проявляться при высокой ЧСС, когда длительность диастолы становится недостаточной для адекватного кровоснабжения миокарда. Следствием этого будет снижение силы сокращения миокарда и в результате снижение УО, а возможно, и прекращение прироста ЧСС в ответ на дальнейший прирост нагрузки. Значимость величины венозного возврата для УО показана в экспериментах на собаках с удаленной селезенкой. Предрабочее увеличение объема крови посредством введения декстрана также приводит к увеличению СВ на 20-30%. Аналогичные результаты были получены и в экспериментах с увеличением объема плазмы у нетренированных людей и высокотренированных велосипедистов.
У высокотренированных спортсменов рост УО во время теста с повышающейся нагрузкой наблюдается вплоть до отказа от работы, что свидетельствует об уникально высокой производительности сердца, при этом ЧСС не выходит на плато и также растет вплоть до отказа от работы.
Целый ряд экспериментов, направленных на изучение лимитирующей роли доставки кислорода сердцем для величины МПК, был проведен при сравнении модели локальной и глобальной мышечной работы. В основу этих экспериментальных работ легло предположение, что при работе локальной мышечной группой (например, сгибание руки в локтевом суставе или разгибание ноги в коленном суставе) возможности организма по доставке кислорода, определяемые СВ, заведомо больше способности данной мышечной группы к утилизации кислорода. После длительной аэробной тренировки мышц-разгибателей коленного сустава одной ноги увеличились общее пиковое ПК и пиковая мощность при работе одной ногой на 16 и 13%, соответственно. Это объясняется, главным образом, увеличением кровотока в ноге и повышением утилизации кислорода. Однако при глобальной работе (велоэргоме-трия) МПК не изменяется, поскольку тренировка в режиме локальной работы не приводит к увеличению максимального Св. Это подтверждает ключевую роль производительности сердца/кровотока как факторов, лимитирующих МПК. Эту же точку зрения подтверждают эксперименты с длительной велоэргометрической тренировкой. В этом случае тренируются не только окислительные возможности мышц ног, но и сердце. После тренировки при работе руками в тесте с возрастающей нагрузкой зарегистрировано сходное увеличение пикового ПК и Св.
Значимость фактора доставки кислорода как лимитирующего пиковое потребление кислорода рабочей мышечной группой (мыш-цы-разгибатели голени) у квалифицированных велосипедистов продемонстрирована при сопоставлении локальной и глобальной работы. Расчетные данные показали, что удельное ПК в мышце при локальной и глобальной работе различается практически в два раза. Несмотря на допущения в методике измерения ПК и расчете удельного ПК, этот результат свидетельствует о значительной роли фактора доставки для определения МПК в мышце у тренированных людей.
Следует отметить, что не все экспериментальные работы однозначно свидетельствуют об увеличении МПК в мышце при увеличении фактора доставки кислорода. После длительной (5 недель) аэробной тренировки мышц-разгибателей голени одной ноги дыхание гипероксическои газовой смесью (F,02 = 0,6) приводит к увеличению доставки кислорода к рабочим мышцам по сравнению с контрольным тестом (после тренировочного цикла). Однако максимальная мощность в тесте с непрерывно возрастающей нагрузкой и МПК тканями рабочей ноги не увеличиваются. Одним из ключевых контраргументов против теории ограничения ПК только факторами доставки кислорода является тот факт, что даже у высокотренированных спортсменов на уровне МПК не наблюдается полной экстракции кислорода из крови. В венозной крови, оттекающей от рабочей мышцы, парциальное давление кислорода у тренированных спортсменов составляет 10—20 мм рт. ст. Можно предполагать, что по крайней мере у высокотренированных спортсменов это не связано с лимитирующей ролью суммарной окислительной способности митохондрий, поскольку, как уже упоминалось выше, увеличение доставки кислорода увеличивает его потребление. Возникает вопрос: почему не происходит полной утилизации кислорода из капиллярной крови и с чем это связано?
Транспорт кислорода из капилляра к митохондрии [ править | править код ]
Последовательность транспорта кислорода от эритроцита до митохондрии включает диссоциацию кислорода от гемоглобина, диффузию через эндотелий, интерстиций и клеточную мембрану, связывание с миоглобином и последующую диссоциацию и диффузию через митохондриальную мембрану.
Транспорт кислорода из капилляра к митохондрии характеризуется диффузионной способностью мышц. Диффузионная способность мышц п это интегральный показатель, который зависит не только от пропускной способности клеточных мембран, но и от параметров доставки и утилизации кислорода.
Факторы, определяющие диффузионную способность мышц. Градиент парциального давления кислорода между плазмой крови и миоплазмой играет важную роль в процессе переноса кислорода. Парциальное давление кислорода в мышечной клетке при максимальной аэробной нагрузке у человека составляет около 3 мм рт. ст. Среднее парциальное давление кислорода в капилляре, полученное расчетным путем, у тренированных людей во время глобальной работы составляет 36-40 мм рт. ст. То есть градиент давления практически полностью определяется средним парциальным давлением кислорода в капилляре. На величину среднего парциального давления кислорода в капилляре влияет скорость доставки крови/кислорода, т.е. величина насыщения гемоглобина кислородом в артериальной крови и скорость кровотока.
С другой стороны, увеличение скорости кровотока неизбежно должно привести к снижению транзитного времени пребывания эритроцита в зоне газообмена (в капилляре). Скорость диссоциации определяется градиентом давления кислорода между гемоглобином и плазмой крови в соответствии с кривой диссоциации гемоглобина. В плазме крови и интерстиции нет молекул-переносчиков кислорода (кислородсвязывающих белков), которые могли бы быстро связывать свободный кислород. Поэтому процесс диссоциации кислорода от гемоглобина относительно медленный. Поскольку расчетная величина транзитного времени нахождения эритроцита в капилляре при максимальном кровотоке составляет всего 100—400 мс, снижение транзитного времени пребывания эритроцита в капилляре, происходящее при увеличении кровотока, действительно может быть основной причиной неполной утилизации кислорода из крови.
Другой важной составляющей, которая определяет диффузионную способность мышц, является площадь диффузионной поверхности. Теоретические расчеты показывают, что снижение контактной суммарной площади может привести к снижению диффузии кислорода. Суммарная площадь поверхности эритроцитов больше, чем суммарная площадь стенок капилляров. На электронно-микроскопических снимках видно, что суммарная площадь поверхности митохондрий в «красной» мышце (т. gracilis) собаки в 200 раз превосходит суммарную площадь капиллярных стенок. Это свидетельствует в пользу того, что ключевая роль в ограничении диффузионной площади принадлежит суммарной площади стенок капилляров, приходящихся на одно волокно, или количеству капилляров, приходящихся на волокно. Так, опыты с мышцами собаки, подвергшимися аэробной тренировке, гипокинезии и не подвергавшимися экспериментальным воздействиям, показали, что МПК мышцей зависит от количества капилляров на волокно и не зависит от диффузионного расстояния и от капиллярной плотности. Косвенно данные результаты подтверждаются тесной взаимосвязью между МПК организмом млекопитающих и количеством капилляров, приходящихся на волокно.
Подытоживая приведенные выше сведения, можно сказать, что наибольшее сопротивление для диффузии кислорода от гемоглобина до митохондрии находится где-то между молекулой гемоглобина и миоплазмой на относительно коротком расстоянии (2-3 мкм). Именно на этом участке наблюдается наиболее высокое соотношение поток диффундирующего кислорода/площадь газообмена. Как отмечалось выше, появление этого функционального барьера обусловлено взаимодействием гемодинамики и химических процессов. Данная точка зрения также подтверждается некоторыми модельными экспериментами.
Теория диффузионного ограничения максимального потребления кислорода мышцей. Значимость показателя диффузионной способности мышц подтверждается как модельными исследованиями, так и экспериментальными работами. В эксперименте на мышцах собаки <т. gastrocnemius) in situ пытались определить влияние фактора диффузии кислорода в мышце на величину МПК мышцей.
Утилизация кислорода [ править | править код ]
Для того чтобы говорить об утилизации кислорода митохондриями, необходимо выяснить, существуют ли в мышечном волокне во время работы аноксические зоны. В начале прошлого века Крогом была выдвинута идея о том, что парциальное напряжение кислорода внутри мышечного волокна зависит от его расположения относительно капилляра (зоны газообмена). Это привело к созданию концепции цилиндра Крога с зонами неадекватного обеспечения кислородом в центре волокна.
Однако данные последних лет опровергают эту гипотезу. Такие данные получены при измерении парциального давления связанного с миоглобином кислорода в «красной» мышце собаки (m. gracilis) с помощью метода криоспектроскопии. Среднее парциальное давление кислорода в мышечных волокнах при работе на уровне МПК равно 1-2 мм рт. ст., что в несколько раз выше критического уровня (0,1—0,5 мм рт. ст.). Более того, не удается обнаружить значимой гетерогенности парциального давления кислорода в различных локусах мышечной клетки при работе на уровне МПК, как в поперечном разрезе, так и вдоль мышечного волокна. Таким образом, продемонстрировано отсутствие зависимости между диаметром мышечного волокна (27-74 мкм) и градиентом давления кислорода внутри клетки. Однако в волокнах некоторых мышц при работе на уровне МПК удается обнаружить гипоксические зоны, в которых парциальное давление кислорода находится около верхней границы критического уровня. Общее число таких волокон может составлять около 2% и не влияет ни на динамику ПК мышцей, ни на развиваемую мышцей силу.
Как отмечалось выше, снижение доставки кислорода к мышце (митохондриям) всегда приводит к снижению ПК отдельной мышцей и организмом в целом (в условиях глобальной работы). Причем снижение величины МПК в этих случаях прямо пропорционально снижению среднего парциального давления кислорода в капиллярной крови. С другой стороны, увеличение доставки кислорода не всегда приводит к увеличению МПК, а если прирост наблюдается, то он, как правило, ниже, чем прирост величины доставки кислорода или среднего парциального давления кислорода в капиллярной крови. Отсюда возникает вопрос, каков характер зависимости между ПК митохондриями и парциальным давлением кислорода в цитоплазме.
Что осуществляет транспорт кислорода в крови
4.1. Транспорт кислорода
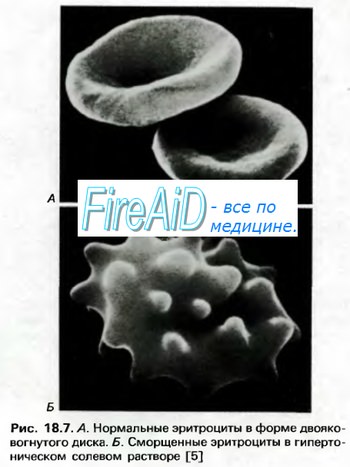
В сложных механизмах транспорта газов кровью и газообмена в тканях важная роль отводится эритроцитам, ответственным за доставку О2 к различным органам и удаление образующегося в процессе метаболизма СО2.
Эритроцит – безъядерная клетка, лишенная митохондрий, основным источником энергии для эритроцита служит глюкоза, метаболизируемая в гексозомонофосфатном шунте или цикле Эмбдена-Мейергофа. Транспорт О2 обеспечивается в значительной мере гемоглобином, состоящим из белка глобина и гема. Последний представляет собой комплексное соединение железа и порфирина. Глобин представляет собой тетрамер полипептидной цепи. Hb A (HbA) – основной гемоглобин взрослых содержит 2 – альфа и 2 – бета – цепи, Hb A2 – содержит две альфа и две дельта цепи.
Гем состоит из иона железа, встроенного в порфириновое кольцо. Ион железа гема обратимо связывает одну молекулу О2. С одной молекулой Hb максимально связываются 4 молекулы О2 с образованием оксигемоглобина.
Гем может подвергаться не только оксигенации, но и истинному окислению, когда железо становится из двухвалентного трехвалентным. Окисленный гем носит название гематина, а молекула гемоглобина становится метгемоглобином. В крови человека метгемоглобин находится в незначительных количествах, его уровень резко возрастает при отравлениях. Метгемоглобин не способен отдавать кислород тканям.
В норме метгемоглобин составляет менее 3% общего Hb крови. Основная форма транспорта О2 – в виде оксигемоглобина. Кислород транспортируется артериальной кровью не только в связи с гемоглобином, но и в растворенном виде. Принимая во внимание тот факт, что 1 г Hb может связать 1,34 мл О2, кислородная емкость крови в среднем у взрослого человека составляет около 200 мл/л крови. Одним из показателей кислородного транспорта является насыщение артериальной крови О2(Sa O2), равного отношению О2, связанного с Hb, к кислородной емкости крови:
SaO2=O2, связанного с Hb/O2 емкость крови* 100%.
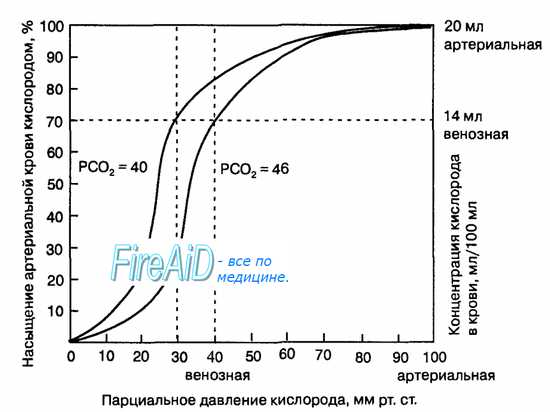
В соответствии с кривой диссоциации оксигемоглобина насыщение артериальной крови кислородом в среднем составляет 97%, в венозной крови – 75%.
PaO2 в артериальной крови около 100 мм. рт. ст., а в венозной – около 40 мм. рт. ст.
Количество растворенного кислорода в крови пропорционально парциальному давлению О2 и коэффициэнту его растворимости.
Последний для О2 составляет 0,0031/100 мл крови/ 1 мм. рт. ст.. Таким образом, 100 мл крови при PaO2, равном 100 мм. рт. ст., содержит менее 0,31 мл O2.
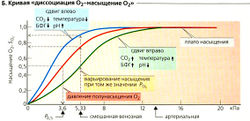
Диссоциация оксигемоглобина в тканях обусловлена главным образом химическими свойствами гемоглобина, а также рядом других факторов – температурой тела, рН среды, р СО2.
При понижении температуры тела наклон кривой диссоциации оксигемоглобина возрастает, а при ее повышении – снижается, и соответственно снижается сродство Hb к О2.
При снижении рН, т.е. при закислении среды, сродство гемоглобина к О2 уменьшается. Увеличение напряжения в крови СО2 также сопровождается снижением сродства Hb к О2 и уплощением кривой диссоциации оксигемоглобина.
Известно, что степень диссоциации оксигемоглобина определяется содержанием в эритроцитах некоторых фосфорорганических соединений, главным из которых является 2,3 – ДФГ (2,3 дифосфоглицерат), а также содержанием в эритроцитах катионов. В случаях развития алкалозов, поглощение О2 в легких увеличивается, но в то же время затрудняется отдача кислорода тканями. При ацидозах наблюдается обратная картина.
4.2.Утилизация кислорода тканями
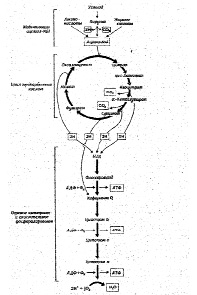
Тканевое или клеточное дыхание включает три стадии. На первой стадии пируват, аминокислоты и жирные кислоты окисляются до двухуглеродных фрагментов ацетильных групп, входящих в состав ацетилкофермента А. Последние на втором этапе окисления включаются в цикл лимонной кислоты, где происходит образование высокоэнергетических атомов водорода и высвобождение СО2 – конечного продукта окисления органических субстратов. На третьей стадии клеточного дыхания атомы водорода делятся на протоны (Н+) и «высокоэнергетические» электроны, передающиеся по дыхательной цепи на молекулярный О2 и восстанавливающие его до НО2. Перенос электронов сопряжен с запасом энергии в форме АТФ, т.е. с окислительным фосфорилированием (рис.6).
Касаясь патогенеза метаболических сдвигов, свойственных гипоксическим состояниям, следует отметить, что в организме человека более 90% всего потребляемого кислорода восстанавливается с участием цитохромоксидазы митохондрий, и лишь около 10% кислорода метаболизируется в тканях с участием оксигеназ: диоксигеназы и монооксигеназы.
Рис.6. Схема тканевого дыхания. Конечные продукты каждой стадии даны в рамке (Ленинджер А., 1999)
Наиболее многочисленны и сложны монооксигеназные реакции, протекающие в эндоплазматическом ретикулуме клеток при участии цитохрома Р-450 и обеспечивающие гидроксилирование субстрата (стероидных гормонов, лекарственных препаратов и различных др. соединений) и, как правило, его инактивацию.
Диоксигеназы катализируют реакции, в которых в молекулу органического субстрата включаются оба атома молекулы кислорода (например, реакция окисления катехола молекулярным кислородом с раскрытием кольца).
В реакциях, связанных с переносом электронов, т.е. в реакциях окисления-восстановления, где, как указывалось выше, используется более 90% потребляемого кислорода, атомы водорода, отщепленные дегидрогеназами от субстратов в цикле лимонной кислоты, передают свои электроны в цепь переноса электронов и превращаются также в Н +. Как известно, помимо 4 пар атомов водорода, поставляемых каждым оборотом цикла лимонной кислоты, образуются и другие атомы водорода, отщепленные дегидрогеназами от пирувата, жирных кислот и аминокислот в процессе их расщепления до Ацетил-СоА и других продуктов.
Таким образом, все атомы водорода, отщепляемые дегидрогеназами от субстратов, передают свои электроны в дыхательную цепь к конечному акцептору электронов – кислороду.
Скорость утилизации О2 в различных тканях различна. В среднем взрослый человек потребляет 250 мл О2 в 1 мин. Максимальное извлечение О2 из притекающей артериальной крови свойственно миокарду.
Кислород используется в клетках, в основном в метаболизме белков, жиров, углеводов, ксенобиотиков, в окислительно-восстановительных реакциях в различных субклеточных фракциях: в митохондриях, в эндоплазматическом ретикулуме, в реакциях липопероксидации, а также в межклеточном матриксе и в биологических жидкостях.
Коэффициент утилизации О2 в тканях равен отношению потребления О2 к интенсивности его доставки, широко варьирует в различных органах и тканях.
В условиях нормы минимальную потребность в О2 проявляют почки и селезенка, а максимальную потребность – кора головного мозга, миокард и скелетные мышцы, где коэффициент утилизации О2 колеблется от 0,4 до 0,6, а в миокарде до 0,7. При крайне интенсивной физической работе коэффициент утилизации О2 мышцами и миокардом может возрастать до 0,9.
Обмен дыхательных газов в тканях происходит в процессе свободной и облегченной диффузии. При этом О2 переносится по градиенту напряжения газа из эритроцитов и плазмы крови в окружающие ткани.
Одновременно происходит диффузия СО2 из тканей в кровь. На выход О2 из крови в ткани влияет диссоциация оксигемоглобина в эритроцитах, что обеспечивает так называемую облегченную диффузию О2. Интенсивность диффузионного потока О2 и СО2 определяется градиентом их напряжения между кровью и тканями, а также площадью газообмена, плотностью капилляров, распределением кровотока в микроциркуляторном русле. Интенсивность окислительных процессов в тканях определяется величиной критического напряжения О2 в митохондриях, которое в условиях нормы должно превосходить 0,1-1 мм рт. ст.
Соответствие доставки О2 к органам и тканям, возросшим потребностям в оксигенации обеспечивается на клеточном, органном уровнях за счет образования метаболитов изнашивания, а также при участии нервных, гормональных и гуморальных влияний.
Основная масса углекислого газа (СО2) образуется в организме как конечный продукт различных метаболических реакций и транспортируется к легким с кровью. Вдыхаемый воздух содержит лишь незначительное количество СО2.
Транспорт СО2 кровью осуществляется в 3-х состояниях: в виде аниона бикарбоната, в растворенной форме и в виде карбаминовых соединений.
СО2 хорошо растворяется в плазме крови и в артериальной крови, около 5% от общей двуокиси углерода содержится в крови в растворенной форме.
Третьей формой транспорта СО2 кровью являются карбаминовые соединения, образованные взаимодействием СО2 с концевыми группами белков крови преимущественно с гемоглобином:
Карбаминовые соединения составляют около 5% от общего количества СО2, транспортируемого кровью.
В оксигенированной артериальной крови напряжение СО2 составляет 40 мм. рт. ст., а в венозной крови Рv СО2 равно 46 мм. рт. ст.
4.4.Связывание гемоглобина с окисью углерода