Что определяют с помощью калориметрической камеры
Калориметрический опыт



Введение
Калориметрия (от лат. calor — тепло и лат. metro — измеряю) — совокупность методов измерения количества теплоты, выделяющейся или поглощаемой при протекании различных физических или химических процессов. Методы калориметрии применяют при определении теплоемкости, тепловых эффектов химических реакций, растворении, смачивании, адсорбции, радиоактивного распада и др. Методы калориметрии также широко применяют в промышленности для определения теплотворной способности топлива.
Калориметрические измерения
Изменение состояния (например, температуры) калориметрической системы позволяет измерить количество теплоты, введённое в калориметр. Нагрев калориметрической системы фиксируется термометром. Перед проведением измерений калориметр градуируют — определяют изменение температуры калориметрической системы при сообщении ей известного количества теплоты (нагревателем калориметра или в результате проведения в камере химической реакции с известным количеством стандартного вещества). В результате градуировки получают тепловое значение калориметра, то есть коэффициент, на который следует умножить измеренное термометром изменение температуры калориметра для определения количества введённой в него теплоты. Тепловое значение такого калориметра представляет собой теплоёмкость (с) калориметрической системы. Определение неизвестной теплоты сгорания или другой химической реакции Q сводится к измерению изменения температуры Δt калориметрической системы, вызванного исследуемым процессом: Q=cΔt. Обычно значение Q относят к массе вещества, находящегося в камере калориметра.
Калориметрический опыт
Калориметрический опыт состоит из трех периодов. В начальном периоде устанавливается равномерное изменение температуры, вызванное регулируемым теплообменом с оболочкой и побочными тепловыми процессами в калориметре, так называемый температурный ход калориметра.
Главный период начинается с момента ввода теплоты в калориметр и характеризуется быстрым и неравномерным изменением его температуры.
В конечном периоде опыта, по завершении изучаемого процесса, температурный ход калориметра снова становится равномерным. В калориметрах с изотермической оболочкой (иногда называют изопериболическими калориметрами) температура оболочки поддерживается постоянной, а температуры калориметрической системы измеряют через равные промежутки времени.
Для вычисления поправки на теплообмен, которая достигает нескольких процентов от dТ используют метод расчета, основанный на законе охлаждения Ньютона. Такие калориметры обычно применяют для определения теплот сравнительно быстрых процессов (продолжительность главного периода опыта 10-20 мин).
В калориметрах с адиабатической оболочкой температуру оболочки поддерживают близкой к температуре калориметрической системы в продолжение всего опыта (температуру последней измеряют только в начальном и конечном периодах опыта). Поправка на теплообмен в этом случае незначительна и вычисляется как сумма поправок на неадиабатичность и на ход температуры. Такие калориметры применяют при определении теплот медленно протекающих процессов.
· По конструкции системы и методике измерения:

В массивном калориметре вместо калориметрической жидкости используют блок из металла с хорошей теплопроводностью (Сu, Al, Ag) с выемками для реакционного сосуда, термометра и нагревателя. Их применяют для измерения энтальпий сгорания, испарения, адсорбции и др., но чаще всего для определения энтальпии веществ при температурах до 3000К по методу смешения. Энтальпию вещества рассчитывают как произведение теплового значения калориметра и изменения температуры блока, измеренных после сбрасывания нагретого до нужной температуры образца в гнездо блока.
Для определения теплоемкости твердых и жидких веществ в области от 0,1 до 1000 К и энтальпий фазовых переходов используют калориметры-контейнеры (рис. 2), в которых калориметрическим сосудом служит тонкостенный контейнер (ампула для вещества) обычно небольшого размера (от 0,3 до 150 см3), изготовленный из меди, серебра, золота, платины, нержавеющей стали.
Адиабатический калориметр-контейнер для определения теплоемкости твердых и жидких веществ при низких температурах:
Калориметры-контейнеры, предназначенные для работы при низких температурах, кроме системы изотермической или адиабатической оболочек, защищают вакуумной рубашкой и помещают в криостат (сосуд Дьюара), заполненный в зависимости от температурной области жидким Не, Н2 или N2.
Теплоемкость газов и жидкостей при постоянном давлении определяют в проточных калориметрах – по разности температур на входе и выходе стационарного потока газа или жидкости, мощности этого потока и джоулевой теплоте, выделенной электрическим нагревателем.
При измерениях небольших тепловых эффектов, а также теплоемкостей применяют двойной калориметр, имеющий две совершенно одинаковые калориметрические системы (жидкостные, массивные, тонкостенные), которые находятся при одной и той же температуре и имеют одинаковый теплообмен с оболочкой. Вместо поправки на теплообмен вводят небольшую поправку на неидентичность калориметрических систем (блоков), определяемую предварительно. При определении тепловых эффектов экзотермических реакций в одном из блоков выделяется неизвестное количество теплоты исследуемой реакции Qx (например, реакции полимеризации), а в другой блок вводится известное количество теплоты Q так, чтобы температуры обоих блоков были равны в продолжение всего опыта, тогда Qx = Q. В случае эндотермических реакций теплота Q вводится в тот блок, в котором протекает процесс. В калориметрах постоянной температуры, или изотермических, количество теплоты измеряют по количеству вещества, изменившего свое агрегатное состояние (плавление льда, нафталина или испарение жидкости).
Величину Q определяют по площади пика на кривой нагревания:
К импульсной калориметрии относится метод калориметрии с нагревом вспышкой лазера, который применяют для исследования металлических и керамических материалов, а также жидких веществ в интервале температур 80-1100 К.
Применение
Калориметрия имеет множество практических и теоретических приложений. Например, измерения теплоты сгорания (количества тепла, выделяемого при сгорании единицы массы или объема вещества) весьма важны при выборе топлива. При проектировании реактивных и ракетных двигателей теплота сгорания топлива является наиболее важным параметром для определения получаемой тяги. Многие технологические процессы происходят при очень высоких или очень низких температурах. Количество тепла, которое надо затратить на подогрев или охлаждение используемых в этих процессах материалов, определяет экономическую целесообразность их применения; выбор материалов при конструировании оборудования производится с учетом их теплоемкости.
В теоретических приложениях калориметрические измерения теплоты реакций и теплоемкости веществ могут быть использованы для определения химической стабильности или реакционной способности материалов и даже для определения их молекулярного строения.
Основоположником калориметрии считают Дж. Блэка, создавшего в середине 18 века первый ледяной калориметр. Термин «калориметр» предложен А. Лавуазье и П. Лапласом в 1780.
Чтобы найти изменение энтальпии на моль вещества A в реакции между двумя веществами A и B, вещества отдельно добавляются в калориметр и отмечаются начальная и конечная температуры (до начала реакции и после ее завершения). Умножение изменения температуры на массу и удельную теплоемкость веществ дает значение энергии, выделяемой или поглощаемой во время реакции. Разделение изменения энергии на количество присутствующих молей A дает изменение энтальпии реакции.
СОДЕРЖАНИЕ
История
Адиабатические калориметры
Адиабатический калориметр калориметр использовал для изучения неконтролируемой реакции. Поскольку калориметр работает в адиабатической среде, любое тепло, выделяемое исследуемым образцом материала, вызывает повышение температуры образца, тем самым подпитывая реакцию.
Реакционные калориметры
Калориметр теплового потока
Рубашка охлаждения / нагрева регулирует либо температуру процесса, либо температуру рубашки. Тепло измеряется путем отслеживания разницы температур между теплоносителем и технологической жидкостью. Кроме того, для получения правильного значения необходимо определить объемы заполнения (т.е. смачиваемую площадь), удельную теплоемкость и коэффициент теплопередачи. С помощью калориметра этого типа можно проводить реакции при кипячении с обратным холодильником, хотя он очень менее точен.
Калориметр теплового баланса
Рубашка охлаждения / нагрева контролирует температуру процесса. Тепло измеряется путем отслеживания тепла, полученного или потерянного теплоносителем.
Компенсация мощности
Компенсация мощности использует нагреватель, расположенный внутри емкости для поддержания постоянной температуры. Энергия, подаваемая в этот нагреватель, может варьироваться по мере необходимости, и калориметрический сигнал выводится исключительно из этой электрической мощности.
Постоянный поток
Калориметрия постоянного потока (или COFLUX, как ее часто называют) выводится из калориметрии теплового баланса и использует специальные механизмы управления для поддержания постоянного теплового потока (или потока) через стенку сосуда.
Калориметры бомбы
По сути, бомбовый калориметр состоит из небольшой чашки, содержащей образец, кислорода, бомбы из нержавеющей стали, воды, мешалки, термометра, емкости Дьюара или изолирующего контейнера (для предотвращения теплового потока от калориметра в окружающую среду) и цепи зажигания. подключен к бомбе. При использовании в бомбе нержавеющей стали реакция будет происходить без изменения объема.
Поскольку нет теплообмена между калориметром и окружающей средой (Q = 0) (адиабатический), работа не выполняется (W = 0)
Таким образом, полное изменение внутренней энергии
Δ E Всего знак равно Q + W знак равно 0 <\ displaystyle \ Delta E _ <\ text
Кроме того, общее изменение внутренней энергии
где теплоемкость бомбы C v <\ displaystyle C _ <\ text
В лаборатории определяется, прогоняя состав с известной теплотой сгорания: C v <\ displaystyle C _ <\ text 
Обычными соединениями являются бензойная кислота ( ) или п-метилбензойная кислота ( ). ЧАС c знак равно 6318 кал / г <\ displaystyle H _ <\ text 
Для калибровки бомбы взвешивается небольшое количество (
1 г) бензойной кислоты или п-метилбензойной кислоты. Длина никелевой плавкой проволоки (
Горение образца (бензойной кислоты) внутри бомбы
Δ ЧАС c знак равно C v Δ Т <\ displaystyle \ Delta H _ <\ text
Сжигание негорючих веществ
Более высокое давление и концентрация O
2 в системе бомбы может сделать горючими некоторые соединения, которые обычно не воспламеняются. Некоторые вещества не сгорают полностью, что затрудняет расчеты, поскольку необходимо учитывать оставшуюся массу, что значительно увеличивает возможную ошибку и ставит под угрозу данные.
При работе с негорючими соединениями (которые могут не сгорать полностью) одним из решений было бы смешать состав с некоторыми легковоспламеняющимися соединениями с известной теплотой сгорания и сделать из смеси поддон. Если известна величина бомбы, теплота сгорания горючего соединения ( C FC ), проволоки ( C W ) и массы ( m FC и m W ), а также изменение температуры (Δ T ), тепловыделение сжигания менее горючего соединения ( C LFC ) можно рассчитать с помощью: C v <\ displaystyle C _ <\ text
Калориметры типа Кальве
Обнаружение основано на трехмерном датчике флюксметра. Элемент флюксметра состоит из кольца, состоящего из нескольких последовательно включенных термопар. Соответствующая термобатарея с высокой теплопроводностью окружает экспериментальное пространство внутри калориметрического блока. Радиальное расположение термобатарей гарантирует почти полную интеграцию тепла. Это подтверждается расчетом коэффициента эффективности, который показывает, что среднее значение 94% ± 1% тепла передается через датчик во всем диапазоне температур калориметра типа Кальве. В этой установке чувствительность калориметра не зависит от тигля, типа продувочного газа или расхода. Основным преимуществом установки является увеличение размера экспериментального сосуда и, следовательно, размера образца, не влияя на точность калориметрических измерений.
Калибровка калориметрических детекторов является ключевым параметром и требует очень тщательного выполнения. Для калориметров типа Кальве была разработана специальная калибровка, так называемый эффект Джоуля или электрическая калибровка, чтобы преодолеть все проблемы, возникающие при калибровке со стандартными материалами. Основные преимущества этого типа калибровки:
Примером калориметра типа Кальве является калориметр C80 (реакционный, изотермический и сканирующий калориметр).
Адиабатические и изопериболические калориметры
C п знак равно W Δ ЧАС M Δ Т <\ displaystyle C _ <\ text
> = <\ frac
Измерение тепла с помощью простого калориметра, такого как калориметр для кофейной чашки, является примером калориметрии постоянного давления, поскольку давление (атмосферное давление) остается постоянным во время процесса. Калориметрия постоянного давления используется для определения изменений энтальпии, происходящих в растворе. В этих условиях изменение энтальпии равно теплоте.
Дифференциальный сканирующий калориметр
В тепловом потоке ДСК обе сковороды располагаются на небольшой пластине материала с известным (откалиброванным) тепловым сопротивлением K. Температура калориметра линейно повышается со временем (сканируется), т. Е. Скорость нагрева
остается постоянным. На этот раз линейность требует хорошей конструкции и хорошего (компьютеризированного) контроля температуры. Конечно, также возможны контролируемое охлаждение и изотермические эксперименты.
Обратите внимание, что эта формула (эквивалентная закону теплового потока Ньютона ) аналогична закону электрического потока Ома и намного старше его :
Когда образец внезапно поглощает тепло (например, когда образец плавится), сигнал отреагирует и покажет пик.
Это дает ряд преимуществ. Это облегчает прямое измерение теплоемкости за одно измерение даже в (квази) изотермических условиях. Он позволяет одновременно измерять тепловые эффекты, которые реагируют на изменение скорости нагрева (реверсивное) и не реагируют на изменение скорости нагрева (нереверсивное). Это позволяет оптимизировать как чувствительность, так и разрешение в одном тесте, обеспечивая медленную среднюю скорость нагрева (оптимизация разрешения) и быстро меняющуюся скорость нагрева (оптимизация чувствительности).
Калориметр для изотермического титрования
В калориметре для изотермического титрования теплота реакции используется для отслеживания эксперимента по титрованию. Это позволяет определять среднюю точку ( стехиометрию ) (N) реакции, а также ее энтальпию (дельта H), энтропию (дельта S) и, что имеет первостепенное значение, аффинность связывания (Ka).
История калориметра, детали, типы и их характеристики
калориметр представляет собой устройство, которое используется для измерения изменения температуры определенного количества вещества (обычно воды) с известной удельной теплоемкостью. Это изменение температуры связано с поглощением или выделением тепла в исследуемом процессе; химический, если это реакция, или физический, если он состоит из изменения фазы или состояния.
В лаборатории самый простой калориметр, который можно найти, это калориметр. Он используется для измерения тепла, поглощенного или выделенного в реакции при постоянном давлении, в водном растворе. Реакции выбираются так, чтобы избежать вмешательства реагентов или газообразных продуктов..
Количество тепла, которое выделяется в реакции = количество тепла, поглощенного калориметром + количество тепла, поглощенного раствором
Количество тепла, поглощаемое калориметром, называется калориметрической емкостью калориметра. Это определяется подачей известного количества тепла в калориметр с заданной массой воды. Затем измеряют повышение температуры калориметра и содержащегося в нем раствора..
С этими данными и использованием удельной теплоемкости воды (4,18 Дж / г ºC) можно рассчитать калорийность калориметра. Эта емкость также называется постоянной калориметра.
С другой стороны, тепло, получаемое водным раствором, равно m · ce · Δt. В формуле m = масса воды, ce = удельная теплоемкость воды и Δt = изменение температуры. Зная все это, можно рассчитать количество тепла, выделяемое экзотермической реакцией..
История калориметра
В 1780 году французский ученый А. Л. Лавуазье, считающийся одним из отцов химии, использовал морскую свинку, чтобы измерить выработку тепла при дыхании..
Как? Использование устройства, похожего на калориметр. О тепле, производимом морской свинкой, свидетельствует таяние снега, окружавшего аппарат.
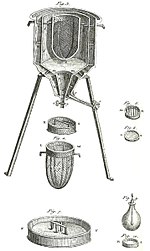
Исследователи А. Л. Лавуазье (1743-1794) и П. С. Лаплас (1749-1827) разработали калориметр, который использовался для измерения удельной теплоты тела методом таяния льда.
Калориметр состоял из луженого цилиндрического стакана, покрытого лаком, удерживаемого штативом и внутренне ограниченного воронкой. Внутри было помещено еще одно стекло, похожее на предыдущее, с трубкой, проходящей через внешнюю камеру и снабженной ключом. Внутри второго стекла была сетка.
В эту сетку помещалось существо или объект, удельное тепло которого было желательно определить. Лед был помещен внутри концентрических сосудов, как в корзине.
Тепло, выделяемое телом, поглощалось льдом, вызывая его слияние. И жидкий водный продукт таяния льда собирали, открывая ключ внутреннего стекла.
И, наконец, при взвешивании воды масса расплавленного льда была известна.
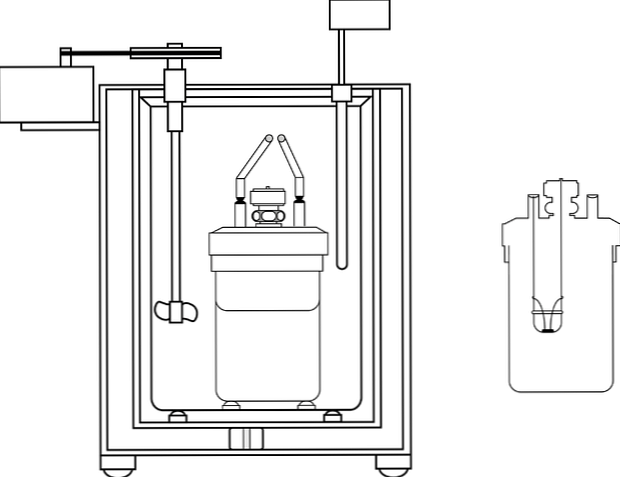
части
Изображение показывает части калориметрического насоса; Тем не менее, можно заметить, что он имеет термометр и мешалку, общие элементы в нескольких калориметрах.
Типы и их характеристики
Кофейная чашка
Это тот, который используется для определения тепла, выделяемого экзотермической реакцией, и тепла, поглощаемого в эндотермической реакции..
Калориметрический насос
Это устройство, в котором измеряется количество тепла, которое выделяется или поглощается в реакции, которая происходит при постоянном объеме..
Реакция протекает в прочном стальном сосуде (насосе), который погружается в большой объем воды. Это делает изменения температуры воды небольшими. Следовательно, предполагается, что изменения, связанные с реакцией, измеряются при постоянной температуре и объеме..
Вышесказанное указывает на то, что при проведении реакции в калориметрическом насосе работа не выполняется..
Реакция начинается с подачи электричества через кабели, подключенные к насосу.
Адиабатический калориметр
Он характеризуется наличием изолирующей структуры, называемой экраном. Экран расположен вокруг ячейки, где происходят изменения температуры и тепла. Он также подключен к электронной системе, которая поддерживает свою температуру очень близко к температуре элемента, чтобы избежать передачи тепла.
В адиабатическом калориметре разница температур между калориметром и его окружением сводится к минимуму; а также минимизировать коэффициент теплопередачи и время теплообмена.
Его части состоят из следующего:
-Ячейка (или контейнер), интегрированная в систему изоляции, с помощью которой пытаются избежать потери тепла.
-Термометр, для измерения изменений температуры.
-Нагреватель, подключенный к контролируемому источнику электрического напряжения.
-И щит, уже упоминавшийся.
В калориметре этого типа могут быть определены такие свойства, как энтропия, температура Дебая и плотность электронного состояния..
Изопериболический калориметр
Это устройство, в котором реакционная ячейка и насос погружены в конструкцию, называемую рубашкой. В этом случае так называемая рубашка состоит из воды, поддерживаемой при постоянной температуре.
Температура ячейки и насоса повышается при выделении тепла во время процесса сгорания; но температура водяной рубашки поддерживается на фиксированной температуре.
Микропроцессор контролирует температуру ячейки и кожуха, внося необходимые поправки в тепло утечки, возникающее в результате различий между двумя температурами..
Эти поправки применяются непрерывно и с окончательной поправкой, основанной на измерениях до и после испытания..
Проточный калориметр
Разработанный Caliendar, он имеет устройство для перемещения газа в контейнере с постоянной скоростью. При добавлении тепла измеряется увеличение температуры в жидкости..
Проточный калориметр характеризуется:
— Точное измерение постоянного расхода.
— Точное измерение количества тепла, вводимого в жидкость через нагреватель.
— Точное измерение повышения температуры в газе, вызванное подводом энергии
— Конструкция для измерения емкости газа под давлением.
Калориметр для дифференциальной сканирующей калориметрии
Он характеризуется наличием двух контейнеров: в одном помещается исследуемый образец, в то время как другой остается пустым или используется контрольный материал.
Два сосуда нагреваются с постоянной скоростью энергии с помощью двух независимых нагревателей. Когда начинается нагрев двух емкостей, компьютер будет отображать разницу тепловых потоков нагревателей в зависимости от температуры, что позволяет определить поток тепла..
Кроме того, можно определить изменение температуры как функции времени; и, наконец, калорийность.
приложений
По физикохимии
-Основные калориметры, типа кофейной чашки, позволяют измерять количество тепла, которое организм выделяет или поглощает. Они могут определить, является ли реакция экзотермической или эндотермической. Кроме того, удельная теплоемкость тела может быть определена.
-С помощью адиабатического калориметра удалось определить энтропию химического процесса и электронную плотность состояния.
В биологических системах
-Микрокалориметры используются для изучения биологических систем, которые включают взаимодействия между молекулами, а также происходящие конформационные изменения молекул; например, при развертывании молекулы. Линия включает в себя как дифференциальное сканирование, так и изотермическое титрование.
-Микрокалориметр используется при разработке лекарственных препаратов малых молекул, биотерапевтических средств и вакцин..
Кислородный насос калориметр и калорийность
Сжигание многочисленных веществ происходит в калориметре кислородного насоса, и его калорийность может быть определена. В число веществ, изученных с помощью этого калориметра, входят: уголь и кокс; пищевые масла, как тяжелые, так и легкие; бензин и все моторные топлива.
А также виды топлива для авиационных реакторов; топливные отходы и размещение отходов; пищевые продукты и добавки для питания человека; кормовые культуры и добавки для кормления животных; строительные материалы; ракетное и ракетное топливо.
Аналогично, калорийность была определена с помощью калориметрии в термодинамических исследованиях горючих материалов; в изучении энергетического баланса в экологии; во взрывчатых веществах и термопорошках и в обучении основным термодинамическим методам.