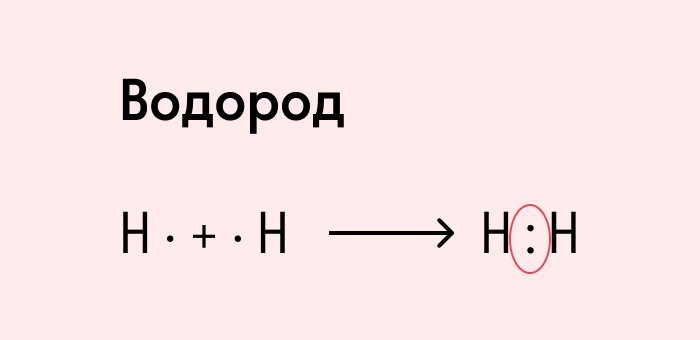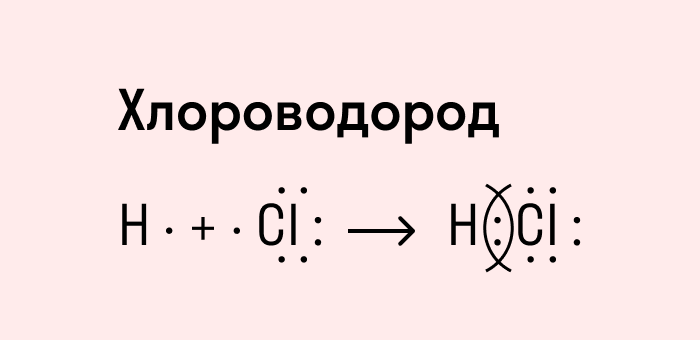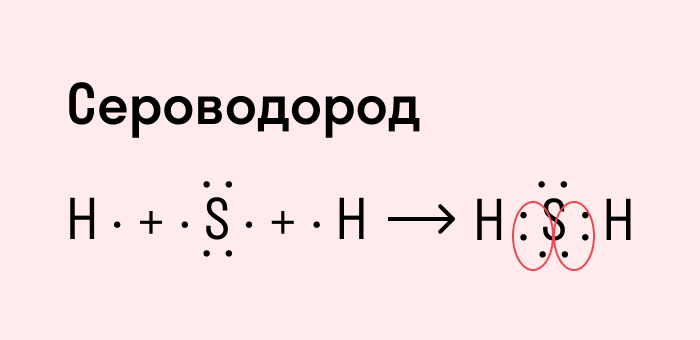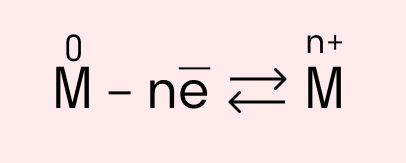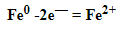Что определяет способность атома образовывать химические связи число нейтронов или число электронов
Химическая связь
Статья находится на проверке у методистов Skysmart.
Если вы заметили ошибку, сообщите об этом в онлайн-чат (в правом нижнем углу экрана).
Химическая связь и строение вещества
Все системы стремятся к равновесию и к уменьшению свободной энергии — так гласит один из постулатов химической термодинамики. Атомы, взаимодействующие в молекуле вещества, тоже подчиняются этому закону. Они стремятся образовать устойчивую конфигурацию — 8-электронную или 2-электронную внешнюю оболочку. Этот процесс взаимодействия называется химической связью, благодаря ему получаются молекулы и молекулярные соединения.
| Химическая связь — это взаимодействие между атомами в молекуле вещества, в ходе которого два электрона (по одному от каждого атома) образуют общую электронную пару либо электрон переходит от одного атома к другому. |
Как понятно из определения химической связи, при взаимодействии двух атомов один из них может притянуть к себе внешние электроны другого. Эта способность называется электроотрицательностью (ЭО). Атом с более высокой электроотрицательностью (ЭО) при образовании химической связи с другим атомом может вызвать смещение к себе общей электронной пары.
Механизм образования химической связи
Существует два механизма взаимодействия атомов:
обменный — предполагает выделение по одному внешнему электрону от каждого атома и соединение их в общую пару;
донорно-акцепторный — происходит, когда один атом (донор) выделяет два электрона, а второй атом (акцептор) принимает их на свою свободную орбиталь.
Независимо от механизма химическая связь между атомами сопровождается выделением энергии. Чем выше ЭО атомов, т. е. их способность притягивать электроны, тем сильнее и этот энергетический всплеск.
| Энергией связи называют ту энергию, которая выделяется при взаимодействии атомов. Она определяет прочность химической связи и по величине равна усилию, необходимому для ее разрыва. |
Также на прочность влияют следующие показатели:
Длина связи — расстояние между ядрами атомов. С уменьшением этого расстояния растет энергия связи и увеличивается ее прочность.
Кратность связи — количество электронных пар, появившихся при взаимодействии атомов. Чем больше это число, тем выше энергия и, соответственно, прочность связи.
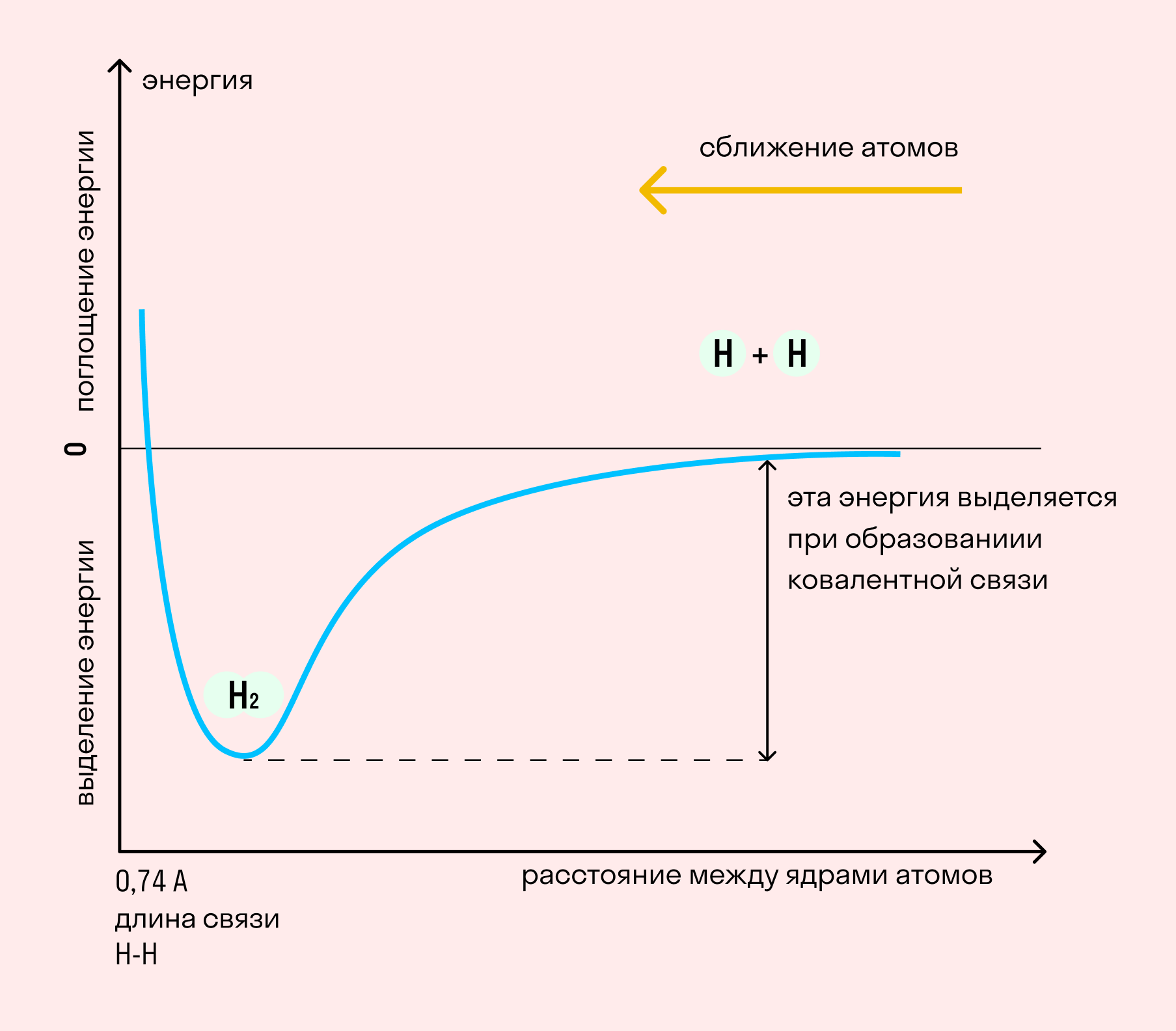
На примере химической связи в молекуле водорода посмотрим, как меняется энергия системы при сокращении расстояния между ядрами атомов. По мере сближения ядер электронные орбитали этих атомов начинают перекрывать друг друга, в итоге появляется общая молекулярная орбиталь. Неспаренные электроны через области перекрывания смещаются от одного атома в сторону другого, возникают общие электронные пары. Все это сопровождается нарастающим выделением энергии. Сближение происходит до тех пор, пока силу притяжения не компенсирует сила отталкивания одноименных зарядов.
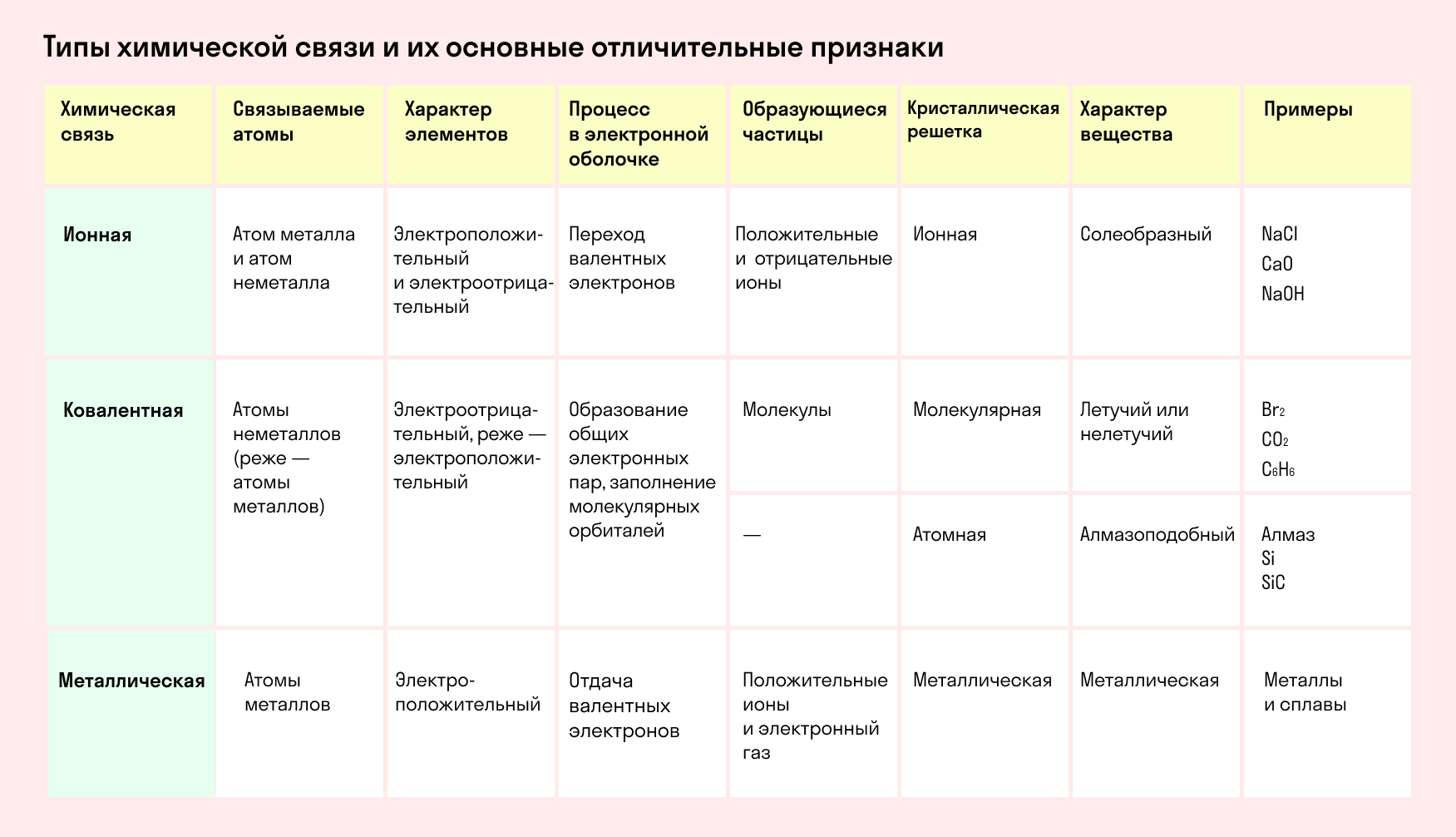
Основные типы химических связей
Различают четыре вида связей в химии: ковалентную, ионную, металлическую и водородную. Но в чистом виде они встречаются редко, обычно имеет место наложение нескольких типов химических связей. Например, в молекуле фосфата аммония (NH4)3PO4присутствует одновременно ионная связь между ионами и ковалентная связь внутри ионов.
Также отметим, что при образовании кристалла от типа связи между частицами зависит, какой будет кристаллическая решетка. Если это ковалентная связь — образуется атомная решетка, если водородная — молекулярная решетка, а если ионная или металлическая — соответственно, будет ионная или металлическая решетка. Таком образом, влияя на тип кристаллической решетки, химическая связь определяет и физические свойства вещества: твердость, летучесть, температуру плавления и т. д.
Основные характеристики химической связи:
насыщенность — ограничение по количеству образуемых связей из-за конечного числа неспаренных электронов;
полярность — неравномерная электронная плотность между атомами и смещение общей пары электронов к одному из них;
направленность — ориентация связи в пространстве, расположение орбиталей атомов под определенным углом друг к другу.
Ковалентная связь
Как уже говорилось выше, этот тип связи имеет два механизма образования: обменный и донорно-акцепторный. При обменном механизме объединяются в пару свободные электроны двух атомов, а при донорно-акцепторном — пара электронов одного из атомов смещается к другому на его свободную орбиталь.
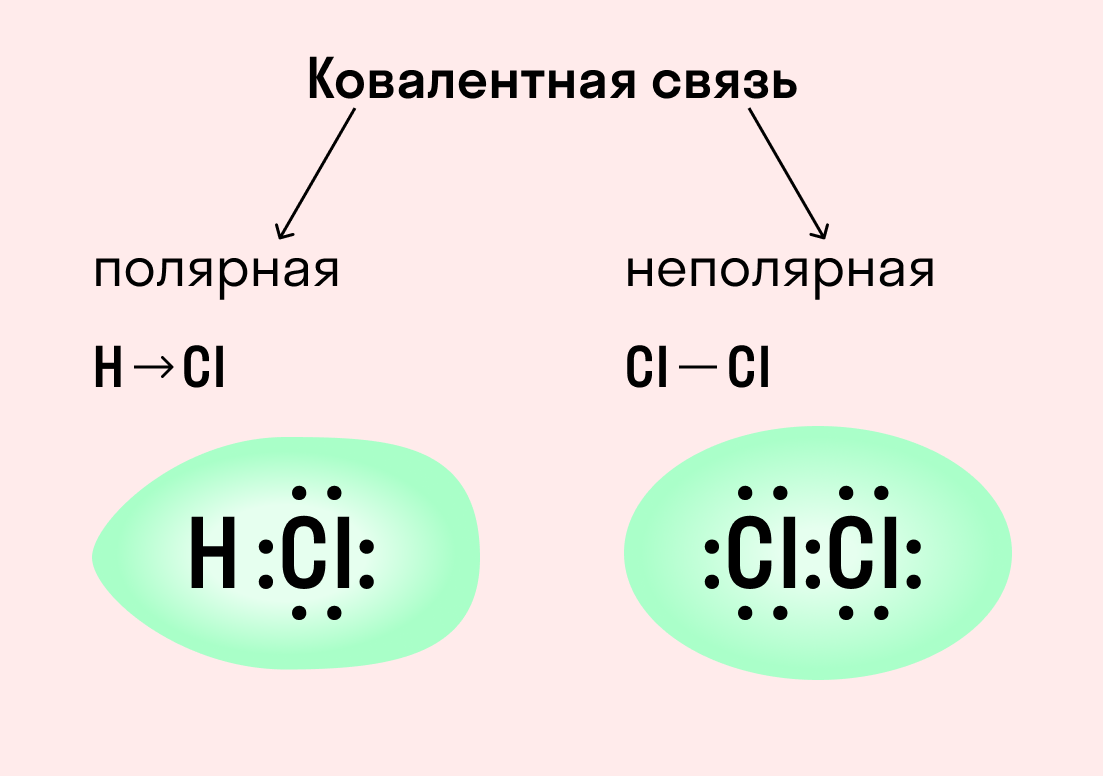
| Ковалентная связь — это процесс взаимодействия между атомами с одинаковыми или близкими радиусами, при котором возникает общая электронная пара. Если эта пара принадлежит в равной мере обоим взаимодействующим атомам — это неполярная связь, а если она смещается к одному из них — это полярная связь. |
Как вы помните, сила притяжения электронов определяется электроотрицательностью атома. Если у двух атомов она одинакова, между ними будет неполярная связь, а если один из атомов имеет большую ЭО — к нему сместится общая электронная пара и получится полярная химическая связь.
Ковалентная неполярная связь образуется в молекулах простых веществ, неметаллов с одинаковой ЭО: Cl2, O2, N2, F2 и других.
Посмотрим на схему образования этой химической связи. У атомов водорода есть по одному внешнему электрону, которые и образуют общую пару.
Ковалентная полярная связь характерна для неметаллов с разным уровнем ЭО: HCl, NH3,HBr, H2O, H2S и других.
Посмотрим схему такой связи в молекуле хлороводорода. У водорода имеется один свободный электрон, а у хлора — семь. Таким образом, всего есть два неспаренных электрона, которые соединяются в общую пару. Поскольку в данном случае ЭО выше у хлора, эта пара смещается к нему.
Другой пример — молекула сероводорода H2S. В данном случае мы видим, что каждый атом водорода имеет по одной химической связи, в то время как атом серы — две. Количество связей определяет валентность атома в конкретном соединении, поэтому валентность серы в сероводороде — II.
Число связей, которые могут быть у атома в молекуле вещества, называется валентностью.
Характеристики ковалентной связи:
Ионная связь
Как понятно из названия, данный тип связи основан на взаимном притяжении ионов с противоположными зарядами. Он возможен между веществами с большой разницей ЭО — металлом и неметаллом. Механизм таков: один из атомов отдает свои электроны другому атому и заряжается положительно. Второй атом принимает электроны на свободную орбиталь и получает отрицательный заряд. В результате этого процесса образуются ионы.
| Ионная связь — это такое взаимодействие между атомами в молекуле вещества, итогом которого становится образование и взаимное притяжение ионов. |
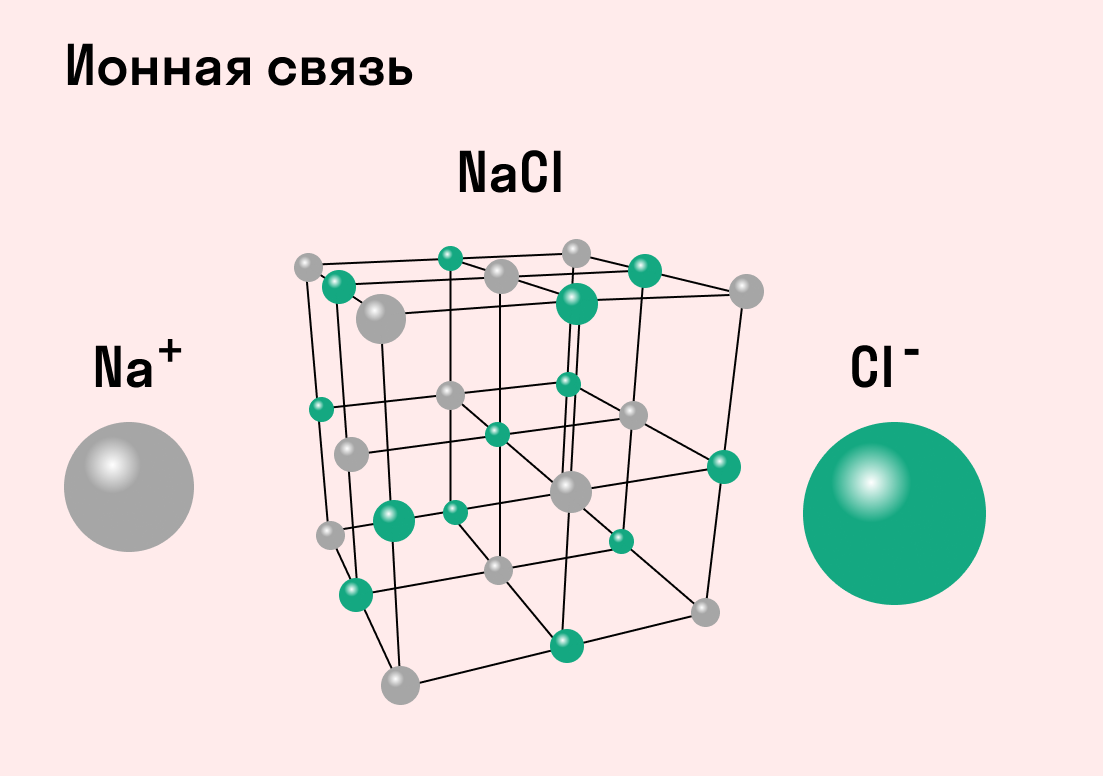
Разноименно заряженные ионы стремятся друг к другу за счет кулоновского притяжения, которое одинаково направлено во все стороны. Благодаря этому притяжению образуются ионные кристаллы, в решетке которых заряды ионов чередуются. У каждого иона есть определенное количество ближайших соседей — оно называется координационным числом.
Обычно ионная связь появляется между атомами металла и неметалла в таких соединениях, как NaF, CaCl2, BaO, NaCl, MgF2, RbI и других. Ниже схема ионной связи в молекуле хлорида натрия.
Характеристики ионной связи:
не имеет направленности.
Ковалентная и ионная связь в целом похожи, и одну из них можно рассматривать, как крайнее выражение другой. Но все же между ними есть существенная разница. Сравним эти виды химических связей в таблице.
Характеризуется появлением электронных пар, принадлежащих обоим атомам.
Характеризуется появлением и взаимным притяжением ионов.
Общая пара электронов испытывает притяжение со стороны обоих ядер атомов.
Ионы с противоположными зарядами подвержены кулоновскому притяжению.
Имеет направленность и насыщенность.
Ненасыщенна и не имеет направленности.
Количество связей, образуемых атомом, называется валентностью.
Количество ближайших соседей атома называется координационным числом.
Образуется между неметаллами с одинаковой или не сильно отличающейся ЭО.
Образуется между металлами и неметаллами — веществами со значимо разной ЭО.
Металлическая связь
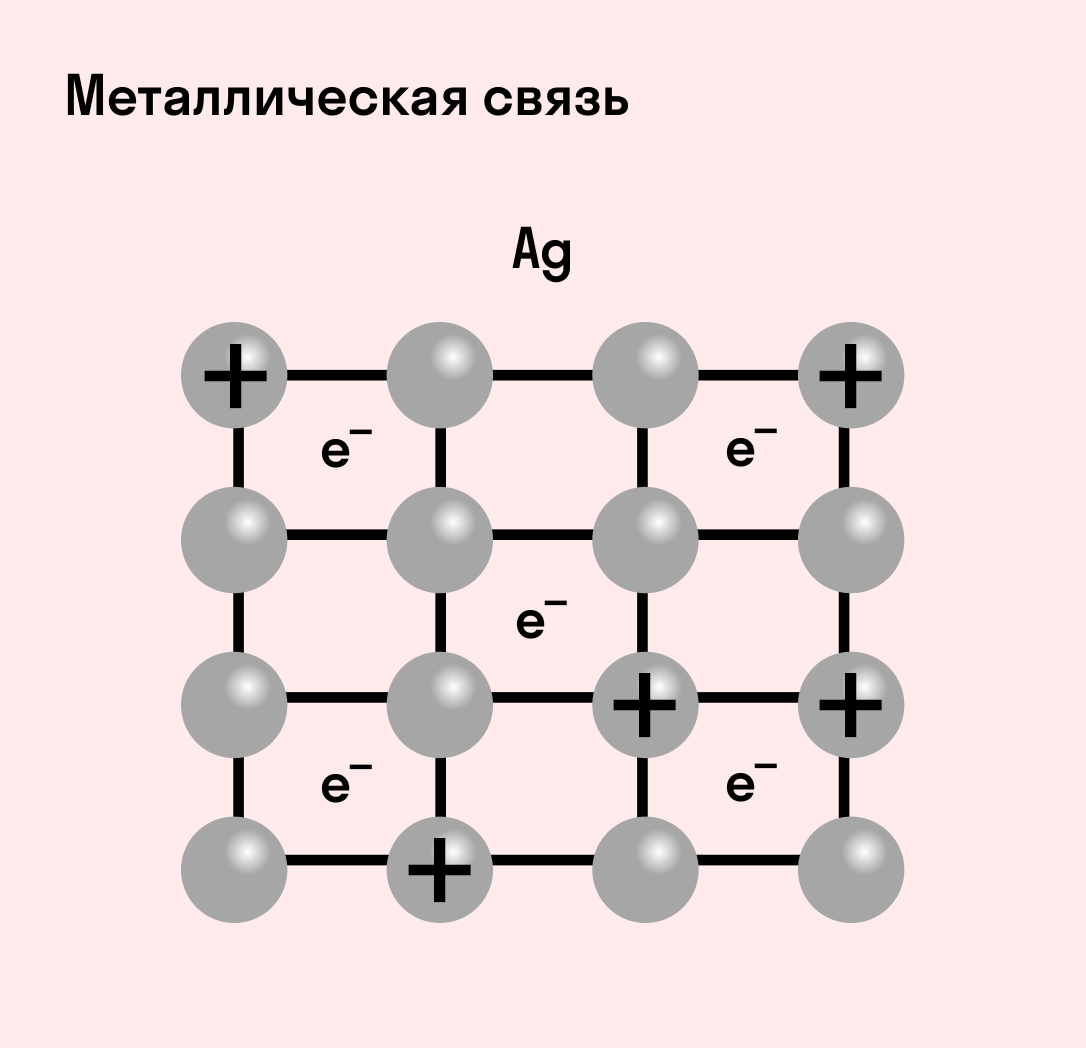
Отличительная особенность металлов в том, что их атомы имеют достаточно большие радиусы и легко отдают свои внешние электроны, превращаясь в положительно заряженные ионы (катионы). В итоге получается кристаллическая решетка, в узлах которой находятся ионы, а вокруг беспорядочно перемещаются электроны проводимости, образуя «электронное облако» или «электронный газ».
Свободные электроны мигрируют от одного иона к другому, временно соединяясь с ними и снова отрываясь в свободное плавание. Этот механизм по своей природе имеет сходство с ковалентной связью, но взаимодействие происходит не между отдельными атомами, а в веществе.
| Металлическая связь — это взаимодействие положительных ионов металлов и отрицательно заряженных электронов, которые являются частью «электронного облака», рассеянного по всему объему вещества. |
Наличие такого «электронного облака», которое может прийти в направленное движение, обусловливает электропроводность металлов. Другие их качества — пластичность и ковкость, объясняются тем, что ионы в кристаллической решетке легко смещаются. Поэтому металл при ударном воздействии способен растягиваться, но не разрушаться.
Характеристики металлической связи:
Металлическая связь присуща как простым веществам — таким как Na, Ba, Ag, Cu, так и сложным сплавам — например, AlCr2, CuAl11Fe4, Ca2Cu и другим.
Схема металлической связи:
M — металл,
n — число свободных внешних электронов.
К примеру, у железа в чистом виде на внешнем уровне есть два электрона, поэтому его схема металлической связи выглядит так:
Обобщим все полученные знания. Таблица ниже описывает кратко химические связи и строение вещества.
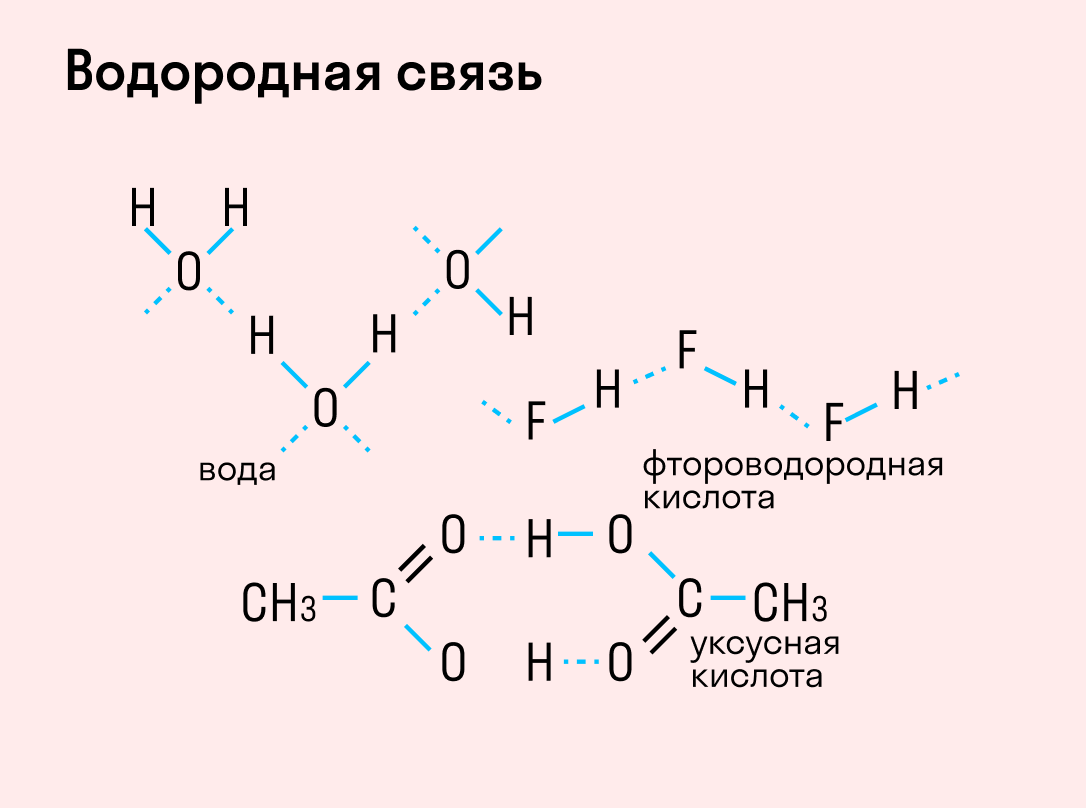
Водородная связь
Данный тип связи в химии стоит отдельно, поскольку он может быть как внутри молекулы, так и между молекулами. Как правило, у неорганических веществ эта связь происходит между молекулами.
| Водородная связь образуется между молекулами, содержащими водород. Точнее, между атомами водорода в этих молекулах и атомами с большей ЭО в других молекулах вещества. |
Объясним подробнее механизм этого вида химической связи. Есть молекулы А и В, содержащие водород. При этом в молекуле А есть электроотрицательные атомы, а в молекуле В водород имеет ковалентную полярную связь с другими электроотрицательными атомами. В этом случае между атомом водорода в молекуле В и электроотрицательным атомом в молекуле А образуется водородная связь.
Такое взаимодействие носит донорно-акцепторный характер. Донором электронов в данном случае выступают электроотрицательные элементы, а акцептором — водород.
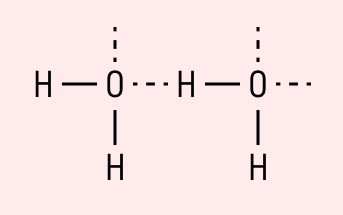
Графически водородная связь обозначается тремя точками. Ниже приведена схема такого взаимодействия на примере молекул воды.
Характеристики водородной связи:
Кратко о химических связях
Итак, самое главное. Химической связью называют взаимодействие атомов, причиной которого является стремление системы приобрести устойчивое состояние. Во время взаимодействия свободные внешние электроны атомов объединяются в пары либо внешний электрон одного атома переходит к другому.
Образование химической связи сопровождается выделением энергии. Эта энергия растет с увеличением количества образованных электронных пар и с сокращением расстояния между ядрами атомов.
Основные виды химических связей: ковалентная (полярная и неполярная), ионная, металлическая и водородная. В отличие от всех остальных водородная ближе к молекулярным связям, поскольку может быть как внутри молекулы, так и между разными молекулами.
Как определить тип химической связи:
Ковалентная полярная связь образуется в молекулах неметаллов между атомами со сходной ЭО.
Ковалентная неполярная связь имеет место между атомами с разной ЭО.
Ионная связь ведет к образованию и взаимному притяжению ионов. Она происходит между атомами металла и неметалла.
Металлическая связь бывает только между атомами металлов. Это взаимодействие положительных ионов в кристаллической решетке и свободных отрицательных электронов. Масса рассеянных по всему объему свободных электронов представляет собой «электронное облако».
Водородная связь появляется при условии, что есть атом с высокой ЭО и атом водорода, связанный с другой электроотрицательной частицей ковалентной связью.
Химическая связь и строение молекулы: типом химической связи определяется кристаллическая решетка вещества: ионная, металлическая, атомная или молекулярная.
Определить тип химической связи в 8 классе поможет таблица.
Что определяет способность атома образовывать химические связи число нейтронов или число электронов
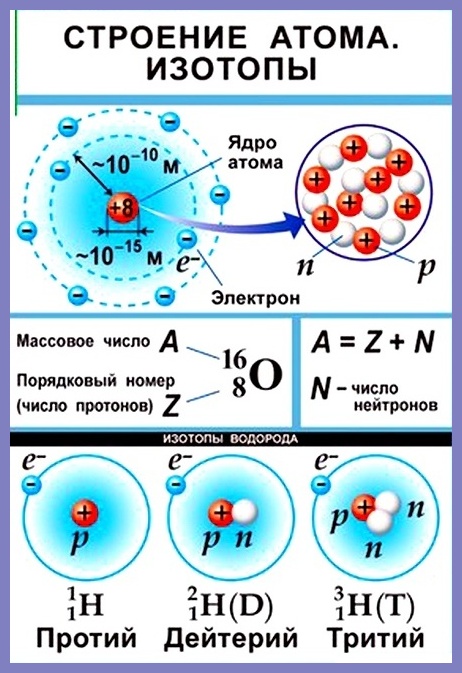
Ключевые слова конспекта: строение атома, элементарные частицы, протоны и электроны в атомах, атомный номер, массовой число, число нейтронов, нуклид, изотопы, ионы, катионы, заряд иона.
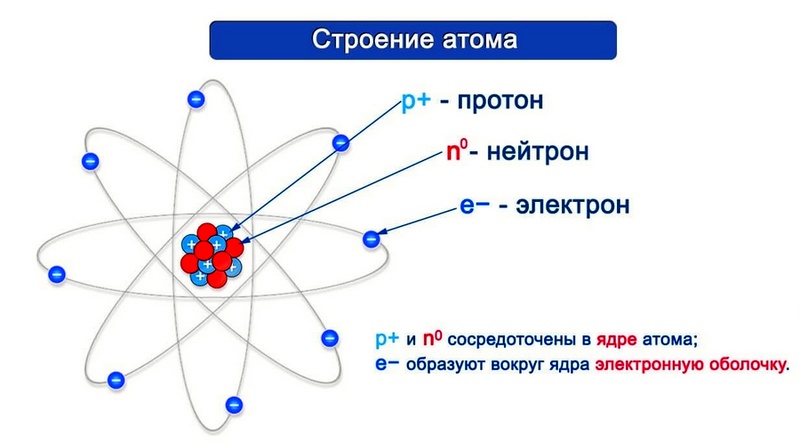
Согласно модели Резерфорда каждый атом состоит из находящегося в его центре ядра и электронной оболочки. Весь положительный заряд и почти вся масса атома сосредоточены в его ядре. Электроны движутся вокруг ядра. Число электронов атома равно положительному заряду ядра.
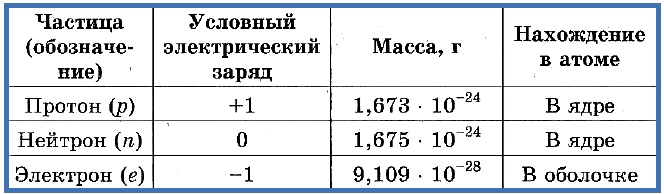
Элементарные частицы — это протоны, электроны и нейтроны, из них состоят все атомы.
Таблица 1. «Элементарные частицы атома»
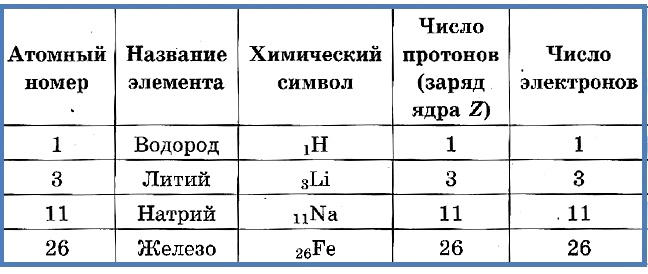
Число протонов разное у атомов различных видов, оно определяет заряд ядра атома и равно атомному номеру элемента в таблице Менделеева. Поскольку атом — электро-нейтральная частица, число электронов в нем равно числу протонов.
Таблица 2. «Протоны и электроны в атомах»
Атомный номер указывают слева внизу от символа элемента, например: 1Н, 26Fe. Обозначение атомного номера — прописная латинская буква Z.
Массовое число атома А — это сумма чисел его протонов и нейтронов в ядре. Массовое число указывают слева вверху от символа элемента или добавляют к названию элемента через дефис, например: 23 Na или натрий-23.
Массовое число кислорода, А( 16 О) = 16 = (8р + 8n).
Число нейтронов N в ядре атома определяют по формуле: N = A — Z. Например, для атома натрия с массовым числом 23, 23 Na: А = 23, Z = 11, N = А – Z = 23 — 11 = 12.
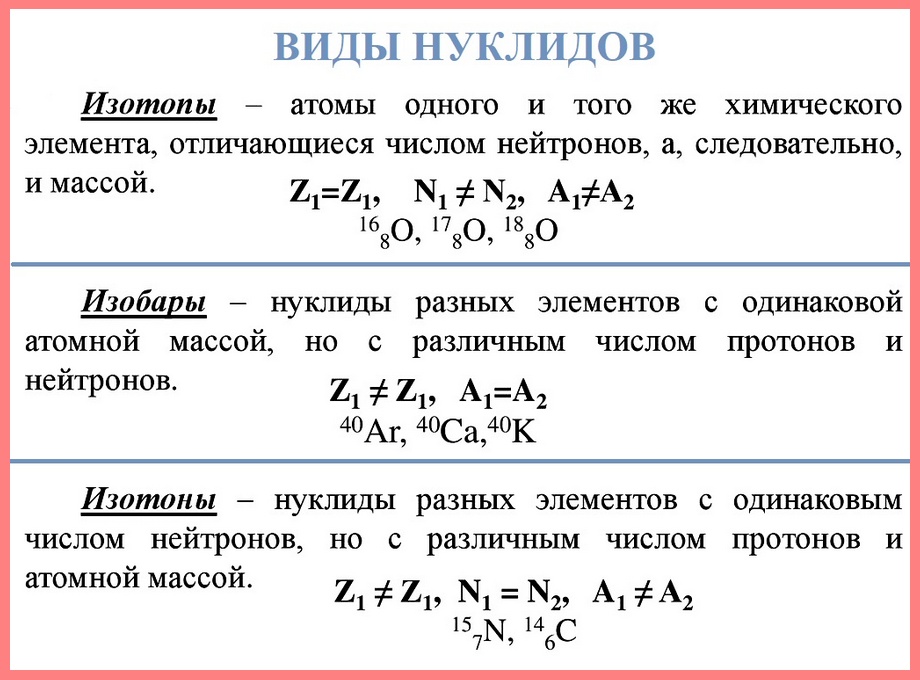
Нуклид — это вид атомов с определенным числом протонов и нейтронов в ядре. Например, в природе встречается три вида нуклидов кислорода: 16 О, 17 О и 18 О.
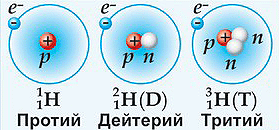
Изотопы — это атомы одного вида с одинаковым числом протонов, но разным числом нейтронов. Так, атомы 16 О, 17 О и 18 О — это изотопы. Природные изотопы урана — 234 U, 235 U и 238 U.
Таблица 3. «Обозначение и название ионов»
Конспект урока по химии «Строение атома».
Просто о химии. Атом.
Для того что бы понимать химические процессы необходимо подробно знать строение атома.
Атом состоит из положительно заряженного ядра и отрицательно заряженных электронов.
Ядро атома состоит из двух видов частиц: нейтронов, не имеющих заряда и положительно заряженных протонов, которые и определяют положительный заряд ядра.
Вокруг ядра атома вращаются отрицательно заряженные электроны, образующие электронное облако – совокупность всех электронов в атоме. О том, что такое электронное облако и электронное строение атома будет отдельная тема.
Число протонов равно числу электронов, поэтому атом – электронейтральная частица. Вспомните из школьного курса химии формулу: A = Z + N
Масса протонов и нейтронов приблизительно одинакова и равна
1,67 * 10^(-27) кг. Масса электрона, в свою очередь, примерно равна 9,11 * 10^(-31) кг, поэтому основная масса атома сосредоточена в ядре.
Рассмотрим основные параметры, характеризующие атом
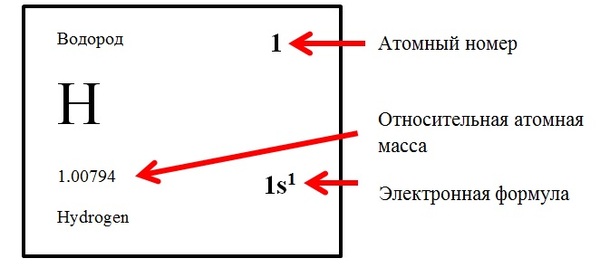
Атомный номер (порядковый номер) Z – номер химического элемента, определяемый по периодической системе элементов. Атомный номер элемента показывает количество протонов и электронов в элементе.
Атомная масса, а точнее относительная атомная масса – масса атома, выраженная в атомных единицах массы (а.е.м.). Она определяется как отношение массы данного атома к 1/12 массы нейтрального изотопа углерода 12С.
К понятию атомная масса близко понятие массовое число А – сумма чисел протонов и нейтронов (нуклонов) атома. Но численно оно равно только для изотопа углерода 12С, для остальных элементов массовое число – целочисленное значение, а относительная атомная масса нет. Например: массовое число изотопа водорода равно 1, а относительная атомная масса 1,00794 (см картинку)
А что такое изотопы?
Электронная формула (конфигурация) – порядок заполнения электронов по различным электронным оболочкам.
Думаю, что на это стоит остановиться, ибо все в одном посте не охватишь.
Следующие посты будут посвящены электронному строению атома, истории открытия атома и развитию представлений о его строении.
Лучше дальше в глубь про элементарные частицы на понятном русском
Про водород не знала. Спасибо.
Будете рассказывать про атомные орбитали, не ограничтесь d и f-орбиталями.
автор решил копировать учебник по химии?
Но ведь доказано, что это коммунистические бредни.
В чем смысл? Это ведь даже баяном назвать нельзя. В любом учебнике, на любом обучающем химии сайте открыл и читаешь. Где так же кратко, где короче, где длиннее. Еще и коряво местами, чу.
Странно, атом неделимый, но он делится. Так может через Х-лет и частички атома начнем делить, а потом частички частичек. Вот будет весело через ХХХ-лет, когда на атоме будут жить наши разумные потомки и недоумевать почему же наша планета неделимая.
Что скрывают протоны?
Двадцать лет назад физики начали исследовать загадочную асимметрию внутреннего строения протона. Результаты их работы, опубликованные в конце февраля 2021 года, объясняют, как антивещество помогает стабилизировать ядро каждого атома.
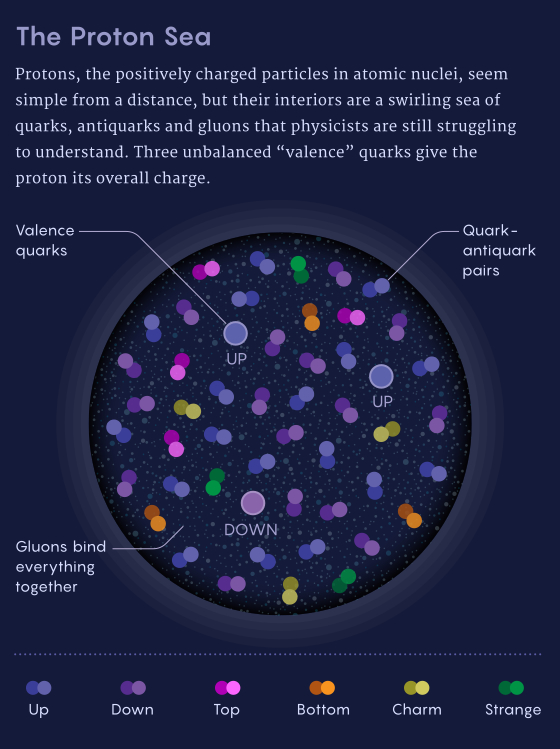
Очень редко упоминается тот факт, что протоны — позитивно заряженные частицы в центре атома — являются отчасти антивеществом.
Издалека кажется, что протон состоит из трех частиц под названием кварки. Но если приглядеться получше, можно увидеть множество появляющихся и исчезающих частиц.
На самом деле, внутри протона вращается вихрь из меняющегося количества шести типов кварков, их противоположно заряженных аналогов из антивещества (антикварков) и глюонов, элементарных безмассовых частиц, которые связывают вместе другие частицы, трансформируются в них и быстро множатся. Каким-то образом этот бурлящий вихрь оказывается совершенно стабильным и на первый взгляд простым, имитируя по определенным аспектам трио кварков. «То, как это все функционирует, честно говоря, похоже на чудо», — отметил Дональд Гисаман, физик-ядерщик из Аргоннской национальной лаборатории в Иллинойсе.
Тридцать лет назад исследователи обнаружили поразительное свойство этого «протонного моря». Теоретики ожидали, что различные типы антивещества в нем будут распределены равномерно, но было похоже, что количество нижних антикварков значительно превышало количество верхних антикварков. Затем десять лет спустя другая группа исследователей заметила намеки на неподдающиеся объяснению вариации в соотношении верхних и нижних антикварков. Но эти результаты были на грани чувствительности эксперимента.
Итак, 20 лет назад Дональд Гисаман и его коллега Пол Раймер начали работать над новым экспериментом, чтобы получше разобраться в этом вопросе. Эксперимент, получивший название SeaQuest («Морской квест»), наконец завершился, и исследователи опубликовали его результаты в журнале Nature. Они измерили внутреннее антивещество протона тщательнее, чем когда бы то ни было, и обнаружили, что на каждый верхний антикварк в среднем приходится 1,4 нижних антикварка.
Самуэль Веласко / Quanta Magazine
Эти данные непосредственно говорят в пользу двух теоретических моделей протонного моря. «Появилось первое реальное доказательство, подтверждающее эти модели», — сказал Раймер.
Одна из них — модель «пионного облака» — это популярный подход, существующий уже несколько десятилетий, который делает упор на тенденцию протона испускать и реабсорбировать частицы под названием пионы, которые принадлежат к группе частиц, известных как мезоны. Вторая, так называемая статистическая модель, рассматривает протон как контейнер, наполненный газом.
Дальнейшие запланированные эксперименты помогут исследователям выбрать одну из этих двух моделей. Но какая бы из них ни была верной, массив данных эксперимента SeaQuest о внутреннем антивеществе протона принесет непосредственную пользу, особенно физикам, которые сталкивают протоны на околосветовых скоростях на Большом адронном коллайдере. Обладая точной информацией о составе сталкиваемых объектов, они смогут более эффективно разбирать продукты, оставшиеся после столкновения, в поисках доказательств существования новых частиц или эффектов. Хуан Рохо из Амстердамского свободного университета, который оказывает помощь в анализе данных БАК, считает, что результаты эксперимента SeaQuest могут иметь большое влияние на поиски новой физики, которые в настоящее время «ограничены нашими знаниями о структуре протона, в частности о его антивеществе».
В течение короткого периода времени около полувека назад физики полагали, что разобрались с протоном.
В 1964 году Мюррей Гелл-Манн и Джордж Цвейг независимо друг от друга предложили модель, получившую впоследствии название кварковая: идея заключалась в том, что протоны, нейтроны и связанные с ними более редкие частицы представляют собой пучки из трех кварков (как их назвал Гелл-Манн), а пионы и другие мезоны состоят из одного кварка и одного антикварка. Такая схема объясняла какофонию частиц, разлетающихся из ускорителей частиц высокой энергии, поскольку спектр их зарядов мог быть построен из двух- и трехчастных комбинаций. Затем, примерно в 1970 году, исследователи, работающие на Стэнфордском линейном ускорителе (SLAC), казалось, подтвердили кварковую модель: выстрелив высокоскоростными электронами в протоны, они увидели, как электроны отрикошетили от объектов внутри.
Но вскоре картина стала менее ясной. «По мере того, как мы все тщательнее пытались измерить свойства этих трех кварков, мы обнаружили, что происходит что-то еще», — сказал Чак Браун, 80-летний член команды SeaQuest из Национальной ускорительной лаборатории им. Энрико Ферми (Фермилаб), работающий над кварковыми экспериментами с 1970-х годов.
Изучение импульса трех кварков показало, что их массы составляют малую часть общей массы протона. Кроме того, когда исследователи на SLAC стреляли электронами на большей скорости в протоны, они увидели, что электроны отталкивают больше частиц внутри. Чем быстрее электроны, тем короче их длина волны, что сделало их чувствительными к более мелким элементам протона; это похоже на увеличение разрешения микроскопа. Открывались все новые и новые внутренние частицы, которым, казалось, нет конца. «Мы не знаем, где предел и какое самое высокое разрешение возможно получить», — сказал Гисаман.
Результаты стали иметь больше смысла, когда физики разработали истинную теорию, к которой кварковая модель лишь приближается: квантовая хромодинамика или КХД. КХД, сформулированная в 1973 году, описывает «сильное взаимодействие», самую большую силу в природе, с помощью которой частицы под названием глюоны связывают пучки кварков.
КХД предсказывает тот самый вихрь, который был выявлен в экспериментах по рассеянию. Сложности возникают из-за того, что глюоны ощущают ту самую силу, которую они несут. Этим они отличаются от фотонов, несущих более простую электромагнитную силу. Это «самоуправство» создает беспорядок внутри протона, давая глюонам полную свободу действий для возникновения, размножения и расщепления на кратковременные пары кварков и антикварков. Уравновешивая друг друга, эти близко расположенные противоположно заряженные кварки и антикварки издалека остаются незамеченными. Только три несбалансированных «валентных» кварка — два верхних и нижний — составляют общий заряд протона. Но физики поняли, что стреляя электронами на большей скорости, они поражали меньшие цели.
Однако странности на этом не закончились.
Из-за самоуправства глюонов уравнения КХД невозможно решить, поэтому у физиков не получалось и до сих пор не получается рассчитать точные прогнозы теории. Но у них не было оснований предполагать, что глюоны будут расщепляться на один тип пары кварк-антикварк (а именно нижний) чаще, чем на другой. «Мы ожидали, что будет появляться равное количество тех и других пар», — сказала Мэри Альберг, теоретик-ядерщик из Сиэтлского университета, объясняя свои доводы того времени.
Мэри Альберг, физик-ядерщик из Сиэтлского университета, и ее соавторы давно утверждают, что пион играет важную роль в формировании сущности протона.
Фото предоставлено Сиэтлским университетом
Вот почему исследователей из New Muon Collaboration в Женеве так шокировали результаты эксперимента по рассеянию мюонов. В 1991г. они столкнули мюоны (более тяжелые родственники электронов) с протонами и дейтронами, состоящими из одного протона и одного нейтрона, сравнили результаты и пришли к выводу, что в протонном море больше нижних антикварков, чем верхних.
Вскоре теоретики предложили несколько возможных вариантов объяснения асимметрии протона.
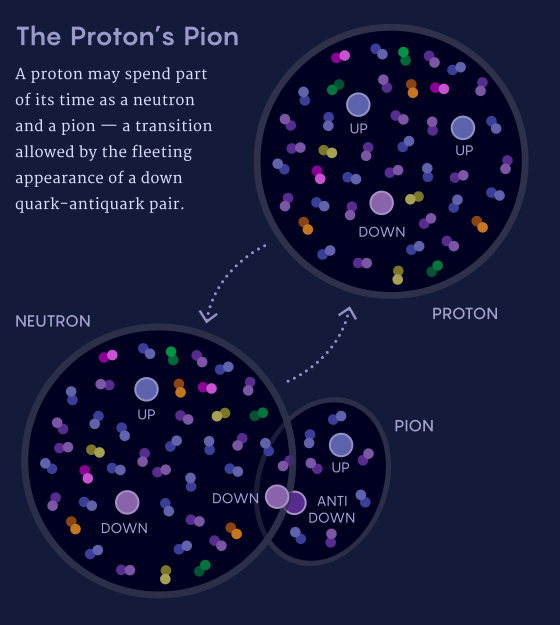
Один из них связан с пионом. С 1940-х годов физики наблюдали, как протоны и нейтроны обмениваются пионами внутри атомных ядер, как игроки в команде, бросающие друг другу баскетбольные мячи, что помогает им держаться вместе. Размышляя над структурой протона, исследователи пришли к выводу, что он также может подбрасывать баскетбольный мяч себе, то есть может ненадолго испускать положительно заряженный пион, превращаясь на это время в нейтрон, и затем реабсорбировать его. «Если во время эксперимента вы думаете, что смотрите на протон, это не так, потому что на какое-то время этот протон будет переходить в состояние пары нейтрон-пион», — сказала Альберг.
Если говорить точнее, протон превращается в нейтрон и пион, состоящий из одного верхнего кварка и одного нижнего антикварка. Поскольку этот призрачный пион имеет нижний антикварк (пион с верхним антикварком не может так легко материализоваться), такие теоретики, как Альберг, Джеральд Миллер и Тони Томас, утверждали, что модель пионного облака объясняет большее количество нижних антикварков протона, выявленное в результате измерений.
Самуэль Веласко / Quanta Magazine
Появились и другие аргументы. Клод Буррели и его коллеги из Франции разработали статистическую модель, которая рассматривает внутренние частицы протона как молекулы газа в комнате, хаотично двигающиеся на разных скоростях, которые зависят от того, целым или полуцелым количеством момента импульса обладает частица. При настройке с учетом данных многочисленных экспериментов по рассеянию модель предположила преобладание антикварков.
Прогнозы двух вышеупомянутых моделей не были идентичными. Большую часть общей массы протона составляют энергии отдельных частиц, которые прорываются в протонное море и из него, и эти частицы несут различные энергии. Модели по-разному спрогнозировали, как должно измениться соотношение верхних и нижних антикварков по мере подсчета антикварков, несущих больше энергии. Физики измеряют связанную с этим величину под названием доля импульса антикварка.
Когда исследователи в Фермилабе в 1999 году в рамках эксперимента NuSea измерили соотношение верхних и нижних антикварков в качестве функции импульса антикварка, результат их работы просто воодушевил всех, вспоминает Альберг. Эти данные свидетельствуют о том, что среди антикварков с большим импульсом (настолько большим, что они находились на грани диапазона обнаружения прибора) внезапно оказалось больше верхних антикварков, чем нижних. «Каждый теоретик говорил: ‘Погодите-ка’, — сказала Альберг, — Почему кривая развернулась, когда эти антикварки получили большую долю импульса?»
Пока теоретики ломали голову над этим вопросом, Гисаман и Раймер, которые работали над экспериментом NuSea и знали, что данным на грани иногда не стоит доверять, решили построить эксперимент, где можно было бы в комфортных условиях исследовать более широкий диапазон импульсов антикварка. Они назвали его SeaQuest.
С кучей вопросов о протоне, но без денег, они начали собирать эксперимент из использованных деталей. «Нашим девизом было: снижай количество отходов, используй повторно, перерабатывай», — сказал Раймер.
Они приобрели несколько старых сцинтилляторов в лаборатории в Гамбурге, оставшиеся детекторы частиц в Лос-Аламосской национальной лаборатории и железные пластины, блокирующие радиацию, которые изначально были использованы в циклотроне Колумбийского университета в 1950-х годах. У них получилось применить магнит размером с комнату, использованный в эксперименте NuSea, и провести свой новый эксперимент на ускорителе протонов в Фермилабе. Получившийся из этих деталей «Франкенштейн» тем не менее был не лишен своего очарования. По словам Брауна, который помог найти все части, звуковой индикатор, сигнализирующий, что протоны поступают в устройство, был сделан 50 лет назад: «Когда он издает звуковой сигнал, становится тепло на душе».
Физик-ядерщик Пол Раймер (сверху) с устройством для эксперимента SeaQuest
Эксперимент в Фермилабе, собранный в основном из использованных деталей
И наконец они его запустили. В эксперименте протоны поражают две цели: пузырек с водородом, который по сути представляет собой протоны, и пузырек с дейтерием, ядро которого состоит из одного протона и одного нейтрона.
При попадании в любую из двух целей, один из валентных кварков протона иногда аннигилирует с одним из антикварков протона или нейтрона мишени. «Аннигиляция имеет уникальную сигнатуру и производит мюон и антимюон», — сказал Раймер. Эти частицы вместе с другим «мусором», образовавшимся в результате столкновения, затем врезаются в старые железные пластины. «Мюоны могут проходить сквозь них, а все остальные частицы блокируются», — сказал он. Обнаружив мюоны на обратной стороне пластин и восстановив их исходные траектории и скорости, «вы можете восстановить хронологию событий, чтобы выяснить, какую долю импульса несут антикварки».
Поскольку протоны и нейтроны зеркально отражают друг друга, там, где у одного расположены частицы верхнего типа, у другого — нижнего типа, и наоборот. Сравнив данные из двух пузырьков, можно сразу увидеть соотношение верхних антикварков и нижних антикварков в протоне, но этому, конечно, предшествовало 20 лет работы.
В 2019 году Альберг и Миллер на основе модели пионного облака рассчитали, к каким результатам должен прийти эксперимент SeaQuest. Их прогноз вполне совпадает с новыми данными SeaQuest.
Новые данные, которые показывают постепенное повышение, а затем выход на плато в соотношении между нижними и верхними антикварками, а не внезапную реверсию, также совпадают с результатами более гибкой статистической модели, разработанной Буррели и его коллегами. И все же Миллер называет эту конкурирующую модель «описательной, а не прогнозирующей», поскольку она настроена, чтобы соответствовать данным, а не выявлять физический механизм, объясняющий преобладание антикварков. «А в наших расчетах я горжусь как раз тем, что они представляют собой истинный прогноз», — сказала Альберг. «Мы не настраивали никакие параметры заранее».
В электронном письме Буррели утверждал, что «статистическая модель более мощная, чем модель Альберга и Миллера», поскольку она учитывает эксперименты по рассеянию как с поляризованными, так и не поляризованными частицами. Миллер категорически не согласился, отметив, что модель пионных облаков объясняет не только состав антивещества протона, но и магнитные моменты различных частиц, распределение зарядов и время распада, а также «связывание и, следовательно, существование всех ядер». Он добавил, что пионный механизм «важен в широком смысле для таких вопросов, как: «Почему существуют ядра? Почему существуем мы?».
В конечном стремлении понять протон решающим фактором может быть спин или собственный момент импульса. Эксперимент по рассеянию мюонов в конце 1980-х показал, что спины трех валентных кварков протона составляют не более 30% от общего спина протона. «Кризис протонного спина» можно выразить следующим вопросом: «что же составляет остальные 70%?» И как снова сказал опытный исследователь Чак Браун, старожил Фермилаб, «должно быть, что-то еще».
Экспериментаторы будут исследовать спин протонного моря в Фермилабе и, затем, в проектируемом электронно-ионном коллайдере Брукхейвенской национальной лаборатории. Альберг и Миллер уже работают над расчетами полного «мезонного облака», окружающего протоны, которое, помимо пионов, включает более редкие «ро-мезоны» (rho mesons). В отличие от пионов, ро-мезоны обладают спином, поэтому они каким-то образом должны влиять на общий спин протона, что Альберг и Миллер и надеются определить.
По словам Брауна, эксперимент Фермилаб SpinQuest, в котором участвуют многие исследователи из SeaQuest и используются детали этого эксперимента, почти готов к работе. «Если повезет, мы получим данные этой весной; это будет зависеть, по крайней мере, частично, от прогресса в разработке вакцины против вируса. Забавно, что решение столь глубокого и непонятного вопроса о внутреннем строении ядра, зависит от ситуации с вирусом COVID в стране. Все в мире взаимосвязано, не так ли?».
Автор оригинала: Natalie Wolchover
«ЧТО ТАКОЕ РЕНТГЕН И ЧЕМ ОН ОТЛИЧАЕТСЯ ОТ ЗИВЕРТА» или «ЕДИНИЦЫ ИЗМЕРЕНИЯ РАДИАЦИИ»
Мы уже рассказывали о том, что такое радиация в принципе (см. мою первую статью здесь же). Теперь так же коротко и очень понятным языком обсудим единицы её измерения. Надо сказать, вопрос этот не слишком сложный, но, тем не менее, иногда здесь происходит некоторая путаница.
Начнём с того, что для измерения активности радиоактивных материалов в системе СИ используется такая единица как беккерель (Бк). Фактически это дело показывает то, сколько распадов в секунду происходит в данном веществе за 1 с. Поэтому 1 Бк = 1 с^-1. То есть, речь идёт именно о процессах «внутри» радионуклида, а не об информации о «радиации вокруг» него. Внесистемная единица измерения активности – кюри (Ки). 1 Ки = 3,7 * 10^7 Бк.
Теперь непосредственно о самой радиации. Существует такое понятие как экспозиционная доза. По сути, она просто характеризует способность фотонного (гамма) излучения ионизировать окружающий воздух и представляет собой отношение суммарного заряда ионов, образованных в результате действия излучения, к массе воздуха, на который это действие оказывалось. Соответственно единица измерения экспозиционной дозы – кулон на килограмм (кл/кг). Внесистемная единица измерения – это тот самый рентген (Р). 1 Р = 2,58*10^-4 кл/кг. Мощность экспозиционной дозы измеряется в амперах на килограмм (А/кг) или в рентгенах в секунду (Р/с). На практике, впрочем, часто используют рентгены в час (Р/ч). А мощность – она и есть мощность. Её значение даёт понять, «насколько сильное» гамма-излучение присутствует в данном месте, «сколько рентген воздействует на объект за секунду или за час».
Также существует понятие поглощённой дозы. Это – величина энергии ионизирующего излучения, переданная веществу. Чтобы было понятно, скажем так. Если экспозиционная доза скорее характеризует само по себе излучение (только гамма), то поглощённая – показывает именно «количество» действия излучения (какого-нибудь) на что-либо, «сколько радиации здесь подействовало на объект». Формулировки, разумеется, мягко говоря, некорректные, но весьма наглядные и понятные. В системе СИ данная величина измеряется в греях (Гр). Один грей равен одному джоулю (энергии) на килограмм (вещества) (Дж/кг). Кроме того, есть несистемная единица под название «рад», равная 0,01 Гр. Фактически именно поглощённая доза является основополагающей в дозиметрии. Она показывает именно действие энергии на вещество и применима к радиоактивному излучению любого вида. В общем и целом, в большинстве случаев можно считать, что «100 рентген гамма-излучения равны 100 радам или 1 грею». То есть, в среднем, объект, помещённый в среду, в которой наблюдается мощность гамма-излучения 100 Р/ч, за час получит дозу в 1 грей. А за 2 часа, как несложно догадаться – 2 грея. Хотя на самом деле там всё будет зависеть от конкретной энергии конкретных частиц. Но в среднем – примерно как-то так.
Теперь самое интересное. Дело в том, что разные виды излучения (альфа, бета, гамма. ) по-разному воздействуют на живые организмы. Ранее мы уже отмечали, что альфа-излучение может быть гораздо опаснее, чем бета (другой вопрос, что оно должно ещё как-то «попасть в организм», а для него это сложнее). Поэтому для оценки биологического эффекта облучения организма была придумана эквивалентная доза излучения, измеряемая в зивертах (Зв). Она равна поглощённой (организмом или его частью) дозе, умноженной на так называемый взвешивающий коэффициент данного вида излучения. То есть, величину энергии, полученной организмом или его частью, просто умножают на коэффициент, который у каждого вида излучения свой. Для гамма-излучения он равен 1. Следовательно, в этом (и самом распространённом) случае эквивалентная доза (в Зв) будет численно равна поглощённой (в Гр). Есть и внесистемная единица измерения эквивалентной дозы: бэр (биологический эквивалент рентгена), который равен 0,01 Зв. Таким образом, если человек пробыл 3 часа в местности, мощность экспозиционной дозы в которой составляет 30 Р/ч, то поглощённая им доза излучения примерно такова: 3 * 30 = 90 (рад) = 0,9 (Гр), что в эквиваленте равно 90 (бэр) или 0,9 (Зв).
Для бета-частиц и рентгеновского излучения взвешивающий коэффициент также равен 1.
Для протонного принимается равным 2.
Для альфа-частиц и осколков деления атомов – 20.
Что касается нейтронного излучения, то оно сильно различается по энергии этих самых нейтронов, и здесь коэффициент может быть от 2 до 21.
Получается, что 1 час воздействия альфа-излучения на организм как бы соответствует целым 20 часам воздействия гамма-излучения.
Всё? Нет, не всё. Излучение ещё и по-разному может действовать на различные ткани и органы организма. Например, глаза могут быть более чувствительны, чем кожа. Для оценки действия излучения на конкретные «места организма» используется ещё один коэффициент, на который умножается суммарная эквивалентная доза облучения организма. Полученная величина называется эффективной дозой и измеряется в тех же единицах, что и эквивалентная. Например, для желудка и лёгких коэффициент равен 0,12, для кожи – 0,01.
Какие конкретно эквивалентные дозы излучения приводят к развитию лучевой болезни? Это тема для отдельного разговора. Если совсем вкратце, то за довольно короткий промежуток времени человек должен успеть получить дозу 100 Р = 1 рад = 1 Гр = 100 бэр = 1 Зв (для гамма-излучения). Да, да, вероятно, именно поэтому знаменитый бар в «Сталкере» был назван именно так.
Автор: Сергей Смолин.
«ЧТО ТАКОЕ РАДИАЦИЯ» и «КАКАЯ ОНА БЫВАЕТ»
Краткая и понятная справка для самых маленьких.
В сети (и не только) иногда попадаются люди, которые не знают даже самых простых вещей про радиацию. Специально для них объясняем. Да, очень вкратце. Да, НЕ совсем научно, а, может быть, даже и НЕ совсем точно, и вообще наивно и по-детски. Но зато очень просто и ясно. А если кому-то нужно больше и правильнее – пожалуйте в Гугл.
Сначала на всякий случай напоминаем. Как известно, вещества состоят из атомов, а атомы состоят из трёх видов частиц: протонов (положительно заряженные частицы), нейтронов (нейтральные частицы), электронов (отрицательно заряженные частицы). Из протонов и нейтронов сделано ядро атома. И тех, и других называют ещё нуклонами. А электроны (которые намного меньше по массе) роятся вокруг этого ядра по специальным «орбитам» (орбиталям). Этот «рой» (облако) электронов нас сейчас не интересует. Все самые захватывающие процессы происходят в ядре.
Все эти нуклоны держатся (обычно) вместе и никуда на разлетаются. На это у них есть веские причины, называемые ядерными силами, из-за которых нуклоны притягиваются друг к другу. Строго говоря, само это явление рассматривается уже не в ядерной физике, а в физике элементарных частиц, в общем, просто поверьте, что оно есть. Помимо ядерных сил на нуклоны действуют некоторые другие силы, например, кулоновские силы отталкивания. У «обычных» стабильных изотопов притяжение нуклонов пересиливает всё остальное. И ничего интересного с такими ядрами не происходит. Однако, при некоторых условиях, например, если нейтронов получается «больше, чем нужно», или при некоторых других, могут начать происходить весьма любопытные явления. Именно это и отличает радиоактивные изотопы элементов от не радиоактивных.
Одним из таких любопытных явлений является альфа-распад. При альфа-распаде из ядра атома вылетают – кто бы мог подумать! – так называемые альфа-частицы. Они представляют собой два протона и два нейтрона (то, есть, по сути, это ядра гелия). Соответственно, в ядре остаётся меньшее число нуклонов, и данный атом становится уже атомом другого элемента. Альфа-частицы не могут улететь далеко от покинутого ядра, их пробег в воздухе составляет несколько сантиметров, а в какой-нибудь там алюминий они могут проникнуть только на доли миллиметра, не говоря уже о чём-то более плотном. Альфа-частицы притягивают к себе часть электронов из окружающей среды, чтобы стать «полноценными» атомами гелия. Соответственно, при контакте с ними соседние атомы вещества часть своих электронов теряют и становятся так называемыми ионами. Ввиду маленькой проникающей способности, альфа-излучение в подавляющем большинстве случаев не представляет опасности для человека и прочих зверюшек, так как эти частицы не способны преодолеть даже верхний омертвевший слой кожи (даже если смогут на неё попасть сквозь окружающий воздух). Однако, вещества, в которых происходит альфа-распад, могут быть чрезвычайно опасны при попадании внутрь организма. Кстати говоря, радиоактивные вещества, попав в организм, могут весьма и весьма надолго там задержаться (а некоторые прям очень надолго), то есть, воздействие получится не только гораздо более сильным, но ещё и долгим (и вот это уже относится к изотопам с любым видам распада, а не только с альфа). Именно поэтому при нахождении в некоторых опасных зонах следует пользоваться защитной одеждой и противогазом.
Второе интересное явление, касающееся предмета нашего рассмотрения – бета-распад. Здесь процесс немного более сложный. Существует такая вещь как слабое взаимодействие (тут опять физика элементарных частиц). И вот это взаимодействие при бета-распаде превращает один из нейтронов атома в протон (или наоборот). При этом, в соответствии с определёнными законами, в ядре также «образуются» две частицы. В зависимости от вида бета-распада (отрицательный или положительный), это могут быть либо электрон и антинейтрино, либо позитрон и нейтрино. «Нейтрины» оставим в покое, нам они сейчас не нужны. А вот такие вылетающие из ядер электроны/позитроны – это и есть бета-частицы. Они способны ионизировать чьи-либо атомы, вызывать химические реакции и вообще делать всякие разные вещи. Их проникающая способность – на порядок больше, чем у альфа-частиц. Пробег в воздухе может исчисляться метрами. Эти малыши вполне способны проникать в кожу человека. Вещества с бета-распадом так же очень опасны при попадании вовнутрь (хотя действие бета-частиц на организм всё-таки намного слабее, чем альфа).
Нейтронное излучение. Как несложно догадаться, это поток нейтронов. Фактически наблюдается не «само по себе», а только при ядерных реакциях (в реакторах или при тех самых ядерных взрывах). Вылетающие нейтроны различаются по своей энергии. В отличие от вышеперечисленных частиц, нейтроны взаимодействуют только с ядрами атомов и лучше поглощаются не тяжёлыми (плотными), а лёгкими атомами, скажем, бором. Так называемые «быстрые» нейтроны (с более высокой энергией) поглощаются вообще плохо, однако, могут быть «замедленны» с помощью, к примеру, водородосодержащих материалов (той же воды). Нейтроны могут «цепляться» к ядрам окружающих веществ, в результате чего эти ядра становятся радиоактивными и начинают сами испускать те или иные частицы (наведённая радиоактивность).
Существует также экзотическое протонное излучение и некоторые другие, но их рассмотрение уже выходит за рамки этого разговора.