Что определяет осмотическое давление
Осмотическое давление
Из Википедии — свободной энциклопедии
Осмотическое давление (обозначается π) — избыточное гидростатическое давление на раствор, отделённый от чистого растворителя полупроницаемой мембраной, при котором прекращается диффузия растворителя через мембрану (осмос). Это давление стремится уравнять концентрации обоих растворов вследствие встречной диффузии молекул растворённого вещества и растворителя.
Мера градиента осмотического давления, то есть различия водного потенциала двух растворов, разделённых полупроницаемой мембраной, называется тоничностью. Раствор, имеющий более высокое осмотическое давление по сравнению с другим раствором, называется гипертоническим, имеющий более низкое — гипотоническим.
Если же подобный раствор находится в замкнутом пространстве, например, в клетке крови, то осмотическое давление может привести к разрыву клеточной мембраны. Именно по этой причине лекарства, предназначенные для внутривенного введения, растворяют в изотоническом растворе, содержащем столько хлорида натрия (поваренной соли), сколько нужно, чтобы уравновесить создаваемое клеточной жидкостью осмотическое давление. Если бы вводимые лекарственные препараты были изготовлены на воде или очень сильно разбавленном (гипотоническом по отношению к цитоплазме) растворе, осмотическое давление, заставляя воду проникать в клетки крови, приводило бы к их разрыву. Если же ввести в кровь слишком концентрированный раствор хлорида натрия (3—10 %, гипертонические растворы), то вода из клеток будет выходить наружу, и они сожмутся. В случае растительных клеток происходит отрыв протопласта от клеточной оболочки, что называется плазмолизом. Обратный же процесс, происходящий при помещении сжавшихся клеток в более разбавленный раствор, — соответственно, деплазмолизом.
Водно-электролитный обмен в организме здорового человека: основные составляющие
Рассмотрение метаболических путей нормально функционирующего организма невозможно без описания обмена низкомолекулярных соединений — минеральных солей и воды. Как известно, вода у взрослого человека составляет 60% от массы тела, то есть 40 — 45 литров. Биологическое значение воды, содержащейся в организме человека, трудно переоценить. Вода и растворенные в ней вещества создают внутреннюю среду организма. Вода обеспечивает транспорт веществ и тепловой энергии по организму. Значительная часть химических реакций организма протекает в водной фазе. Вода участвует в реакциях гидролиза, гидратации, дегидратации. Определяет пространственное строение и свойства гидрофобных и гидрофильных молекул. Поскольку вода является средой, в которой осуществляются процессы обмена веществ в клетках, органах и тканях, непрерывное поступление воды в организм является одним из основных условий поддержания его жизнедеятельности. Основная масса (около 71 %) всей воды в организме входит в состав протоплазмы клеток, составляя так называемую внутриклеточную воду. Внеклеточная вода входит в состав межклеточной, или интерстициалъной, жидкости (около 21%) и воды плазмы крови (около 8%). Содержание воды в организме варьирует в зависимости от органов и тканей. В головном мозге содержится 70-84% воды от всей массы органа, в почках – 82%, в сердце и легких – 79%, в мышцах – 76%, в коже – 72%, в печени – 70%, в костной ткани – 10%. Вода, которая поступает алиментарным путем называется экзогенной, а образовавшаяся в качестве продукта биохимических превращений – эндогенной. Кроме того, различают свободную воду, связанную воду и конституционную воду. Связанная вода удерживается коллоидными системами в виде так называемой воды набухания, Конституционная или внутримолекулярная вода входит в состав молекул белков, жиров и углеводов и освобождается при их окислении. Разные ткани характеризуются различным соотношением свободной, связанной и конституционной воды. Вся вода организма обновляется примерно через месяц, а внеклеточное водное пространство — за неделю.
Водный баланс организма складывается из отребления и выделения воды. С пищей человек получает в сутки около 1100 мл воды, в виде напитков и чистой воды — около 1200 мл. Около 300 мл воды образуется в процессе метаболизма при окислении белков, углеводов и жиров. При испарении с поверхности кожи и альвеол легких в сутки выделяется около 900 мл воды. 1500 мл воды необходимо для растворения экскретируемых почкой осмотически активных веществ при максимальной осмолярности мочи. Секреция воды в пищеварительную трубку составляет 8200 мл, реабсорбция — 8100 мл. 100 мл воды выводится с фекалиями. Простые подсчеты показывают. что средняя суточная потребность человека в воде составляет около 2500 мл.
Водный баланс организма человека.
Средние величины параметров водного баланса организма человека (мл/сут)
Потребление и образование воды
Питье и жидкая пища
Эндогенная «вода окисления»
С выдыхаемым воздухом
Внутренний цикл жидкостей желудочно-кишечного тракта (мл/сут)
Итого 8200 — 8100 = вода в кале 100 мл
Очевидно, что обмен воды неразрывно связан в организме с обменом электролитов. Системы регуляции водно-солевого обмена обеспечивают поддержание общей концентрации ионов натрия, калия, кальция, магния, хлора в плазме крови, во внутриклеточной и внеклеточной жидкости на одном и том же уровне. В плазме крови человека концентрация ионов поддерживается с высокой степенью постоянства и составляет (в ммоль/л): натрия — 130—156, калия — 3, 4—5, 3, кальция — 2, 3—2, 75 (в т. ч. ионизированного, не связанного с белками — 1, 13), магния — 0, 7—1, 2, хлора — 97—108, бикарбонатного иона — 27, сульфатного иона — 1, 0, неорганического фосфата — 1—2. По сравнению с плазмой крови и межклеточной жидкостью клетки отличаются более высоким содержанием ионов калия, магния, фосфатов и низкой концентрацией ионов натрия, кальция, хлора и ионов бикарбоната. Различия в солевом составе плазмы крови и тканевой жидкости обусловлены низкой проницаемостью капиллярной стенки для белков. Точная регуляция водно-солевого обмена у здорового человека позволяет поддерживать не только постоянный состав, но и постоянный объем жидкостей тела, сохраняя практически одну и ту же концентрацию осмотически активных веществ и кислотно-щелочное равновесие.
Минеральные вещества поступают в организм в свободном или связанном виде. Ионы всасываются уже в желудке, основная часть минеральных веществ – в кишечнике путем активного транспорта при участии белков–переносчиков. Из желудочно-кишечного тракта минеральные вещества поступают в кровь и лимфу, где связываются со специфическими транспортными белками. Выделяются минеральные вещества главным образом в виде солей и ионов. С мочой выделяются натрий, калий, кальций, магний, хлор, кобальт, йод, бром, фтор. С калом выделяются железо, кальций, медь, цинк, марганец, молибден, и тяжелые металлы.
Наиболее важное значение в водно-электролитном гомеостазе имеют ионы натрия, калия, кальция, хлора. Натрий (Na+) является основным катионом внеклеточных жидкостей. Его содержание во внеклеточной среде в 6—12 раз превышает содержание в клетках. Натрий в количестве 3—6 г в сутки поступает в организм в виде NaCl и всасывается преимущественно в тонком отделе кишечника. Натрий участвует в поддержании равновесия кислотно-основного состояния, осмотического давления внеклеточных и внутриклеточных жидкостей, принимает участие в формировании потенциала действия, оказывает влияние на деятельность практически всех систем организма. Баланс натрия в организме в основном поддерживается деятельностью почек.
Калий (К+) является основным катионом внутриклеточной жидкости. В клетках содержится 98% калия. Суточная потребность человека в калии составляет 2—3 г. Основным источником калия в пище являются продукты растительного происхождения. Особое значение калий имеет благодаря своей потенциалобразующей роли как на уровне поддержания мембранного потенциала, так и в генерации потенциала действия. Мембранный потенциал покоя, т. е. разность потенциалов между клеточным содержимым и внеклеточной средой, сознается благодаря способности клетки активно с затратой энергии поглощать ионы К+ из внешней среды в обмен на ионы Na+ (так называемый К+, Na+-насос) и вследствие более высокой проницаемости клеточной мембраны для ионов К+ чем для ионов Na+. Из-за высокой проницаемости неточной мембраны для ионов К+ дает небольшие сдвиги в содержании калия в клетках (в норме это величина постоянная) и плазму крови ведут к изменению величины мембранного потенциала и возбудимости нервной и мышечной ткани. Калий принимает также участие в регуляции кислотно-основного состояния на конкурентных взаимодействиях между ионами К+ и Na+, а также К+ и Н+ и является фактором поддержания осмотического давления в клетках. Регуляция его выведения осуществляется преимущественно почками.
Кальций (Са2+) обладает высокой биологической активностью. Он является основным структурным компонентом костей скелета, где содержится около 99% всего Са2+. В сутки взрослый человек должен получать с пищей 800—1000 мг кальция. Всасывается кальций преимущественно в двенадцатиперстной кишке в виде одноосновных солей фосфорной кислоты. Примерно 3/4 кальция выводится пищеварительным трактом, куда эндогенный кальций поступает с секретами пищеварительных желез, остальная часть выводится почками. Кальций принимает участие в генерации потенциала действия, в инициации мышечного сокращения, является необходимым компонентом свертывающей системы крови, повышает рефлекторную возбудимость спинного мозга и обладает симпатикотропным действием.
Магний (Mg2+) по содержанию в организме занимает четвертое место среди катионов организма и второе место среди внутриклеточных катионов. Количество общего магния, содержащегося в организме взрослого, составляет 20–28 г. Около 1 % магния находится во внеклеточной жидкости, приблизительно 60 % — в костях, 20% — в мышцах. Остальные 20% приходятся на другие ткани организма, причем большая часть сосредоточена в клетках печени. В плазме крови концентрация магния составляет 0, 75–1, 25 ммоль/л. Из этого количества 55–60 % магния плазмы ионизировано, 15 % связано с органическими и неорганическими кислотами. Биологически активным является только ионизированный магний, концентрация которого в плазме составляет 0, 45–0, 75 ммоль/л. Магний выполняет следующие физиологические функции: входит в состав костей, является антагонистом кальция, влияет на проницаемость биологических мембран, активирует фибринолиз, участвует в функционировании многих ферментов, связанных с обменом АТФ, в качестве кофактора.
Содержание хлора (Cl—) в организме составляет около 100 г. В плазме (сыворотке) крови его концентрация достигает 97–108 ммоль/л. Его физиологическая функция связана с участием в формировании трансмембранного потенциала. Являясь основным анионом внеклеточной жидкости, ион хлора активно участвует в обеспечение электронейтральности. Благодаря наличию в мембранах клеток и митохондрий специальных хлорных каналов, хлорид ионы регулируют объем жидкости, трансэпителиальный транспорт ионов, что создает и стабилизирует мембранный потенциал Механизмы регуляции хлора связаны с процессами, стабилизирующими содержание натрия. В связи с тем, что хлорид-ионы способны проникать через мембрану клеток, они вместе с ионами натрия и калия поддерживают осмотическое давление и регулируют водно-солевой обмен. Хлор является составной частью соляной кислоты желудочного сока, денатурирующей белки и активирующей пепсиноген. создают благоприятную среду в желудке для действия протеолитических ферментов желудочного сока. Кроме того, ионы хлора участвуют в создании и поддержании рН в клетках и биологических жидкостях организма.
Статья добавлена 31 мая 2016 г.
Осмос и осмотическое давление



Если разделить раствор и растворитель при помощи полупроницаемой перегородки (мембраны), пропускающей свободно молекулы растворителя и задерживающей молекулы растворенного вещества, то наблюдается односторонняя диффузия растворителя.
Такого рода диффузия обусловливается тем, что число молекул растворителя в единице объема больше, чем в таком же объеме раствора, так как в растворе часть объема занимают молекулы растворенного вещества. В результате молекулярного движения перемещение молекул растворителя через мембрану из растворителя в раствор преобладает над перемещением их в обратном направлении.
Односторонняя диффузия растворителя к раствору называется осмосом, а сила, обусловливающая осмос, отнесенная к единице поверхности полупроницаемой мембраны, называется осмотическим давлением.
Механизм осмоса нельзя объяснить только тем, что полупроницаемые мембраны играют роль сита с ячейками, через которые свободно проходят молекулы растворителя, но не проходят молекулы растворенного вещества.
По-видимому, механизм осмоса значительно сложнее. Здесь большую роль играют строение и состав мембраны.
В зависимости от природы мембраны механизм осмоса будет различен. В одних случаях через мембрану свободно проходят только те вещества, которые в ней растворяются, в других случаях мембрана взаимодействует с растворителем, образуя промежуточные непрочные соединения, которые легко распадаются, и, наконец, она может представлять и пористую перегородку с определенными размерами пор.
Для измерения осмотического давления в сосуд с полупроницаемыми стенками наливают исследуемый раствор и плотно закрывают пробкой, в которую вставлена трубка, соединенная с манометром. Такой прибор для измерения осмотического давления называется осмометром.
Осмометр с раствором погружают в сосуд с растворителем. В начале процесса растворитель из наружного сосуда диффундирует в осмометр с большей скоростью, чем из него, поэтому уровень жидкости в трубке осмометра поднимается, что создает в ней гидростатическое давление, которое постепенно увеличивается. По мере увеличения гидростатического давления скорости диффузии растворителя в осмометр и из осмометра уравниваются, в результате чего наступает состояние динамического равновесия, подъем жидкости в трубке осмометра прекращается.
Гидростатическое давление, установившееся в результате осмоса, служит мерой осмотического давления.
Измерение осмотического давления при помощи осмометра не всегда возможно с достаточной точностью, так как не существует мембран, способных задерживать все частицы растворенного вещества. Измеряемое значение осмотического давления для одного и того же раствора будет, следовательно, в какой-то мере зависеть от природы мембраны.
Осмотическое давление возникает лишь на границе между раствором и растворителем (или раствором другой концентрации), если эта граница образована полупроницаемой перегородкой. Раствор, содержащийся в обыкновенном сосуде, не оказывает на его стенки никакого иного давления, кроме обычного гидростатического. Поэтому осмотическое давление надо рассматривать не как свойство растворенного вещества, или растворителя, или самого раствора, а как свойство системы из растворителя и раствора с полупроницаемой перегородкой между ними.
Зако́ны Ра́уля — общее название открытых французским химиком Ф. М. Раулем в 1887 г. количественных закономерностей, описывающих некоторые коллигативные (зависящие отконцентрации, но не от природы растворённого вещества) свойства растворов.
Первый закон Рауля [править]
Первый закон Рауля связывает давление насыщенного пара над раствором с его составом; он формулируется следующим образом:
· Парциальное давление насыщенного пара компонента раствора прямо пропорционально его мольной доле в растворе, причём коэффициент пропорциональности равен давлению насыщенного пара над чистым компонентом.
Для бинарного раствора, состоящего из компонентов А и В (компонент А считаем растворителем) удобнее использовать другую формулировку:
· Относительное понижение парциального давления пара растворителя над раствором не зависит от природы растворённого вещества и равно его мольной доле в растворе.
На поверхности оказывается меньше способных испаряться молекул растворителя, ведь часть места занимает растворённое вещество.
Растворы, для которых выполняется закон Рауля, называются идеальными. Идеальными при любых концентрациях являются растворы, компоненты которых очень близки по физическим и химическим свойствам (оптические изомеры, гомологи и т. п.), и образование которых не сопровождается изменением объёма и выделением либо поглощением теплоты. В этом случае силы межмолекулярного взаимодействиямежду однородными и разнородными частицами примерно одинаковы, и образование раствора обусловлено лишь энтропийным фактором.
Отклонения от закона Рауля [править]
Растворы, компоненты которых существенно различаются по физическим и химическим свойствам, подчиняются закону Рауля лишь в области очень малых концентраций; при больших концентрациях наблюдаются отклонения от закона Рауля. Случай, когда истинные парциальные давления паров над смесью больше, чем вычисленные по закону Рауля, называют положительными отклонениями. Противоположный случай, когда парциальные давления паров компонентов оказываются меньше вычисленных — отрицательные отклонения.
Причиной отклонений от закона Рауля является то обстоятельство, что однородные частицы взаимодействуют друг с другом иначе, чем разнородные (сильнее в случае положительных и слабее в случае отрицательных отклонений).
Реальные растворы с положительными отклонениями от закона Рауля образуются из чистых компонентов с поглощением теплоты (ΔНраств > 0); объём раствора оказывается больше, чем сумма исходных объёмов компонентов (ΔV > 0). Растворы с отрицательными отклонениями от закона Рауля образуются с выделением теплоты (ΔНраств −1 ·кг соответственно. Поскольку одномоляльный раствор не является бесконечно разбавленным, второй закон Рауля для него в общем случае не выполняется, и величины этих констант получаютэкстраполяцией зависимости из области малых концентраций до m = 1 моль/кг.
Для водных растворов в уравнениях второго закона Рауля моляльную концентрацию иногда заменяют молярной. В общем случае такая замена неправомерна, и для растворов,плотность которых отличается от 1 г/см³, может привести к существенным ошибкам.
Второй закон Рауля даёт возможность экспериментально определять молекулярные массы соединений, неспособных к диссоциации в данном растворителе; его можно использовать также для определения степени диссоциации электролитов.
Растворы электролитов [править]
Законы Рауля не выполняются для растворов (даже бесконечно разбавленных), которые проводят электрический ток — растворов электролитов. Для учёта этих отклонений Вант-Гоффвнёс в приведённые выше уравнения поправку — изотонический коэффициент i, неявно учитывающий диссоциацию молекул растворённого вещества:
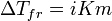
Неподчинение растворов электролитов законам Рауля и принципу Вант-Гоффа послужили отправной точкой для создания С. А. Аррениусом теории электролитической диссоциации.
Эбуллиоскопическая константа– разница между температурой кипения раствора и температурой чистого растворителя.
Криоскопическая константа– разница между температурой замерзания раствора и температурой чистого растворителя.
74. Явление осмоса, его роль в биологических системах. Осмотическое давление. Закон Вант-Гоффа.
Растворы изотонические, гипо- и гипертонические.
Явление осмоса наблюдается в тех средах, где подвижность растворителя больше подвижности растворённых веществ. Важным частным случаем осмоса является осмос через полупроницаемую мембрану. Полупроницаемыми называют мембраны, которые имеют достаточно высокую проницаемость не для всех, а лишь для некоторых веществ, в частности, для растворителя. (Подвижность растворённых веществ в мембране стремится к нулю). Как правило, это связано с размерами и подвижностью молекул, например, молекула воды меньше большинства молекул растворённых веществ. Если такая мембрана разделяет раствор и чистый растворитель, то концентрация растворителя в растворе оказывается менее высокой, поскольку там часть его молекул замещена на молекулы растворённого вещества (см. Рис. 1). Вследствие этого, переходы частиц растворителя из отдела, содержащего чистый растворитель, в раствор будут происходить чаще, чем в противоположном направлении. Соответственно, объём раствора будет увеличиваться (а концентрация вещества уменьшаться), тогда как объём растворителя будет соответственно уменьшаться.
Значение осмоса [править]
Осмос играет важную роль во многих биологических процессах. Мембрана, окружающая нормальную клетку крови, проницаема лишь для молекул воды, кислорода, некоторых из растворённых в крови питательных веществ и продуктов клеточной жизнедеятельности; для больших белковых молекул, находящихся в растворённом состоянии внутри клетки, она непроницаема. Поэтому белки, столь важные для биологических процессов, остаются внутри клетки.
Осмос участвует в переносе питательных веществ в стволах высоких деревьев, где капиллярный перенос не способен выполнить эту функцию.
Осмос широко используют в лабораторной технике: при определении молярных характеристик полимеров, концентрировании растворов, исследовании разнообразных биологических структур. Осмотические явления иногда используются в промышленности, например при получении некоторых полимерных материалов, очистке высоко-минерализованной воды методом обратного осмоса жидкостей.
Клетки растений используют осмос также для увеличения объёма вакуоли, чтобы она распирала стенки клетки (тургорное давление). Клетки растений делают это путём запасания сахарозы. Увеличивая или уменьшая концентрацию сахарозы в цитоплазме, клетки могут регулировать осмос. За счёт этого повышается упругость растения в целом. С изменениями тургорного давления связаны многие движения растений (например, движения усов гороха и других лазающих растений). Пресноводные простейшие также имеют вакуоль, но задача вакуолей простейших заключается лишь в откачивании лишней воды из цитоплазмы для поддержания постоянной концентрации растворённых в ней веществ.
Осмос также играет большую роль в экологии водоёмов. Если концентрация соли и других веществ в воде поднимется или упадёт, то обитатели этих вод погибнут из-за пагубного воздействия осмоса.
Осмотическое давление (обозначается π) — избыточное гидростатическое давление на раствор, отделённый от чистого растворителя полупроницаемой мембраной, при котором прекращается диффузия растворителя через мембрану. Это давление стремится уравнять концентрации обоих растворов вследствие встречной диффузии молекул растворённого вещества и растворителя.
ЗАКОН ВАНТ-ГОФФА описывает зависимость ОСМОТИЧЕСКОГО ДАВЛЕНИЯ разбавленных растворов от температуры и молярной концентрации раствора:
Вант-Гофф пришел к заключению, что закон Авогадро справедлив и для разбавленных растворов. Он экспериментально установил, что осмотическое давление, представляющее собой меру стремления двух различных растворов по обе стороны мембраны к выравниванию концентрации, в слабых растворах зависит не только от концентрации, но и от температуры и, следовательно, подчиняется законам термодинамики газов. Вант-Гофф выразил осмотическое давление формулой РV = iRT, где Р означает осмотическое давление вещества, растворенного в жидкости; V – объем; R – газовую постоянную; Т – температуру и i – коэффициент, который для газов часто равен 1, а для растворов, содержащих соли, – больше единицы. Вант-Гофф смог объяснить, почему изменяется значение i, связав этот коэффициент с числом ионов, находящихся в растворе. Проведенные Вант-Гоффом исследования разбавленных растворов явились обоснованием теории электролитической диссоциации С.Аррениуса. Впоследствии Аррениус приехал в Амстердам и работал вместе с Вант-Гоффом.
Гипотонические растворы отличаются от изотонического меньшей концентрацией и соответственно меньшим осмотическим давлением. При контакте с тканями вода из гипотонических растворов поступает в клетки тканей. Вследствие этого они набухают, а при чрезмерном накоплении в них воды наступает разрыв клеточных оболочек, т. е. лизис клеток.
Применение гипотонических растворов натрия хлорида в практике очень ограничено. В ряде случаев они используются для приготовления растворов веществ, применяемых для инфильтрационной анестезии. Действиеанестетиков в гипотонических растворах усиливается, так как последние способствуют более глубокому проникновению веществ в ткани.
Гипертонические растворы, растворы, осмотическое давление которых выше осмотического давления в растительных или животных клетках и тканях. В зависимости от функциональной, видовой и экологической специфики клеток осмотическое давление в них различно, и раствор, гипертоничный для одних клеток, может оказаться изотоничным или даже гипотоничным для др. При погружении растительных клеток в Г. р. он отсасывает воду из клеток, которые уменьшаются в объёме, а затем дальнейшее сжатие прекращается и протоплазма отстаёт от клеточных стенок (см. Плазмолиз). Эритроциты крови человека и животных в Г. р. также теряют воду и уменьшаются в объёме. Г. р. в сочетании с гипотоническими растворами иизотоническими растворами применяют для измерения осмотического давления в живых клетках и тканях.










