Что нового в лечении болезни паркинсона ученые в сколково
Ученые из России совершили прорыв в диагностике болезни Паркинсона
Группа ученых из «Сколково» и Федерального медицинского биофизического центра создали систему, которая позволяет диагностировать болезнь Паркинсона на начальной стадии. Базируется разработка на искусственном интеллекте. Благодаря ему программа производит анализ видео, где больные выполняют простые действия. На основе полученных данных медики определяют, есть ли заболевание, на какой оно стадии, а также назначают терапию.
Важность изобретения
С каждым годом количество пожилых людей с болезнью Паркинсона увеличивается. Усугубляет ситуацию то, что диагностировать заболевание на раннем этапе практически невозможно. Кроме этого, болезнь имеет схожие симптомы с другими двигательными нарушениями. Также нет и единого биологического маркера недуга. Чтобы поставить диагноз, врачу необходимо основываться исключительно на результатах внешних наблюдений.
Учитывая все эти нюансы, ученые приняли решение разработать систему, которая бы анализировала движения пациента способами машинного обучения. Программа анализирует видео человека и становится дополнительным, оказывающим помощь «вторым мнением» врача и больного. Благодаря системе врачу легче определить стадию недуга и скорректировать лечение, если в этом есть необходимость.
Процесс разработки
Во время исследования программу тестировали на 83 участниках эксперимента. Среди них были больные с двигательными нарушениями (болезнь Паркинсона, эссенциальный тремор) и здоровые люди. Всем предлагалось выполнить пятнадцать одинаковых несложных упражнений – встать, взять ложку или лечь. Эксперимент записывался на камеру. После полученная информация классифицировалась и проходила компьютерный анализ.
Екатерина Коваленко, аспирант «Сколково» отмечает, что во время создания системы ученые тесно сотрудничали с врачами-неврологами. Они помогали разрабатывать упражнения для каждого вероятного проявления болезни Паркинсона.
В ходе эксперимента ученые сравнили движения здоровых людей с пациентами, у которых есть подозрение на недуг в ранней стадии. После сравнительный анализ проходил с больными, у которых диагноз уже подтвержден.
Полученные данные приятно удивили разработчиков. Уже на этой стадии стало ясно, что система отличается высокой эффективностью в обнаружении вероятных симптомов болезни. Кроме этого, программа отделяет ее от эссенциального тремора, который имеет массу схожих признаков с болезнью Паркинсона.
Незаменимая помощь врачу
Разработчики утверждают, что программа не в силах заменить лечащего врача, но значительно улучшает и облегчает ему работу. Теперь специалисту легче составить для себя более объективную картину для диагностики. Он может обнаружить незаметные особенности и характерные черты разных стадий болезни, которые невозможно увидеть при простом внешнем осмотре.
В команду разработчиков входили врачи, математики и инженеры. Ученые намерены продолжить работу и сделать систему диагностики лучше. Разработчики хотят, чтобы программа индивидуально подбирала способы терапии и указывала на необходимость нейрохирургического лечения.
МРФУЗ — новая надежда больных с эссенциальным тремором и тремором при болезни Паркинсона
МРФУЗ — новая надежда больных с тремором и тремором при болезни Паркинсона
Современное неинвазивное лечение двигательных нарушений, тремора, болезни Паркинсона
Тряска рук, головы, ноги, которые не дают нормально жить пациентам с эссенциальным тремором и болезнью Паркинсона теперь могут быть излечены за одну-две процедуры. Это делается без разрезов, без имплантов и всего за 3-5 часов. Чтобы устранить дрожание рук применяется новейший метод лечения — фокусированный ультразвук под контролем магнитно-резонансной томографии (МРФУЗ). И ура, в 2020 году в России открылся первый центр МРФУЗ лечения эссенциального и связанного с болезнью Паркинсона тремора!
Технология фокусированного ультразвука под контролем МРТ позволяет найти и устранить очаг, вызывающий тремор или другие двигательные нарушения.
Как это делается?
Магнитно-резонансная томография строит изображение головного мозга. На карте головного мозга нейрохирурги рассчитывают предположительное место, вызывающее тремор. После чего, ультразвуком «усыпляется» на время эта область мозга. Размер этой области меньше 1 мм. Далее можно оценить вероятность побочных эффектов и правильность попадания.
При расположении очага там, где произведена эта гибернация (усыпление) нейронов, врачи видят исчезновение симптомов и отсутствие побочных эффектов. Тогда после этого воздействие в точке производится повторно и уже необратимо. Тремор проходит.
Если очаг расположен в другом месте, воздействие прекращается. Все нейроны «просыпаются» через 2-3 минуты. По карте взаимного расположения ядер головного мозга врач определяет следующую точку воздействия.
Таким образом, достигается контролируемое, необратимое воздействие. Поэтому возможно предотвратить большую часть побочных эффектов. Они проявляются на этапе усыпления (преднагрева), проходят самостоятельно через пару минут и не переводятся в необратимые.
Наглядное видео о методике:
Методика является хорошо апробированной. Сейчас уже никто из современных врачей не говорит, что она экспериментальная
Методика одобрена Росздравнадзором и FDA. В мире сделано более двух тысяч операций МРФУЗ с хорошими показателями эффективности и безопасности.
Карту мировых лидеров использующих эту методику можно увидеть на сайте производителя оборудования, компании Insightec. В Европе это: Великобритания, Испания, Германия, Швейцария, Италия и теперь Россия!
Что лучше DBS (глубокая стимуляция мозга), лечение лекарствами (консервативно), таламотомия гамма-ножом, радиочастотной аблацией (РЧА) или фокусированный ультразвук под контролем МРТ (МРФУЗ)?
Существует консервативная терапия. Но эффект от нее снижается со временем, есть побочные действия приема лекарств. Когда лекарственная терапия перестает быть эффективной, остаются следующие альтернативы: глубокая стимуляция мозга, таламотомия радиочастотной аблацией, таламотомия гамма-ножом.
Глубокая стимуляция мозга — эффективный метод, но он связан с проведением и имплантацией электродов в головной мозг! Для открытой операции с имплантацией инородного тела возможны следующие осложнения: кровотечение (геморрагический инсульт), инфекция и нагноение. Кроме того, электрод, в сравнении с миллиметровой точкой воздействия МРФУЗ достаточно громоздкий. Нужно понимать, что электрод тянется к стимулятору, который требует замены через каждые несколько лет в связи с разрядкой батареи. Электроды иногда переламываются.
Таламотомия радиочастотной аблацией, так же как и глубокая стимуляция мозга, требует разреза. В ткань мозга проводится электрод для аблации, который потом удаляется. Но в связи с работой инструментом через ткань мозга возможны кровотечения, инфекции, повреждения важных структур. Правильность воздействия проводится путем пробуждения пациента и проведением тестов.
Таламотомия гамма-ножом не позволяет изменить точку приложения воздействия. Поэтому, у части пациентов, которые имеют очаг в нетипичном месте, эффекта не будет. Возможно появление новых неврологических симптомов. Такая группа пациентов может быть достаточно большой.
При проведении МРФУЗ переносить расчетную точку воздействия в связи с отклонением в расположении очага приходится достаточно часто, почти в половине случаев. К счастью для МРФУЗ, перенос точки воздействия обратим и не приводит к побочным эффектам. Это отличает метод от других, когда воздействие либо механическое, либо лучевое.
Электроды, гамма-излучение, РЧА всегда оказывают какое-либо травмирующее воздействие сразу при их нанесении. Очаг воздействия облучения от гамма-ножа больше по размеру, если сравнивать с МРФУЗ.
Какие плюсы лечения эссенциального тремора (трясущихся рук) и тремора при болезни Паркинсона фокусированным ультразвуком под контролем МРТ
Для МРФУЗ не нужно разрезов, не нужно наркоза, не нужно имплантов, не нужно облучения. Пациент может идти домой в день процедуры. Методика позволяет сначала «прощупать» место воздействия, перед тем как воздействовать. А это настоящая мечта хирурга — скальпель, который режет только тогда, когда он приложен безошибочно туда, куда нужно.
Какие минусы МРФУЗ?
Прием лекарств после процедуры при болезни Паркинсона
Для пациентов с болезнью Паркинсона прием лекарств требуется в связи с измененным обменом веществ. Процедуры DBS, РЧА, ФУЗ убирают симптомы, но не устраняют болезнь. Это так же, как стентирование коронарного сосуда или шунтирование. Они не излечивают ишемическую болезнь сердца, а устраняют ее проявления. Паркинсоникам необходимо пить свои препараты, чтобы заболевание не прогрессировало, в том числе для контроля ригидности, депрессии и других симптомов. Устранение тремора позволяет пациентам самим обслуживать себя, улучшает качество жизни, устранив тремор они могут сами есть, пить чай, писать смс и звонить, спокойно спать.
МРФУЗ при эссенциальном треморе
Методика МРФУЗ при эссенциальном треморе очень эффективна. Именно при эссенциальном треморе фокусированный ультразвук под контролем МРТ сначала был одобрен FDA. FDA является одной из самых требовательных к эффективности и безопасности организаций в мире. МРФУЗ при эссенциальном треморе дает очень длительный результат, сравнимый с пожизненным.
Художественный короткометражный фильм об излечении пациента с эссенциальным тремором и первом центре в России
Всемирно известный пионер нейрохирургии профессор Jin Woo Chang (Director, Brain Research Institute Professor Department of Neurosurgery YONSEI UNIVERSITY COLLEGE OF MEDICINE) проводит лечение тремора при болезни Паркинсона.
Видео с результатами лечения тремора.
Я счастлив, что имею отношение к этому проекту, потому что всегда мечтал делать операции без разрезов, без боли, без необходимости наркоза и предсказуемо.
Болезнь Паркинсона и астроциты: новый взгляд на лечение нейродегенеративных заболеваний
Болезнь Паркинсона и астроциты: новый взгляд на лечение нейродегенеративных заболеваний
Ученые из Калифорнийского университета в Сан-Диего показали успешную трансформацию астроцитов в нейроны in situ для лечения болезни Паркинсона. Поможет ли эта работа приблизиться к созданию успешной терапии?
Автор
Редакторы
Статья на конкурс «Био/Мол/Текст»: Болезнь Паркинсона до сих пор остается неизлечимой. Однако в июне 2020 года в журнале Nature вышла статья, способная произвести революцию в терапии этого недуга. В этой работе мы рассмотрим, какие предыдущие исследования привели к такому результату и как это может повлиять на будущее всей нейробиологии.
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.
Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Дисклеймер
Обычно «Биомолекула» не публикует статьи по одинаковым инфоповодам, но в этом году мы приняли две работы, базирующиеся на одной и той же публикации в Nature 2020 года. Статья, которую вы читаете, — обзорная, а вот и ее парная новостная [16].
Болезнь Паркинсона является вторым по распространенности нейродегенеративным расстройством. Она характеризуется отмиранием нейронов в черной субстанции мозга. Существующая терапия направлена на ограниченное сдерживание заболевания. Эффективного лекарства до сих пор не существует. Недавнее исследование может в корне изменить плачевную ситуацию. Хао Цянь из Калифорнийского университета в Сан-Диего (США) вместе с коллегами из Пекинского университета (Китай) продемонстрировал успешное превращение астроцитов в нейроны in situ на мышиной модели болезни Паркинсона. Однако начнем с общей характеристики этого заболевания.
Болезнь Паркинсона: история и молекулярный патогенез
В 1817 году английский врач Джеймс Паркинсон [1] опубликовал работу «Эссе о дрожательном параличе», в которой дал описание неврологического недуга, а также провел анализ и выявил общие закономерности. В названии отражено необычное сочетание основных симптомов — тремор, скованность мышц и неспособность удерживать равновесие [2].
Кстати, одним из ученых, который помог разгадать тайны патогенеза болезни Паркинсона, стал русский невропатолог Константин Николаевич Третьяков, занимавший в 1916–1923 годах должность заведующего лабораторией мозга имени Шарко кафедры нервных болезней Парижского университета (Франция). Он предложил нигральную теорию патогенеза болезни Паркинсона, согласно которой, проявления заболевания были связаны с утратой черной субстанции головного мозга.
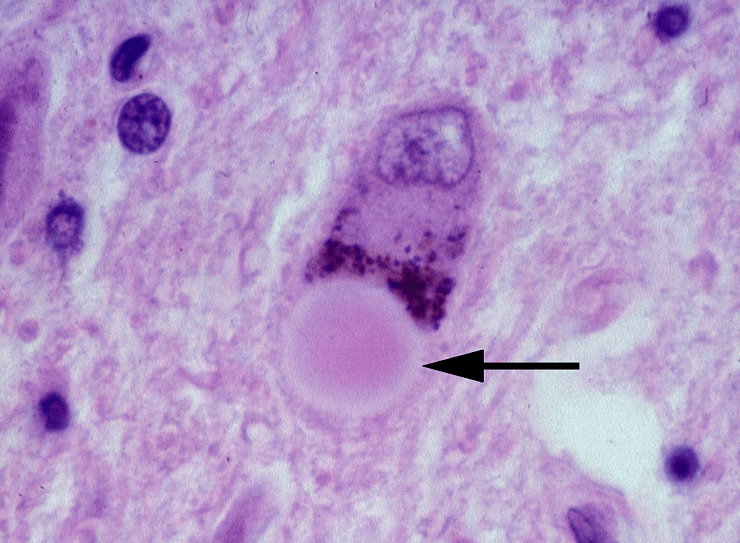
Сегодня известно, что болезнь Паркинсона развивается вследствие дегенерации дофаминергических нейронов в черной субстанции, что приводит к снижению уровня вырабатываемого дофамина — нейромедиатора, ответственного за чувство удовлетворения и привязанности. Клинические проявления связаны с нейротоксическим эффектом: по мере прогрессирования заболевания в клетках накапливается белок альфа-синуклеин [3]. Альфа-синуклеин в норме задействован в механизме транспорта и высвобождения везикул с нейротрансмиттерами. Однако у пациентов с болезнью Паркинсона наблюдается фосфорилирование и аномальное свертывание этого белка с образованием агрегатов — телец Леви (рис. 1). В 2018 году группа ученых из научно-исследовательского института Скриппса (США) обнаружила, что фосфорилированная форма альфа-синуклеина локализуется в митохондриях, вызывая их фрагментацию [4].
Рисунок 1. Тельце Леви в нейроне черной субстанции головного мозга
Возможности сегодняшней терапии
Сейчас существует только симптоматическое лечение, направленное на облегчение имеющихся проявлений заболевания. Одним из наиболее эффективных и широко применяемых лекарств является леводопа, или 3-гидрокси-L-тирозин [5]. Леводопа — биологический предшественник дофамина. Помимо леводопы, иногда используется ряд других лекарственных средств. Агонисты дофаминовых рецепторов имеют химическую структуру, похожую на дофамин, и за счет этого могут стимулировать его рецепторы [6]. Ингибиторы моноаминоксидазы B способны блокировать высвободившийся дофамин и продлевать время его действия. Ингибиторы катехол-О-метилтрансферазы подавляют распад принятой леводопы и удлиняют время ее действия в организме.
Также для терапии болезни Паркинсона применяют так называемые нейротрофические факторы — регуляторные белки, которые поддерживают жизнеспособность и функционирование нейронов. Хотя было проведено множество исследований по использованию нейротрофических факторов в клинической практике, у них есть ряд недостатков. Во-первых, они нуждаются в точной доставке к месту назначения. Для этого используют специальные катетеры. Во-вторых, нейротрофические факторы целесообразно использовать только в том случае, если у пациента еще не повреждены аксоны дофаминергических нейронов. Если же транспортная система в черной субстанции нарушена или уничтожена, то такое лечение не даст никаких положительных эффектов [7].
Часть из вышеперечисленных способов борьбы с болезнью широко используется, однако ничего из этого не поможет вернуть человеку его утраченные нейроны. Поэтому были попытки разработать терапию, направленную на восстановление популяции дофаминергических нейронов. В 2018 году группа ученых из японского Университета Киото [8] пересадила в мозг пациента индуцированные плюрипотентные стволовые клетки (ИПСК) [9], способные превращаться в любую клетку организма. Перед тем как применять ИПСК для лечения болезни Паркинсона у человека, были проведены исследования эффективности и безопасности этой терапии на приматах [10]. У семи людей изъяли ИПСК для их последующего превращения в клетки нейронного ряда. Для трансформации использовали двойное подавление сигнального пути SMAD, участвующего в процессах клеточного роста, дифференциации и смерти. За специализацию дофаминергических нейронов в черной субстанции отвечает сигнальный путь Sonic hedgehog (Shh). Подавление SMAD и активация Shh привели к дифференцировке ИПСК в клетки-предшественники дофаминергических нейронов, которые начали синтезировать нейронные маркеры [11]. Однако трансплантация стволовых клеток для лечения болезни Паркинсона у человека не применяется из-за сложности и недостаточных данных об эффективности.
Астроциты — возможное лекарство?
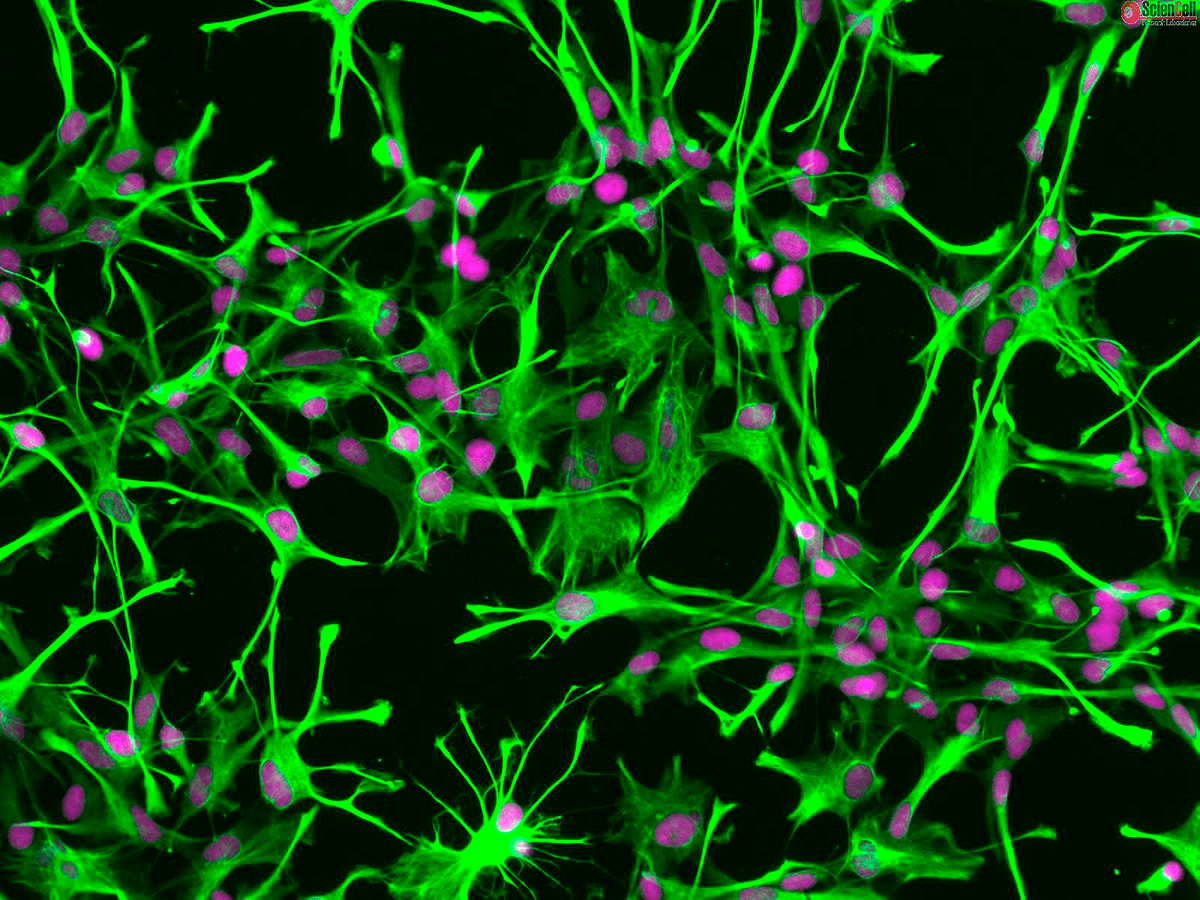
В последнее время было опубликовано несколько научных работ по превращению различных клеток в дофаминергические нейроны. В основном, исследователи останавливали свой выбор на астроцитах — клетках, поддерживающих жизнедеятельность нейронов. Свое название они получили за характерную звездчатую форму (рис. 2). В обязанности этих клеток входит обеспечение метаболических потребностей нейронов, участие в своевременном высвобождении нейротрансмиттеров из нервных окончаний, запас питательных веществ и регуляция активности нейронов.
Рисунок 2. Вспомогательные клетки нервной системы — астроциты. В норме они обеспечивают жизнедеятельность нейронов, но воздействуя на молекулярные процессы, протекающие в астроцитах, можно добиться их «превращения» в нейроны любого типа.
Но больше всего ученых интересует их репаративная функция. В 2014 году группа ученых из Лундского университета и Каролинского института обнаружила, что при повреждении нервной ткани после инсульта астроциты способны замещать погибшие нейроны [12]. При этом у них «выключается» сигнальный путь Notch1, имеющий ключевое значение в процессах пролиферации и дифференцировки клеток. В здоровом головном мозге этот путь активен и блокирует превращение астроцитов в нейроны. Однако после инсульта этот механизм подавляется, и астроциты могут начать трансформироваться в нейроны.
Идея для исследования, проведенного группой из Калифорнийского университета, не нова. Еще в 2017 году группа шведских ученых с помощью вирусных векторов превратила человеческие астроциты в нейроны in vitro. После этого трансформировали и мышиные астроциты, но уже in vivo. Для репрограммирования они использовали три транскрипционных фактора (NEUROD1, ASCL1 и LMX1A) и микроРНК miR218 [13]. Трансформация астроцитов in vitro была улучшена с помощью молекул, способных провоцировать перестройку хроматина и активировать несколько сигнальных путей.
Однако в исследовании 2020 года предлагается куда более простой метод перепрограммирования астроцитов: достаточно просто заблокировать производство одного-единственного белка.
Механизм трансформации астроцитов
В качестве мишени для репрограммирования астроцитов Цянь и коллеги выбрали РНК-связывающий белок PTB1 [14]. Этот белок синтезируется в астроцитах и ингибирует дифференцировку в нейроны. Снижение производства PTB1 вызывает продукцию его нейронного варианта nPTB1.
Сначала ученые провели трансформацию астроцитов in vitro. Астроциты выделили из среднего мозга и коры мыши и из коры человека. Исследователи использовали РНК-шпильку к гену Ptbp1, который кодирует белок PTB1. РНК-шпильки работают по принципу РНК-интерференции: они взаимодействуют с информационной РНК конкретного гена и вызывают ее деградацию, что приводит к неспособности клетки произвести белок. Уровень PTB1 в астроцитах упал, что привело к трансформации астроцитов в нейроны.
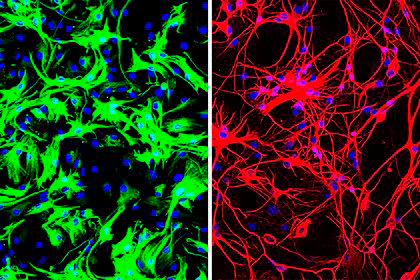
Затем исследователи перешли к экспериментам in vivo: они истощали запасы белка PTB1 в мозге мыши. Симптомы болезни Паркинсона у мышей были вызваны с помощью токсичного аналога дофамина, 6-OHDA, вызывающего гибель дофаминергических нейронов. Цянь и коллеги использовали трансгенных мышей, продуцирующих cre-рекомбиназу. Это позволяло нацелить вирусный вектор непосредственно на астроциты. Чтобы убедиться, что вирус достиг своей цели, в него встроили ген красного флуоресцентного белка. В составе вирусного вектора была маленькая РНК-шпилька (shPTB), которая блокировала ген Ptbp1. Такая стратегия также привела к преобразованию астроцитов в нейронные клетки и восстановлению двигательной активности (рис. 3).
Рисунок 3. Слева: астроциты мыши. Справа: нейроны, полученные в ходе репрограммирования астроцитов.
Результаты
Цянь и коллеги обнаружили, что истощение запасов PTB1 в астроцитах стимулирует их трансформацию в нейроны. Результат такой трансформации зависит от области мозга, в которой находятся целевые астроциты. Обнаружено, что астроциты в среднем мозге синтезируют низкие уровни факторов транскрипции Lmx1a и Foxa2. Эти факторы являются маркерами предшественников дофаминергических нейронов во время развития среднего мозга. Однако истощение белка PTB1 усиливало продукцию этих факторов транскрипции в астроцитах среднего мозга. С другой стороны, воздействие на корковые астроциты приводило к увеличению синтеза факторов транскрипции, характерных для корковых нейронов.
Спустя 4 недели после воздействия на астроциты in vitro 50–80% клеток стали морфологически похожи на нейроны и дали положительный результат на нейронные маркеры TUJ1 и MAP2.
При экспериментах in vivo спустя 3 недели после введения shPTB около 20% клеток, получивших красный флуоресцентный белок, синтезировали маркер нейронов NeuN. После 10 недель было уже около 80% клеток с NeuN. При этом клетки переставали продуцировать GFAP — белок, присутствующий в астроцитах.
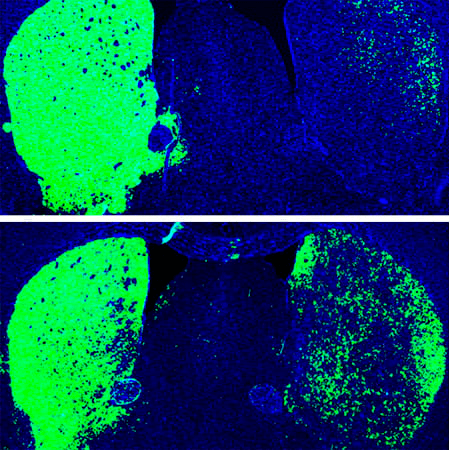
Спустя 12 недель 30–35% этих клеток трансформировались в дофаминергические нейроны. Другими словами, перепрограммирование астроцитов помогло восстановить более 600 погибших дофаминергических нейронов (рис. 4).
Рисунок 4. Мозг мыши с «односторонней» болезнью Паркинсона. Сверху — до репрограммирования с помощью shPTB. Снизу — после. Зеленым показаны дофаминергические нейроны.
Более того, новоиспеченные нейроны стали активно производить дофамин. Воздействие 6-OHDA привело к снижению уровня нейромедиатора до 25% от нормальных показателей. После терапии концентрация дофамина поднялась до 65% нормального уровня.
Будет ли создана новая терапия болезни Паркинсона?
Пока что слишком рано говорить о перспективах использования метода репрограммирования астроцитов для лечения болезни Паркинсона у реальных пациентов. Однако уже сейчас можно сказать, что это исследование помогло понять, как лучше подступиться к созданию новых направлений терапии этого недуга. Хотя эта многообещающая терапевтическая стратегия в будущем может быть применима и для лечения других нейродегенеративных заболеваний, сами авторы указывают, что «применение нашего подхода к людям потребует преодоления многих препятствий, включая возрастные ограничения перепрограммирования и потенциальные побочные эффекты». Вдобавок, в дальнейших экспериментах необходимо определить, сохранят ли перепрограммированные клетки свою функциональную активность в течение длительных промежутков времени.
Новый препарат в лечении пациентов с болезнью Паркинсона и психозом
Актуальность
SEP-363856 представляет собой недопаминовый антипсихотический препарат, который изучается у пациентов с шизофренией. Данный препарат может улучшать симптомы психоза у пациентов с болезнью Паркинсона без ухудшения двигательных симптомов. Такие данные были получены в исследовании proof-of-principle, представленном в рамках конгресса американской ассоциации неврологов в апреле 2021 года.
SEP-363856 – агонист активности TARR1, который регулирует допамин, ноадреналин и серотонин, действует на рецептор серотонина 5-HT1A, но не оказывает влияния на допаминовый рецептор 2 типа.
Эксперты говорят о потенциальной пользе нового препарата, учитывая отсутствие необходимости терапевтического мониторинга, как например на фоне терапии пимавансерином, единственном препарате для лечения психоза, ассоциированного с болезнью Паркинсона, одобренного Food and Drug Administration.
Дизайн исследования
В исследование включили 38 пациентов, 24 из которых получали SEP-363856. Пациенты получали различные дозы препаратов: 25 мг, 50 мг и 75 мг.
В качестве первичной конечной точки оценивали сумму баллов по шкале Scale for the Assessment of Positive Symptoms for Parkinson’s Disease Psychosis (SAPS-PD) после 6 недель терапии.
Результаты
Источник: Richard Mark Kirkner. Nondopamine Antipsychotic Shows Clinical Signal in PD Psychosis. Medscape. April 2021.