Что называют сплавом железа с углеродом
Сплав железа с углеродом



Сплавы на основе железа и особенно железоуглеродистые сплавы – стали и чугуны – являются важнейшими материалами, применяемыми в промышленности. Для правильного понимания природы свойств разнообразных марок сталей и чугунов, необходимо иметь хорошее представление о диаграмме железо-углерод, разобраться в структурно-фазовом составе. На рис. 2.1 приведена диаграмма состояния Fe-C, на которой одной из важнейших фаз, влияющих на свойства сплавов, указан карбид железа Fe3C или цементит. Из диаграммы видно, что цементит ведет себя как самостоятельный компонент. Поэтому на диаграмме даны две согласующиеся друг с другом шкалы концентраций: одна показывает содержание углерода, а другая – цементита в процентах. Содержание углерода в цементите – 6,67%. Следовательно, левая ордината показывает содержание чистого железа, а правая – цементита.
Железо может находиться в двух аллотропических формах, которым соответствуют решетки ОЦК и ГЦК. Точки N (1392°С) и G(910°С) соответствуют полиморфному превращению α-Fe↔ γ-Fe. То при сплавлении с углеродом эта температура может понизиться до 727°С линия PSK. Температура плавления железа 1539°С. Температура плавления цементита 1250°С.
Основными фазами и структурными составляющими данной системы, от которых зависят свойства сплавов и их поведение при нагреве, охлаждении и нагружении являются феррит (Ф), аустенит (А) и цементит (Ц).
Рис. 2.1. Диаграмма состояния Fe-C (Fe-Fe3C)
Цементит является самой твердой и хрупкой фазой и структурной составляющей в рассматриваемом ряду сплавов, его твердость составляет 8000МПа (второе место после алмаза), а пластичность равна нулю. Следовательно при увеличении углерода в сплаве и возрастании количества твердого и хрупкого цементита и уменьшения доли мягкого и пластичного феррита твердость и прочность сплава должна повышаться, а пластичность и вязкость уменьшаться. Такой широкий диапазон противоречий механических свойств железо-углеродистых сплавов в левой части высокая пластичность, вязкость и небольшая твердость и огромная твердость с малыми пластичностью и вязкостью – в правой, дали возможность делить сплавы на стали и чугуны.
К сталям формально относятся сплавы содержащие менее 2,14% С, остальные сплавы причисляются к чугунам. Перечисленные ранее входящие в состав сталей и чугунов фазы (аустенит, феррит, цементит), могут находиться в них в виде зерен или мелких продолговатых включений и образовывать структурные составляющие – механические смеси – перлит и ледебурит.
Перлит– механическая смесь тонких пластинок цементита и более толстых пластинок феррита. Он образуется при 727°С, при охлаждении аустенита до 727°С, т.е. линии PSK, приобретает концентрацию 0,8% С, распадается: А0,8→Ф0,02+Ц6,67 (индексы при фазовых составляющих означают содержание в них углерода). Перлит образуется как в сталях, так и в чугунах и играет важную роль в формировании их свойств.
Ледебурит – механическая смесь одновременно кристаллизующихся из жидкой фазы зерен аустенита и цементита при постоянной температуре 1147°С, такая смесь называется эвтектической. Ледебурит содержит 4,3% С, т.е. при охлаждении жидкой фазы до Т=1147°С (линии ECF) и снижении углерода до 4,3% С происходит одновременная кристаллизация аустенита и цементита:
При понижении температуры до 727°С растворимость углерода в аустените снижается по линии ES до 0,8% и аустенит превращается в перлит. На диаграмме ледебурит с аустенитом обозначен ЛА, а с перлитом ЛП.
2.2. Выплавка чугуна
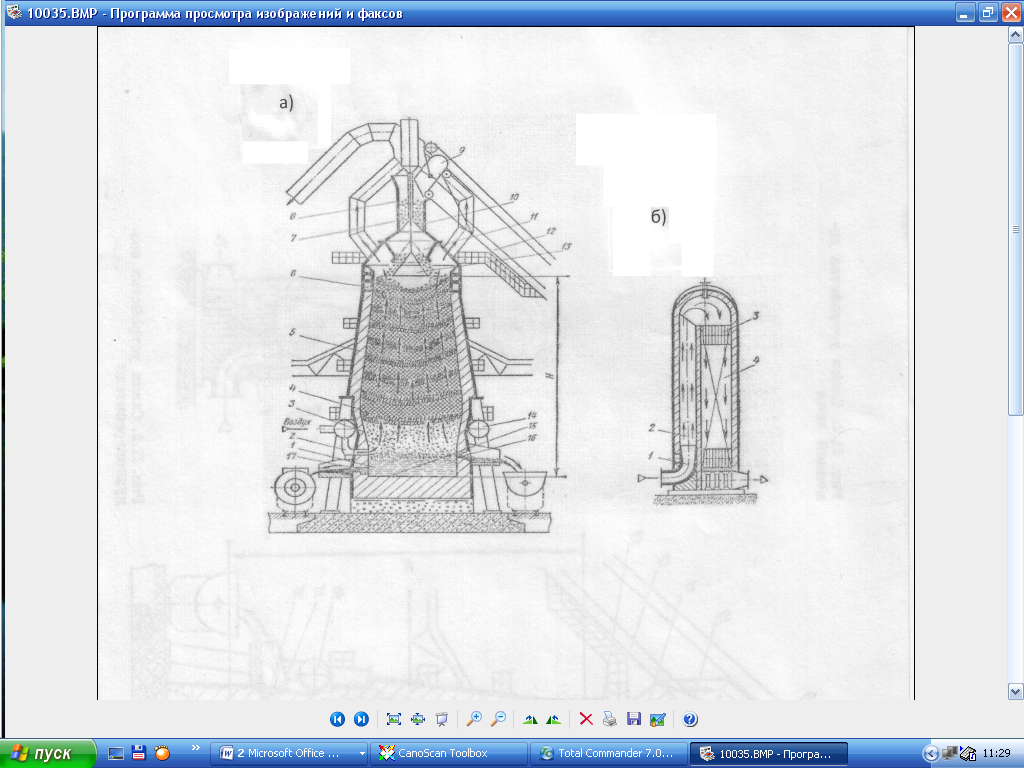
Чугун получают из железных руд (железо в руде находится в виде оксидов Fe2O3, Fe3O4 или FeO) плавильных агрегатах называемых доменными печами (рис. 2.2).
Для восстановления железа в доменную печь загружают топливо (кокс) и флюс (известняк CaCO3). Коксслужит источником теплоты и восстановителем железа в виде CO, твердого углерода, углеводорода.
Флюс – известняк в сочетании с пустой породой – SiO2 – образует легкоплавкую смесь с меньшей плотностью, чем у чугуна, скапливается над ним в виде шлака. Но загружаемые в доменную печь руда, кокс и известняк всегда содержат какое-то количество вредных примесей, попадающих в чугун, а из него в сталь в виде сульфидов FeS, FeS2, фосфидов в виде (FeO)3P2О5, (CaО)3P2O5.
Схема восстановления железа из руды при получении чугуна:
Железо в доменных печах восстанавливается косвенным путем газами СО, Н2, С2Н4 на первых двух ступнях, а на последней ступени взаимодействуют сильно разогретые закись железа и углерод кокса происходит прямое восстановление, образуя губчатое железо. Последнее науглераживается до 4,3%С, образуя легкоплавкую ледебуритную смесь, которая плавится и стекает на дно доменной печи.
Одновременно с восстановлением железа из MnO2 и SiO2 восстанавливаются и растворяются в жидком чугуне марганец и кремний:
В образующемся жидком чугуне растворяются также сера и фосфор, образуя сульфиды железа, сульфиды марганца, фосфиды железа, силикаты железа. Все эти примеси при переплавке чугуна переходят в сталь.
Следовательно, сущность производства чугуна заключается в восстановлении железа из его химических соединений при температуре С, СО, Н2, С2Н4. и насыщение его углеродом и восстановленными примесями в результате получается чугун.
Чугун периодически через 3-4 часа выпускается из доменной печи в ковш. По назначению выплавляется два вида чугуна: литейный для получения отливок и передельный для получения стали.
2.3. Чугуны
Железоуглеродистые сплавы в правой части диаграммы – рис. 2.1. Чугуны являются двухкомпонентными белыми чугунами, в которых весь углерод связан с железом в цементит. В реально получаемых чугунах определенная часть углерода может находиться в свободном состоянии в виде графита – темного кристаллического вещества с гексагональной кристаллической решеткой. Поэтому, чугуны принято делить на белые и серые. Белые имеют светлый излом в виду отсутствия графита и серые чугуны, имеющие темный излом из-за графита.
Графитными включениями можно управлять, придавая чугуну те или иные механические свойства в зависимости от формы и размеров этих включений.
В серых чугунах (СЧ) графитные включения имеют форму пластинок. Такой чугун является с готовыми концентраторами напряжений. Чем больше пластинок графита и чем они крупнее, тем ниже прочность серого чугуна. Серые чугуны по металлической массе бывают ферритные (феррит + графит), феррито-перлитные (феррит+графит+ перлит) и перлитные (перлит+графит). Металлическая масса в серых чугунах зависит от скорости охлаждения и наличия модификаторов.
Структура этих чугунов – мелкопластинчатый перлит (сорбит).
Высокопрочный чугун (ВЧ). Высокопрочный чугун с шаровидным графитом получают путем модифицирования серого чугуна магнием (0,03-0,07%) или магниевых лигатур с никелем 8-10%.
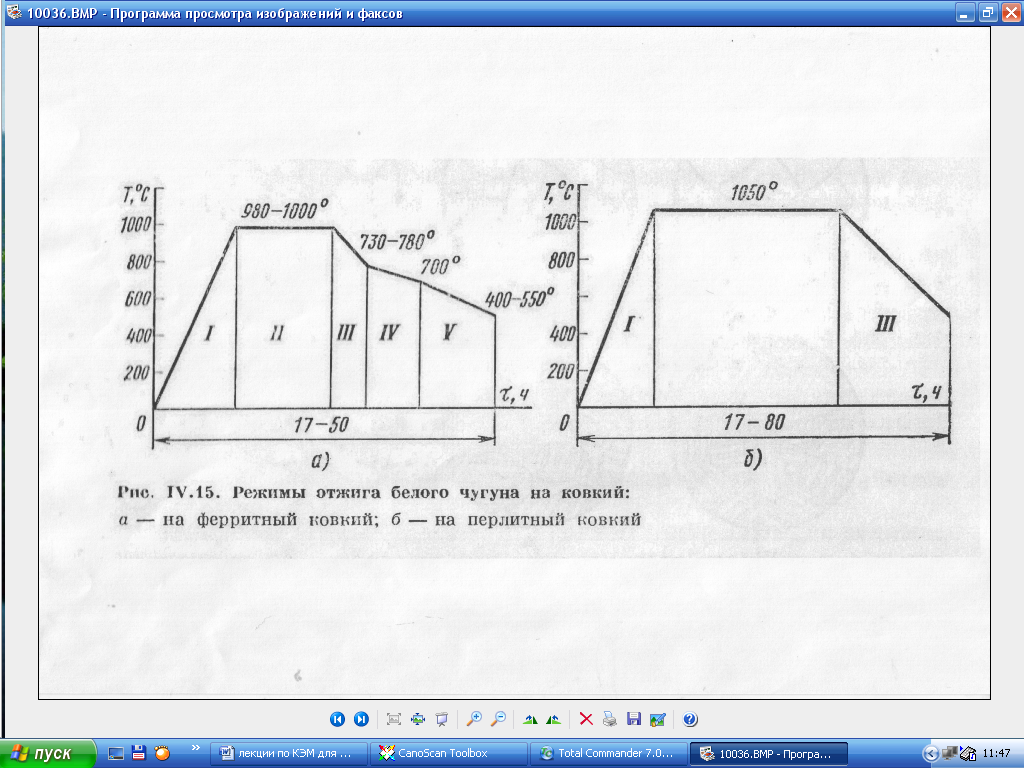
Ковкий чугун (КЧ). Ковкий чугун получают длительным (70-80ч) графитизирующим отжигом при высоких температурах (950-970°С) отливок из белого чугуна, что способствует образованию графита хлопьевидной формы. Металлическая основа ковкого чугуна: ферритный КЧ и перлитный КЧ. Наибольшей пластичностью обладает ферритный ковкий чугун. Толщина стенок отливки не должна превышать 40-50 мм.
Отжиг белого чугуна проводят в две стадии: нагрев до 950-970°С и выдержка для протекания первой стадии графитизации, т.е. распад цементита, входящего в состав ледебурита (А+Fe3CI) и получим А+графит (рис. 2.3). В результате распада цементита диффузионным путем образуется хлопьевидный графит (углерод отжиг).
Рис. 2.3. Схемы отжига ковкого чугуна.
Затем отливки охлаждают до температуры эвтектоидного превращения. В результате охлаждения до температур эвтектоидного превращения из аустенита выделяется вторичный цементит и его распад, что приводит к росту графитных включений. В эвтектоидном температурном интервале охлаждения резко замедляют и дают выдержку для протекания II стадии графитизации при распаде аустенита с образованием ферритно-графитной структуры. Излом ферритного КЧ бархатисто-черный вследствие большого количества графита. Если не проводить выдержку ниже эвтектоидной температуры и не снижать скорость охлаждения, то образуется перлитный ковкий чугун (П+Г), имеющий светлый сталистый излом.
Ферритные ковкие чугуны. КЧ37-12 и КЧ35-10 используют для изготовления деталей, эксплуатируемых при высоких динамических нагрузках (картеры редукторов, ступицы, крюки), а КЧ30-6 и КЧ33-8 – для менее ответственных деталей (головки, хомутики, гайки, глушители, фланцы, муфты и т.д.).
Перлитные ковкие чугуны. КЧ50-5, КЧ55-4 обладают высокой прочностью, удельной пластичностью, хорошей износостойкостью из него изготовляют вилки карданных валов, звенья и ролики цепных конвейеров, втулки, муфты, тормозные колодки и т.д. Для повышения твердости, износостойкости и прочности ковкого чугуна применяют нормализацию при 800-850°С, или закалку от 850-900°С и отпуск при 450-700°С. Закалка с последующим высоким отпуском позволяет получить структуру зернистого перлита.
Сталь (сплав железа с углеродом)
Для феррита характерны относительно низкие прочность и твёрдость, но высокие пластичность и ударная вязкость. Цементит хрупок, но весьма твёрд и прочен. Перлит обладает ценным сочетанием прочности, твёрдости, пластичности и вязкости. Соотношение между этими фазами в структуре С. определяется главным образом содержанием в ней углерода; различные свойства этих фаз и обусловливают многообразие свойств С. Так, С., содержащая
0,1% С (в её структуре преобладает феррит), характеризуется большой пластичностью; С. этого типа используется для изготовления тонких листов, из которых штампуют части автомобильных кузовов и др. деталей сложной формы. С., в которой содержится
Классификация сталей. В современной металлургии С. выплавляют главным образом из чугуна и стального лома. По типу сталеплавильного агрегата (кислородный конвертер, мартеновская печь, электрическая дуговая печь) С. называется кислородно-конвертерной, мартеновской или электросталью. Кроме того, различают металл, выплавленный в основной или кислой (по характеру футеровки) печи; С. при этом называется соответственно основной или кислой (например, кислая мартеновская С.).
По характеру застывания металла в изложнице различают спокойную, полуспокойную и кипящую С. Поведение металла при кристаллизации обусловлено степенью его раскисленности: чем полнее удалён из С. кислород, тем спокойнее протекает процесс затвердевания; при разливке малораскисленной С. в изложнице происходит бурное выделение пузырьков окиси углерода ‒ С. как бы «кипит». Полуспокойная С. занимает промежуточное положение между спокойной и кипящей С. Каждый из этих видов металла имеет достоинства и недостатки; выбор технологии раскисления и разливки С. определяется её назначением и технико-экономическими показателями производства.
Маркировка сталей. Единой мировой системы маркировки С. не существует. В СССР проведена большая работа по унификации обозначений различных марок С., что нашло отражение в государственных стандартах и технических условиях. Марки углеродистой С. обыкновенного качества обозначаются буквами Ст и номером (Ст0, Ст1, Ст2 и т.д.). Качественные углеродистые С. маркируются двузначными числами, показывающими среднее содержание С в сотых долях процента: 05, 08, 10, 25, 40 и т.д. Спокойную С. иногда дополнительно обозначают буквами сп, полуспокойную ‒ пс, кипящую ‒ кп (например, СтЗсп, Ст5пс, 08кп). Буква Г в марке С. указывает на повышенное содержание Mn (например, 14Г, 18Г). Автоматные С. маркируются буквой А (А12, А30 и т.д.), углеродистые инструментальные С. ‒ буквой У (У8, У10, У12 и т.д. ‒ здесь цифры означают содержание С. в десятых долях процента).
Лит.: Сталеплавильное производство. Справочник, под ред. А. М. Самарина, т. 1‒2, М., 1964; Меськин В. C., Основы легирования стали, 2 изд., М., 1964; Гудремон Э., Специальные стали, пер. с нем., 2 изд., т. 1‒2, М., 1966; Дреге В., Сталь как конструкционный материал, пер. с нем., М., 1967; Гуляев А. П., Чистая сталь, М., 1975.
Лит.: Тульские «златокузнецы». [Альбом], Л., 1974.
СПЛАВЫ ЖЕЛЕЗА С УГЛЕРОДОМ



Сплавы железа с углеродом являются основой так называемых черных сплавов — сталей и чугунов, которые служат важнейшими конструкционными материалами в технике. Структура и свойства любого сплава зависят прежде всего от свойств базового компонента и элементов-добавок, а также от характера их взаимодействия.
Чистое железо — металл серебристо-белого цвета; тугоплавкий. Температура плавления железа 1539°С. Железо имеет две полиморфные модификации, a и g.
При температурах ниже 910°С железо имеет объемно-центрированную кубическую решетку. Эту модификацию называют a-железо; a-железо магнитно до температуры 768°С (точка Кюри).
При нагреве железа его объемно-центрированная кубическая решетка при 910°С превращается в гранецентрированную кубическую решетку, a-железо превращается в g железо; g-железо существует при температуре 910-1392°С.
Углерод является неметаллическим элементом. Температура плавления углерода 3500°С. Углерод в природе может существовать в двух полиморфных модификациях: алмаз и графит. Форма алмаза в сплавах не встречается.
В железоуглеродистых сплавах в свободном виде углерод находится в форме графита. Кристаллическая структура графита слоистая. Прочность и пластичность его весьма низкие.
Углерод растворим в железе в жидком и твердом состояниях, может образовывать химическое соединение — цементит, может находиться в свободном виде в форме графита.
Железоуглеродистые сплавы могут иметь следующие структурные составляющие.
Феррит (Ф) — твердый раствор внедрения углерода и других элементов в a-железе. Имеет объемно-центрированную кубическую решетку. Растворимость углерода в феррите очень мала: при комнатной температуре до 0,005 %; наибольшая растворимость 0,02 % при 727°С. Феррит высокопластичен и мягок, хорошо обрабатывается давлением в холодном состоянии.
Аустенит (А) — твердый раствор углерода и других элементов в g-железе. Существует только при высоких температурах. Предельная растворимость углерода в g-железе 2,14% при температуре 1147°С и 0,8 % при 727°С. Эта температура является нижней границей существования аустенита в железоуглеродистых сплавах. Аустенит высокопластичен, но более тверд, чем феррит.
Цементит (Ц)— химическое соединение железа с углеродом (карбид железа Fe3C). В цементите содержится 6,67 % углерода. Температура плавления цементита около 1600°С. Имеет сложную кристаллическую решетку. Самая твердая и хрупкая составляющая железоуглеродистых сплавов. Цементит неустойчив и в определенных условиях распадается с образованием свободного углерода в виде графита по реакции: Fe3C > 3Fe + С.
Чем больше цементита в железоуглеродистом cплаве, тем выше его твердость.
Графит — аллотропическая модификация углерода. Графит мягок, прочность его очень низкая. В чугунах и графитизированной стали содержится в виде включений различных форм. Форма графитовых включений влияет на механические и технологические свойства сплава.
Перлит (П) — механическая смесь феррита и цементита, содержащая 0,8 % углерода. Образуется при перекристаллизации (распаде) аустенита при температуре 727°С. Этот распад называется эвтектоидным, а перлит — эвтектоидом. Перлит обладает высокими прочностью, твердостью и повышает механические свойства сплава.
Ледебурит — механическая смесь аустенита и цементита, содержащая 4,3 % углерода. Образуется в результате эвтектического превращения при температуре 1147°С. При температуре 727°С аустенит превращается в перлит, и после охлаждения ледебурит представляет собой смесь перлита с цементитом. Ледебурит имеет высокую твердость и большую хрупкость. Содержится во всех белых чугунах.
Диаграмма состояния железо — цементит представлена в упрощенном виде на рис. 14. Она показывает фазовый состав и структуру железоуглеродистых сплавов с концентрацией от чистого железа до цементита (6,67 % углерода).
В рассматриваемой системе существуют следующие фазы: жидкий сплав, твердые растворы (феррит и аустенит), химических соеденений
(в упрощенном виде): А — аустенит, П — перлит, Л — ледебурит,
Ф.— феррит, Ц — цементит
Жидкий сплав (Ж. С.) существует выше линии ликвидус ACD. Цементит Fe3C (Ц) — вертикальная линия DFKL. Область феррита (Ф) располагается левее линии GPQ. Область аустенита (А) — AESG.
На диаграмме точка А (1539°С) соответствует температуре плавления железа, а точка D (1600°С) — температуре плавления цементита. Точка С (911 °С) — температура полиморфного превращения железа a 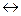
Точка С соответствует предельному содержанию углерода в аустените (2,14 % при температуре 1147°С). При понижении температуры растворимость углерода в аустените уменьшается полинии ES. В точке S она составляет 0,8 % при 727°С.
Точка Р — предельное содержание углерода в феррите 0,02 % при 727°С. При охлаждении до комнатной температуры растворимость углерода в феррите уменьшается по линии PQ до 0,005 %.
При температуре 1147°С жидкий сплав, содержащий 4,3 % углерода, кристаллизуется с образованием эвтектики (механической смеси двух фаз аустенита и цементита). При этом образуется структура ледебурита. Точка С на диаграмме — точка эвтектики, линия ECF— линия кристаллизации эвтектики.
При температуре 727°С аустенит, содержащий 0,8 % углерода, распадается на две фазы — цементит и феррит, т. е. происходит эвтектоидное превращение. При этом образуется структура, называемая перлитом. На диаграмме точка S — точка эвтектоида, линия PSK— линия эвтектоидного превращения.
Рассмотрим кристаллизацию сплавов, содержащих различное количество углерода.
Сплавы,содержащие до 2,14% углерода, кристаллизуются в интервале температур, ограниченном линиями АС (линия ликвидус) и АЕ (линия солидус). После затвердевания сплавы имеют однофазную структуру — аустенит.
При кристаллизации доэвтектических сплавов, содержащих от 2,14 до 4,3% С, из жидкой фазы при температурах, соответствующих линии ликвидус АС, сначала выделяются кристаллы аустенита. При температуре 1147°С оставшаяся жидкость, имеющая эвтектический состав (4,3 % С), кристаллизуется, образуя эвтектику ледебурит. После затвердевания доэвтектические сплавы состоят из аустенита и ледебурита.
В заэвтектических сплавах, содержащих от 4,3 до 6,67 % С, с понижением температуры до линии ликвидус CD зарождаются и растут кристаллы цементита. При температуре 1147°С жидкость достигает эвтектической концентрации и затвердевает с образованием ледебурита. После затвердевания заэвтектические чугуны состоят из первичного цементита (кристаллизовавшегося из жидкого сплава) и ледебурита.
Эвтектический сплав (4,3% C) кристаллизуется при постоянной температуре с образованием только эвтектики — ледебурита (А + Fe3C).
После затвердевания железоуглеродистые сплавы претерпевают фазовые и структурные изменения. Это связано с полиморфным превращением железа и с изменением растворимости углерода в аустените и в феррите с понижением температуры.
Сплавы, содержащие до 0,02% С (точка Р), испытывают при охлаждении и при нагреве полиморфное превращение a 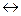
Сплавы, содержащие 0,02—0,8% С, называют доэвтектоидными. Эти стали после кристаллизации состоят из аустенита. При температурах ниже линии GOS начинают расти зерна феррита. При достижении 727°С аустенит, не претерпевший превращения, имеет эвтектоидную концентрацию (0,8 % С) и распадается с одновременным выделением из него феррита и цементита, образующих эвтектоидную структуру перлит. После окончательного охлаждения доэвтектоидные сплавы имеют структуру феррит + перлит.
В эвтектоидном сплаве (0,8% С) при температуре 727°С (точка S) весь аустенит превращается в перлит.
При охлаждении заэвтектоидных сплавов(от 0,8 до 2,14% С) до температур, соответствующих линии SE, из аустенита выделяется цементит (вторичный) в результате уменьшения растворимости углерода в аустените. При температуре 727°С аустенит, содержащий 0,8 % С, превращается в перлит. После охлаждения заэвтектоидные сплавы состоят из перлита и цементита.
В доэвтектических сплавах вследствие уменьшения растворимости углерода при охлаждении (линия SE) происходит частичный распад аустенита с выделением кристаллов вторичного цементита. При 727°С аустенит эвтектоидного состава превращается в перлит. Структура доэвтектических сплавов после окончательного охлаждения состоит из перлита, вторичного цементита и ледебурита (перлит + цементит).
Эвтектический сплав (4,3 % С) при температурах ниже 727°С состоит только из ледебурита (перлит + цементит).
Заэвтектические сплавы после полного охлаждения состоят из первичного цементита и ледебурита (перлит + цементит).
При температурах ниже 727° С железоуглеродистые сплавы имеют различную структуру, но фазовый состав их одинаков. Они состоят из двух фаз феррита и цементита.
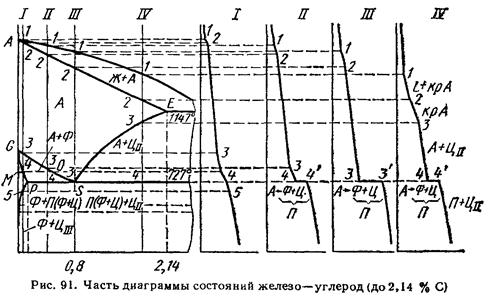
Все сплавы, содержащие до 2,14%С, после окончания кристаллизации имеют структуру аустенита. В сплавах, содержащих до 0,1 % С (до точки Н), при охлаждении вначале происходит кристаллизация Fеδ (С) с последующим превращением его в аустенит. В сплавах, содержащих 0,1—0,5 % С (до точки В), образование аустенита происходит по линии HJВ при 1499 °С по перитектической реакции ЖB + ФH ↔ АJ. Поэтому часто пользуются более упрощенной диаграммой Fе—Fе3С, где линия солидуса АHJЕ представлена в виде простой линии АЕ (рис. 91).
На рис. 91 изображена левая часть диаграммы Fе—Fе3С.
Сплав I содержит меньше 0,02% С, т. е. расположен левее точки Р. Он представляет собой технически чистое железо.
Кристаллизация аустенита начинается в точке 1 и заканчивается в точке 2. До точки 3 в сплаве I не происходит никаких фазовых превращений: сплав просто охлаждается.
Чем больше в стали углерода, т. е. чем ближе располагается сплав к точке 5, тем большее время необходимо для этого превращения (отрезок 4-4′ на кривой охлаждения будет больше) и в структуре сплава будет больше перлита. После охлаждения структура таких сплавов состоит из Ф+ П.
Сплав III содержит 0,8 % С, т. е. по составу отвечает точке эвтектоидного превращения 5. При его охлаждении до 727 °С аустенит не испытывает никаких превращений, поэтому при температуре 727 °С весь аустенит превратится в перлит,
При 727°С (точка 4) происходит эвтектоидное превращение. Таким образом, после окончательного охлаждения сплав будет иметь структуру П + ЦII. По сравнению с ЦIII выделение ЦII происходит при более высоких температурах, когда скорости диффузии велики. Поэтому ЦII образуется по границам зерен в виде сетки.
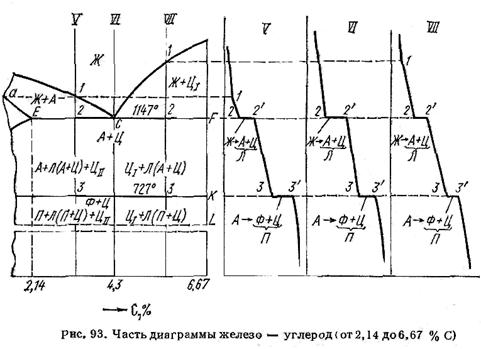
Особенностью всех сплавов с содержанием углерода от 2,14 до 6,67 % является наличие в их структуре ледебурита (рис. 93).
Кривая охлаждения сплава V типична для всех сплавов, содержащих от 2,14 до 4,3 % углерода (т. е. расположенных от точки Е до точки С). Кристаллизация зерен аустенита начинается в точке 1 и заканчивается в точке 2. С понижением температуры состав аустенита изменяется по линии солидуса от точки а до точки Е, а состав жидкой фазы — от точки 1 до точки С. При 1147 °С (точка 2) оставшаяся жидкость претерпевает эвтектическое превращение
При температурах между линиями ЕСF и РSК сплав имеет структуру А + Л (А + Ц) + ЦII. И в этих сплавах образуется ЦII, так как при охлаждении состав аустенита также будет изменяться по линии GS.
При 727 °С (линия РSК) происходит эвтектоидное превращение АS ↔ эвтектоид(ФР + ЦK) и ниже этой температуры сплав будет иметь структуру П + Л (П + Ц) + ЦII. Вторичный цементит сливается с цементитом ледебурита.
При охлаждении сплава VI (4,3 % С) при температуре 1147 о С (точка С) вся жидкость превращается в ледебурит, который с понижением температуры испытывает превращения, аналогичные сплаву V.
В сплавах, содержащих углерода от 4,3 до 6,67 % (сплав VII), в точке 1 начинается образование кристаллов цементита. Чтобы отметить характер выделения, такой цементит называют первичным и обозначают ЦI. Поскольку при кристаллизации ЦI выделяется из жидкой фазы, его кристаллы обычно бывают крупными (грубые выделения). В точке 2 происходит эвтектическое превращение. Структура сплава между линиями ЕСF и РSК ЦI + Л (А + Ц), При 727 о С происходит эвтектоидное превращение аустенита. Окончательная структура сплава (ниже 727°С) ЦI + Л (П + Ц). Химические и физические свойства ЦI, ЦII и ЦIII одинаковы. Влияние на механические свойства сплавов оказывает различие в размерах, количестве и расположении этих выделений.
Влияние углерода и примесей на свойства сталей
Углеродистые стали являются основными. Их свойства определяются количеством углерода и содержанием примесей, которые взаимодействуют с железом и углеродом.
Влияние углерода на свойства сталей показано на рис. 10.1.
С ростом содержания углерода в структуре стали увеличивается количество цементита, при одновременном снижении доли феррита. Это приводит к уменьшению пластичности, к повышению прочности и твердости. Прочность повышается до содержания углерода около 1%, а затем она уменьшается, так как образуется грубая сетка цементита вторичного.
Углерод влияет на вязкие свойства. Увеличение содержания углерода повышает порог хладоломкости и снижает ударную вязкость.
Повышаются электросопротивление, снижаются магнитная проницаемость и плотность магнитной индукции.
Рис.10.1. Влияние углерода на свойства сталей
Углерод оказывает влияние и на технологические свойства. Повышение содержания углерода ухудшает литейные свойства стали (для изготовления отливок используются стали с содержанием углерода до 0,4 %), обрабатываемость давлением и резанием, свариваемость. Следует учитывать, что стали с низким содержанием углерода также плохо обрабатываются резанием.
В углеродистых сталях всегда присутствуют примеси, которые делятся на четыре группы.
1. Постоянные примеси: кремний, марганец, сера, фосфор.
Марганец и кремний вводятся в процессе выплавки стали для раскисления, они являются технологическими примесями.
Содержание марганца не превышает 0,5…0,8 %. Марганец повышает прочность, не снижая пластичности, и резко снижает красноломкость стали, вызванную влиянием серы. Он способствует уменьшению содержания сульфида железа FeS, так как образует с серой соединение сульфид марганца MnS. Частицы сульфида марганца располагаются в виде отдельных включений, которые деформируются и оказываются вытянутыми вдоль направления прокатки.
Содержание кремния не превышает 0,35…0,5 %. Кремний, дегазируя металл, повышает плотность слитка. Кремний растворяется в феррите и повышает прочность стали, особенно повышается предел текучести, 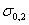
Содержание фосфора в стали 0,025…0,05 %. Фосфор, растворяясь в феррите, искажает кристаллическую решетку и увеличивает предел прочности 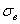
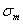
Располагаясь вблизи зерен, увеличивает температуру перехода в хрупкое состояние, вызывает хладоломкость, уменьшает работу распространения трещин. Повышение содержания фосфора на каждую 0,01 % повышает порог хладоломкости на 20…25 o С.
Хладноломкость Ст3кп – 0 о С, а у Ст3сп – «-40 о С», поэтому применение кипящей стали для северных районов не допустимо.
Фосфор обладает склонностью к ликвации, поэтому в центре слитка отдельные участки имеют резко пониженную вязкость. Для некоторых сталей возможно увеличение содержания фосфора до 0,10…0,15 %, для улучшения обрабатываемости резанием.
Сера S – уменьшается пластичность, свариваемость и коррозионная стойкость. Р–искажает кристаллическую решетку.
Содержание серы в сталях составляет 0,025…0,06 %. Сера – вредная примесь, попадает в сталь из чугуна. Сера нерастворима в железе, она образует с ним химическое соединение – сульфид железа FeS, которое, в свою очередь, образует с железом легкоплавкую эвтектику (Fе + FеS) с температурой плавления988 o С. Поэтому при нагреве стальных заготовок для пластической деформации выше 900 °С эвтектика плавится, нарушаются связи между зернами, сталь становится хрупкой. При деформации в местах расположения эвтектики возникают надрывы и трещины, заготовка разрушается – явление красноломкости (повышение хрупкости при высоких температурах).
Для уменьшения вредного влияния серы добавляют марганец (соединение MnS имеет tпл=1620 о С, пластично и не вызывает красноломкости).
Сера снижает механические свойства, особенно ударную вязкость а 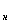
Азот и кислород находятся в стали в виде хрупких неметаллических включений: окислов (FeO, SiO2, Al2O3 ) нитридов (Fe 2N), в виде твердого раствора или в свободном состоянии, располагаясь в дефектах (раковинах, трещинах).
Примеси внедрения (азот N, кислород О) повышают порог хладоломкости и снижают сопротивление хрупкому разрушению. Неметаллические включения (окислы, нитриды), являясь концентраторами напряжений, могут значительно понизить предел выносливости и вязкость.
Очень вредным является растворенный в стали водород, который значительно охрупчивает сталь. Он приводит к образованию в катанных заготовках и поковках флокенов.
Флокены – тонкие трещины овальной или округлой формы, имеющие в изломе вид пятен – хлопьев серебристого цвета. Металл с флокенами нельзя использовать в промышленности, при сварке образуются холодные трещины в наплавленном и основном металле. Если водород находится в поверхностном слое, то он удаляется в результате нагрева при 150…180 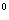
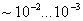
Сталь считают легированной хромом или никелем, если содержание этих элементов составляет 1 % или более.
При содержании ванадия, молибдена, титана, ниобия и других элементов более 0,1—0,5 % стали считают легированными этими элементами.
Сталь является легированной и в том случае, если в ней содержатся только элементы, характерные для углеродистой стали, марганец или кремний, но их количество должно превышать 1 %.
В конструкционных сталях легирование осуществляют с целью улучшения механических свойств — прочности, пластичности и т. д. Кроме того, при введении в сталь легирующих элементов меняются физические, химические и другие ее свойства.
Нужный комплекс свойств достигается не только легированием, но и рациональной термической обработкой, в результате которой получается необходимая структура.
Как правило, легирующие элементы существенно повышают стоимость стали, а некоторые из них к тому же являются дефицитными металлами, поэтому добавление их в сталь должно быть строго обосновано.