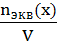Что называют раствором классификация растворов примеры
Растворы
Классификация растворов
Раствор — гомогенная (однородная) система, состоящая из частиц растворенного вещества, растворителя и продуктов их взаимодействия.
Растворы подразделяются на:
•молекулярные — водные растворы неэлектролитов — органических веществ (спирт, глюкоза и т. д.);
•молекулярно-ионные — растворы слабых электролитов (азотистой, сероводородной кислот и др.);
•ионные — растворы сильных электролитов (щелочей, солей, кислот — NaOH, K2SO4, HNO3).
Растворимость многих веществ небезгранична и зависит от температуры. Насыщенным называется такой раствор, в котором при данной температуре вещество больше не растворяется. В ненасыщенном растворе содержится меньше вещества, а в перенасыщенном — больше, чем в насыщенном.
В работе с веществами важно знать их растворимость в воде. Вещество считается хорошо растворимым, если при комнатной температуре в 100 г воды растворяется 1 г этого вещества; если меньше, то вещество считается малорастворимым; при растворимости менее 0,001 г — нерастворимым.
Поведение веществ в растворе
Растворение — это физико-химический процесс. Он сочетает в себе физический процесс (дробление до молекул) и химическое воздействие компонентов (образование в воде непрочных соединений — гидратов). В процессе растворения молекулы воды разрушают кристаллы растворяемого вещества. Это разрушение происходит в месте соприкосновения кристалла с водой. Чем больше площадь поверхности соприкосновения, тем быстрее разрушаются кристаллы. В результате диффузии происходит самопроизвольное распределение частиц одного вещества между частицами другого, что приводит к образованию раствора. Для улучшения контакта вещества с растворителем увеличивают площадь поверхности соприкосновения, вещества измельчают и раствор перемешивают.
В результате химического взаимодействия вещества с водой образуются соединения — гидраты. О химическом взаимодействии говорят такие признаки химических реакций, как тепловые явления при растворении: растворение H2SO4 сопровождается выделением тепла, растворение NaCl, NH4 NO3 — охлаждением. Косвенным доказательством гидратации является существование твердых кристаллогидратов — солей, в состав которых входят вода, например медный купорос CuSO4 х 5Н2O.
Массовая доля вещества. Концентрация растворов
Массовая доля растворенного вещества — это отношение его массы m к массе раствора mр-ра. Ее обозначают буквой ω («омега»).
ω(Х) = m(Х)/mр-ра (в долях единицы);
Аналогично массовой доле определяется и объемная доля газообразного вещества в газовой смеси, обозначаемая греческой буквой φ («фи»).
Концентрация (С) — это содержание растворенного вещества в единице массы или объема.
Процентная концентрация раствора — это отношение массы растворенного вещества m (в граммах) к массе раствора (в граммах).
Молярная концентрация — это отношение количества растворенного вещества n (в молях) к объему раствора V (в литрах). Ее обозначают буквой С.
Классификация растворов



Раствор как гомогенная система. Растворитель, растворенное вещество. Классификация растворов по степени дисперсности, по растворимости в воде, по способности к диссоциации.
Раствор— находящаяся в состоянии равновесия гомогенная система переменного состава из двух или более веществ.
Под переменным составом раствора понимают то простое обстоятельство, что соотношение смешанных друг с другом веществ может непрерывно изменяться в определенных пределах.
Растворитель — компонент, агрегатное состояние которого не изменяется при образовании раствора. (В случае же растворов, образующихся при смешении газа с газом, жидкости с жидкостью, твёрдого вещества с твёрдым, растворителем считается компонент, количество которого в растворе преобладает)
Любой раствор состоит из растворенных веществ и растворителя. Вещества, составляющие раствор, называются компонентами раствора.
Растворенное вещество — Компонент жидкого или твердого раствора, который присутствует в меньшем или незначительном количестве; компонент растворяется в Растворителе.
Классификация растворов
по растворимости в воде:
В лабораторной практике различают концентрированные растворы (содержание растворенного вещества соизмеримо с содержанием растворителя) и разбавленные растворы (содержание растворенного вещества мало по сравнению с содержанием растворителя).
А ниже это уже про растворимость веществ, не нужно здесь.
по способности к диссоциации:
по степени дисперсности:
| Грубодисперсные системы (взвеси) | Коллоидные системы (кровь, лимфа, слюна, белки) | Истинные растворы (раствор соли в воде) |
| Размер частиц дисперсной фазы | ||
| Больше 100 нм 10 –7 –10 –5 м | 1-100 нм 10 –9 –10 –7 | меньше 1 нм |
I. Взвеси – это дисперсные системы, в которых размеры распределённых частиц сравнительно велики (10 –7 –10 –5 м). Взвеси делятся на суспезии и эмульсии; в первых распределённое вещество твёрдое, во вторых – жидкое. Частицы взвеси видны простым глазом или в обычный оптический микроскоп. Взвеси – системы мутные и непрозрачные. Взвеси неустойчивы, частицы диспергированного вещества выпадают в осадок (песок + вода), а если плотность диспергированного вещества меньше плотности среды, то диспергированное вещество всплывает (глина + масло). Процесс разделения взвесей называется седиментацией (для суспензий) и расслоением(для эмульсий).
II. Коллоидные системы – это такие дисперсные системы, в которых частицы распределённого вещества имеют размеры порядка 10 –9 –10 –7 м. Каждая такая частица может содержать большое число атомов или молекул. Такие частицы невидимы через обычный микроскоп, но видимы в ультрамикроскоп, где свет падает сбоку или сзади, в результате чего в поле зрения видны светлые точки, возникающие в результате рассеяния света диспергированными частицами.
III. Истинные растворы или просто растворы – это дисперсные системы, в которых диспергированное вещество распределено в среде в виде молекул или ионов; частицы имеют размеры порядка 10 –10 –10 –7 м. Растворы системы однородные, устойчивые.
Способ выражении концентрации растворов: массовая доля вещества в растворе, молярная концентрация, молярная концентрация эквивалента(или нормальная концентрация), массовая концентрация или титр.
Концентрацией вещества называют величину, измеряемую количеством растворенного вещества, содержащегося в определенной массе или объеме раствора или растворителя.
ω (х)=
Численно массовая доля равна числу граммов вещества, растворенного в 100г раствора.
См=
1моль/л = 1М раствор – одномолярный раствор (в 1 л раствора содержится 1 моль растворенного вещества);
0,1М – децимолярный раствор;
0,01М – сантимолярный раствор;
0,001М – милимолярный раствор.
3. Нормальная концентрация (молярная концентрация эквивалента, СN)- количество моль- эквивалентов вещества, содержащегося в 1 л раствора.
СN=
Единица измерения моль-экв/л, Сокращенно обозначается буквой N. Например, 0.1N HCL означает, что в 1 литре такого раствора содержится 0,1моль- эквивалент НСl.
3. Массовая концентрация или титр раствора T(Х) измеряют в кг/см^3, г/см^3, г/мл,
Титр (Т)— масса растворенного вещества, содержащаяся в 1 мл раствора, выраженная в граммах. Определятся по формуле:
Раствор с известным титром называется титрованным раствором.
Классификация растворов



Растворимость. Способы выражения концентрации растворов. Растворение как физико-химический процесс.
Цели:
− Сформировать представление о понятиях: «раствор», «растворение», «растворимость», «концентрация».
− Рассмотреть физическую, химическую и современную теорию растворов.
− Показать значение растворов в жизни человека.
− Закрепить знания, умения и навыки учащихся по решению задач на тему растворы.
− Развитие у студентов навыков наблюдения, логического мышления, умений делать выводы и заключения.
Ход лекции
I. Организационный момент. Проверка знаний по скорости химической реакции.
II. Объяснение нового материала.
Учитель: Растворы играют важную роль в природе, технике и науке.
Где используются растворы? (ответы учащихся)
Учитель: Велика роль растворов в возникновении и развитии жизни на Земле. Одной из теорий возникновения организмов является теория зарождения жизни в первичном океане, который представлял собой воду с растворенными в ней веществами. Из этого раствора организмы получали необходимые для роста и развития ионы и молекулы.
В организме человека находятся физиологически важные растворы. Какие? (кровь, желудочный сок и др.)
Раствор – это гомогенная система, состоящая из двух или более компонентов, содержание которых можно изменять в определенных пределах без нарушения однородности.
Раствор – гомогенная (однородная) система, состоящая из частиц растворенного вещества, растворителя и продуктов их взаимодействия.
Классификация растворов
• по агрегатному состоянию:газовые(воздух), жидкие(морская вода), твердые (сплавы)
• по составу растворителя (водные, аммиачные, бензольные и др.)
По размеру частиц или по степени измельченности (дисперстности):
Приведите примеры природных грубодисперсных систем?
Коллоидные растворы отличаются тем, что их частицы сильно рассеивают проходящий через них свет и делают заметным путь пропущенного светового луча (эффект Тиндаля).
Концентрация насыщенного раствора наз. растворимостью с указанием температуры, при которой она определена.
n Растворимость — число моль растворенного в-ва в одном литре раств-ля (в состоянии насыщения)
Раствори́мость — способность вещества образовывать с другими веществами однородные системы — растворы, в которых вещество находится в виде отдельных атомов, ионов, молекул или частиц. Растворимость выражается концентрацией растворённого вещества в его насыщенном растворе либо в процентах, либо в весовых или объёмных единицах Растворимость газов в жидкости зависит от температуры и давления. Растворимость жидких и твёрдых веществ — практически только от температуры.
Истинные растворы – термодинамически устойчивые системы, неограниченно стабильные во времени.
Движущими силами образования растворов являются энтропийный и энтальпийный факторы. При растворении газов в жидкости энтропия всегда уменьшается ΔS 0). Чем сильнее взаимодействие растворенного вещества и растворителя, тем больше роль энтальпийного фактора в образовании растворов. Знак изменения энтальпии растворения определяется знаком суммы всех тепловых эффектов процессов, сопровождающих растворение, из которых основной вклад вносят разрушение кристаллической решетки на свободные ионы (ΔH > 0) и взаимодействие образовавшихся ионов с молекулами растворителя (сольтивация, ΔH
Механизм образования растворов.
Раствор – гомогенная система, в которой присутствуют больше 2х веществ. Это могут быть составы: газ – жидкость, газ – твердое вещество, жидкость – твердое вещество, а могут быть и однородные смеси.
Классификация растворов.
1. В зависимости от агрегатного состояния растворы различают:
Газообразные растворы – это воздух и другие газовые смеси.
Жидкие растворы – гомогенные растворы жидкостей, твердых тел и газов.
Твердые растворы – сплавы.
Растворители: вода, бензол, спирты, эфиры, ацетон и т.д.
В ходе растворения ионы растворимого вещества под действием беспорядочно движущихся частиц растворителя переходят в раствор, в результате чего образуется новая однородная система.
Вода – полярный растворитель, кислород может притягивать к себе электронную пару Na-Cl.
В результате колебательного движения часть молекул поваренной соли переходят в раствор (в воду), в следствие чего «открывается» следующий слой кристалла. Постепенно таким образом все слои переходят в раствор, в результате чего кристалл растворяется, а вода приобретает солоноватость. В следствие диффузии частицы, которые перешли в раствор, распределяются по всему объему растворителя.
Виды растворов:
2. По числу растворенных веществ растворы различают:
3. По характеру веществ растворы бывают:
Растворы. Состав раствора. Классификация растворов



Растворы— это твердая или жидкая гомогенная система, состоящая из молекул растворителя, молекул растворённого вещества и продуктов их взаимодействия.
По размеру растворенных веществ все многокомпонентные растворы разделяют на:
· грубодисперсные системы (смеси);
· тонкодисперсные системы (коллоидные растворы);
· высокодисперсные системы (истинные растворы).
По фазовому состоянию растворы бывают:
По составу растворенных веществ, проводящие электрический ток жидкие растворы рассматривают как:
По составу фаз: гомогенные и гетерогенные
Если молекулярные или ионные частицы, распределённые в жидком растворе присутствуют в нём в таком количестве, что при данных условиях не происходит дальнейшего растворения вещества, раствор называется насыщенным. (Например, если поместить 50 г NaCl в 100 г H2O, то при 20ºC растворится только 36 г соли). Насыщенным называется раствор, который находится в динамическом равновесии с избытком растворённого вещества.
При нагревании смеси соли с водой до 100°C произойдёт растворение 39,8 г NaCl в 100 г воды. Если теперь удалить из раствора нерастворившуюся соль, а раствор осторожно охладить до 20ºC, избыточное количество соли не всегда выпадает в осадок. В этом случае мы имеем дело с перенасыщенным раствором. Перенасыщенные растворы очень неустойчивы. Помешивание, встряхивание, добавление крупинок соли может вызвать кристаллизацию избытка соли и переход в насыщенное устойчивое состояние.
Растворимость. Влияние различных факторов на растворимость веществ.
Раствори́мость — способность вещества образовывать с другими веществами однородные системы — растворы, в которых вещество находится в виде отдельных атомов, ионов, молекул или частиц. Растворимость выражается концентрацией растворённого вещества в его насыщенном растворе либо в процентах, либо в весовых или объёмных единицах.
Растворимость зависит от растворяемого вещества, растворителя, температуры, давления, наличия в растворителе других веществ.
Растворимость большинства газов растет с ростом давления и уменьшается с ростом температуры. Для твердых и жидких веществ влияние давления на растворимость менее значимо, чем для газов.
В большинстве случаев при увеличении температуры растет растворимость (обратной зависимостью обладают, например, многие соли кальция). Так как растворяемое вещество часто увеличивает температуру кипения растворителя, растворимость при атмосферном давлении может быть измерена и выше температуры кипения растворителя. При повышенном давлении и температуре растворимость может сильно увеличиваться (например, в воде при высоком давлении и температуре относительно хорошо растворяются углеводороды и кварц, которые почти нерастворимы при обычных условиях).
Наличие в растворителе других веществ может сильно влиять на растворимость.
Примеры: 1) добавление в водный раствор неполярных веществ солей может привести к выделению неполярного вещества в осадок, за счет эффекта высаливания,
2) наличие растворённого кислорода сильно влияет на растворимость ртути в воде за счет эффектов поверхностного окисления,
3) наличие небольшого количества влаги в абсолютном этаноле может сильно изменить растворимость неполярных веществ.