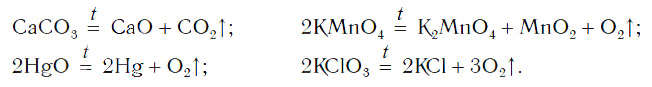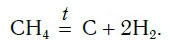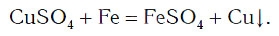Что называют хим реакцией
Химическая реакция
Хими́ческая реа́кция — превращение одного или нескольких исходных веществ (реагентов) в отличающиеся от них по химическому составу или строению вещества (продукты реакции). В отличие от ядерных реакций, при химических реакциях ядра атомов не меняются, в частности не изменяется их общее число, изотопный состав химических элементов, при этом происходит перераспределение электронов и ядер и образуются новые химические вещества.
Химические реакции происходят при смешении или физическом контакте реагентов самопроизвольно, при нагревании, участии катализаторов (катализ), действии света (фотохимические реакции), электрического тока (электродные процессы), ионизирующих излучений (радиационно-химические реакции), механического воздействия (механохимические реакции), в низкотемпературной плазме (плазмохимические реакции) и т. п. Взаимодействие молекул между собой происходит по цепному маршруту: ассоциация — электронная изомеризация — диссоциация, в котором активными частицами являются радикалы, ионы, координационно-ненасыщенные соединения. Скорость химической реакции определяется концентрацией активных частиц и разницей между энергиями связи разрываемой и образуемой.
Содержание
Классификация
Существует большое количество признаков, по которым можно классифицировать химические реакции.
По фазовому составу реагирующей системы
По изменению степеней окисления реагентов
В данном случае различают
Пример окислительно-восстановительной реакции — горение водорода (восстановитель) в кислороде (окислитель) с образованием воды:
Пример реакции диспропорционирования — реакция разложения нитрата аммония при нагревании. Окислителем в данном случае выступает азот (+5) нитрогруппы, а восстановителем — азот (-3) катиона аммония:
По тепловому эффекту реакции
Все реакции сопровождаются тепловыми эффектами. При разрыве химических связей в реагентах выделяется энергия, которая, в основном, идет на образование новых химических связей. В некоторых реакциях энергии этих процессов близки, и в таком случае общий тепловой эффект реакции приближается к нулю. В остальных случаях можно выделить:
Тепловой эффект реакции (энтальпию реакции, ΔrH), часто имеющий очень важное значение, можно вычислить по закону Гесса, если известны энтальпии образования реагентов и продуктов. Когда сумма энтальпий продуктов меньше суммы энтальпий реагентов (ΔrH 0) — поглощение.
По типу превращений реагирующих частиц
Химические реакции всегда сопровождаются физическими эффектами: поглощением и выделением энергии, например в виде теплопередачи, изменением агрегатного состояния реагентов, изменением окраски реакционной смеси и др. Именно по этим физическим эффектам часто судят о протекании химических реакций.
Химические процессы, протекающие в веществе, отличаются и от физических процессов, и от ядерных превращений. В физических процессах каждое из участвующих веществ сохраняет неизменным свой состав (хотя вещества могут образовывать смеси), но могут изменять внешнюю форму или агрегатное состояние.
В химических процессах (химических реакциях) получаются новые вещества с отличными от реагентов свойствами, но никогда не образуются атомы новых элементов. В атомах же участвующих в реакции элементов обязательно происходят видоизменения электронной оболочки.
В ядерных реакциях происходят изменения в атомных ядрах всех участвующих элементов, что приводит к образованию атомов новых элементов.
С помощью химических реакций можно получать практически важные вещества, которые в природе находятся в ограниченных количествах, например азотные удобрения, либо вообще не встречаются по каким-либо причинам, например сульфаниламиды и другие синтетические лекарственные препараты, полиэтилен и другие пластмассы. Химия позволяет синтезировать новые, неизвестные природе вещества, необходимые для жизнедеятельности человека. Вместе с тем, неумелое или безответственное химическое воздействие на окружающую среду и на протекающие природные процессы может привести к нарушению установившихся естественных химических циклов, что делает актуальной экологическую проблему (загрязнение окружающей среды) и усложняет задачу рационального использования природных ресурсов и сохранения естественной среды обитания на Земле.
Химическая реакция
Из Википедии — свободной энциклопедии
Хими́ческая реа́кция — превращение одного или нескольких исходных веществ (реагентов) в другие вещества, при котором ядра атомов не меняются, при этом происходит перераспределение электронов и ядер, и образуются новые химические вещества. В отличие от ядерных реакций, при химических реакциях не изменяется общее число ядер атомов и изотопный состав химических элементов.
Химические реакции происходят при смешении или физическом контакте реагентов самопроизвольно, при нагревании, участии катализаторов (катализ), действии света (фотохимические реакции), электрического тока (электродные процессы), ионизирующих излучений (радиационно-химические реакции), механического воздействия (механохимические реакции), в низкотемпературной плазме (плазмохимические реакции) и т. п. Взаимодействие молекул между собой происходит по цепному маршруту: ассоциация — электронная изомеризация — диссоциация, в котором активными частицами являются радикалы, ионы, координационно-ненасыщенные соединения. Скорость химической реакции определяется концентрацией активных частиц и разницей между энергиями связи разрываемой и образуемой.
Химические процессы, протекающие в веществе, отличаются и от физических процессов, и от ядерных превращений. В физических процессах каждое из участвующих веществ сохраняет неизменным свой состав (хотя вещества могут образовывать смеси), но могут изменять внешнюю форму или агрегатное состояние.
В химических процессах (химических реакциях) получаются новые вещества с отличными от реагентов свойствами, но никогда не образуются атомы новых элементов, так как ядра остаются прежними, а все изменения происходят в электронной оболочке.
В ядерных реакциях происходят изменения в атомных ядрах всех участвующих элементов, что приводит к образованию атомов новых элементов.
ХИМИЧЕСКАЯ РЕАКЦИЯ
Смотреть что такое «ХИМИЧЕСКАЯ РЕАКЦИЯ» в других словарях:
химическая реакция — — [http://www.eionet.europa.eu/gemet/alphabetic?langcode=en] EN chemical reaction A change in which a substance is transformed into one or more new substances. (Source: MGH) [http://www.eionet.europa.eu/gemet/alphabetic?langcode=en]… … Справочник технического переводчика
химическая реакция — cheminė reakcija statusas T sritis chemija apibrėžtis Vienų medžiagų virtimas kitomis. atitikmenys: angl. chemical reaction; reaction rus. реакция; химическая реакция ryšiai: sinonimas – reakcija … Chemijos terminų aiškinamasis žodynas
химическая реакция — cheminė reakcija statusas T sritis fizika atitikmenys: angl. chemical reaction vok. chemische Reaktion, f rus. химическая реакция, f pranc. réaction chimique, f … Fizikos terminų žodynas
Химическая реакция — Химическая реакция превращение одного или нескольких исходных веществ (реагентов) в отличающиеся от них по химическому составу или строению вещества (продукты реакции). В отличие от ядерных реакций, при химических реакциях ядра атомов не… … Википедия
химическая реакция — ▲ взаимодействие ↑ химический реакция взаимодействие атомов, сопровождающееся качественной перестройкой их электронных оболочек; превращение одних веществ в другие; процесс, связанный с изменением состава молекул. химическое явление. реагент.… … Идеографический словарь русского языка
ХИМИЧЕСКАЯ РЕАКЦИЯ — превращение одних в в в другие, отличающиеся от исходных по составу и св вам. При X. р. молекулы одного соединения обмениваются атомами с молекулами др. соединений (напр., BaCl2 + H2SO4 = BaSO4 + 2НС1), разлагаются на молекулы с меньшим числом… … Большой энциклопедический политехнический словарь
радиационно-химическая реакция — Химическая реакция, инициированная радиационным воздействием на полимерный материал. Примечание Частный случай цепная радиационно химическая реакция. [ГОСТ 25645.321 87] Тематики полимерные и др. материалы EN radiation chemical reaction … Справочник технического переводчика
восстановление (химическая реакция) — — [http://www.dunwoodypress.com/148/PDF/Biotech Eng Rus.pdf] Тематики биотехнологии EN reduction … Справочник технического переводчика
Реакция (действие) — Реакция (лат. re… против + лат. actio действие) действие, возникающие в ответ на какое либо воздействие. Содержание 1 В химии и физике 2 В биологии и медицине 3 В э … Википедия
Урок 13. Типы химических реакций
В уроке 13 «Типы химических реакций» из курса «Химия для чайников» мы узнаем о типах химических реакций; подробно рассмотрим каждый тип и научимся их различать.
Мир химических реакций весьма разнообразен. Самые различные химические реакции постоянно происходят в природе, осуществляются человеком. Можно ли классифицировать химические реакции? Что положить в основу их классификации? Сущность всякой химической реакции состоит в превращении веществ: разрушаются исходные вещества и образуются продукты реакций, меняется число и состав исходных веществ и продуктов реакции. Характер этих изменений и положен в основу классификации химических реакций.
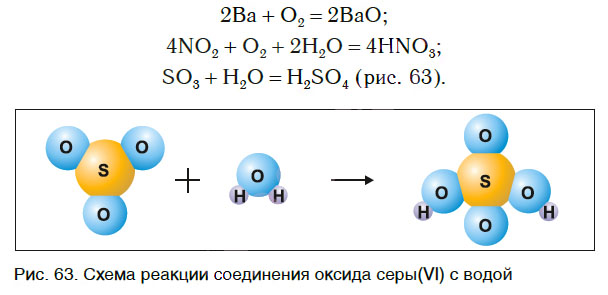
Реакции соединения
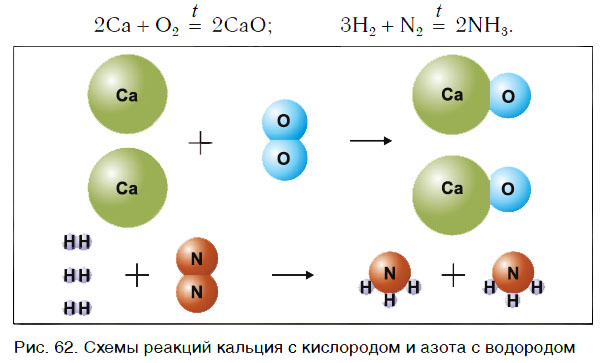
Рассмотрим уравнения следующих реакций (рис. 62):
Чем сходны данные реакции между собой? Тем, что в результате взаимодействия двух веществ получается только одно вещество. Такие реакции получили название реакций соединения.
Реакции соединения — это реакции, в результате которых из двух или нескольких веществ образуется одно новое сложное вещество.
В одних случаях из двух простых веществ получается одно сложное, в других — соединяются два и более простых или сложных веществ:
Реакции разложения
Рассмотрим уравнения следующих реакций:
Можно заметить, что из одного сложного вещества получается два или более новых веществ. Это реакции разложения. В них могут образовываться как простые, так и сложные вещества.
Реакции разложения — это реакции, в результате которых из одного сложного вещества образуется несколько новых веществ.
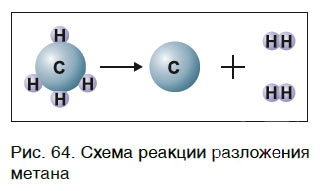
Для начала реакции разложения обычно необходимо нагреть исходные вещества. Например, негашеную известь CaO в промышленности получают нагреванием известняка CaCO3, реакция разложения происходит при температуре около 1000 °С. К такому типу реакций относится и реакция разложения метана CH4 (рис. 64) — составной части природного газа:
Реакции замещения
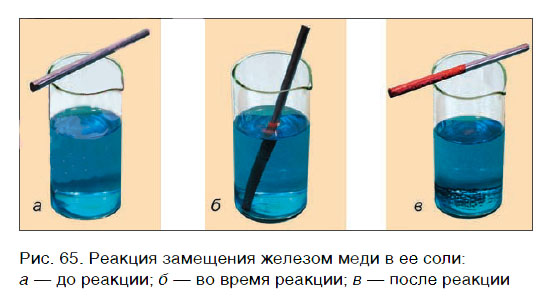
А могут ли взаимодействовать между собой два вещества: одно простое и одно сложное? Проверим это на опыте. В раствор медного купороса опустим небольшой кусочек железа — кнопку, гвоздь, канцелярскую скрепку с хорошо очищенной поверхностью. Через 2—3 мин извлечем железо из раствора и увидим, что на его поверхности образовался темно-красный налет меди. В химическую реакцию вступили простое (Fe) и сложное (CuSO4) вещества, и образовались новое простое (Cu) и новое сложное (FeSO4) вещества:
Из опыта и уравнения химической реакции хорошо видно, что атомы железа заместили атомы меди в сложном веществе (рис. 65). Такие химические реакции относятся к реакциям замещения.
Реакции замещения — это реакции, в результате которых атомы простого вещества замещают атомы одного из элементов в сложном веществе.
Для протекания таких реакций необходимо соблюдать некоторые особые условия. Не все простые вещества обязательно должны взаимодействовать со сложными веществами. В дальнейшем при изучении химии вы познакомитесь с этими условиями, а также с другими типами химических реакций.
Краткие выводы урока:
Надеюсь урок 13 «Типы химических реакций» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Если вопросов нет, то переходите к следующему уроку.
Виды химических реакций
Во время химических реакций из одних веществ получаются другие (не путать с ядерными реакциями, в которых один химический элемент превращается в другой).
Любая химическая реакция описывается химическим уравнением:
Реагенты → Продукты реакции
Стрелка указывает направление протекания реакции.
Числа, расположенные перед компонентами химической реакции, называются коэффициентами реакции.
Существует несколько видов химических реакций. Самые распространенные:
Реакции соединения
В реакциях соединения хотя бы два элемента образуют один продукт:
Если же количество кислорода недостаточно, то образуется смертельно опасный угарный газ:
2C(т) + O2 (г) → 2CO(г)
Реакции разложения
Эти реакции являются, как бы, противоположными по сути, реакциям соединения. В результате реакции разложения вещество распадается на два (3, 4. ) более простых элемента (соединения):
Реакции одинарного замещения
В результате реакций одинарного замещения, более активный элемент замещает в соединении менее активный:
Цинк в растворе сульфата меди вытесняет менее активную медь, в результате чего образуется раствор сульфата цинка.
Степень активности металлов по возрастанию активности:
Ионное уравнение вышеприведенной реакции будет иметь вид:
Ионная связь CuSO4 при растворении в воде распадается на катион меди (заряд 2+ ) и анион сульфата (заряд 2- ). В результате реакции замещения образуется катион цинка ( который имеет такой же заряд, как и катион меди: 2- ). Обратите внимание, что анион сульфата присутствует в обеих частях уравнения, т.е., по всем правилам математики его можно сократить. В итоге получится ионно-молекулярное уравнение:
Реакции двойного замещения
В реакциях двойного замещения происходит замещение уже двух электронов. Такие реакции еще называют реакциями обмена. Такие реакции проходят в растворе с образованием:
Реакции осаждения
При смешивании раствора нитрата серебра (соль) с раствором хлорида натрия образуется хлорид серебра:
Если соединение растворимое, оно будет находиться в растворе в ионном виде. Если соединение нерастворимое, оно будет осаждаться, образовывая твердое вещество.
Реакции нейтрализации
Это реакции взаимодействия кислот и оснований, в результате которых образуются молекулы воды.
Например, реакция смешивания раствора серной кислоты и раствора гидроксида натрия (щелока):
Реакции окисления
Метан относится к углеводородам (соединения из углерода и водорода). При реакции углеводорода с кислородом выделяется много тепловой энергии.
Окислительно-восстановительные реакции
Это реакции при которых происходит обмен электронами между атомами реагентов. Рассмотренные выше реакции, также являются окислительно-восстановительными реакциями:
Максимально подробно окислительно-восстановительные реакции с большим количеством примеров решения уравнений методом электронного баланса и методом полуреакций описаны в разделе Окислительно-восстановительные реакции для «чайников».
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе