Что называют энергетическим подуровнем
Энергетические подуровни
| Орбитальное квантовое число l | Форма электронного облака в подуровне | Изменение энергии электронов в пределах уровня | |
| буквенные обозначения | цифровые значения | ||
| s | сферическая |  | энергия электрона возрастает |
| p | гантелеобразная |  | |
| d | 4-х лепестковая розетка |  | |
| f | более сложная форма |
Согласно пределам изменений орбитального квантового числа от 0 до (n-1), в каждом энергетическом уровне возможно строго ограниченное число подуровней, а именно: число подуровней равно номеру уровня:
| n | l | Обозначение подуровней | Число подуровней |
| 1s | один | ||
| 0, 1 | 2s, 2p | два | |
| 0, 1, 2 | 3s, 3p, 3d | три | |
| 0, 1, 2, 3 | 4s, 4p, 4d, 4f | четыре |
Сочетание главного (n) и орбитального (l) квантовых чисел полностью характеризует энергию электрона. Запас энергии электрона отражается суммой (n+l).
Так, например, электроны 3d-подуровня обладают более высокой энергией, чем электроны 4s-подуровня:
Порядок заполнения уровней и подуровней в атоме электронами определяется правилом В.М. Клечковского:заполнение электронных уровней атома происходит последовательно в порядке возрастания суммы (n+1).
В соответствии с этим определена реальная энергетическая шкала подуровней, по которой построены электронные оболочки всех атомов:
1s ï 2s2p ï 3s3p ï 4s3d4p ï 5s4d5p ï 6s4f5d6p ï 7s5f6d…
3. Магнитное квантовое число (ml )характеризует направление электронного облака (орбитали) в пространстве.
Чем сложнее форма электронного облака (т.е. чем выше значение l), тем больше вариаций в ориентации данного облака в пространстве и тем больше существует отдельных энергетических состояний электрона, характеризующихся определенным значением магнитного квантового числа.
Обозначим каждую отдельную атомную орбиталь в пространстве как энергетическую ячейку ð, тогда число таких ячеек в подуровнях составит:

4. Спиновое квантовое число ms характеризует собственное вращение электрона вокруг своей оси и принимает всего два значения: + 1 /2 и – 1 /2, в зависимости от направления вращения в ту или другую сторону. Согласно принципу Паули, в одной орбитали может расположиться не более 2 электронов с противоположно направленными (антипараллельными)
p- подуровень спинами: 
Такие электроны называютсяспаренными.Неспаренныйэлектрон схематически изображается одной стрелкой: 
Зная емкость одной орбитали (2 электрона) и число энергетических состояний в подуровне (ms), можно определить количество электронов в подуровнях:
| Подуровень | Число орбиталей | Число электронов в подуровне |
| S | ||
| P | ||
| D | ||
| F |
Эти цифры необходимо хорошо запомнить для правильного написания электронных формул атома.
Итак, четыре квантовых числа – n, l, ml, ms – полностью определяют состояние каждого электрона в атоме. Все электроны в атоме с одинаковым значением n составляют энергетический уровень, с одинаковыми значениями n и l – энергетический подуровень, с одинаковыми значениями n, l и ml – отдельную атомную орбиталь (квантовую ячейку). Электроны одной орбитали отличаются спинами.
Учитывая значения всех четырех квантовых чисел, определим максимальное количество электронов в энергетических уровнях (электронных слоях):
| Уровень | Подуровни | Количество электронов | |
| по подуровням | суммарное | ||
| K | n=1 | s | s 2 |
| L | n=2 | s, p | s 2 p 6 |
| M | n=3 | s, p, d | s 2 p 6 d 10 |
| N | n=4 | s, p, d, f | s 2 p 6 d 10 f 14 |
Большие количества электронов (18,32) содержатся только в глубоко лежащих электронных слоях атомов, внешний электронный слой может содержать от 1 (у водорода и щелочных металлов) до 8 электронов (инертные газы).
Важно помнить, что заполнение электронами электронных оболочек происходит по принципу наименьшей энергии: сначала заполняются подуровни с минимальным значением энергии, затем с более высокими значениями. Эта последовательность соответствует энергетической шкале подуровней В.М. Клечковского.
Электронную структуру атома отображают электронные формулы, в которых указываются энергетические уровни, подуровни и число электронов в подуровнях.
При составлении электронной формулы атома марганца 25Mn необходимо учесть последовательность возрастания энергии подуровней: 1s2s2p3s3p4s3d…
Окончательная электронная формула атома марганца (с учетом удаленности электронов от ядра) выглядит так:
1s 2  | 2s 2 2p 6  | 3s 2 3p 6 3d 5  | 4s 2  |
Электронная формула марганца полностью соответствует положению его в периодической системе: число электронных слоев (энергетических уровней) – 4 равно номеру периода; во внешнем слое 2 электрона, предпоследний слой не завершен, что характерно для металлов побочных подгрупп; общее количество подвижных, валентных электронов (3d 5 4s 2 ) – 7 равно номеру группы.
В зависимости от того, какой из энергетических подуровней в атоме –s-, p-, d- или f- застраивается в последнюю очередь, все химические элементы подразделяются на электронные семейства: s-элементы (H, He, щелочные металлы, металлы главной подгруппы 2-й группы периодической системы); p-элементы (элементы главных подгрупп 3, 4, 5, 6, 7, 8-й групп периодической системы); d-элементы (все металлы побочных подгрупп); f- элементы (лантаноиды и актиноиды).
Электронные структуры атомов являются глубоким теоретическим обоснованием структуры периодической системы, длина периодов (т.е. количество элементов в периодах) непосредственно вытекает из емкости электронных слоев и последовательности возрастания энергии подуровней:
| Емкость энергетических подуровней | 1s 2 | 2s 2 2p 6 | 3s 2 3p 6 | 4s 2 3d 10 4p 6 | 5s 2 4d 10 5p 6 | 6s 2 4f 14 5d 10 6p 6 | 7s 2 5f 14 6d 5 |
| Количество элементов в периодах | I период | II период | III период | IV период | V период | VI период | VII период незаконченный |
Каждый период начинается s-элементом со структурой внешнего слоя s 1 (щелочной металл) и заканчивается p-элементом со структурой внешнего слоя …s 2 p 6 (инертный газ). I-й период содержит только два s-элемента (H и He), II-й и III-й малые периоды содержат по два s-элемента и шесть p-элемента. В IV-м и V-м больших периодах между s- и p-элементами «вклиниваются» по 10 d-элементов – переходных металлов, выделенных в побочные подгруппы. В VI и VII периодах к аналогичной структуре добавляется еще по 14 f-элементов, по свойствам близких соответственно лантану и актинию и выделенных в виде подгрупп лантаноидов и актиноидов.
При изучении электронных структур атомов обратите внимание на их графическое изображение, например:
13Аl 1s 2 2s 2 2p 6 3s 2 3p 1













































применяют оба варианта изображения: а) и б):
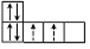
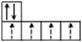
Для правильного расположения электронов на орбиталях необходимо знать правило Гунда: электроны в подуровне располагаются так, чтобы их суммарный спин был максимальным. Иными словами, электроны прежде по одному занимают все свободные ячейки данного подуровня.
Например, если необходимо разместить три p-электрона (p 3 ) в p-подуровне, который всегда имеет три орбитали, то из двух возможных вариантов правилу Гунда отвечает первый вариант:
| P 3 |  |  |
| +½+½+½= 3 /2 | +½-½+½=½ |
В качестве примера рассмотрим графическую электронную схему атома углерода:
6C·1s 2 2s 2 2p 2
Количество неспаренных электронов в атоме – очень важная характеристика. Согласно теории ковалентной связи, только неспаренные электроны могут образовывать химические связи и определяют валентные возможности атома.
Если в подуровне имеются свободные энергетические состояния (незанятые орбитали), атом при возбуждении «распаривает», разъединяет спаренные электроны, и его валентные возможности повышаются:
6C· 1s 2 2s 2 2p 3
Углерод в нормальном состоянии 2-х-валентен, в возбужденном – 4-х-валентен. Атом фтора не имеет возможностей для возбуждения (т.к. все орбитали внешнего электронного слоя заняты), поэтому фтор в своих соединениях одновалентен.
Пример 1. Что такое квантовые числа? Какие значения они могут принимать?

Каковы энергетические подуровни?
подуровни энергии в атоме они представляют собой форму, в которой электроны организованы в электронных слоях, их распределение в молекуле или атоме. Эти энергетические подуровни называются орбитали.
Электроны располагаются в электронных слоях атома определенным образом с помощью комбинации квантовых состояний. В тот момент, когда одно из этих состояний занято электроном, остальные электроны должны быть переведены в другое состояние..
введение
Орбитали обозначаются буквами s, p, d и f, то есть Sharp, Principle, Diffuse и Fundamental, и объединяются, когда атомы соединяются, образуя большую молекулу. Эти комбинации орбиталей находятся в каждом слое атома.
Например, в слое 1 атома есть S-орбитали, в слое 2 есть S и P-орбитали, внутри слоя 3 атома есть S, P и D-орбитали и, наконец, в слое 4 атома есть все S, P, D и F орбитали.
Также на орбиталях мы находим различные подуровни, которые в свою очередь могут хранить больше электронов. Орбитали на разных уровнях энергии похожи друг на друга, но занимают разные области в пространстве.
Первая орбита и вторая орбита имеют те же характеристики, что и орбита S, имеющие радиальные узлы, имеют большую вероятность сферического объема и могут содержать только два электрона. Тем не менее, они расположены на разных уровнях энергии и, следовательно, занимают разные места вокруг ядра.
Расположение в периодической таблице элементов
Таким образом, использование периодической таблицы для определения конфигурации электронов в атомах является ключевым. Элементы делятся на группы в соответствии с их электронными конфигурациями следующим образом:
Эта группа элементов имеет электрон, который обычно легко теряется, образуя положительно заряженный ион. Они самые активные металлы и самые реактивные.
Водород в данном случае является газом, но он входит в группу 1 Периодической таблицы элементов, поскольку у него также есть только один электрон. Водород может образовывать ионы с одним положительным зарядом, но для достижения его единственного электрона требуется гораздо больше энергии, чем для удаления электронов из других щелочных металлов. При образовании соединений водород обычно генерирует ковалентные связи.
Однако при очень высоких давлениях водород становится металлическим и ведет себя подобно остальным элементам своей группы. Это происходит, например, внутри ядра планеты Юпитер.
Группа 2 соответствует щелочноземельным металлам, так как их оксиды обладают щелочными свойствами. Среди элементов этой группы мы находим магний (Mg) и кальций (Ca). Их орбитали также принадлежат уровню S.
Переходные металлы, которые соответствуют группам от 3 до 12 в периодической таблице, имеют орбитали типа D.
Элементы таблицы, относящиеся к группе 13-18, соответствуют P. orbitals, и, наконец, элементы, известные как лантаноиды и актиниды, имеют орбитали с именем F.
Расположение электрона на орбитали
Электроны находятся на орбиталях атома как способ уменьшения энергии. Поэтому, если вы стремитесь увеличить энергию, электроны заполнят главные орбитальные уровни, удаляясь от ядра атома.
Мы должны учитывать, что электроны обладают свойством, известным как спин. Это квантовое понятие, которое определяет, среди прочего, спин электрона внутри орбитали. Что важно для определения вашей позиции на энергетических подуровнях.
Правила, определяющие положение электронов на орбиталях атома, следующие:
Это означает, что атомная орбита является энергетическим состоянием.
Электроны заполнят все орбитали на подуровнях, прежде чем столкнутся с противоположными спинами.
Специальные электронные конфигурации
Есть также атомы с особыми случаями энергетических подуровней. Когда два электрона занимают одну и ту же орбиту, они должны не только иметь разные спины (как указано в принципе исключения Паули), но и связь электронов немного увеличивает энергию.
В случае энергетических подуровней, наполовину полный и один полностью полный подуровни уменьшают энергию атома. Это приводит атом к большей стабильности.
Энергетические уровни и подуровни
Каждой орбитали отвечает определенная энергия. Обозначение орбитали включает номер энергетического уровня и букву, отвечающую соответствующему подуровню: 1s, 3p, 4d и т.п. Для каждого энергетического уровня, начиная со второго, возможно существование трех равных по энергии p-орбиталей, расположенных в трех взаимно перпендикулярных направлениях. На каждом энергетическом уровне, начиная с третьего, имеется пять d-орбиталей, имеющих более сложную четырехлепестковую форму. Начиная с четвертого энергетического уровня, появляются еще более сложные по форме f-орбитали; на каждом уровне их семь. Атомную орбиталь с распределенным по ней зарядом электрона нередко называют электронным облаком.
Вопрос 12.
Горизонтальная периодичность
Горизонтальная периодичность заключается в появлении максимальных и минимальных значений свойств простых веществ и соединений в пределах каждого периода. Она особенно заметна для элементов VIIIБ-группы и лантаноидов (например, лантаноиды с четными порядковыми номерами более распространены, чем с нечетными).
В таких физических свойствах, как энергия ионизации и сродство к электрону, также проявляется горизонтальная периодичность, связанная с периодическим изменением числа электронов на последних энергетических подуровнях:
| Элемент | Li | Be | B | C | N | O | F | Ne |
| Ei | ||||||||
| Ae | −60 | −27 | −122 | +7 | −141 | −328 | ||
| Электронная формула (валентные электроны) | 2s 1 | 2s 2 | 2s 2 2p 1 | 2s 2 2p 2 | 2s 2 2p 3 | 2s 2 2p 4 | 2s 2 2p 5 | 2s 2 2p 6 |
| Число неспаренных электронов |
Вопрос 13.
Вопрос 14.
Магнитные характеристики атома
Электрон обладает собственным магнитным моментом, который квантуется по направлению параллельно или противоположно приложенному магнитному полю. Если два электрона, занимающие одну орбиталь, имеют противоположно направленные спины (согласно принципу Паули), то они гасят друг друга. В этом случае говорят, что электроны спаренные. Атомы, имеющие только спаренные электроны, выталкиваются из магнитного поля. Такие атомы называются диамагнитными. Атомы, имеющие один или несколько неспаренных электронов, втягиваются в магнитное поле. Они называются диамагнитными.
Магнитный момент атома, характеризующий интенсивность взаимодействия атома с магнитным полем, практически пропорционален числу неспаренных электронов.
Особенности электронной структуры атомов различных элементов отражаются в таких энергетических характеристиках, как энергия ионизации и сродство к электрону.
Энергия ионизации
В изменении первых потенциалов ионизации, соответствующих удалению одного электрона, атомов явно выражена периодичность при увеличении порядкового номера атома:
Для одного и того же атома вторая, третья и последующие энергии ионизации всегда увеличиваются, так как электрон приходится отрывать от положительно заряженного иона. Например, для атома лития первая, вторая и третья энергии ионизации равны 520,3, 7298,1 и 11814,9 кДж/моль, соответственно.
Сродство к электрону
Наибольшим сродством к электрону обладают атомы галогенов. Например, для атома фтора присоединение электрона сопровождается выделением 327,9 кДж/моль энергии. Для ряда элементов сродство к электрону близко к нулю или отрицательно, что значит отсутствие устойчивого аниона для данного элемента.
Обычно сродство к электрону для атомов различных элементов уменьшается параллельно с ростом энергии их ионизации. Однако для некоторых пар элементов имеются исключения:
| Элемент | Ei, кДж/моль | Ae, кДж/моль |
| F | −238 | |
| Cl | −349 | |
| N | ||
| P | −71 | |
| O | −141 | |
| S | −200 |
Объяснение этому можно дать, основываясь на меньших размерах первых атомов и большем электрон-электронном отталкивании в них.
Вопрос 15.
Вопрос 16.
Горизонтальная периодичность заключается в появлении максимальных и минимальных значений свойств простых веществ и соединений в пределах каждого периода. Она особенно заметна для элементов VIIIБ-группы и лантаноидов (например, лантаноиды с четными порядковыми номерами более распространены, чем с нечетными).
В таких физических свойствах, как энергия ионизации и сродство к электрону, также проявляется горизонтальная периодичность, связанная с периодическим изменением числа электронов на последних энергетических подуровнях: