Что называется теплотой плавления
ТЕПЛОТА ПЛАВЛЕНИЯ
Полезное
Смотреть что такое «ТЕПЛОТА ПЛАВЛЕНИЯ» в других словарях:
теплота плавления — количество теплоты, которое необходимо сообщить твёрдому кристаллическому веществу при постоянном давлении, чтобы полностью перевести его в жидкое состояние. Теплота плавления единицы массы вещества называется удельной теплотой плавления. * * *… … Энциклопедический словарь
ТЕПЛОТА ПЛАВЛЕНИЯ — количество теплоты, которое необходимо cообщить твердому кристаллическому веществу при постоянном давлении, чтобы полностью перевести его в жидкое состояние. Теплоту плавления единицы массы вещества называют удельной теплотой плавления … Большой Энциклопедический словарь
теплота плавления — [fusion heat] количество теплоты, необходимое веществу в равновесном изобарно изотермическом процессе для перехода из твердого (кристаллического) состояния в жидкое (то же количество теплоты выделяется при кристаллизации вещества). Теплота… … Энциклопедический словарь по металлургии
ТЕПЛОТА ПЛАВЛЕНИЯ — – количество теплоты, которое необходимо сообщить веществу в равновесном процессе, чтобы перевести его из твердого (кристаллического) состояния, в жидкое (то же количество теплоты выделяется при кристаллизации вещества). Теплота плавления… … Металлургический словарь
теплота плавления — lydymosi šiluma statusas T sritis Standartizacija ir metrologija apibrėžtis Šilumos kiekis, reikalingas medžiagai išlydyti. atitikmenys: angl. fusion heat; melting heat vok. Schmelzwärme, f rus. теплота плавления, f pranc. chaleur de fusion, f … Penkiakalbis aiškinamasis metrologijos terminų žodynas
теплота плавления — lydymosi šiluma statusas T sritis chemija apibrėžtis Šilumos kiekis, reikalingas medžiagai išlydyti. atitikmenys: angl. fusion heat; melting heat rus. теплота плавления … Chemijos terminų aiškinamasis žodynas
теплота плавления — lydymosi šiluma statusas T sritis fizika atitikmenys: angl. fusion heat; melting heat vok. Schmelzwärme, f rus. теплота плавления, f pranc. chaleur de fusion, f … Fizikos terminų žodynas
теплота плавления — lydymosi šiluma statusas T sritis Energetika apibrėžtis Šiluma, reikalinga kietai kristalinei medžiagai paversti skysčiu, esant pastoviai lydymosi temperatūrai. Būna savitoji ir molinė lydymosi šiluma. Jų matavimo vienetai – džaulis kilogramui… … Aiškinamasis šiluminės ir branduolinės technikos terminų žodynas
Теплота плавления — количество теплоты, которое необходимо сообщить веществу в равновесном изобарно изотермическом процессе, чтобы перевести его из твёрдого (кристаллического) состояния в жидкое (то же количество теплоты выделяется при кристаллизации… … Большая советская энциклопедия
ТЕПЛОТА ПЛАВЛЕНИЯ — кол во теплоты, к рое необходимо сообщить тв. кристаллич. в ву при пост. давлении, чтобы полностью перевести его в жидкое состояние. Т. п. единицы массы в ва наз. удельной Т. п … Естествознание. Энциклопедический словарь
Молекулярная физика. Плавление и кристаллизация.
Переход вещества из твердого кристаллического состояния в жидкое называется плавлением. Чтобы расплавить твердое кристаллическое тело, его нужно нагреть до определенной температуры, т. е. подвести тепло. Температура, при которой вещество плавится, называется температурой плавления вещества.
Обратный процесс — переход из жидкого состояния в твердое — происходит при понижении температуры, т. е. тепло отводится. Переход вещества из жидкого состояния в твердое называется отвердеванием, или кристал лизацией. Температура, при которой вещество кристаллизуется, называется температурой кристалли зации.
Опыт показывает, что любое вещество кристаллизуется и плавится при одной и той же температуре.
На рисунке представлен график зависимости температуры кристаллического тела (льда) от времени нагревания (от точки А до точки D) и времени охлаждения (от точки D до точки K). На нем по горизонтальной оси отложено время, а по вертикальной — температура.
Вид рассмотренного графика объясняется следующим образом. На участке АВ благодаря подводимому теплу средняя кинетическая энергия молекул льда увеличивается, и температура его повышается. На участке ВС вся энергия, получаемая содержимым колбы, тратится на разрушение кристаллической решетки льда: упорядоченное пространственное расположение его молекул сменяется неупорядоченным, меняется расстояние между молекулами, т.е. происходит перестройка молекул таким образом, что вещество становится жидким. Средняя кинетическая энергия молекул при этом не меняется, поэтому неизменной остается и температура. Дальнейшее увеличение температуры расплавленного льда-воды (на участке CD) означает увеличение кинетической энергии молекул воды вследствие подводимого горелкой тепла.
При охлаждении воды (участок DE) часть энергии у нее отбирается, молекулы воды движутся с меньшими скоростями, их средняя кинетическая энергия падает — температура уменьшается, вода охлаждается. При 0°С (горизонтальный участок EF) молекулы начинают выстраиваться в определенном порядке, образуя кристаллическую решетку. Пока этот процесс не завершится, температура вещества не изменится, несмотря на отводимое тепло, а это означает, что при отвердевании жидкость (вода) выделяет энергию. Это как раз та энергия, которую поглотил лед, превращаясь в жидкость (участок ВС). Внутренняя энергия у жидкости больше, чем у твердого тела. При плавлении (и кристаллизации) внутренняя энергия тела меняется скачком.
Металлы, плавящиеся при температуре выше 1650 ºС, называют тугоплавкими (титан, хром, молибден и др.). Самая высокая температура плавления среди них у вольфрама — около 3400 °С. Тугоплавкие металлы и их соединения используют в качестве жаропрочных материалов в самолетостроении, ракетостроении и космической технике, атомной энергетике.
Подчеркнем еще раз, что при плавлении вещество поглощает энергию. При кристаллизации оно, наоборот, отдает ее в окружающую среду. Получая определенное количество теплоты, выделяющееся при кристаллизации, среда нагревается. Это хорошо известно многим птицам. Недаром их можно заметить зимой в морозную погоду сидящими на льду, который покрывает реки и озера. Из-за выделения энергии при образовании льда воздух над ним оказывается на несколько градусов теплее, чем в лесу на деревьях, и птицы этим пользуются.
Наличие определенной точки плавления — это важный признак кристаллических веществ. Именно по этому признаку их можно легко отличить от аморфных тел, которые также относят к твердым телам. К ним, в частности, относятся стекла, очень вязкие смолы, пластмассы.
Аморфные вещества (в отличие от кристаллических) не имеют определенной температуры плавления — они не плавятся, а размягчаются. При нагревании кусок стекла, например, сначала становится из твердого мягким, его легко можно гнуть или растягивать; при более высокой температуре кусок начинает менять свою форму под действием собственной тяжести. По мере нагревания густая вязкая масса принимает форму того сосуда, в котором лежит. Эта масса сначала густая, как мед, затем — как сметана и, наконец, становится почти такой же маловязкой жидкостью, как вода. Однако указать определенную температуру перехода твердого тела в жидкое здесь невозможно, поскольку ее нет.
Причины этого лежат в коренном отличии строения аморфных тел от строения кристаллических. Атомы в аморфных телах расположены беспорядочно. Аморфные тела по своему строению напоминают жидкости. Уже в твердом стекле атомы расположены беспорядочно. Значит, повышение температуры стекла лишь увеличивает размах колебаний его молекул, дает им постепенно все большую и большую свободу перемещения. Поэтому стекло размягчается постепенно и не обнаруживает резкого перехода «твердое—жидкое», характерного для перехода от расположения молекул в строгом порядке к беспорядочному.
Теплота плавления — это количество теплоты, которое необходимо сообщить веществу при постоянном давлении и постоянной температуре, равной температуре плавления, чтобы полностью перевести его из твердого кристаллического состояния в жидкое. Теплота плавления равна тому количеству теплоты, которое выделяется при кристаллизации вещества из жидкого состояния. При плавлении вся подводимая к веществу теплота идет на увеличение потенциальной энергии его молекул. Кинетическая энергия не меняется, поскольку плавление идет при постоянной температуре.
Изучая на опыте плавление различных веществ одной и той же массы, можно заметить, что для превращения их в жидкость требуется разное количество теплоты. Например, для того чтобы расплавить один килограмм льда, нужно затратить 332 Дж энергии, а для того чтобы расплавить 1 кг свинца — 25 кДж.
Физическая величина, показывающая, какое количество теплоты необходимо сообщить кристаллическому телу массой 1 кг, чтобы при температуре плавления полностью перевести его в жидкое состояние, называется удельной теплотой плавления.
Удельную теплоту плавления измеряют в джоулях на килограмм (Дж/кг) и обозначают греческой буквой λ (лямбда).
Удельная теплота кристаллизации равна удельной теплоте плавления, поскольку при кристаллизации выделяется такое же количество теплоты, какое поглощается при плавлении. Так, например, при замерзании воды массой 1 кг выделяются те же 332 Дж энергии, которые нужны для превращения такой же массы льда в воду.
Чтобы найти количество теплоты, необходимое для плавления кристаллического тела произвольной массы, или теплоту плавления, надо удельную теплоту плавления этого тела умножить на его массу:
Количество теплоты, выделяемое телом, считается отрицательным. Поэтому при расчете количества теплоты, выделяющегося при кристаллизации вещества массой m, следует пользоваться той же формулой, но со знаком «минус»:
Теплота сгорания (или теплотворная способность, калорийность) — это количество теплоты, выделяющейся при полном сгорании топлива.
Для нагревания тел часто используют энергию, выделяющуюся при сгорании топлива. Обычное топливо (уголь, нефть, бензин) содержит углерод. При горении атомы углерода соединяются с атомами кислорода, содержащегося в воздухе, в результате чего образуются молекулы углекислого газа. Кинетическая энергия этих молекул оказывается большей, чем у исходных частиц. Увеличение кинетической энергии молекул в процессе горения называют выделением энергии. Энергия, выделяющаяся при полном сгорании топлива, и есть теплота сгорания этого топлива.
Теплота сгорания топлива зависит от вида топлива и его массы. Чем больше масса топлива, тем больше количество теплоты, выделяющейся при его полном сгорании.
Физическая величина, показывающая, какое количество теплоты выделяется при полном сгорании топлива массой 1 кг, называется удельной теплотой сгорания топлива. Удельную теплоту сгорания обозначают буквой q и измеряют в джоулях на килограмм (Дж/кг).
Количество теплоты Q, выделяющееся при сгорании m кг топлива, определяют по формуле:
Чтобы найти количество теплоты, выделяющееся при полном сгорании топлива произвольной массы, нужно удельную теплоту сгорания этого топлива умножить на его массу.
Что такое удельная теплота плавления
Возьмем предварительно нагретое до температуры плавления вещество массой 1 кг. Будем сообщать ему тепловую энергию, чтобы расплавить это вещество.
Та энергия, которую мы затратим, чтобы расплавить 1 кг вещества, называется удельной теплотой плавления.
Эту теплоту называют удельной величиной, так как она приходится на 1 кг вещества.
Удельная теплота плавления — это энергия, которую мы затратим, чтобы расплавить 1 кг вещества, если это вещество предварительно было нагрето до температуры плавления.
Эту величину обозначают маленькой греческой буквой \(\large \lambda\) — лямбда.
\(\large \lambda \left( \frac<\text<Дж>><\text<кг>>\right)\) – удельная теплота плавления.
Примечания:
Перед тем, как расплавить вещество, нужно нагреть его до температуры плавления.
Процессы плавления и кристаллизации
Будем рассматривать такие процессы, как плавление и кристаллизация (затвердевание):
Благодаря процессам кристаллизации зимой замерзает вода, образуется лед и можно кататься на коньках.
Весной, лед сначала нагреется от минусовой температуры до температуры плавления 0 градусов Цельсия, когда получит количество теплоты (тепловую энергию) от нагревающего его солнца. А затем, будет таять – то есть, плавиться, получая от солнца дополнительную тепловую энергию (теплоту). Покуда весь лед не расплавится, его температура подниматься не будет. Но как только весь лед превратится в воду, ее температура при нагревании начнет повышаться.
Чем отличается удельная теплота плавления от количества теплоты
Запомнить, чем удельная теплота плавления отличается от количества теплоты, можно так (рис. 1):
Количество теплоты – это энергия плавления нескольких килограммов вещества, предварительно нагретого до температуры плавления.
Удельная теплота плавления – это энергия плавления 1-го килограмма вещества, предварительно нагретого до температуры плавления.
Как связаны количество теплоты и удельная теплота плавления — формула
Если вещество предварительно нагрето до температуры плавления, и
то легко посчитать общую тепловую энергию – т. е. количество теплоты.
Для этого используем формулу:
\(\large Q \left( \text <Дж>\right) \) – количество теплоты, т. е. общая тепловая энергия;
\(\large \lambda \left( \frac<\text<Дж>><\text<кг>> \right) \) – удельная теплота плавления (кристаллизации);
\(\large m \left( \text <кг>\right) \) – масса вещества;
Примечание: Если умножить удельную теплоту плавления \(\large \lambda \) на количество килограммов m расплавленного вещества, то можно вычислить общее количество теплоты \(\large Q \), затраченной на плавление.
Фазовые переходы и уравнение теплового баланса
теория по физике 🧲 термодинамика
Фазовые переходы — это термодинамические процессы, приводящие к изменению агрегатного состояния вещества.
Плавление и отвердевание
Для расчета количества теплоты, необходимого для процесса плавления, следует применять формулу:
m — масса вещества, λ (Дж/кг) — удельная теплота плавления.
Плавление каждого вещества происходит при определенной температуре, которую называют температурой плавления. Все проводимое тепло идет на разрушение кристаллической решетки, при этом увеличивается потенциальная энергия молекул. Кинетическая энергия остается без изменения и температура в процессе плавления не изменяется.
Удельная теплота плавления показывает, какое количество теплоты необходимо сообщить 1 кг данного вещества, чтобы перевести его из твердого состояния в жидкое при условии, что оно уже нагрето до температуры плавления. В процессе отвердевания 1 кг данной жидкости, охлажденной до температуры отвердевания, выделится такое же количество теплоты.
Внимание! Удельная теплота плавления — табличная величина.
Определение Отвердевание, или кристаллизация — переход состояния из жидкого состояния в твердое (это процесс, обратный плавлению).
Отвердевание происходит при той же температуре, что и плавление. В процессе отвердевания температура также не изменяется. Количество теплоты, выделяемое в процессе отвердевания:
Парообразование и конденсация
Количество теплоты, необходимое для процесса кипения, вычисляют по формуле:
m — масса вещества, r (Дж/кг) — удельная теплота парообразования.
Парообразование происходит при определенной температуре, которую называют температурой кипения. В отличие от испарения, процесс парообразования идет со всего объема жидкости. Несмотря на то, что к кипящему веществу подводят тепло, температура не изменяется. Все затраты энергии идут на увеличение промежутком между молекулами. Температура кипения зависит от рода вещества и внешнего атмосферного давления.
Удельная теплота парообразования показывает, какое количество теплоты необходимо затратить, чтобы перевести в пар 1 кг жидкости, нагретой до температуры кипения. Такое же количество теплоты выделится в процессе конденсации 1 кг пара, охлажденного до температуры конденсации.
Внимание! Удельная теплота парообразования — табличная величина.
Определение Конденсация — процесс, обратный кипению. Это переход вещества из газообразного состояния в жидкое.
Конденсация происходит при температуре кипения, которая также не изменяется во время всего процесса. Количество теплоты, выделяемое в процессе конденсации:
Тепловые процессы при нагревании и охлаждении
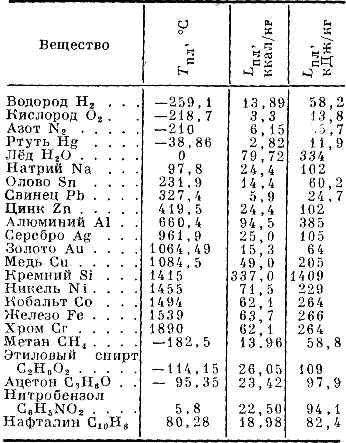
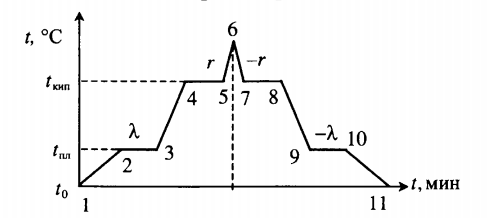
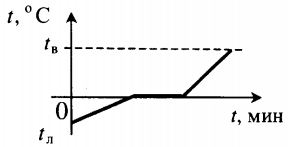
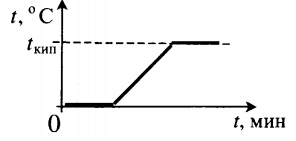
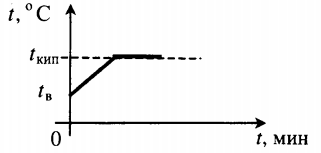
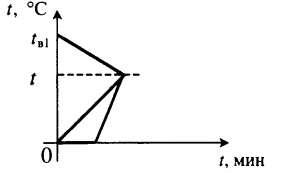
Все фазовые переходы, а также процессы нагревания и остывания вещества можно отобразить графически. Посмотрите на график фазовых переходов вещества:
Он показывает зависимость температуры вещества от времени в процессе его нагревания и остывания. Опишем процессы, отображаемые на графике, в таблице.


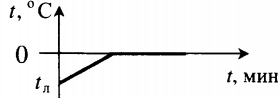
 Уравнение теплового баланса:
Уравнение теплового баланса: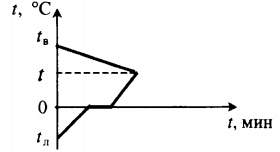 Уравнение теплового баланса:
Уравнение теплового баланса: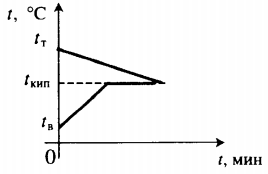 Уравнение теплового баланса:
Уравнение теплового баланса: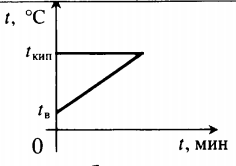 Уравнение теплового баланса:
Уравнение теплового баланса: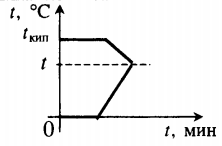 Уравнение теплового баланса:
Уравнение теплового баланса: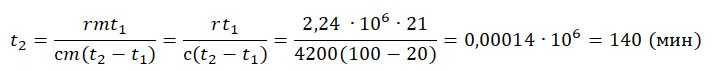
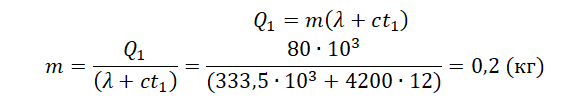
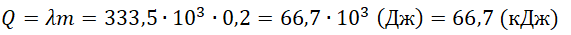
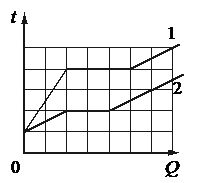 На рисунке представлены графики зависимости температуры t двух тел одинаковой массы от сообщённого им количества теплоты Q. Первоначально тела находились в твёрдом агрегатном состоянии.
На рисунке представлены графики зависимости температуры t двух тел одинаковой массы от сообщённого им количества теплоты Q. Первоначально тела находились в твёрдом агрегатном состоянии.