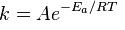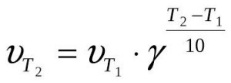Что называется скоростью химической реакции в каких единицах она измеряется
Скорость химической реакции
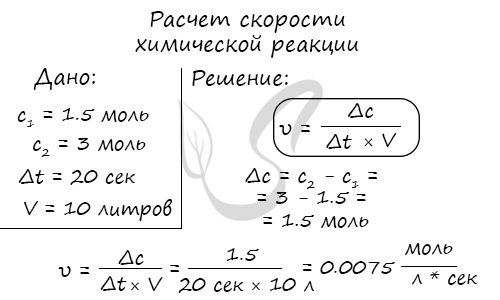
Скорость реакции отражает изменение концентраций реагирующих веществ за единицу времени. Единицы измерения для гомогенной реакции: моль/л * сек. Физический смысл в том, что каждую секунду какое-то количество одного вещества превращается в другое в единице объема.
Мне встречались задачи, где была дана молярная концентрация вещества до реакции и после, время и объем. Требовалось посчитать скорость реакции. Давайте решим подобное несложное задание для примера:
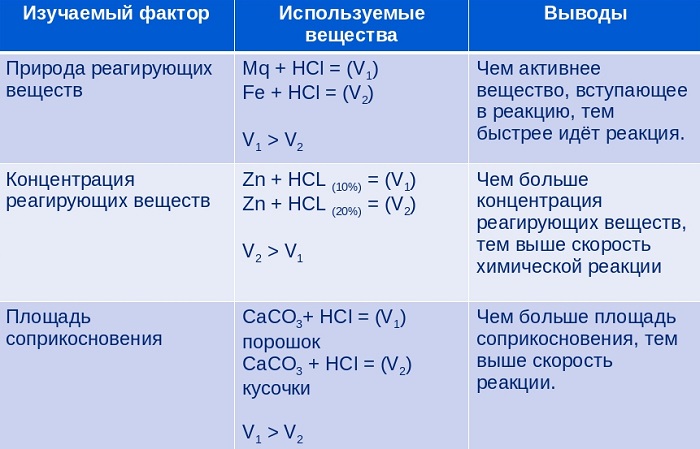
Влияние природы реагирующих веществ
При изучении агрегатных состояний веществ возникает вопрос: где же быстрее всего идут реакции: между газами, растворами или твердыми веществами?
Запомните, что самая высокая скорость реакции между растворами, в жидкостях. В газах она несколько ниже.
Если реакция гетерогенная: жидкость + твердое вещество, газ + твердое вещество, жидкость + газ, то большую роль играет площадь соприкосновения реагирующих веществ.
Химическая активность также играет важную роль. Например, отвечая на вопрос: какой из металлов Li или K быстрее прореагирует с водой? Мы отдадим предпочтение литию, так как в ряду активности металлов он стоит левее калия, а значит литий активнее калия.
Иногда для верного ответа на вопрос о скорости реакции требуется знание активности кислот. Мы подробнее обсудим эту тему в гидролизе, однако сейчас я замечу: чем сильнее (активнее) кислота, тем быстрее идет реакция.
Например, реакцию магния с серной кислотой протекает гораздо быстрее реакции магния с уксусной кислотой. Причиной этому служит то, что серная кислота относится к сильным (активным) кислотам, а активность уксусной кислоты меньше, она является слабой кислотой.
Как я уже упомянул, слабые и сильные кислоты и основания изучаются в теме гидролиз.
Влияние изменения концентрации
Замечу деталь, которая может оказаться важной, если в реакции участвуют газы: при увеличении давления концентрация вещества на единицу объема возрастает (представьте, как газ сжимается). Поэтому увеличение давление, если среди исходных веществ есть газ, увеличивает скорость реакции.
Закон действующих масс устанавливает соотношение между концентрациями реагирующих веществ и их продуктами. Скорость простой реакции aA + bB → cC определяют по уравнению:
Записанное выше следствие закона действующих масс нужно не только «зазубрить», но и понять. Поэтому мы решим пару задач, где потребуется написать подобную формулу.
Окисление диоксида серы протекает по уравнению: 2SO2(г) + O2 = 2SO3(г). Как изменится скорость этой реакции, если объемы системы уменьшить в три раза?
По итогу решения становится ясно, что скорость реакции в таком случае возрастет в 27 раз.
Решим еще одну задачу. Дана реакция синтеза аммиака: N2 + ЗН2 = 2NH3. Как изменится скорость прямой реакции образования аммиака, если уменьшить концентрацию водорода в два раза?
В результате решения мы видим, что при уменьшении концентрации водорода в два раза скорость реакции замедлится в 8 раз.
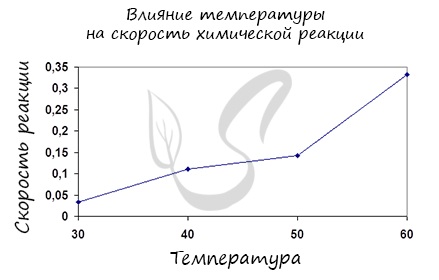
Влияние изменения температуры на скорость реакции
Постулат, который рекомендую временно взять на вооружение: «Увеличение температуры увеличивает скорость абсолютно любой химической реакции: как экзотермической, так и эндотермической. Исключений нет!»
Правило Вант-Гоффа, голландского химика, позволяет точно оценить влияние температуры на скорость химической реакции. Оно звучит так: «При повышении температуры на каждые 10 градусов константа скорости гомогенной элементарной реакции увеличивается в два — четыре раза»
Если по итогам решения задач у вас получится температурный коэффициент меньше 2 или больше 4, то, скорее всего, где-то вы допустили ошибку. Используйте этот факт для самопроверки.
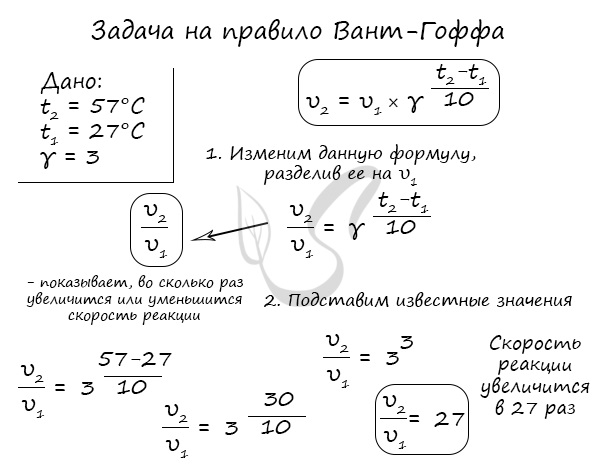
Для тренировки решим пару задач, в которых потребуется использование правило Вант-Гоффа.
Как изменится скорость гомогенной реакции при повышении температуры от 27°C до 57°C при температурном коэффициенте, равном трем?
Иногда в задачах требуется рассчитать температурный коэффициент, как, например, здесь: «Рассчитайте, чему равен температурный коэффициент скорости, если известно, что при понижении температуры от 250°C до 220°C скорость реакции уменьшилась в 8 раз».
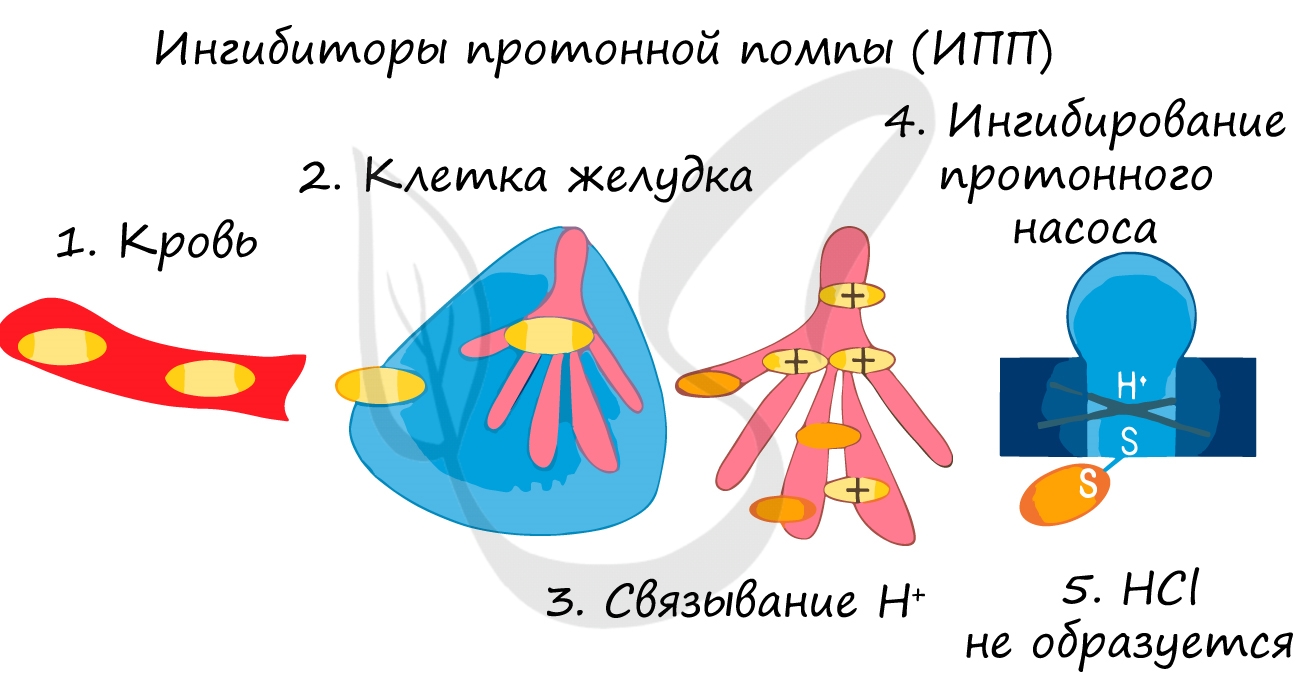
Катализаторы и ингибиторы
Ингибиторы применяют для замедления коррозии металла, окисления топлива, старения полимеров. Многие лекарственные вещества являются ингибиторами.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Блиц-опрос по теме Скорость химической реакции
Что называют скоростью химической реакции.
Вопросы:
1. Что называют скоростью химической реакции? В каких единицах ее измеряют? От каких факторов она зависит?
2. Перечислите факторы, от которых зависит скорость химической реакции. Приведите примеры, иллюстрирующие ответ.
3. Сравните понятия «скорость движения» и «скорость химической реакции». Что между ними Общего?
5. Как классифицируют реакции по участию в них катализаторов? Приведите примеры таких реакций, запишите их уравнения.
6. Что такое катализаторы? На какие группы их можно разделить? Где наиболее эффективно можно использовать ингибиторы?
7. Что такое ферменты? Сравните их с неорганическими катализаторами. Назовите области применения ферментов.
8. Почему при обработке порезов и других ран пероксидом водорода наблюдается его бурное «вскипание»?
9. Сухой хлор хранят в железных баллонах. Влажный хлор разрушает железо. Какую роль играет вода в этом процессе?
10. Сформулируйте закон Вант-Гоффа.
11. Для реакции были взяты вещества при температуре 40 °С. Затем их нагрели до температуры 70 °С. Как изменится скорость химической реакции, если температурный коэффициент ее равен 2?
12. Почему продукты питания хранят в холодильниках?
Скорость химической реакции — определение довольно древнее, но по-прежнему актуальное, так как является базовым понятием в химической науке и её прикладном значении. Сама возможность влияния человека на скорость и объем химического процесса позволила в свое время сделать резкий прорыв в этой и многих других областях, потому что больше не приходилось дожидаться результата так же долго, сколько он занимает в естественной природной среде.
Соответственно, наличие катализаторов позволяет ученым и сейчас ускорять прогресс науки, достигать поставленных задач. Такой раздел знаний изучает химическая кинетика — наука, определяющая закономерности влияния физических и химических условий на протекание химических реакций.
Скорость химической реакции — изменение количества одного из реагентов за промежуток времени в реакционном пространстве. Эта скорость является фундаментальным понятием химической кинетики. Она измеряется путём изменения концентрации одного из веществ. Как правило, рассчитывается в молях (классическая единица измерения) на литр за единицу времени.
Стоит сказать, что абсолютно все химические реакции рассматриваются только в системе, т. е. в совокупности отдельно взятых веществ и объектов.
Скорость реакции в гомогенной системе
В химии различают гомогенные (одинаковые фазы внешней среды) и гетерогенные (различающиеся фазы окружающей среды) реакции в зависимости от фаз среды.
Реакции в гомогенной системе происходят только в однородной фазе в общем объеме реакционной системы. Реакция происходит исключительно при взаимодействии растворов жидкостей или газов.
Скорость химической реакции в гомогенной системе — это изменение концентрации одного из веществ, участвующих в химической реакции, за единицу времени.
Ниже приведены примеры таких реакций и нужная формула:
NaOH(р-р) + HCl(р-р) = NaCl(р-р) + H2O.
Скорость реакции в гетерогенной системе
В гетерогенных же системах химические реакции протекают только на поверхности раздела разных фаз.
Поверхность раздела фаз — это граничная поверхность между двумя веществами, вступающими в реакцию, в контакт между собой.
Например, при взаимодействии железа с соляной кислотой: Fe + 2HCl → FeCl2 + H2.
Факторы, влияющие на скорость химической реакции
Как ранее было сказано, скорость химической реакции зависит от нескольких параметров:
соотношения концентраций реагентов;
природы взятых реагентов;
площади соприкосновения реагентов;
давления (применимо, если в случае реагентов взяты газообразные вещества).
Температура
Правилом Вант-Гоффа и уравнением Аррениуса определяется скорость взаимодействия реагентов. Сванте Аррениус искал взаимосвязь скорости и температуры. Он установил, что химические процессы поддаются равенству константы скорости:
Еа — min энергия для запуска реакции;
A — постоянная, указывающая на вероятность возможного взаимодействия молекул.
Удобно пользоваться и правилом Якоба Вант-Гоффа, смысл которого гласит, что увеличивается v реакции от двух до четырех раз при росте температуры на десять градусов (по Цельсию). Для простоты расчётов было создано уравнение:
Соотношение концентраций реагентов
Обусловленность скорости от концентрации реагентов в системе известна в науке, как закон действующих масс. Его открыли Като Гульдберг и Петер Вааге.
Скорость этих реакций выражается уравнением:
v — скорость взаимодействия веществ;
cA и cB — концентрации реагентов;
k —коэффициент скорости.
Катализаторы
Самым распространённым способом изменить скорость реакции является добавление к ней катализатора (ускорителя) или ингибитора (замедлителя).
Основное преимущество таких веществ в том, что они не являются расходным материалом и не влияют на равновесие в продуктах внутри системы.
Для простоты возьмем реакцию разложения пероксида водорода: 2Н2О2 = 2Н2О + О2.
Без дополнительных веществ эта простая реакция протекает довольно медленно, но если добавить оксид марганца (MnO2), то сразу заметим наличие газа (O2).
Природа веществ
Скорость реакции также зависит от природы взятых веществ. Здесь тоже не все так просто, ведь имеет вес почти каждая мелочь этого вещества: характер и прочность кристаллической решетки и химических связей, строение оболочки атомов и расположения на ней электронов (согласно периодическому закону Д. И. Менделеева о порядке веществ в таблице).
Для простоты объяснения приведем пример: согласно строению веществ, натрий (Na) гораздо легче отдает свои электроны, чем олово (Sn), соответственно, реагировать с одним и тем же веществом он будет быстрее.
Площадь соприкосновения реагентов
Что касается смесей твердых и жидких фаз, то тут для увеличения скорости реакции поможет увеличение площади соприкосновения этих веществ.
Приведем пример: если мы возьмем часть щелочного метала в водном растворе, то реакция пойдет достаточно быстро, однако, если мы сделаем из кусочка металла порошок, то скорость взаимодействия увеличится.
Давление
В случае химической реакции, реагентами которой являются газы, то изменить скорость взаимодействия можно увеличением давления в системе, потому что таким образом повышается и концентрация газа. Зависимость скорости от давления будет прямо пропорциональной.
Что называется скоростью химической реакции в каких единицах она измеряется
Ключевые слова конспекта: Скорость химической реакции. Факторы, влияющие на скорость реакции: природа реагирующих веществ, площадь их соприкосновения, температура, концентрация, катализатор. Катализ. Ферменты. Ингибиторы.
Скорость — это отношение изменения какой-либо величины к промежутку времени, за которое это изменение произошло. Химические реакции протекают с разными скоростями. Одни практически мгновенно, например смесь водорода с кислородом (гремучая смесь) взрывается за доли секунды. Быстро протекает реакция нейтрализации, т. е. взаимодействие растворов кислоты со щёлочью (основанием):
Другие реакции протекают значительно медленнее, например брожение глюкозы или коррозия металлов:
Что же понимается под скоростью химической реакции? Предположим, некоторое взаимодействие протекает по схеме А + В = АВ. В ходе реакции вещества А и В расходуются, превращаясь в новое вещество АВ. Изменение количества веществ, участвующих в химической реакции, характеризует такая величина, как концентрация.
| Концентрация — количество вещества в единице объёма; её измеряют в моль/л. |
В ходе реакции концентрация исходных веществ (реагентов) уменьшается, а концентрация продукта реакции увеличивается. Изменение концентраций во времени и характеризует скорость химической реакции.
| Скорость химической реакции — отношение изменения концентрации реагента ко времени, за которое это изменение произошло. |
Математически эту закономерность можно выразить следующей формулой:
Если в приведённой формуле С1 и С2 — это начальная и конечная концентрации одного из реагентов, то разность С2 – С1 имеет отрицательное значение, ведь С2 0.
Размерность скорости реакции легко определить: концентрация измеряется в моль/л, время — в секундах, следовательно, единицей скорости реакции является 1 моль/(л • с).
Управление скоростью химической реакции имеет большое значение. Увеличение скорости реакции позволяет получить больше продуктов реакций: стали, пластмасс, химических удобрений, лекарств, топлива и др. Замедление скорости реакции позволяет уменьшать потери металла от коррозии, дольше сохранять продукты питания и т. д.
Рассмотрим, какие факторы влияют на скорость химической реакции.
✅ 1. Природа (состав и строение) реагирующих веществ. Реакции между органическими веществами протекают медленнее подобных реакций между неорганическими веществами. По-разному взаимодействуют галогены с водородом: фтор — со взрывом, хлор — со взрывом лишь при нагревании, бром — без взрыва, а реакция водорода с йодом является эндотермической и протекает медленно. Интенсивность взаимодействия щелочных металлов с водой зависит от их восстановительных свойств, которые усиливаются с увеличением радиуса атома.
✅ 2. Температура. Зависимость скорости химической реакции от температуры была установлена в конце 1884 г. голландским учёным Якобом Хендриком Вант-Гоффом.
Математическое выражение правила Вант-Гоффа записывают следующим образом:
где υ2 — скорость реакции при температуре t2;
υ1 — скорость реакции при температуре t1;
t2 — конечная температура реакции;
t1 — начальная температура реакции,
γ (греческая буква «гамма») — температурный коэффициент реакции, который соответствует изменению скорости химической реакции (увеличивает или уменьшает её) при изменении температуры на 10 градусов.
Например, температурный коэффициент какой–либо реакции близок к 3. Это означает, что при повышении температуры на 20 °С скорость реакции возрастёт в 9 раз:
✅ 3. Площадь соприкосновения реагирующих веществ. Этот фактор учитывается для гетерогенных реакций. Напомним, что гетерогенными (от греч. heteros — другой) называются реакции, идущие между веществами разного агрегатного состояния, т. е. имеющими поверхность раздела. Например, на поверхности соприкосновения жидкости или газа с твёрдым веществом и т. д.
Понятно, что, чем больше площадь соприкосновения реагирующих веществ, тем выше скорость химической реакции. Чтобы увеличить её, в промышленности используют особый метод, который называется «кипящий слой». Твёрдое вещество измельчают до очень мелких частиц, через которые затем пропускают снизу второй реагент, как правило, в газообразном состоянии. При прохождении этого реагента через слой измельчённого вещества наблюдается эффект, напоминающий кипение. Метод «кипящего слоя» используется при производстве серной кислоты для обжига серного колчедана, при каталитическом крекинге нефтепродуктов.
✅ 4. Концентрация реагирующих веществ. Зависимость была установлена норвежскими учёными Като Максимилианом Гульдбергом и Петером Вааге в 1867 г. и получила название закона действующих масс.
| Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в степенях, равных их коэффициентам в уравнении реакции. |
Математическое выражение закона действующих масс для реакции aА + bВ = dD выглядит так:
где υ — скорость химической реакции, СА и СB — концентрации реагентов А и В, а и b — коэффициенты в уравнении реакции, k — коэффициент пропорциональности — константа скорости реакции, которая показывает скорость химической реакции при концентрации реагирующих веществ, равных 1 моль/л.
Например, для второй стадии производства азотной кислоты, которая описывается уравнением 2NO + O2 = 2NO2↑, закон действующих масс отражает формула υ = k • C 2 (NO) • С(O2)
Если в гетерогенной реакции принимает участие твёрдое вещество, его концентрация не входит в уравнение закона. Например, для реакции между раскалённым оксидом меди(II) и водородом СuО + Н2 = Сu + Н2O справедливо следующее выражение: υ = k • С(Н2)
Это означает, что внесение дополнительного количества твёрдого вещества (оксида меди(II)) не оказывает влияния на скорость реакции.
✅ 5. Катализатор. Напомним, что катализаторами (от греч. katalysis — разрушение) называются вещества, изменяющие скорость химической реакции и не входящие в состав продуктов реакции.
Современную химическую промышленность невозможно представить без использования катализаторов. С их помощью ускоряют химические процессы, чтобы быстрее получить нужные вещества и уничтожить вредные (например, химические отходы). Производство минеральных кислот, аммиака и метанола, уксусной кислоты и полимеров, нефтепереработка и производство лекарственных препаратов — около 90 % всех химических производств основано на применении катализаторов.
С помощью катализаторов удаётся повысить производительность химических процессов и уменьшить себестоимость продукции. Катализаторы также позволяют сделать производство экологически более безопасным, т. е. уменьшить загрязнение окружающей среды вредными выбросами.
Катализаторы вошли в жизнь человека, когда он стал использовать процессы брожения для получения уксуса из виноградного сока, варить сыр и выпекать хлеб. Ведь все эти процессы протекают в присутствии биологических катализаторов, или ферментов (от лат. fermentum — закваска). Их также называют энзимами.
Ферменты содержатся во всех живых клетках. Они направляют, регулируют и многократно ускоряют биологические процессы, играя тем самым важную роль в обмене веществ и энергии.
Область применения биологических катализаторов шире, чем неорганических: ежегодный рост их производства в мире составляет 15%, а неорганических — всего 3%. Ферменты «трудятся» в медицине, сельском хозяйстве, пищевой промышленности, защищают окружающую среду, помогают в быту. Например, использование стирального порошка с ферментами — залог успешной стирки. Зная, что ферменты имеют белковую природу и под действием высокой температуры способны денатурировать, вы понимаете, насколько важно следовать инструкции по применению таких порошков.
Обратное влияние на скорость химической реакции оказывают ингибиторы (от лат. inhibere — сдерживать, останавливать) — вещества, подавляющие или задерживающие течение физиологических и физико-химических (главным образом, ферментативных) процессов. Такие вещества важны, как и катализаторы: ингибиторы коррозии, например, помогают сохранить металлы от разрушения.
Конспект урока по химии «Скорость химических реакций». В учебных целях использованы цитаты из пособия «Химия. 11 класс : учеб, для общеобразоват. организаций : базовый уровень / О. С. Габриелян, И. Г. Остроумов, С. А. Сладков. — М. : Просвещение». Выберите дальнейшее действие:
Скорость химической реакции
Говорить об осуществимости процесса можно по изменению энергии Гибсса системы. Но данная величина не отражает настоящую возможность протекания, механизм и скорость химической реакции.
Понятие скорости химической реакции
Для полноценного представления химической реакции, надо иметь знания о том, какие существуют временные закономерности при ее осуществлении, т.е. скорость химической реакции и ее детальный механизм.
Определение скорости химической реакции:
Скорость химической реакции — это изменение концентрации реагирующих веществ в единицу времени
Скорость и механизм реакции изучает химическая кинетика – наука о химическом процессе.
С точки зрения химической кинетики, реакции можно классифицировать на простые и сложные.
Простые реакции – процессы, протекающие без образования промежуточных соединений. По количеству частиц, принимающих в ней участие, они делятся на мономолекулярные, бимолекулярные, тримолекулярные. Соударение большего чем 3 числа частиц маловероятно, поэтому тримолекулярные реакции достаточно редки, а четырехмолекулярные — неизвестны.
Сложные реакции – процессы, состоящие из нескольких элементарных реакций.
Любой процесс протекает с присущей ему скоростью, которую можно определить по изменениям, происходящим за некий отрезок времени.
Среднюю скорость химической реакции выражают изменением количества вещества n израсходованного или полученного вещества в единице объема V за единицу времени t.
Если вещество расходуется, то ставим знак «-», если накапливается – «+»
При постоянном объеме:
Единица измерения скорости реакции — моль/л·с
В целом, υ — величина постоянная и не зависит от того, за каким участвующим в реакции веществом, мы следим.
Зависимость концентрации реагента или продукта от времени протекания реакции представляют в виде кинетической кривой, которая имеет вид:
Вычислять υ из экспериментальных данных удобнее, если указанные выше выражения преобразовать в следующее выражение:
| υ = — ΔC/Δt [моль/л·с] | |
Закон действующих масс. Порядок и константа скорости реакции
Одна из формулировок закона действующих масс звучит следующим образом:
Скорость элементарной гомогенной химической реакции прямо пропорциональна произведению концентраций реагентов.
Т.е. скорость прямой химической реакции зависит от концентраций исходных веществ.
Если исследуемый процесс представить в виде:
а А + b В = продукты
то скорость химической реакции можно выразить кинетическим уравнением:
а и b – стехиометрические коэффициенты простой реакции,
k – константа скорости реакции.
Химический смысл величины константы скорости реакции k — это скорость реакции при единичных концентрациях.
То есть, если концентрации веществ А и В равны 1, то υ = k.
Надо учитывать, что в сложных химических процессах коэффициенты а и b не совпадают со стехиометрическими.
Закон действующих масс выполняется при соблюдении ряда условий:
К сложным процессам закон действия масс применить нельзя!
Это можно объяснить тем, что сложный процесс состоит из нескольких элементарных стадий, и его скорость будет определяться не суммарной скоростью всех стадий, лишь одной самой медленной стадией, которая называется лимитирующей.
Каждая реакция имеет свой порядок. Определяют частный (парциальный) порядок по реагенту и общий (полный) порядок.
Например, в выражении скорости химической реакции для процесса
а А + b В = продукты
a – порядок по реагенту А
Для простых процессов порядок реакции указывает на количество реагирующих частиц (совпадает со стехиометрическими коэффициентами) и принимает целочисленные значения.
Для сложных процессов порядок реакции не совпадает со стехиометрическими коэффициентами и может быть любым.
Факторы, влияющие на скорость химической реакции
Определим факторы, влияющие на скорость химической реакции υ:
1. Зависимость скорости реакции от концентрации реагирующих веществ
определяется законом действующих масс:
Очевидно, что с увеличением концентраций реагирующих веществ, скорость реакции υ увеличивается, т.к. увеличивается число соударений между участвующими в химическом процессе веществами.
Причем, важно учитывать порядок реакции:
если это n = 1 по некоторому реагенту, то ее скорость прямо пропорциональна концентрации этого вещества.
Если по какому-либо реагенту n = 2, то удвоение его концентрации приведет к росту скорости реакции в 2 2 = 4 раза.
А увеличение концентрации в 3 раза ускорит реакцию в 3 2 = 9 раз.
2. Зависимость скорости реакции от давления
Таким образом, изменение концентрации в системе, а следовательно и скорости реакции имеет прямую зависимость от изменения давления.
Например, для реакции первого порядка, увеличение давления в 2 раза вызовет рост концентрации вещества в 2 раза, что непременно изменит скорость реакции υ – она станет в 2 раза больше.
3. Зависимость скорости реакции от площади поверхности
Для гетерогенных реакций скорость реакции зависит от площади соприкосновения частиц:
Δn — изменение количества веществ, принимающих участие в реакции (исходных веществ или продуктов реакции), моль;
Δt — промежуток времени, с;
Единица измерения скорости гетерогенной реакции, моль/м 2 ⋅с.
Таким образом, вещества реагируют быстрее, если площадь поверхности, на которой может происходить взаимодействие веществ больше.
Растворяя вещество, мы уменьшаем его размеры до размеров молекулы, увеличивая тем самым площадь поверхности.
Поэтому химические процессы между веществами, находящимися в растворенном, жидком или газообразном состоянии имеют большую скорость, чем взаимодействия между твердыми веществами.
В этом случае, большое значение имеет строение электронной оболочки атома, тип химической связи и ее прочность в молекулах, структура вещества, прочность его кристаллической решетки.
Например, натрий будет активнее взаимодействовать с водой, чем олово. Поэтому и скорость взаимодействия натрия с водой выше скорости взаимодействия олова с водой.
5. Зависимость скорости реакции от температуры
определяется правилом Вант-Гоффа и уравнением Аррениуса
Повышая температуру, мы сообщаем молекулам дополнительную энергию (увеличивая, тем самым, энергию активации), которая способствует протеканию реакции.
Поэтому, при повышении температуры скорость химической реакции увеличивается.
Сванте Аррениус в 1889 году, изучая зависимость скорости реакции υ от температуры, установил, что большинство химических процессов подчиняются уравнению:
где k — константа скорости реакции
Еа -энергия активации – минимальная (критическая) энергия, необходимая для осуществления реакции, единица измерения Дж/моль
Т — абсолютная температура
R – газовая постоянная, R = 8,314 Дж/моль·град
A — предэкспоненциальный множитель (частотный фактор), единица измерения совпадает с k. Эта константа выражает вероятность того, что при столкновении молекулы будут ориентированы так, чтобы взаимодействие было возможно.
Если известна константа скорости k при одной температуре Т1, а требуется найти константу скорости k при некой другой температуре Т2, то это легко сделать, если взять логарифм уравнения Аррениуса при Т1 и Т2:
Вычитая второе равенство из первого, получаем:
Если принять, что концентрации веществ А и В постоянны и прологарифмировать данное выражение, то получим следующее выражение:
Правило Вант-Гоффа
Также удобно пользоваться эмпирическим правилом, которое сформулировал Якоб Вант-Гофф:
увеличение температуры на каждые 10 градусов, приводит к росту скорости реакции в 2 – 4 раза.
Правило Вант-Гоффа имеет математическое выражение:
γ — температурный коэффициент реакции, значения которого лежат в интервале от 2 до 4.
Приведем пример применения правила Вант-Гоффа.
υT1/υT2 = 3 2 = 9. Это означает, что υ возросла в 9 раз.
6. Зависимость скорости реакции от присутствия катализатора
Катализ – это любое изменение скорости реакции под действием катализатора. Он может быть положительным и отрицательным. Суть катализа – генерирование активного субстрата или реагента с участием катализаторов.
Катализатор представляет собой вещество, которое селективно ускоряет химическую реакцию, вступая при этом в промежуточную стадию, но регенирируясь к ее концу (к моменту образования конечных продуктов). Например, в биохимической среде в качестве катализаторов выступают ферменты.
Если такое вещество замедляет химическую реакцию, то оно называется ингибитором.
Влияние катализатора на скорость реакции основывается на том, что он изменяет энергию активации Еа. Понижение энергии активации под действием катализатора схематично представлено на рисунке ниже:
Видно, что веществам А и В требуется большое количество энергии, чтобы образовать конечные продукты. Но в присутствии катализатора для получения конечных продуктов требуется гораздо меньше энергии, т.к. идет понижение полной энергии активации, и тем самым, увеличение скорости реакции.
Обращаю ваше внимание на то, что энергии как начальных, так и конечных веществ остаются одинаковыми в обеих реакциях.