Что называется продуктами реакции в химии
Химические реакции
Химическая реакция — это процесс, во время которого из одних веществ получаются другие. В процессе химической реакции происходит разрыв одних и образование других химических связей, т.е. атомы одного вещества разрывают связь друг с другом и соединяются с атомами другого вещества, тем самым образуя абсолютно новое вещество.
Признаки химических реакции
ЗАПОМНИ! Вещества, вступающие в химическую реакцию, называются реагентами. Продукты реакции — это вещества, полученные в результате химической реакции. Скорость, с которой происходит изменение вещества, называется скоростью реакции.
Где происходят химические реакции?
Если ты думаешь, что единственное место, где могут происходить химические реакции, — научная лаборатория, ты глубоко заблуждаешься. На самом деле такие реакции ежеминутно происходят в любой точке нашей планеты, даже в человеке. К примеру, когда ты принимаешь пищу, твой организм превращает ее в энергию именно при помощи химических реакций. Горение дерева, покрытие металла ржавчиной, фотосинтез у растений — все это примеры химических реакций.
Скорость реакции
На скорость реакции могут оказывать влияние различные факторы: солнечный свет, тепло, давление или электричество существенно увеличивают ее.
Как начинаются реакции?
Тепло приходит и уходит
Экзотермические реакции протекают с выделением теплоты. В быту примером такой реакции является работа многоразовой солевой грелки. Грелка представляет собой емкость с перенасыщенным солевым раствором, внутри которой находится аппликатор. Когда мы перегибаем аппликатор, солевой раствор из жидкого состояния переходит в твердое. Процесс сопровождается выделением теплоты, и грелка нагревается. Эндотермические реакции протекают с поглощением теплоты. Один из примеров такой реакции — приготовление пищи. Чтобы сырой продукт превратился в пригодный для употребления, в нем должны произойти разные химические реакции, большинству из которых необходимо постоянное поступление тепла из внешней среды.
Примеры нехимических реакций
Во время таяния лед из твердого состояния переходит в жидкое. Казалось бы, изменение очевидно! Но это не химическая реакция, так как вещество осталось прежним, просто вода изменила свое состояние.
Образование смесей и растворов также не является химической реакцией, так как вещества, входящие в состав смесей или растворов, не превращаются в другие.
Химическая реакция
Хими́ческая реа́кция — превращение одного или нескольких исходных веществ (реагентов) в отличающиеся от них по химическому составу или строению вещества (продукты реакции). В отличие от ядерных реакций, при химических реакциях ядра атомов не меняются, в частности не изменяется их общее число, изотопный состав химических элементов, при этом происходит перераспределение электронов и ядер и образуются новые химические вещества.
Химические реакции происходят при смешении или физическом контакте реагентов самопроизвольно, при нагревании, участии катализаторов (катализ), действии света (фотохимические реакции), электрического тока (электродные процессы), ионизирующих излучений (радиационно-химические реакции), механического воздействия (механохимические реакции), в низкотемпературной плазме (плазмохимические реакции) и т. п. Взаимодействие молекул между собой происходит по цепному маршруту: ассоциация — электронная изомеризация — диссоциация, в котором активными частицами являются радикалы, ионы, координационно-ненасыщенные соединения. Скорость химической реакции определяется концентрацией активных частиц и разницей между энергиями связи разрываемой и образуемой.
Содержание
Классификация
Существует большое количество признаков, по которым можно классифицировать химические реакции.
По фазовому составу реагирующей системы
По изменению степеней окисления реагентов
В данном случае различают
Пример окислительно-восстановительной реакции — горение водорода (восстановитель) в кислороде (окислитель) с образованием воды:
Пример реакции диспропорционирования — реакция разложения нитрата аммония при нагревании. Окислителем в данном случае выступает азот (+5) нитрогруппы, а восстановителем — азот (-3) катиона аммония:
По тепловому эффекту реакции
Все реакции сопровождаются тепловыми эффектами. При разрыве химических связей в реагентах выделяется энергия, которая, в основном, идет на образование новых химических связей. В некоторых реакциях энергии этих процессов близки, и в таком случае общий тепловой эффект реакции приближается к нулю. В остальных случаях можно выделить:
Тепловой эффект реакции (энтальпию реакции, ΔrH), часто имеющий очень важное значение, можно вычислить по закону Гесса, если известны энтальпии образования реагентов и продуктов. Когда сумма энтальпий продуктов меньше суммы энтальпий реагентов (ΔrH 0) — поглощение.
По типу превращений реагирующих частиц
Химические реакции всегда сопровождаются физическими эффектами: поглощением и выделением энергии, например в виде теплопередачи, изменением агрегатного состояния реагентов, изменением окраски реакционной смеси и др. Именно по этим физическим эффектам часто судят о протекании химических реакций.
Химические процессы, протекающие в веществе, отличаются и от физических процессов, и от ядерных превращений. В физических процессах каждое из участвующих веществ сохраняет неизменным свой состав (хотя вещества могут образовывать смеси), но могут изменять внешнюю форму или агрегатное состояние.
В химических процессах (химических реакциях) получаются новые вещества с отличными от реагентов свойствами, но никогда не образуются атомы новых элементов. В атомах же участвующих в реакции элементов обязательно происходят видоизменения электронной оболочки.
В ядерных реакциях происходят изменения в атомных ядрах всех участвующих элементов, что приводит к образованию атомов новых элементов.
С помощью химических реакций можно получать практически важные вещества, которые в природе находятся в ограниченных количествах, например азотные удобрения, либо вообще не встречаются по каким-либо причинам, например сульфаниламиды и другие синтетические лекарственные препараты, полиэтилен и другие пластмассы. Химия позволяет синтезировать новые, неизвестные природе вещества, необходимые для жизнедеятельности человека. Вместе с тем, неумелое или безответственное химическое воздействие на окружающую среду и на протекающие природные процессы может привести к нарушению установившихся естественных химических циклов, что делает актуальной экологическую проблему (загрязнение окружающей среды) и усложняет задачу рационального использования природных ресурсов и сохранения естественной среды обитания на Земле.
Классификация реакций
Существует несколько классификаций реакций, протекающих в неорганической и органической химии.
По характеру процесса
Так называют химические реакции, где из нескольких простых или сложных веществ получается одно сложное вещество. Примеры:
В результате реакции разложения сложное вещество распадается на несколько сложных или простых веществ. Примеры:
В ходе реакций замещения атом или группа атомов в молекуле замещаются на другой атом или группу атомов. Примеры:
К реакциям обмена относятся те, которые протекают без изменения степеней окисления и выражаются в обмене компонентов между веществами. Часто обмен происходит анионами/катионами:
AgF + NaCl = AgCl↓ + NaF
Окислительно-восстановительные реакции (ОВР)
Замечу, что окислителем и восстановителем могут являться только исходные вещества (а не продукты!) Окислитель всегда понижает свою СО, принимая электроны в процессе восстановления. Восстановитель всегда повышает свою СО, отдавая электроны в процессе окисления.
ОВР уравнивают методом электронного баланса, с которым мы подробно познакомимся в разделе «Решения задач».
Обратимые и необратимые реакции
Классическим примером обратимой реакции является синтез аммиака и реакция этерификации (из органической химии):
Необратимые реакции протекают только в одном направлении, до полного расходования одного из исходных веществ. Главное отличие их от обратимых реакций в том, что образовавшиеся продукты реакции не взаимодействуют между собой с образованием исходных веществ.
Примеры необратимых реакций:
NaOH + HCl = NaCl + H2O (образуется вода)
2Na + 2H2O = 2NaOH + H2 (сопровождается выделением большого количества тепла)
Реакции и агрегатное состояние фаз
Фазой в химии называют часть объема равновесной системы, однородную во всех своих точках по химическому составу и физическим свойствам и отделенную от других частей того же объема поверхностью раздела. Фаза бывает жидкой, твердой и газообразной.
К гетерогенным реакциям относятся следующие реакции (примеры): жидкость + газ, газ + твердое вещество, твердое вещество + жидкость. Примером такой реакции может послужить взаимодействие твердого цинка и раствора соляной кислоты:
К гомогенным реакциям относятся (примеры): жидкость + жидкость, газ + газ. Примером такой реакции может служить взаимодействие между растворами уксусной кислоты и едкого натра.
Реакции и их тепловой эффект
NaOH + HCl = NaCl + H2O + 56 кДж
К экзотермическим реакциям часто относятся реакции горения, соединения.
Исключением является взаимодействие азота и кислорода, при котором тепло поглощается:
Как уже было отмечено выше, если тепло выделяется во внешнюю среду, значит, система реагирующих веществ потеряло это тепло. Поэтому не должно казаться противоречием, что внутренняя энергия веществ в результате экзотермической реакции уменьшается.
Энтальпией называют (обозначение Н), количество термодинамической (тепловой) энергии, содержащееся в веществе. Иногда с целью «запутывания» в реакции вместо явного +Q при экзотермической реакции могут написать ΔH 0, так как внутренняя энергия веществ увеличивается. Например:
CaCO3 = CaO + CO2↑ ; ΔH > 0 (значит реакция эндотермическая, так как внутренняя энергия увеличивается)
Замечу, что не все реакции разложения являются эндотермическими. Широко известная реакция разложения дихромата аммония («вулканчик») является примером экзотермического разложения, при котором тепло выделяется.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Что называется продуктами реакции в химии
Химическая реакция — это превращение одних веществ (реагентов) в другие, отличающиеся по химическому составу или строению (продукты реакции).
ПРИЗНАКИ ХИМИЧЕСКИХ РЕАКЦИЙ
Химическое превращение от физического всегда можно отличить по наличию одного или нескольких признаков:
· образование слабодиссоциированных веществ (например, воды);
· выделение энергии (тепловой или световой).
ТИПЫ КЛАССИФИКАЦИЙ ХИМИЧЕСКИХ РЕАКЦИЙ
Существует несколько подходов к классификации химических реакций, основные из них представлены на схеме ниже.
Рассмотрим их подробнее.
КЛАССИФИКАЦИЯ ПО ЧИСЛУ И СОСТАВУ РЕАГИРУЮЩИХ И ОБРАЗУЮЩИХСЯ ВЕЩЕСТВ
Первая реакция является реакцией соединения (иногда говорят присоединения), поскольку из двух веществ получается одно. Во второй реакции, наоборот, из одного вещества получается два и это реакция разложения.
В реакциях замещения простое вещество замещает один из элементов в сложном веществе, в результате чего получается новое просто вещество и новое сложное вещество. Например:
В реакциях обмена два сложных вещества обмениваются своими составными частями и образуется два новых сложных вещества:
КЛАССИФИКАЦИЯ ПО ИЗМЕНЕНИЮ СТЕПЕНИ ОКИСЛЕНИЯ
Окислительно-восстановительные реакции (ОВР) — реакции, протекающие с изменением степеней окисления элемента(ов).
В любой окислительно-восстановительной реакции (ОВР) всегда должен быть как минимум один элемент, повышающий степень окисления ( восстановитель ), и другой — понижающий степень окисления ( окислитель ).
Если же эти элементы входят в состав одной молекулы, такие реакции называются внутримолекулярными ОВР.
6 KOH (конц.) + 3 Cl 2 = KClO 3 + 5 KCl + 3 H 2 O
Cl 0 2 + 1 ⋅ 2 e ¯→ 2 Cl − | 5 окислитель, процесс восстановление
Cl 0 2 − 5 ⋅ 2 e ¯→ 2 Cl +5 | 1 восстановитель, процесс окисление
В этой реакции хлор простое вещество одновременно и окислился (до KClO 3 ) и восстановился (до KCl ). Такие реакции называются реакциями диспропорционирования.
S +4 + 4 e ¯→ S 0 | 1 окислитель, процесс восстановление
S −2 − 2 e ¯→ S 0 | 2 восстановитель, процесс окисление
КЛАССИФИКАЦИЯ ПО ТЕПЛОВОМУ ЭФФЕКТУ
Тепловой эффект реакции — ΔH — теплота, поглощаемая или выделяемая системой в ходе химической реакции.
2. Е реагентов В этом случае для протекания реакции необходима дополнительная энергия, которая может быть получена извне в виде дополнительного нагревания, УФ-облучения или в других формах. При этом температура реагирующей системы должна понижаться за счет поглощения энергии.
Экзотермические реакции — реакции, протекающие с выделением тепла (+Q)
Самые типичные экзотермические реакции — это реакции горения. Иногда энергетический «выигрыш» настолько велик, что происходит выделение и тепловой и световой энергии, что чаще всего принято называть взрывом. Например, горение метана в атмосфере воздуха.
В случае, если на образование новых химических связей требуется энергия большая, чем выделилась при разрыве старых связей, то системе требуется дополнительная подача тепла.
Эндотермические реакции — реакции, протекающие с поглощением тепла (-Q)
Термохимические уравнения — уравнения химических реакций с указанием теплового эффекта реакции.
Подробнее термохимические уравнения будут рассмотрены в соответствующем разделе.
КЛАССИФИКАЦИЯ ПО АГРЕГАТНОМУ СОСТОЯНИЮ РЕАГЕНТОВ
Напомним, что существует четыре агрегатных состояния вещества: газ, жидкость, твердое и плазма (последнее встречается крайне редко).
Граница раздела фаз присутствует в системе, образованной, например, жидкостью и твердым телом (металл и кислота), твердым телом и газом (гетерогенный катализ), двумя несмешивающимися жидкостями (масло и вода). Чаще всего химические реакции являются гетерогенными.
Агрегатное состояние вещества обычно обозначается буквами русского алфавита нижним индексом в скобках : (г) — газ, (ж) — жидкость, (т) — твердое.
КЛАССИФИКАЦИЯ ПО НАЛИЧИЮ КАТАЛИЗАТОРА
Катализатор — вещество, которое ускоряет скорость химической реакции, но само при этом не расходуется.
Ингибитор — вещество, замедляющее или предотвращающее протекание химической реакции.
Следует понимать, что катализатор участвует в реакции и претерпевает ряд изменений (каталитический цикл), превращается в промежуточные соединения, которые разрушаются к концу каталитического цикла, превращаясь в исходный катализатор. Поэтому иногда в учебниках встречается формулировка: «катализатор в реакции не расходуется».
Ингибиторы используются в быту и в промышленности для подавления протекания нежелательных процессов: старения полимеров, окисления топлива и смазочных масел, пищевых жиров и др. Например, ортофосфорная кислота замедляет процессы окисления железа (коррозию), поэтому ее используют для предотвращения ржавления. Часто ингибиторы используются в медицине, в лекарственных препаратах, например ингибиторы образования ферментов и др.
КЛАССИФИКАЦИЯ ПО НАПРАВЛЕНИЮ ПРОТЕКАНИЯ РЕАКЦИИ
Реакции, которые при заданных условиях протекают как в прямом, так и в обратном направлении, называют обратимыми.
Обратимые реакции очень распространены в химии. К ним относятся диссоциация воды и слабых кислот, гидролиз некоторых солей, реакции водорода с бромом, иодом и азотом, многие промышленно важные реакции, такие как:
Химическая кинетика



Химическая кинетика устанавливает временные закономерности протекания химических реакций, связь между скоростью реакции и условиями ее проведения, выявляет факторы, влияющие на скорость и направление химических реакций.
Любой химический процесс представляет собой превращение реагентов в продукты реакции:
реагенты→ переходное состояние→ продукты реакции.
Реагенты (исходные вещества)— вещества, вступающие в процесс химического взаимодействия.
Продукты реакции— вещества, образующиеся в конце процесса химического превращения. В обратимых процессах продукты прямой реакции являются реагентами обратной реакции.
Химические реакции могут быть как необратимыми, так и обратимыми.
Необратимые реакции— реакции, протекающие при данных условиях практически в одном направлении (обозначают знаком →).
Обратимые реакции— реакции, протекающие одновременно в двух противоположных направлениях (обозначают знаком ).
Переходное состояние (активированный комплекс)— это состояние химической системы, являющееся промежуточным между исходными веществами (реагентами) и продуктами реакции. В этом состоянии происходит разрыв старых химических связей и образования новых химических связей. Далее активированный комплекс превращается в продукты реакции.
Большинство химических реакций являются сложными и состоят из нескольких стадий, называемых элементарными реакциями.
Элементарная реакция— единичный акт образования или разрыва химической связи. Совокупность элементарных реакций, из которых складывается химическая реакция, определяет механизм химической реакции.
В уравнении химической реакции обычно указывается начальное состояние системы (исходные вещества) и её конечное состояние (продукты реакции). В то же время фактический механизм химической реакции может быть достаточно сложным и включать в себя целый ряд элементарных реакций. К сложным химическим реакциям относятся обратимые, параллельные, последовательные и другие многостадийные реакции(цепные реакции, сопряженные реакции и пр.).
Если скорости различных стадий химической реакции существенно различаются, то скорость сложной реакции в целом определяется скоростью самой медленной ее стадии. Такую стадию (элементарную реакцию) называют лимитирующей стадией.
В зависимости от фазового состояния реагирующих веществ, различают два типа химических реакций: гомогенныеигетерогенные.
Фазойназывается часть системы, отличающаяся по своим физическим и химическим свойствам от других частей системы и отделенная от них поверхностью раздела. Системы, состоящие из одной фазы, называются гомогенными системами, из нескольких фаз – гетерогенными. Примером гомогенной системы может быть воздух, представляющий собой смесь веществ (азот, кислород и др.), находящихся в одинаковой газовой фазе. Суспензия мела (твердого вещества) в воде (жидкость) является примером гетерогенной системы, состоящей из двух фаз.
Соответственно, реакции, в которых взаимодействующие вещества находятся в одной фазе, называются гомогенными реакциями. Взаимодействие веществ в таких реакциях происходит по всему объёму реакционного пространства.
К гетерогенным реакциям относят реакции, протекающие на границе раздела фаз. Примером гетерогенной реакции может служить реакция цинка (твердая фаза) с раствором соляной кислоты (жидкая фаза). В гетерогенной системе реакция всегда происходит на поверхности раздела двух фаз, так как только здесь реагирующие вещества, находящиеся в разных фазах, могут сталкиваться между собой.
Скорости химических реакций могут существенно отличаться. Химические реакции могут протекать крайне медленно, а могут протекать практически мгновенно.
Скорость химической реакции служит количественной мерой интенсивности ее протекания.
В общем случае под скоростью химической реакции понимают число элементарных актов реакции, происходящих в единицу времени в единице реакционного пространства.
Так как для гомогенных процессов реакционным пространством является объем реагирующих веществ, то для гомогенных реакций скорость химической реакции определяется количеством вещества, прореагировавшего в единицу времени в единице объема.
Учитывая, что количество вещества, содержащееся в определенном объеме, характеризует концентрацию вещества, то скорость реакции— это величина, показывающая изменение молярной концентрации одного из веществ в единицу времени.
Это определение можно записать в виде производной:
v – скорость реакции; t – время, c – концентрация.
Эту скорость легко определить, если есть экспериментальные данные по зависимости концентрации вещества от времени. По этим данным можно построить график, который называется кинетической кривой.
Если время измерять в секундах, а концентрацию – в молях на литр, то скорость реакции измеряется в единицах моль/(л·с). Таким образом, скорость реакции не зависит от объема реакционной смеси. Величина dt всегда положительна, тогда как знак dc зависит от того, как изменяется со временем концентрация – уменьшается (для исходных веществ) или увеличивается (для продуктов реакции). Для того чтобы скорость реакции всегда оставалась величиной положительной, в случае ее определения по изменению концентрации исходных веществ перед производной ставят знак минус:
Если реакция идет в газовой фазе, то вместо концентрации веществ в уравнении скорости часто используют давление. Если газ близок к идеальному, то давление р связано с концентрацией с простым уравнением:
Так как для гетерогенных реакций реакционным пространством является поверхность, на которой протекает реакция, то для гетерогенных химических реакций скорость реакции относится к единице площади поверхности, на которой протекает реакция.
Скорость химической реакции зависит от целого ряда факторов:
• природы реагирующих веществ;
• концентрации реагирующих веществ;
• давления (для газовых систем);
• температуры системы;
• площади поверхности (для гетерогенных систем);
• наличия в системе катализатора и других факторов.
Закон действующих масс гласит: скорость элементарной химической реакции при постоянной температуре прямо пропорциональна произведению молярных концентраций реагирующих веществ в степенях, равных их стехиоме-трическим коэффициентам.
Уравнение, выражающее зависимость скорости реакции от концентрации каждого вещества, называют кинетическим уравнением реакции.
В общем случае, если в элементарную реакцию вступают одновременно т молекул вещества А и n молекул вещества В:
то уравнение для скорости реакции (кинетическое уравнение) имеет вид:
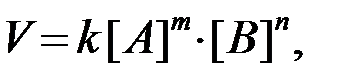
k— коэффициент пропорциональности, который называется константой скорости химической реакции;
m и n— стехиометрические коэффициенты в уравнении реакции.
Константа скорости реакции k численно равна скорости реакции, в которой концентрации реагирующих веществ (или их произведение в кинетических уравнениях) равны единице.
Константа скорости реакции k зависит от природы реагирующих веществ и температуры, но не зависит от значения концентрации реагентов.
Для гетерогенных реакций концентрация твердой фазы в выражение для скорости химической реакции (кинетическое уравнение) не включается.
Например, в реакции синтеза метана:
С(т) + 2H2(г) 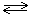
согласно закону действующих масс, скорость реакции определяется только концентрацией водорода, а площадь поверхности твердого углерода учитывается константой скорости химической реакции k. Кинетическое уравнение для этой реакции будет имеет вид:
Зависимость скорости реакции от температуры определяется правилом Вант-Гоффа:
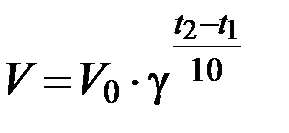
V1 – скорость реакции при начальной температуре системы t1,
V2 – скорость реакции при конечной температуре системы t2,
γ – температурный коэффициент реакции (коэффициент Вант-Гоффа), равный 2÷4.
Знание величины температурного коэффициента γ дает возможность рассчитать изменение скорости реакции при увеличении температуры от Т1 до Т2. В этом случае можно использовать формулу:
Очевидно, что при повышении температуры в арифметической прогрессии скорость реакции возрастает в геометрической прогрессии. Влияние температуры на скорость реакции тем значительнее, чем больше значение температурного коэффициента реакцииg.
Катализаторы—это вещества, которые повышают скорость химической реакции. Они вступают во взаимодействие с реагентами с образованием промежуточного химического соединения и освобождаются (регенирируются) в конце реакции.
Явление ускорения химических реакций при введении катализаторов называется катализом.
Различают гомогенный катализ (катализатор образует с реагирующими веществами гомогенную систему, например, газовую смесь) и гетерогенный катализ (катализатор и реагирующие вещества находятся в разных фазах и каталитический процесс идет на поверхности раздела фаз).
Вещества, повышающие активность катализатора называют промоторами (или активаторами). При этом, сами промоторы могут и не обладать каталитическими свойствами.
Каталитические яды— посторонние примеси в реакционной смеси, приводящие к частичной или полной потере активности катализатора. Так, следы фосфора и мышьяка вызывают быструю потерю катализатором V2O5 активности в реакции окисления SO2 в SO3.
Биохимические реакции в растительных и животных организмах ускоряются биохимическими катализаторами — ферментами.