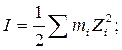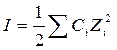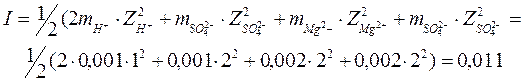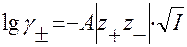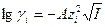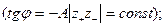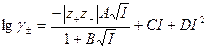Что называется ионной атмосферой какими величинами определяется ее размер
Ионная атмосфера
Смотреть что такое «Ионная атмосфера» в других словарях:
ионная атмосфера — joninė atmosfera statusas T sritis chemija apibrėžtis Joną supanti priešjonių visuma. atitikmenys: angl. ionic atmosphere rus. ионная атмосфера … Chemijos terminų aiškinamasis žodynas
ИОННАЯ АТМОСФЕРА — см. Дебая Хюккеля теория … Химическая энциклопедия
ионная атмосфера — ионное облако … Cловарь химических синонимов I
ионное облако — ионная атмосфера … Cловарь химических синонимов I
ЭЛЕКТРОПРОВОДНОСТЬ ЭЛЕКТРОЛИТОВ — способность электролитов проводить электрич. ток при приложении электрич. напряжения. Носителями тока являются положительно и отрицательно заряженные ионы катионы и анионы, к рые существуют в р ре вследствие электролитич. диссоциации. Ионная Э. э … Химическая энциклопедия
Электропроводность электролитов — обусловлена наличием в них положительных и отрицательных ионов (катионов и анионов). Доли общего количества электричества, переносимого катионами и анионами, называются переноса числами (См. Переноса число). Э. э. количественно… … Большая советская энциклопедия
Теория Дебая — Хюккеля — Теория сильных электролитов Дебая Хюккеля предложенная Петером Дебаем и Эрихом Хюккелем в 1923 году статистическая теория разбавленных растворов сильных электролитов, согласно которой каждый ион действием своего электрического заряда поляризует… … Википедия
Метод Дебая — Хюккеля — Теория сильных электролитов Дебая Хюккеля предложенная Петером Дебаем и Эрихом Хюккелем в 1923 году статистическая теория разбавленных растворов сильных электролитов, согласно которой каждый ион действием своего электрического заряда поляризует… … Википедия
Теория Дебая — Теория сильных электролитов Дебая Хюккеля предложенная Петером Дебаем и Эрихом Хюккелем в 1923 году статистическая теория разбавленных растворов сильных электролитов, согласно которой каждый ион действием своего электрического… … Википедия
Основные положения теории Дебая-Гюккеля
Ионная сила раствора. Правило ионной силы (или закон ионной силы Льюиса и Рендалла).
Концентрацию растворов сильных электролитов можно характеризовать не только активностью а, но и ионной силой. Активность а характеризует концентрацию одного электролита в растворе, а через ионную силу можно выражать концентрацию как одного, так и нескольких электролитов. Таким образом, ионная сила показывает суммарную концентрацию всех электролитов в растворе с учетом взаимодействия между ионами.
Ионная сила раствора (I, размерность концентрации) – это полусумма произведений концентраций всех ионов в растворе на квадрат их заряда.
где 
Пример: раствор содержит 0,001 моль H2SO4 и 0,002 моль MgSO4 на 1000 грамм H2O. Какова ионная сила раствора?
От ионной силы раствора зависит γ±. Эта зависимость выражается правилом ионной силы (или закон ионной силы Льюиса и Рендалла):
коэффициенты активности ионов не зависят от конкретного вида ионов, находящихся в растворе, а зависят от ионной силы I раствора.
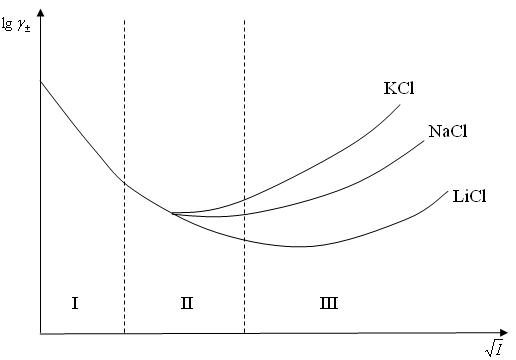
Это эмпирическое правило строго выполняется при концентрациях до 0,01 моль/кг и приближенно до 0,1 моль/кг (рис. 2).
В области концентраций 0,01 – 0,1 моль/кг существуют следующие закономерности:
1. зависимость 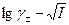
2. для соединений одного валентного типа γ± одинаков (т. к. в области низких концентраций тангенс угла наклона прямой одинаков).
Рис. 2. Средние коэффициенты активности HCl и HBr в растворах галогенидов щелочных металлов при 25 0 С.
В 1923 г. Дебай и Гюккель разработали электростатическую теорию растворов сильных электролитов (или теория сильных электролитов Дебая-Хюккеля).
Теория сильных электролитов Дебая-Хюккеля справедлива только для разбавленных растворов сильных электролитов.
Основные положения теории:
1. собственными размерами ионов можно пренебречь по сравнению с расстоянием между ними, поскольку растворы разбавленные.
2. учитываются только кулоновские взаимодействия между ионами и не учитываются другие виды взаимодействия (ион-дипольное, образование ассоциатов за счет водородной связи и т. д.)
3. электростатическое взаимодействие между ионами рассматривается как взаимодействие между центральным ионом и его ионной атмосферой.
4. вследствие кулоновского взаимодействия ионы в растворе расположены упорядочено, а растворы являются неидеальными.
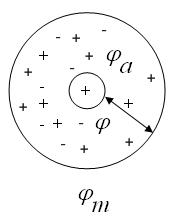
Ионная атмосфера состоит из ионов противоположных по знаку центральному иону.
В отсутствие внешнего электрического поля ионная атмосфера имеет шаровую симметрию, а ее заряд равен по величине и противоположен по знаку заряду центрального иона. Плотность ионной атмосферы уменьшается по мере удаления от центрального иона.
Ионную атмосферу можно характеризовать следующими параметрами:
1) потенциал ионной атмосферы:
потенциал электрического поля φm вокруг какого-либо иона состоит из потенциала центрального иона (φ) и потенциала ионной атмосферы (φа):
Поскольку раствор электролита электронейтрален, то потенциал электрического поля вокруг иона равен 0:
Тогда, потенциал ионной атмосферы равен потенциалу центрального иона с противоположным знаком:
2) эффективный радиус ионной атмосферы (r):
это расстояние вдоль прямой от центрального иона, на котором плотность ионной атмосферы уменьшается приблизительно в е раз.
Чем больше величина r, тем медленнее изменяется плотность ионной атмосферы.
Согласно теории Дебая-Хюккеля можно вычислить величину среднего коэффициента активности γ± сильного электролита по уравнениям трех приближений теории Дебая-Гюккеля.
I приближение теории Дебая-Гюккеля(или предельный закон Дебая-Гюккеля) для среднего коэффициента активности γ±:
I – ионная сила раствора; 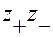
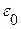
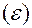
Для вычисления коэффициентов активности отдельных ионов используется уравнение:
I приближение теории Дебая-Гюккеля справедливо для сильно разбавленных растворов с ионной силой до 0,01 моль/кг. При этом размером ионов пренебрегают (считают их материальными точками). Согласно уравнению І приближения теории Дебая-Гюккеля зависимость 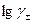
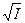
Рис. 3. Приближения теории Дебая-Хюккеля
Выводы из I приближения теории Дебая-Гюккеля:
1. для сильных разбавленных растворов электролитов 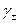
2. в области низких концентраций (когда I раствора мала) 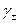
3. предельный закон Дебая-Гюккеля дает теоретическое обоснование эмпирическому правилу ионной силы.
II Приближение теории Дебая-Гюккеля: справедливо для I раствора до 0,1 моль/кг. При этом учитываются размеры ионов. Уравнение II приближения Дебая-Гюккеля описывает зависимость (рис. 3), когда с ростом концентрации (т. е. I раствора) величина 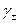
где В – эмпирический параметр, который связан с эффективным диаметром ионов в растворе. Эффективным диаметром называется такой диаметр иона, если бы он был в кристаллической решетке.
Приближенной формой II приближения теории Дебая-Гюккеля является уравнение Гюнтельберга:
где В = 1 для всех электролитов. Это уравнение удобно тем, что не содержит эмпирических параметров и удовлетворительно описывает поведение электролитов до концентрации 0,1 моль/кг.
III Приближение теории Дебая-Гюккеля: справедливо для растворов электролитов с ионной силой до 1 моль/кг; учитывает сольватацию иона молекулами растворителя. Уравнение III приближения описывает зависимость (рис. 3), когда с ростом 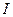
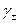
где С – эмпирический параметр, который учитывает поляризацию молекул растворителя вокруг иона растворенного вещества.
Уравнение III приближения теории Дебая-Гюккеля было усовершенствовано путем введения дополнительного слагаемого:
где D – эмпирический параметр. Это уравнение Харнеда и Оуэна, которое позволяет описывать поведение многих электролитов до 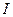
В области больших концентраций (более 1–5моль/кг) поведение растворов сильных электролитов невозможно точно описать, в частности зависимость 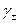
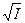
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Шпаргалки к экзаменам и зачётам
студентам и школьникам
Теория электролитов Дебая и Гюккеля: вывод первого приближения теории.
Поскольку ионная атмосфера обладает шаровой симметрией, то уравнение Пуассона, записанное в сферической системе координат, принимает вид
Для раствора в целом и для любого заданного его объема, достаточно большого по сравнению с размерами иона, справедливо условие электронейтральности
они ограничились только двумя его первыми членами, получив для r следующее уравнение:
(так как первый член правой части уравнения по условию электронейтральности равен нулю). Если ввести обозначение
то после подстановки выражения для r в уравнение Пуассона получаем дифференциальное уравнение вида
Общее решение этого уравнения второго порядка имеет вид
что является вторым пограничным условием. Если е – c r разложить в ряд, то получим
При r ® 0 всеми членами ряда можно пренебречь по сравнению с 1. Тогда
Для вычисления энергии взаимодействия необходимо определить потенциал ионной атмосферы в точке нахождения центрального иона, то есть найти предел y а при r ® 0. Это можно сделать, используя тот же прием – разлагая показательную функцию в ряд и пренебрегая высшими членами разложения:
В первом приближении теории Дебая и Гюккеля предполагается, что энергия межионного взаимодействия имеет электростатическое происхождение. Энергия взаимодействия ионов может быть определена поэтому как энергия заряжения центрального иона в электрическом поле ионной атмосферы. Известно, что энергия заряжения частицы от 0 до заряда q в поле y равна
(вместо q подставили заряд центрального иона, а вместо y – величину y ¢ ).
Найдем выражение для коэффициента активности электролита. Коэффициенты активности первоначально были введены как эмпирические величины; необходимость их введения в уравнения для идеальных систем обусловлена различием между реальными и идеальными растворами. Коэффициенты активности не зависят от метода их определения и при заданных условиях и составе будут иметь одно и то же значение для любых типов равновесия. Таблицы, в которых приведены эмпирические коэффициенты активности, представляют большую ценность. В то же время в пределах теории Льюиса коэффициенты активности оказываются лишь формальными поправочными множителями, не связанными непосредственно с природой растворов и не поддающимися теоретическим расчетам.
Реальные растворы отличаются от идеальных энергией взаимодействия образующими их частиц. Сопоставление выражений для химических потенциалов частиц в реальных растворах
Таким образом, коэффициент активности отражает изменение энергетического состояния ионов, обусловленное межионным (межчастичным) взаимодействием. Расчет взаимодействия, а следовательно, и коэффициента активности возможен, если известны структура раствора и природа сил взаимодействия между образующими его частицами. Ни то, ни другое не известно с достаточной степенью точности, поэтому для решения проблемы приходится прибегать к некоторым предположениям и создавать модели растворов электролитов.
По модели Дебая и Гюккеля, энергия взаимодействия иона с ионной атмосферой, равная энергии заряжения, определяется выражением
Заряд элемента объема будет равен
а плотность заряда
Для коэффициента активности
Подстановка значения c приводит к
После перехода к десятичному логарифму и подстановки численных значений постоянных величин
Для данного растворителя и определенной Т можно написать
Для водных растворов при 25 о С, допуская равенство диэлектрических проницаемостей раствора и растворителя (78,54), h = 0,51. Для 1-1 зарядных электролитов
Большая Энциклопедия Нефти и Газа
Толщина ионной атмосферы зависит от концентрации ионов каждого рода и их валентности. Она падает с увеличением валентности ионов электролита, а по мере уменьшения концентрации электролита и повышения температуры или возрастания диэлектрической постоянной растворителя возрастает. [1]
Толщина ионной атмосферы зависит от температуры, диэлектрической проницаемости растворителя, числа и заряда ионов. Величина х непосредственно связана с термодинамическими свойствами ионов. [2]
Знание толщины ионной атмосферы необходимо для оценки не только ионной, но и диффузной компонент расклинивающего давления. [3]
Значение толщины ионной атмосферы необходимо для оценки не только ионной, но и диффузной компонент расклинивающего давления. [4]
Уменьшение толщины ионных атмосфер приводит к тому, что электростатические силы отталкивания действуют с заметной интенсивностью только на очень малых расстояниях. [5]
С ростом температуры толщина ионной атмосферы увеличивается, но при этом уменьшается диэлектрическая проницаемость, что вызывает противоположный эффект. [8]
С ростом температуры толщина ионной атмосферы увеличивается, но при этом уменьшается диэлектрическая проницаемость, что вызывает противоположный эффект. [9]
С ростом температуры Т толщина ионной атмосферы увеличивается, но при этом уменьшается диэлектрическая проницаемость е, что вызывает противоположный эффект. [10]
Как можно видеть, толщина ионной атмосферы зависит от температуры, диэлектрической проницаемости растворителя, числа ионов и их заряда. Величина х имеет большое значение в теории растворов электролитов, она непосредственно связана с термодинамическими свойствами ионов. [11]
Отношение этого расстояния к толщине ионной атмосферы k / rx / fiy служит мерой относительной несимметричности атмосферы. Приближенное значение направленной силы Aky, вызванной этой несимметричностью, получается умножением этой величины на общую силу, действующую между попом и его атмосферой. [13]
Отношение этого расстояния к толщине ионной атмосферы kyix / py служит мерой относительной несимметричности атмосферы. Приближенное значение направленной силы Aky, вызванной этой несимметричностью, получается умножением этой величины на общую силу, действующую между ионом и его атмосферой. [14]
Теория Дебая – Хюккеля позволяет рассчитывать коэффициенты активности ионов в растворах, содержащих другие ионы. Для наглядности представим себе большой многозарядный ион, например, положительно заряженную коллоидную частицу, которая помещается в раствор электролита. Вблизи этой частицы происходит перераспределение ионов, возникает избыток анионов и недостаток катионов в сравнении со средней по раствору концентрацией. Если зафиксировать это распределение, или ионную атмосферу, и убрать из раствора коллоидную частицу, то в месте, где она располагалась, обнаружится потенциал, создаваемый ионной атмосферой. Ясно, что если вернуть частицу обратно в раствор, то её энергия будет зависеть от электрического потенциала в точке, где она находится. Задача теории состоит в определении коэффициента активности (g) заряженной частицы, зависящего от энергии её взаимодействия с ионной атмосферой. Выводы теории оказываются справедливыми не только для коллоидных частиц, но и для частиц небольшого размера, включая однозарядные ионы.
Энергия взаимодействия иона со своей ионной атмосферой E равна разности химических потенциалов иона в реальном растворе (растворе с ионной силой I) и растворе с нулевой ионной силой (I = 0), который мы будем считать идеальным:
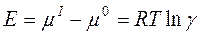
Напомним, что ионной силой раствора называется величина
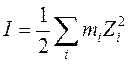
где mi – моляльная концентрация иона сорта i, Zi – его заряд.
Важно заметить, что рассчитываемый таким образом коэффициент активности учитывает неидеальность раствора, связанную только с влиянием ионной силы.
Логика дальнейшего расчёта, который мы не будем приводить полностью, состоит в следующем.
Потенциал y на расстоянии r от иона (коллоидной частицы) с зарядом Z в среде с диэлектрической проницаемостью e и нулевой ионной силой равен
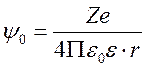
Распределение других присутствующих в растворе катионов и анионов вокруг центрального иона в таком потенциале задаётся формулой Больцмана. Потенциал, создаваемый всеми зарядами на расстоянии r от иона, можно получить, решая уравнение Пуассона. Решение для раствора с ионной силой I (моль/м 3 ) при некоторых упрощающих предположениях выглядит так:
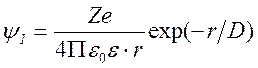
Величина D называется радиусом ионной атмосферы и равна
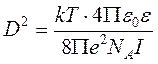
Как и следовало ожидать, присутствие ионной атмосферы приводит к тому, что потенциал вокруг центрального иона падает более быстро, чем при нулевой ионной силе, поскольку заряд центрального иона частично экранируется. При I 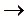
Ясно, что потенциал y а, создаваемый только ионной атмосферой без учёта вклада центрального иона, можно найти как разность величин y I и y 0.
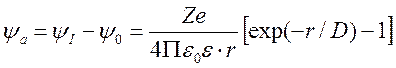
В системе CGSE эта формула выглядит так:
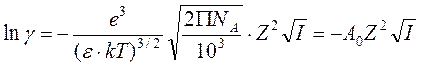
где k = 1,3810 — 16 эрг/К, e = 4,810 — 10 единиц заряда электрона в системе CGSE. В таком виде она часто фигурирует в литературе.
Если вместо натурального логарифма использовать десятичный, а ионную силу подставлять в моль/л, то для воды при 25 0 С величина A0 равна 0,509:
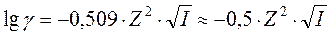
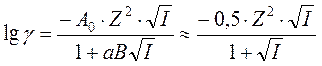
В знаменателе перед корнем стоит размерный коэффициент (aB), a – диаметр иона, В – константа, зависящая от произведения eT. Как видно из таблицы, для ионов диаметром 0,3 нм, находящихся в водном растворе, коэффициент (аВ) примерно равен единице.
Чтобы распечатать файл, скачайте его (в формате Word).