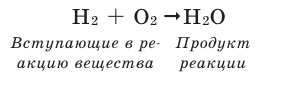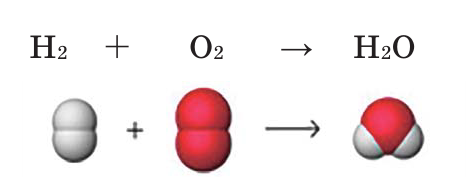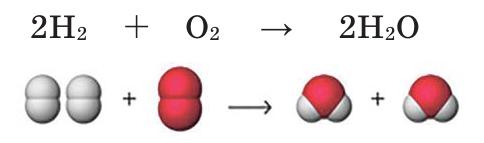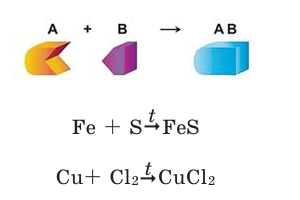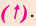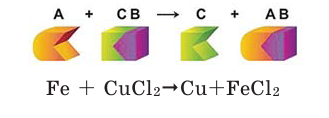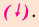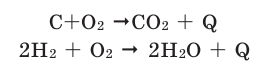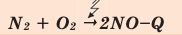Что называется химическим явлением
Изменения состояния вещества
Содержание:
Переход из одного агрегатного состояния в другое (при постоянном давлении) происходит при строго определённой температуре и всегда связан с выделением или поглощением некоторого количества тепла. Переход вещества из одного состояния в другое происходит не мгновенно, а в течении некоторого времени, когда два состояния вещества существуют одновременно в тепловом равновесии.
На странице -> решение задач по химии собраны решения задач и заданий с решёнными примерами по всем темам химии.
Изменения состояния вещества
Агрегатное состояние — состояние какого-либо вещества, имеющее определенные свойства: способность сохранять форму и объем, иметь дальний или ближний порядок и другие. При изменении агрегатного состояния вещества происходит изменение физических свойств, а также плотности, энтропии и свободной энергии.
Физические и химические явления
Вокруг нас постоянно происходят различные изменения с веществами: вода испаряется или затвердевает, осенью меняется окраска листьев у растении (разрушается хлорофилл). Эти изменения с веществами называются явлениями.
Физическими явлениями называют такие явления, при которых не происходит превращения одних веществ в другие.
Например, при переходе в газообразное состояние молекулы воды практически не изменяются и находятся на большом расстоянии (рис. 6).
Рис. 6. Испарение воды
Явления, в результате которых из одних веществ образуются другие, называются химическими явлениями, или химическими реакциями.
При химических явлениях происходит разрушение структурных частиц веществ, вступающих в реакцию, и образование новых структурных частиц, а следовательно, новых веществ.
При горении водорода в кислороде разрушаются молекулы водорода и кислорода, в результате перегруппировки атомов образуются молекулы воды (рис. 7). Метод получения сложных веществ из более простых называется синтезом (от греч. «соединять»).
Рис. 7. Образование молекулы воды
При горении угля в кислороде (рис. 8) атомы кислорода из молекул кислорода соединяются с атомами углерода и образуются молекулы углекислого газа.
Рис. 8. Горение угля
С помощью химических явлений (химических реакций) можно получать из одних веществ другие. Это — металлы, их сплавы, пластмассы, синтетические волокна, краски, лекарства, минеральные удобрения, взрывчатые вещества и др.
Сложные биохимические процессы, протекающие в живых организмах растении и человека, также связаны с различными химическими превращениями.
Обрабатывая металлы, пластмассы, стекла, волокна, можно получать различные предметы. Существует много видов обработки материалов: прокат, штамповка, литье, резание, шитье, приклеивание и многое др. Это физические явления. Физические и химические явления взаимосвязаны и играют важную роль в природе.
Кто из нас не наблюдал явления, происходящего при обрабатывании пореза раствором пероксида водорода? При попадании на кровоточащую ранку пероксид вскипает, что свидетельствует об образовании газа, а это, как вам известно, является признаком химической реакции.
Это интересно
Приготовление пищи является эндотермической реакцией, а фейерверк — экзотермической реакцией.
Знаешь ли ты?
Запах мокрой земли, который мы чувствуем после дождя, — это органическое вещество геосмин, которое вырабатывают живущие на поверхности земли цианобактерии и актинобактерии.
Любая химическая реакция сопровождается внешними признаками, по которым мы и судим о ее протекании; поглощение или выделение теплоты (иногда света), изменение окраски, появление запаха, выделение газа, образование осадка.
Признаки химических реакций
Изменение цвета. Часто химические реакции сопровождаются изменением цвета. Например, если разложить малахит, то получится черное вещество оксид меди и бесцветный углекислый газ. К примеру, каждый из вас наблюдал появление бурой ржавчины на серых стальных изделиях. В обоих случаях наблюдается изменение цвета веществ.
Осаждение. В некоторых химических реакциях появляется твердое вещество, называемое осадком (изображается 
Выделение или поглощение теплоты. В ходе протекания многих реакций происходит выделение теплоты или поглощение теплоты.
Выделение газов. В ходе некоторых реакции происходит газообразование (изображают 
Условия возникновения и течения химических реакций
Что нужно сделать, чтобы началась химическая реакция?
Прежде всего необходимо привести в тесное соприкосновение реагирующие вещества. Чем более измельчены вещества, тем теснее соприкасаются их частички, тем легче идет реакция между ними. Кусок сахара трудно зажечь, а тонко измельченный сахар на воздухе сгорает мгновенно, со взрывом (взрывы сахарной пыли происходят иногда на сахарных заводах). При растворении происходит тонкое дробление. Поэтому многие реакции проводят в растворах.
В некоторых случаях соприкосновения веществ, например железа с влажным воздухом, достаточно, чтобы происходила реакция. Но так бывает не всегда.
Например, медь не вступает в реакцию с кислородом воздуха при невысокой температуре около 20—25°С. Чтобы вызвать реакцию соединения меди с кислородом, нам пришлось бы прибегнуть к нагреванию.
На возникновение и течение химических реакций нагревание влияет по-разному. Для одних реакции требуется непрерывное нагревание. Прекращается нагревание — прекращается и химическая реакция. Это мы можем наблюдать на примере разложения сахара.
В других случаях нагревание требуется лишь для возникновения реакции, дает ей как бы толчок, а дальше реакция течет сама собой. Так происходит при горении древесины и других горючих веществ.
Таким образом, для протекания химических реакций необходимы следующие условия: соприкосновение веществ, измельчение (растворение) веществ, нагревание, применение ускорителей реакции, освещение веществ.
Изучение физических и химических явлений
Для ознакомления с физическими и химическими явлениями возьмем кусочек сахара и металлическую ложку. Вначале поместим сахар в ложку и нагреем его на пламени газовой горелки, сахар расплавится — произошло физическое явление. Если сахар продолжать нагревать, он станет коричневым — произошло химическое явление. Именно так получают карамель.
Самое важное
Различают два вила явлении: физические и химические. При физическом явлении меняются агрегатное состояние, форма вещества, а при химическом явлении происходит превращение одного вещества в другое. Химическое явление называется химической реакцией. Признаки химической реакции: появление осадка, выделение газа, выделение или поглощение тепла (энергии), появление запаха, изменение цвета вещества.
Агрегатные состояния вещества
Нас окружают различные тела. Они состоят из различных веществ. Мельчайшей частицей вещества является молекула этого вещества, она обладает всеми его химическими свойствами. Каждое конкретное вещество состоит из собственных молекул: вода — из молекул воды, кислород — из молекул кислорода. Вещества в обычных условиях находятся в различных состояниях: вода — жидкость, кислород — газ, поваренная соль — твердое. Эти состояния — твердое, жидкое и газообразное — называют агрегатными состояниями вещества. А каковы основные особенности молекулярного строения твердого, жидкого и газообразного тел? Какими свойствами будет обладать вещество в зависимости от особенностей его молекулярной структуры?
Достанем из холодильника заранее подготовленный кусочек льда, переложим его в прозрачную термостойкую посуду, начнем разогревать. В процессе мы увидим, что при нагревании лед постепенно тает, превращаясь в воду, — переходит из твердого состояния в жидкое. Этот процесс называется плавлением . Если жидкость довести до кипения и покипятить несколько минут, ее объем в колбе уменьшится. Этот процесс называется кипением. Куда делась вода? Она превратилась в пар, невидимый для глаза. Если дома оставить чашку с водой на столе, то вода также превратится в пар и без кипячения — этот процесс называется испарением, он более длительный. Когда в природе вода испаряется, мы наблюдаем образование облаков и тумана. Водяной пар — это еще одно из трех состоянии воды. Вода в обычных условиях может существовать в твердом, жидком и газообразном состоянии одновременно. Различные агрегатные состояния существуют практически у любого вещества, только наблюдать их бывает достаточно сложно.
Любое вещество, состоящее из атомов или молекул, в зависимости от условий может находиться в одном из трех агрегатных состояний: твердом, жидком, газообразном (рис. 9). Вещества могут переходить из одного агрегатного состояния в другое, и на практике это широко используется.
Рис. 9. Агрегатные состояния вещества: а — твердое; б — жидкое; в — газообразное
Молекулы любого вещества не изменяются при переходе этого вещества из одного агрегатного состояния в другое. Молекула воды в любом состоянии не изменится ни по размеру, ни по составу, также и молекула кислорода, и любая другая. Строение вещества определяется не только взаимным расположением атомов в молекулах, но и расположением этих частиц в пространстве.
Что же отличает одно агрегатное состояние вещества от другого?
Каковы особенности строения газов, жидкостей и твердых веществ?
Твердое состояние вещества
Частицы твердого вещества расположены близко друг к другу, расстояние между ними сравнимо с размером молекул. Атомы прочно связаны друг с другом и очень плотно упакованы. Они не могут удаляться друг от друга и лишь совершают небольшие колебательные движения. Вещество, находящееся в твердом состоянии, имеет наибольшую плотность, а также сохраняет объем и форму (рис. 10а).
Жидкое состояние вещества
Жидкое состояние вещества — промежуточное между твердым и газообразным. Молекулы подвижны, поэтому жидкости не сохраняют форму: они могут течь, их легко перелить (рис. 10б). Но сжать их трудно, так как при этом молекулы сближаются и между ними возникает отталкивание.
Жидкости сохраняют объем, но не сохраняют форму, принимая форму сосуда, в котором находятся.
Так, если мы возьмем литр молока или воды и перельем его из кувшина в банку, то молока в банке будет опять же литр, но оно примет уже другую форму — форму банки.
Газообразное состояние вещества
Расстояние между молекулами газа во много раз больше самих молекул, они почти не притягиваются и свободно движутся. Поэтому газы заполняют весь предоставленный объем, не имеют формы и легко сжимаются.
Рис. 10. Расположение молекул веществ: а — твердое; б — жидкое; в — газообразное
Молекулы газов движутся с огромными скоростями. Опыт с одеколоном при наблюдении явления диффузии доказывает нам это.
Скорости газов зависят не только от того, какой это газ, но и от температуры. При увеличении температуры скорости возрастают (рис. 10в).
Изменение агрегатных состояний вещества
Но как из одного состояния вещества получить другое? Нужно создать для такого перехода определенные условия.
Так. для того чтобы лед растаял, необходимо сначала нагреть его до температуры плавления льда — 0°С. Мы можем увидеть, как лед, который мы достали из холодильника, не сразу стал таять — это значит, что его начальная температура была ниже 0°С, поэтому мы его нагревали до указанной температуры. Чтобы быстро превратить воду в пар, ее необходимо вскипятить, так как вода кипит при температуре 100°С.
Температура плавления и кипения веществ
| Вещество | Температура плавления, °С | Температура кипения, °С |
| Гелий | -272 | -269 |
| Кислород | -218 | -183 |
| Вода | 0 | 100 |
| Алюминий | 660 | 2467 |
| Вольфрам | 3410 | 5555 |
Самая высокая температура кипения у вольфрама — 5555°С.
Плазма
Имеется еще и четвертое состояние вещества, которое физики склонны относить к числу агрегатных. При особых условиях вещество может находиться в плазменном состоянии. Плазма — наиболее распространенное состояние вещества в природе. Солнце, большинство звезд, туманности — это плазма. Верхняя часть земной атмосферы — ионосфера — тоже представляет собой плазму. Полярные сияния, молнии, в том числе и шаровые, — все это виды плазмы. В технике применяют плазму, например, в люминесцентных лампах.
Все процессы перехода вещества из одного состояния в другое носят определенные названия. Таких процессов шесть (схема 4).
Процесс, когда вещество из твердого состояния переходит в жидкое, называется плавлением.
Процесс перехода «жидкость—твердое вещество» называется кристаллизацией.
Процесс перехода вида «жидкость—газ» называется парообразованием.
Обратный процесс перехода вида «газ — жидкость» называется конденсацией.
Иногда бывает так, что вещество из твердого состояния сразу переходит в газ, минуя жидкую фазу. Процесс перехода из твердого состояния в газообразное называется сублимацией, или возгонкой. Любое вещество в твердом состоянии, если оно имеет запах, сублимирует.
Процесс, обратный сублимации, — десублимация.
Знаешь ли ты?
Мы считаем, что у вещества существует три агрегатных состояния. На самом же деле их как минимум пятнадцать, при этом список продолжает расти с каждым днем.
Опыт с пустой закрытой пластиковой бутылкой
Пустую пластиковую бутылку плотно закройте пробкой и поставьте в холодильник. Буквально через минуту вы увидите, что стенки бутылки втянулись вовнутрь, будто кто-то откачал из нее часть воздуха. Почему так произошло? Примет ли бутылка прежнюю форму, если ее вынуть из холодильника?
| Металлы с наибольшей плотностью | |
| Металлы |  |
| 1. Осмий | 22.59 |
| 2. Придий | 22.56 |
| 3. Платина | 21.45 |
| 4. Рений | 21.01 |
| 5. Нептуний | 20.47 |
| 6. Плутоний | 20.26 |
| 7. Золото | 19.32 |
| 8. Вольфрам | 19.26 |
| 9. Уран | 19.05 |
| 10. Тантал | 16.67 |
| Наиболее низкие температуры плавления | |
| Вещество |  |
| 1. Гелий | -272 |
| 2. Водород | -259 |
| 3. Неон | -249 |
| 4. Фтор | -220 |
| 5. Кислород | -218 |
| 6. Азот | -210 |
| 7. Аргон | -189 |
| 8. Криптон | -157 |
| 9. Ксенон | -112 |
| 10. Хлор | -101 |
Самое важное
Агрегатные состояния вещества — твердое, жидкое и газообразное. Различные агрегатные состояния существуют практически у любого вещества, только наблюдать их бывает достаточно сложно. Молекулы твердых веществ расположены близко друг к другу. Твердые вещества сохраняют форму и объем. Молекулы жидких веществ подвижны. Жидкости не сохраняют форму, они могут течь, их легко перелить, но они сохраняют объем, принимая форму сосуда, в котором находятся. Расстояние между молекулами газа во много раз больше их самих. Молекулы газа свободно движутся и заполняют весь объем, не имеют форму и легко сжимаются.
Услуги по химии:
Лекции по химии:
Лекции по неорганической химии:
Лекции по органической химии:
Присылайте задания в любое время дня и ночи в ➔
Официальный сайт Брильёновой Натальи Валерьевны преподавателя кафедры информатики и электроники Екатеринбургского государственного института.
Все авторские права на размещённые материалы сохранены за правообладателями этих материалов. Любое коммерческое и/или иное использование кроме предварительного ознакомления материалов сайта natalibrilenova.ru запрещено. Публикация и распространение размещённых материалов не преследует за собой коммерческой и/или любой другой выгоды.
физические и химические явление кратко объясните. нужно кратко и ясно
Вещества подвергаются различным изменениям, например, плавление льда, сгорания топлива, гниения травы. Эти изменения с веществами относят к физическим и химических явлений. Физическими явлениями называют такие превращения веществ, вследствие которых образуются новые соединения. К физическим явлениям относятся: изменение агрегатного состояния вещества (плавление, кипение, кристаллизация), образования звука (при взрыве), изменение цвета вещества, выделение теплоты, появление света.
Химическими называют такие явления, вследствие которых происходит изменение химического состава исходных веществ. Химические явления называются химическими превращениями, или химическими реакциями. При химических реакциях исходные вещества превращаются в другие вещества, которые проявляют иные свойства. Химические реакции могут сопровождаться внешними эффектами. К таким внешним эффектам относятся: выделение теплоты (иногда света), изменение окраски, появление запаха, образование осадка, выделение газа.
Например, при кипении воды происходит изменение агрегатного состояния воды (из жидкого в газообразное), поэтому кипения воды является физическим явлением. При скисании молока происходит биохимический процесс превращения лактозы с работодателем бактерий в молочную кислоту, поэтому скисания молока является химическим явлением. При горении свечи происходит процесс взаимодействия парафина (вещество, из которого изготавливают свечи) с кислородом, поэтому горения свечи относится к химических явлений. Однако горение (свечение) лампочки является физическим явлением.
Существует два типа явлений природы:
1) явления, при которых молекулы веществ не изменяются – физические явления;
2) явления, при которых молекулы веществ изменяются – химические явления.
Что же происходит с веществами при этих явлениях?
В первом случае молекулы сталкиваются и разлетаются, не изменившись; во втором – молекулы, столкнувшись, реагируют друг с другом, при этом одни молекулы (старые) разрушаются, а другие (новые) образуются.
Химические явления (химические реакции) – явления, при которых одни химические вещества превращаются в другие
Признаки химических явлений: появление запаха, изменение цвета вещества, появление осадка, выделение газа или резкое изменение температуры при смешивании прозрачных жидкостей
В строительстве большое количество разных строительных материалов с помощью определенных технологий превращается в здание или сооружение. Это требует знаний о свойствах строительных материалов и о процессах, происходящих при их переработке. Основой для этого являются такие естественные науки, как ФИЗИКА, ХИМИЯ, а также ЭЛЕКТРОТЕХНИКА.
При возведении здания или сооружения необходимо учитывать большое число химических и физических процессов.
2.1. Химические основы
Химия занимается построением, составом, изготовлением и свойствами материалов, а также их превращениями и происходящими при этом процессами.
Тело и вещество
Каждое тело, будучи твердым, жидким или газообразным, занимает пространство. Там, где находится одно тело, не может находиться одновременно второе тело. Каждое тело состоит из одного определенного вещества, называемого также материей. Понятия «тело» и «вещество» пересекаются и поэтому применяются часто однозначно ( 2.1).
Синтетическая оценка
Свойства веществ горючие, негорючие, кислые, пресные, вкусные, хорошо пахнущие, плохо пахнущие. ядовитые, неядовитые, устойчивые против коррозии, разъедающие, разлагающиеся, хорошо вступающие в реакции Свойства тел твердые, жедкие, газообрезные, холодные, теплые, тяжелые, легкие, большие, маленькие, покоящиеся, находящиеся в движении, в виде кубиков, цилиндрические
Каждое тело занимает определенное пространство и состоит из определенного вещества. Каждое вещество занимает пространство и образует, таким образом, тело. Тела и вещества могут различаться по своим свойствам.
СВОЙСТВА ТЕЛ в основном включают:
• форму агрегатного состояния;
• объем;
• энергетическое состояние. СВОЙСТВА ВЕЩЕСТВ в основном включают:
• способность к реакциям с другими веществами;
• запах и вкус;
• устойчивость против коррозии.
Физика занимается состоянием тел и изменением их агрегатных состояний при физических процессах. Состав веществ при этом не изменяется.
Химия занимается веществами, их составом и свойствами, а также вещественными изменениями при химических процессах.
Химические и физические процессы
Химический процесс
При химических процессах из одного или нескольких исходных материалов получаются новые вещества с полностью другими свойствами, отличными от исходных веществ. При ХИМИЧЕСКИХ ПРОЦЕССАХ возникает новое вещество.
Физический процесс
При ФИЗИЧЕСКИХ ПРОЦЕССАХ не возникает новое вещество. Изменяется агрегатное состояние, положение или величина вещества или тела. При физическом процессе изменяется состояние вещества, вещество остается прежним.
По составу материалов различаются смеси или смеси материалов, химические соединения и элементы или основные вещества.
Содержание:
Физические и химические явления:
Сравните картинки. В результате какого явления гвозди ржавеют, черешня сгнивает, а вода превращается из жидкого состояния в твёрдое или газообразное состояния. Чем отличаются эти явления друг от друга? Как это можно объяснить? Какие признаки имеют химические реакции?
Каждому из нас в повседневной жизни доводилось наблюдать, как нагретая вода, превратившись в пар, «исчезает» (переходит в состояние невидимого газа), и как этот пар при соприкосновении с холодной поверхностью предмета вновь превращается в капельки воды. Точно так же все видели превращение воды в лед в выставленной наружу в холодный морозный день посуде и обратный переход его в жидкое состояние при внесении в помещение. Образуется ли новое вещество при этих превращениях?
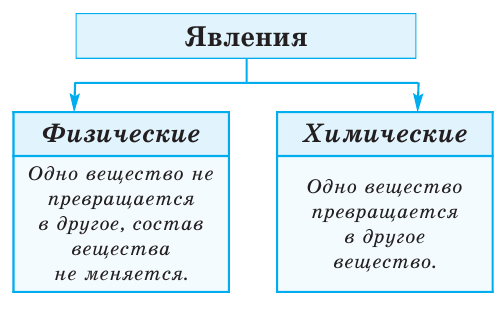
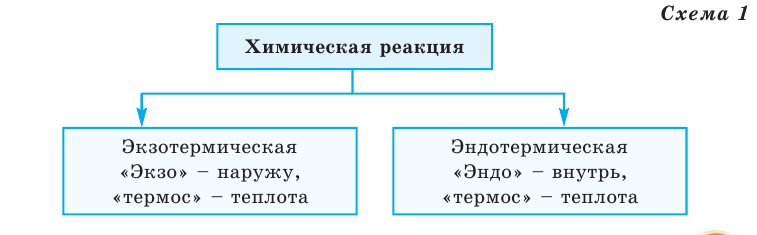
Все происходящие в природе явления делятся на 2 группы (схема 1)
Схема 1
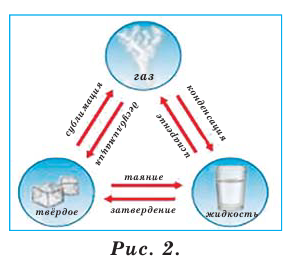
Во время физических явлений изменяются лишь агрегатное состояние, форма, размеры, объём, давление, температура и скорочть движения вещества (рис.2). Например, замерзание воды, таяние льда, кипение воды и др.
1. Нагрейте медную проволку. 2. В отстоявшуюся известковую воду с помощью трубочки вдуньте воздух или же добавьте немного раствора соды. 3. Подожгите кусочек серы размером с горошину. Что вы наблюдаете в каждом случае?
Во время химических явлений из исходного вещества образуются новые вещества. Например, такие химические явления, как горение, брожение, гниение, электролиз, разложение на составные части, ржавление (коррозия) и др. называют химическими реакциями.
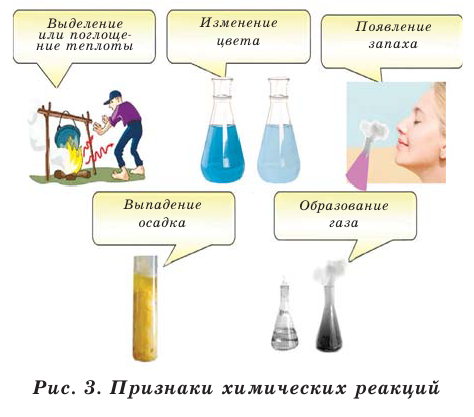
Химические реакции имеют несколько признаков. Эти признаки показывают протекание химических реакций (рис. 3).
Химические явления всегда сопровождаются физическими явлениями. Например, при горении природного газа, наряду с образованием углекислого газа и воды (химическое явление), также выделяются свет и теплота (физическое явление).
Значение физических и химических явлений
Из курса «Познание мира» вам известно, какое значение имеют физические явления, происходящие вокруг нас. Так, например, испарение воды, конденсация водяных паров и выпадение дождя составляют круговорот воды в природе. В промышленном производстве, придавая металлам, пластмассам и другим материалам определенную форму (штамповка, прокатка), получают разнообразные предметы.
Химические реакции имеют огромное значение. Ими пользуются для получения различных металлов (железа, алюминия, меди, цинка, свинца, олова и др.), а также пластмасс, минеральных удобрений, лекарственных препаратов и т.д. Выделяемая при сгорании топлива энергия используется в быту и в промышленности.
Условия начала и хода химических реакций бывают разными. Для протекания ряда реакций (например, реакций горения) достаточно соприкосновения (трения) частиц веществ и подогревания до определенной температуры. Доведение реакции до конца обеспечивается за счет выделяемой тепловой энергии.
Некоторые же реакции (например, разложение воды на кислород и водород) требуют подачи дополнительной энергии до конца.
В природе физические и химические явления (реакции) протекают непрерывно, постоянно, обеспечивая этим циркуляцию веществ, климатические изменения, условия жизни для живых организмов.
Химические уравнения. Знаки сохранения массы веществ
Происходящие в природе химические превращения в письменном виде выражают посредством химических уравнений. Условная запись химической реакции посредством формул, знаков и коэффициентов называется химическим уравнением.
Химическое уравнение составляется на основе нижеприведённых правил:
Например, составим уравнение реакции горения водорода в кислороде:
Здесь количество атомов в правой и левой частях неодинаковое. Такую запись называют схемой реакции. Для того, чтобы превратить данную схему в уравнение, следует уравнять число атомов в левой и правой частях уравнения.
Уравнивание количества атомов элементов в правой и левой частях уравнения называют коэффицированием уравнения. Определим число атомов элементов, входящих в состав веществ в реакции образования воды.
Если обратим внимание на реакцию, то увидим, что количество атомов водорода в обеих частях одинаковое. А количество атомов кислорода в правой части на единицу меньше количества атомов кислорода в левой части. Вследствие этого, вначале уравним число атомов кислорода. Для этого число атомов в правой части реакции умножается на 2, и на основе этого определяется коэффициент веществ на левой стороне.
В результате количество атомов водорода и кислорода в левой и правой частях уравнивается и получается уравнение химической реакции. 2 молекулы водорода, вступая в реакцию с 1 молекулой кислорода, образуют 2 молекулы воды.
Впервые в 1748-ом году знаменитым русским учёным М.В.Ломоносовым, и независимо от него, в 1789-ом году французским учёным А.Лавуазье был открыт закон о том, что во время химических реакций сумма масс, вступающих в реакцию веществ, равна сумме масс, полученных в результате реакции веществ.
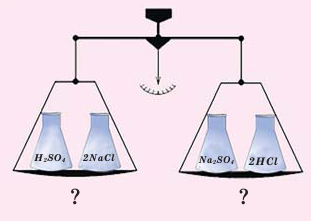
Закон сохранения массы веществ выражается следующим образом: Сумма масс веществ, вступивших в химическую реакцию, равна сумме масс веществ, полученных в результате реакции.
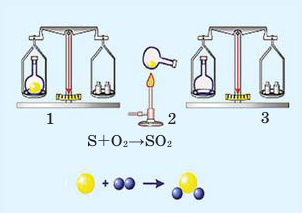
В колбу насыпают небольшое количество серы, после этого её закупоривают пробкой и взвешивают на весах (1). Затем колбу вместе с серой осторожно нагревают (2). На основе появления в колбе дыма, состоящего из частиц оксида серы (IV), можно определить протекание химической реакции.
При повторном взвешивании обнаруживается, что в результате реакции масса вещества осталась неизменной (3).
Типы химических реакций
Поместите в керамический тигель немного бихромата аммония 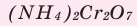
Что вы видите? Изложите свои соображения относительно происходящего процесса и запишите уравнение реакции. Почему эту реакцию называют «химическим вулканом»?
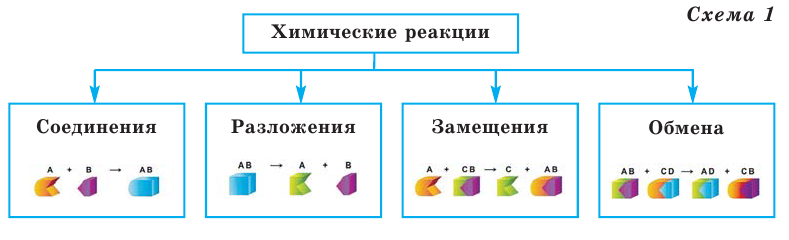
Химические реакции классифицируются по различным признакам. По количеству веществ, вступивших в реакцию и полученных в результате реакции, химические реакции подразделяются на 4 типа (схема 1):
Реакции соединения
Реакции, при которых из двух и более простых или сложных веществ получают одно сложное вещество, называют реакциями соединения.
Для протекания химических реакций иногда требуется нагревание. В таком случае в уравнениях реакций над стрелкой ставится
знак t.
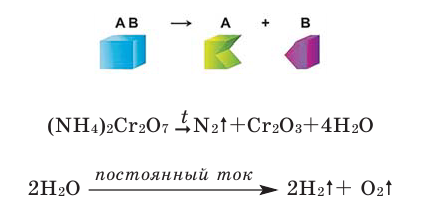
Реакции разложения
Реакции, при которых из одного сложного вещества получают два и более простых или сложных веществ, называют реакциями разложения.
Если во время реакции выделяется газ, в таком случае, рядом с её химической формулой проставляется стрелка, направленная вверх
Реакции замещения
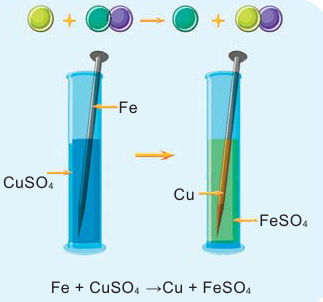
Если в реакциях, протекающих между простым и сложным веществом, атомы одного из элементов сложного вещества замещаются атомами простого вещества, то такие реакции называются реакциями замещения.
Опустите в раствор сульфата меди (II) 
Если во время реакции выпадает осадок, в таком случае, рядом с химической формулой полученного вещества проставляется стрелка, направленная вниз
Реакции обмена
Если в реакциях, протекающих между двумя сложными веществами, составные части сложных веществ, меняясь местами, образуют новые сложные вещества, то такие реакции называются реакциями обмена.
Тепловой эффект химических реакций
Наблюдаете ли вы за тем, какие изменения происходят в вашем организме во время занятий спортом, приготовления уроков и приёма пищи? Как в это время изменяется ваша энергия?
В жизни мы постоянно принимаем пищу, а также занимаемся определённой деятельностью (умственной и физической). Вначале мы, приняв пищу, увеличиваем свою энергию, а занимаясь различной деятельностью, тратим ту энергию, которую получили благодаря приёму пищи (т.е. наша энергия уменьшается), и в результате мы чувствуем себя усталыми и утомлёнными. Как и человек, каждое химическое вещество обладает определённым запасом энергии. Химические реакции веществ сопровождаются выделением или поглощением теплоты.
Количество выделяемой или поглощаемой в ходе химической реакции теплоты называется тепловым эффектом.
Тепловой эффект обозначается буквой Q, а единица его измерения — кДж. В зависимости от выделения или поглощения теплоты химические реакции делятся на 2 группы (схема 1)
Химические реакции, протекающие с выделением теплоты, называются экзотермическими реакциями. В уравнениях экзотермических реакций выделяемая теплота (Q) указывается в правой стороне реакции знаком «+» (Q>0).
Химические реакции, протекающие с поглощением теплоты, называются эндотермическими реакциями. В уравнениях эндотермических реакций поглощённая теплота указывается в правой стороне реакции знаком «— ». То есть Q
При копировании любых материалов с сайта evkova.org обязательна активная ссылка на сайт www.evkova.org
Сайт создан коллективом преподавателей на некоммерческой основе для дополнительного образования молодежи
Сайт пишется, поддерживается и управляется коллективом преподавателей
Whatsapp и логотип whatsapp являются товарными знаками корпорации WhatsApp LLC.
Cайт носит информационный характер и ни при каких условиях не является публичной офертой, которая определяется положениями статьи 437 Гражданского кодекса РФ. Анна Евкова не оказывает никаких услуг.