Что назначают при цитокиновом шторме
Почему происходит цитокиновый шторм?
На сегодняшний день у науки нет однозначного ответа не этот вопрос. В некоторых случаях речь может идти о генетической предрасположенности. Также ненормальную активность иммунной системы могут спровоцировать некоторые аутоиммуные заболевания (например, волчанка или ревматоидный артрит), а также некоторые виды терапии, которые повышают активность иммунной системы. Еще одна вероятная причина – сепсис, прием некоторых препаратов, а также некоторые вирусы.
Так, исследователи полагают, что «испанка» — разновидность гриппа, эпидемию которого мир пережил в 1918-1919 годах, вызывалась вирусом, который был способен спровоцировать цитокиновый шторм.
Какие симптомы цитокинового шторма?
Какой бы ни была причина, вызвавшая чрезмерный иммунный ответ, симптомы практически всегда одинаковые:
Но важно помнить, что для окончательной диагностики шторма необходимы лабораторные анализы крови (при гиперреакции иммунной системы будут сильно повышены С-реактивный белок и ферритин), также необходимы исследование почек и другие.
Как лечат цитокиновый шторм?
Только в реанимации. Помимо терапии лекарствами, подавляющими иммунитет, необходима постоянная поддержка организма, который при цитокиновом шторме буквально разрывается от разного рода воспалений. К сожалению, терапия далеко не всегда завершается удачей: это слишком опасное состояние, лечить которое мы пока не умеем.
Действительно ли коронавирус вызывает цитокиновый шторм?
Эта версия была очень популярна в начале пандемии коронавируса. Действительно, клиническая картина во многом напоминала повышенную активность иммунной системы: сильнейшее воспаление, которое быстро развивалось и поражало многие внутренние органы.
Цитокиновый шторм при различных вариантах течения COVID-19
В декабре 2019 года в городе Ухань, Китай, был обнаружен новый штамм коронавируса, вызывающий тяжелый острый респираторный синдром — коронавирус 2 (SARS-CoV-2). Наряду с SARS-CoV и коронавирусом, ассоциированным с ближневосточным респираторным синдромом — (MERS-CoV), SARS-CoV-2 является третьим коронавирусом, вызывающим тяжелые респираторные заболевания у людей, объединенных под названием «коронавирусная болезнь 2019 года» (COVID-19). Эта вспышка была признана Всемирной организацией здравоохранения (ВОЗ) в марте 2020 года пандемией и оказала значительное влияние на экономику и здравоохранение во всем в мире.
Хотя ситуация развивается стремительно, тяжелое течение заболевания, проявляющееся лихорадкой и пневмонией, приводящее к острому респираторному дистресс-синдрому (ОРДС), было описано в 20 % случаев COVID-19. Это напоминает течение ОРДС, вызванного синдромом выброса цитокинов (цитокиновый шторм), и вторичный гемофагоцитарный лимфогистиоцитоз, наблюдаемый у пациентов с SARS-CoV и MERS-CoV, а также у пациентов с лейкемией, получающих Т-клеточную терапию. Учитывая этот опыт, необходимо создание терапевтических средств, основанных на подавлении синдрома выброса цитокинов, таких как тоцилизумаб, которые прошли клинические испытания для лечения COVID-19.
SARS-CoV-2 — это бета-коронавирус, который наиболее тесно связан с SARS-CoV. Оба вируса используют рецептор ангиотензинпревращающего фермента, связанный с карбоксипептидазой (ACE2), чтобы проникнуть в клетки. Этот рецептор повсеместно экспрессируется в сердечной и легочной ткани, а также в некоторых кроветворных клетках, включая моноциты и макрофаги. Ключевой особенностью инфекции COVID-19 является лимфопения (низкий уровень лимфоцитов в крови), которая коррелирует с клинической тяжестью процесса. При SARS-CoV инфицируются моноциты и дендритные клетки, тогда как при MERS-CoV инфицируются моноциты и Т-клетки через дипептидилпептидазу 4 (DPP4). Возможно, что SARS-CoV-2 также поражает дендритные клетки. Апоптоз и истощение пула Т-клеток в результате нарушения процессов активации из-за дисфункции дендритных клеток может способствовать патологии иммунной системы при COVID-19. Однако лимфопения не является специфическим биомаркером неблагоприятного прогноза при COVID-19, поскольку она также является биомаркером, который коррелирует с летальным исходом в пандемии гриппа A (H1N1) 2009 года.
Было установлено, что цитокиновый шторм является основным фактором тяжелого течения SARS-CoV и MERS-CoV у пациентов. Повышенные сывороточные концентрации интерлейкина-6 (IL-6) и других провоспалительных цитокинов являются признаками тяжелого течения инфекции MERS-CoV. Синдром высвобождения цитокинов часто встречается у пациентов с COVID-19, а повышенный уровень IL-6 в сыворотке коррелирует с дыхательной недостаточностью, ОРДС и неблагоприятными клиническими исходами. Повышенный уровень C-реактивного белка (CРБ),экспрессия которого стимулируется IL-6, также является биомаркером тяжелой бета-коронавирусной инфекции.
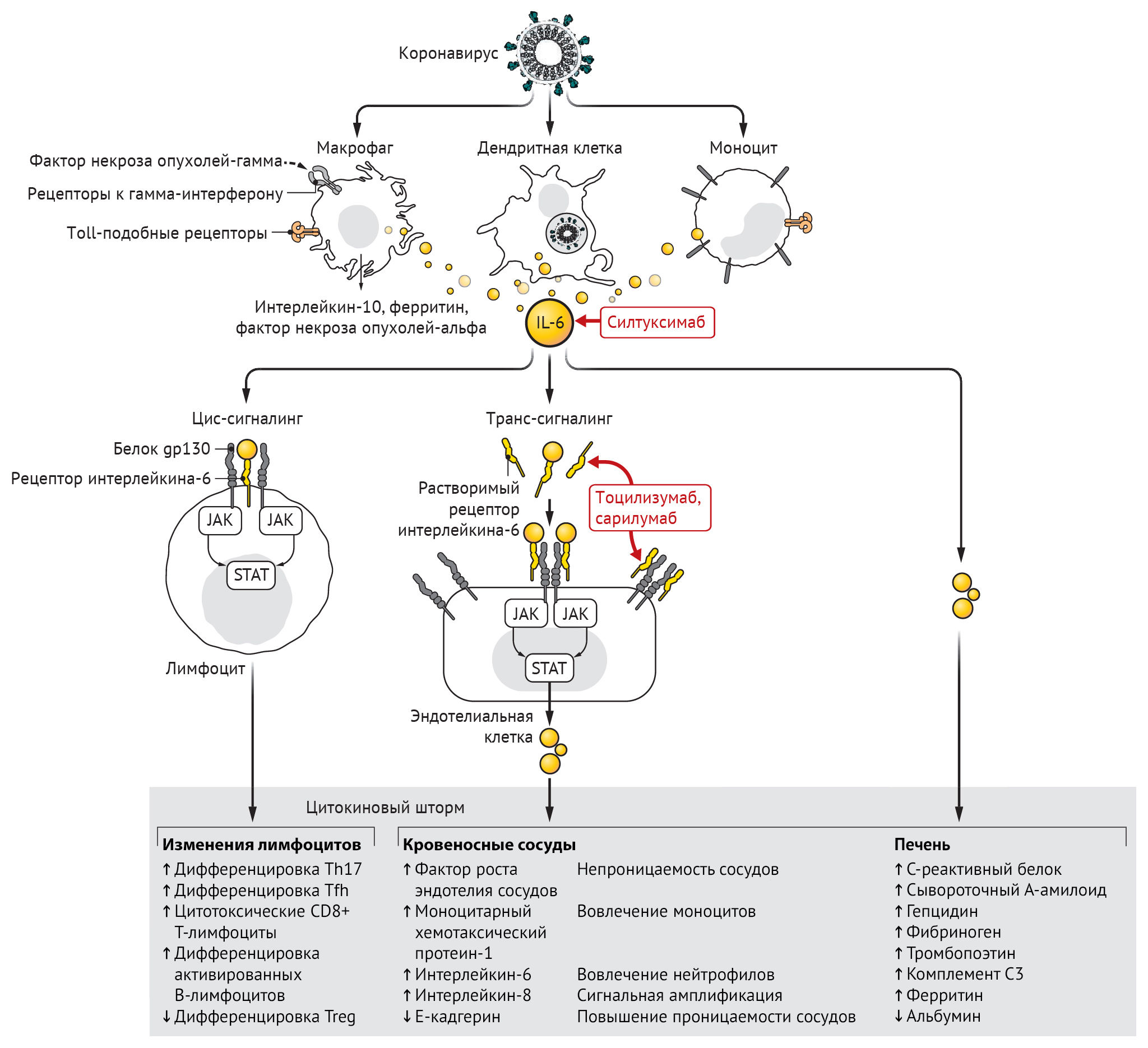
Инфицирование бета-коронавирусом моноцитов, макрофагов и дендритных клеток приводит к их активации и секреции IL-6 и других провоспалительных цитокинов. IL-6 обладает выраженными провоспалительными свойствами (см. рис. 1). IL-6 может передавать сигналы по двум основным путям, которые называются классической цис-передачей или транс-передачей. При передаче цис-сигналов IL-6 связывается с мембраносвязанным рецептором IL-6 (mIL-6R) в комплексе с gp130; нисходящая сигнальная трансдукция опосредуется, в свою очередь, JAKs (Janus kinases) и STAT3 (сигнальный преобразователь и активатор транскрипции-3). Связанный с мембраной комплекс gp130 экспрессируется повсеместно, в отличие от mIL-6R, экспрессия которого ограничена в основном иммунными клетками. Активация передачи сигналов в рамках цис-передачи приводит к плейотропным эффектам на приобретенный иммунитет (В- и Т-клетки), а также врожденную иммунную систему [нейтрофилы, макрофаги и естественные клетки-киллеры (NK)], которые могут вносить вклад в возникновение цитокинового шторма.
При передаче сигналов высокие концентрации циркулирующих IL-6 связываются с растворимой формой IL-6R (sIL-6R), образуя комплекс с димером gp130 на всех клеточных поверхностях. В результате сигнальный каскад IL-6-sIL-6R-JAK-STAT-3 активируется в клетках, которые не экспрессируют mIL-6R, таких как эндотелиальные клетки. Это приводит к системному «цитокиновому шторму», включающему секрецию сосудистого эндотелиального фактора роста (VEGF), хемоаттрактантного белка моноцитов–1 (МСР-1), IL-8 и дополнительного IL-6, а также снижение экспрессии E-кадгерина на эндотелиальные клетки. VEGF и пониженная экспрессия E-кадгерина способствуют проницаемости сосудов, которые участвуют в патофизиологии гипотонии и легочной дисфункции при ОРДС.
Вторичный гемофагоцитарный лимфогистиоцитоз — это гипервоспалительный синдром, характеризующийся высвобождением цитокинов, цитопенией (низкое количество клеток крови) и полиорганной недостаточностью (включая печеночную). У взрослых вторичный гемофагоцитарный лимфогистиоцитоз чаще всего связан с тяжелыми вирусными инфекциями, но также встречается у пациентов с лейкемией, получающих специальную Т-клеточную терапию. В дополнение к повышенным уровням цитокинов для вторичного гемофагоцитарного лимфогистиоцитоза характерны высокие уровни ферритина в сыворотке крови. Экспрессирующие CD163 макрофаги выступают в качестве источника ферритина. Учитывая их роль в передаче сигналов ретикулоэндотелиального железа, вторичный гемофагоцитарный лимфогистиоцитоз известен также как синдром активации макрофагов. Ретроспективное исследование пациентов с COVID-19 показало, что повышение сывороточного ферритина и IL-6 коррелировало с уровнем выживаемости и наблюдалось у погибших.
У пациентов, получающих CART-терапию (лечение Т-клетками химерного рецептора антигена (chimeric antigen receptor — CAR)), также могут развиться как цитокиновый шторм, так и вторичный гемофагоцитарный лимфогистиоцитоз. CART-терапия включает перепрограммирование Т-лимфоцитов пациента с целью повышения экспрессии на них молекул CAR, которые распознают антигены на опухолевых клетках. При переливании этих перепрограммированных клеток обратно пациенту они нацеливаются на опухолевые клетки, тем самым активируя противоопухолевый иммунный ответ. Эмили Уайтхед, первый пациент, получивший CD19-нацеленные Т-клетки CAR-19 с целью лечения острого лимфобластного лейкоза в 2012 году, побочным эффектом получила тяжелую форму цитокинового шторма и вторичного гемофагоцитарного лимфогистиоцитоза, что привело к развитию ОРДС, полиорганной недостаточности и гипотонии, которая была невосприимчива к стандартному лечению стероидами. Из-за значительного повышения сывороточного IL-6 у этой пациентки эмпирически было принято решение о начале терапии тоцилизумабом, антагонистом IL-6R, одобренным в то время для лечения ревматических состояний, таких как ювенильный идиопатический артрит. Она получала однократную дозу тоцилизумаба на 7-й день после введения CARТ-лимфоцитов. Спустя несколько часов у пациентки снизилась температура, после чего было принято решение об отмене лечения гипотонии и отказ от поддержки ИВЛ после разрешения ОРДС. В настоящее время тоцилизумаб с подтвержденной эффективностью и минимальными побочными эффектами у сотен пациентов одобрен Управлением по контролю за продуктами и лекарствами США (FDA) для лечения заболеваний, протекающих с синдромом цитокинового шторма, вызванного CARТ-терапией.
Эффективность антагонистов IL-6-IL-6R для лечения цитокинового шторма и вторичного гемофагоцитарного лимфогистиоцитоза подчеркивает центральную роль передачи сигналов IL-6 в патофизиологии цитокин-управляемых гипервоспалительных синдромов. Тяжелые случаи COVID-19 можно лечить как раз путем ингибирования пути IL-6, учитывая связанные с цитокиновым штормом и подобным вторичному гемофагоцитарному лимфогистиоцитозу повышения цитокинов в сыворотке крови. Действительно, предварительные результаты исследования 21 пациента с COVID-19, получавшего тоцилизумаб в Китае, обнадеживают: лихорадка спадала у всех пациентов в течение первого же дня приема тоцилизумаба. Потребность в кислороде была снижена у 75 % пациентов.
Во всем мире проводятся контролируемые клинические испытания с целью тестирования эффективности антагонистов IL-6 и IL-6R для лечения пациентов с COVID-19 с тяжелыми респираторными осложнениями. Один вопрос, который необходимо решить, заключается в том, будет ли иметь место дифференциальная эффективность между антагонистами IL-6 и антагонистами IL-6R. Относительно этого поднимается вопрос, что ингибиторы IL-6R могут подавлять как цис-, так и транс-передачу сигналов, а также транс-презентацию, недавно описанный третий способ передачи сигналов. Транс-презентация включает связывание IL-6 с mIL-6R, экспрессируемым на иммунной клетке, которая образует комплекс с gp130 на клетках T-хелпера-17 (TH17), что приводит к передаче сигналов Т-клеток вниз по каскаду, который может приводить к ОРДС. Однако ингибиторы IL-6 могут подавлять только цис- и транс-передачу сигналов. Непосредственная цель применения антагонистов IL-6 состоит в том, чтобы облегчить течение тяжелых случаев COVID-19 и свести к минимуму потребности в интенсивной терапии данных пациентов. Долгосрочная цель должна заключаться в разработке противовирусных препаратов и вакцин, которые предотвращают инфекцию или облегчают ее течение.
Есть ряд предостережений, которые необходимо брать во внимание, учитывая глобальную потребность в терапии COVID-19. При сепсис-ассоциированном ОРДС часто назначают кортикостероиды. Однако применение кортикостероидов у пациентов с SARS и MERS не улучшило показатели выживаемости и не привело к каким-либо изменениям вирусного клиренса. В результате консенсус экспертов-инфекционистов из профильных институтов и ВОЗ рекомендует клиницистам избегать системных кортикостероидов у пациентов с COVID-19 в настоящее время. Теоретическая возможность состоит в том, что подавление воспаления антагонистами IL-6 может задержать выведение вируса из организма. Однако блокада IL-6 также приводит к быстрому снижению сывороточного IL-10, иммуносупрессивного цитокина, секретируемого макрофагами, что может смягчить опасения по поводу продления клиренса вируса. Более того, одна или две дозы антагониста IL-6 вряд ли приведут к таким осложнениям, как грибковые инфекции или остеонекроз челюсти, возникающие у пациентов, которым ежемесячно вводят эти препараты для лечения хронических состояний, например, ревматоидного артрита. Примечательно, что тоцилизумаб был впервые одобрен для лечения ревматических заболеваний, а затем — цитокинового шторма у пациентов, получающих CARТ-терапию, и в настоящее время подвергается «перепрофилированию» для борьбы с пандемией COVID-19. Вполне возможно, что направленная на IL-6 терапия будет использоваться в лечении пациентов на случай будущих пандемий, вызванных другими вирусами, таких как грипп и лихорадка Эбола.
Что назначают при цитокиновом шторме
В связи с пандемией коронавируса все чаще мы стали слышать про цитокиновый шторм, который является следствием заражения вирусными инфекциями, в том числе SARS-CoV-2. Что это такое? Почему он появляется при COVID-19? Давайте разбираться вместе.
Начнем с того, что такое цитокины. Цитокины – группа информационных гормоноподобных белков и пептидов, которые выделяются клетками иммунной системы и некоторыми другими. При атаке вирусной инфекции, организм начинает усиленно вырабатывать эти молекулы. Они выполняют четыре функции:
• управляют различными иммунными реакциями (гомеостаз, восстановление);
• регулируют гемопоэз (кровотворение).
Избыточная выработка цитокиновых молекул приводит к цитокиновому шторму.
Цитокиновый шторм – агрессивная иммунная реакция организма на вирусную инфекцию и лекарственные препараты, влекущее за собой системное воспаление и нарушение правильной работы иммунитета. При цитокиновом шторме в организме нарушается функция свертываемости крови, вырабатывается избыточное количество медиаторов воспаления, а также очагов разрушения собственных клеток и тканей. При усилении этих процессов иммунная реакция становится неконтролируемой – интерфероны, хемокины, ФНО (факторы некорза опухоли) и другие молекулы из группы цитокинов начинают активно высвобождаться.
При развитии цитокинового шторма, в ответ на атаку вируса, возникает иммуно-воспалительная реакция, из-за которой уровень цитокинов резко возрастает – именно поэтому заболевание имеет в названии слово «шторм». Лимфоциты атакуют не только инфекционный возбудитель, но и жизненно важные клетки, в результате чего прекращается работа целых органов.
Главная опасность цитокинового шторма при COVID-19 – иммунная недостаточность, т.к. она облегчает присоединение бактериальных инфекций. Воспалительный процесс и системное повреждение тканей может привести к нарушению работы внутренних органов и смерти.
На данный момент механизм развития цитокинового шторма до конца не изучен, однако COVID-19 является одной из причин его возникновения. Вы можете постараться избежать заражения путем вакцинации и соблюдения всех мер предосторожности. Будьте здоровы.
Цитокиновый шторм
Цитокиновый шторм (гиперцитокинемия) — агрессивная иммунная реакция организма на вирусную инфекцию и лекарственные препараты, в ходе которой активно продуцируются пептидные молекулы — цитокины, развивается обширное системное воспаление, нарушается правильная работа иммунитета.
Цитокинами называют группу информационных гормоноподобных белков и пептидов, которые выделяются клетками иммунной системы и некоторыми другими. При атаке вирусной инфекции, организм начинает усиленно вырабатывать эти молекулы. Они выполняют четыре функций:
Избыточная и неконтролируемая выработка цитокиновых молекул наблюдается при коронавирусных, бактериальных инфекциях, токсическом воздействии некоторых лекарств, опухолевых процессах. Агрессивная ответная реакция иммунитета при цитокиновом шторме вызывает нарушение свертываемости крови, выработку избыточного количества медиаторов воспаления, очаговое разрушение собственных клеток и тканей.
По мере интенсификации этих процессов агрессивная иммунная реакция становится неконтролируемой — активно высвобождаются интерфероны, хемокины, ФНО (факторы некроза опухоли) и другие молекулы из группы цитокинов.
Развитие цитокинового шторма
Первично в ответ на атаку вируса или иного патогенного микроорганизма возникает иммунно-воспалительная реакция — уровень цитокинов возрастает настолько резко и стремительно (шторм, гиперцитокинемия), что атака иммунных клеток (лимфоцитов) приходится не только на враждебный инфекционный возбудитель, но и на родные жизненно важные клеточные компоненты. В результате они погибают, прекращается работа целых органов.
Симптомы цитокинового шторма
Симптомы проявляются по-разному, в зависимости от органов и целых систем, подверженных обширному воспалительному процессу. К общим симптомам относятся:
К специфическим для разных органов:
Цитокиновый шторм при коронавирусе
В 2020 году было выявлено, что наименее благоприятный прогноз у пациентов, больных коронавирусом SARS-CoV-2 с признаками нарушения пневмотизации легких, связан с развитием «цитокинового шторма» и обострением острого респираторного дистресс-синдрома (ОРДС). Обширный воспалительный процесс и системное повреждение тканей могут привести к нарушению работы внутренних органов и смерти.
Выявлены индикаторы, которые позволяют прогнозировать развитие цитокинового шторма у 70% пациентов:
Цитокиновый шторм при коронавирусе приводит к иммунной недостаточности, облегчая присоединение бактериальной инфекции.
Механизм развития цитокинового шторма еще недостаточно изучен. Это генерализованное поражение организма, возникающее вследствие агрессивного ответа иммунной системы может проявиться и у абсолютно здорового человека на фоне других инфекций, ревматических, аутоиммунных, онкологических заболеваний (например, при свином гриппе, туберкулезе, пневмонии, сепсисе — заражении крови.
Текст подготовил
Котов Максим Анатольевич, главный врач центра КТ «Ами», кандидат медицинских наук, доцент. Стаж 19 лет
Если вы оставили ее с 8:00 до 22:00, мы перезвоним вам для уточнения деталей в течение 15 минут.
Если вы оставили заявку после 22:00, мы перезвоним вам после 8:00.
О лечении полиорганной недостаточности при COVID-19 рассказали в Сеченовском Университете

Согласно патогенезу, «цитокиновый шторм» является опосредованным последствием влияния коронавируса на иммунную систему человека. Шанс его возникновения может повыситься в случае тяжёлого течения заболевания и заражения побочными бактериальными инфекциями. А также другими факторами – средне-тяжёлым или тяжёлым течением заболевания, склонностью к тромбообразованию и быстрое прогрессирование болезни. Впоследствии он может привести к многочисленным осложнениям даже при успешном его погашении – для лёгких, сердца, сосудов и других органов.
«Краеугольным камнем в лечении коронавирусной инфекции является поддержание гипокоагуляции. Посредством прямого или опосредованного действия вируса выявляется склонность к тромбообразованию. Здесь в каждом учреждении необходимо использовать индивидуальный подход, руководствуясь рекомендациями, которые мы имеем на данный момент», – объяснил Борислав Силаев.
Он также напомнил, что необходимо проводить компьютерную томографию хотя бы раз в 7 суток, чтобы отследить динамику заболевания и потенциальные риски.
При лечении бактериального воспаления при коронавирусной инфекции важно знать о риске возникновения цитокинового шторма и своевременно проводить скрининг двух белков – прокольцитонина и C-реактивного белка. Диагностическими критериями возникновения цитокинового шторма являются нормальный или сниженный уровень прокальцитонина, фебрильная лихорадка, прогрессирующая полиорганная недостаточность, а также специфические показатели анализа крови.
Цитокиновый шторм – опасное явление, которое можно лечить как медикаментозно, так и экстрапорально. Но предпочтительнее не допускать его возникновения, и принимать меры для его предотвращения, подчеркнул эксперт.
Код вставки на сайт
О лечении полиорганной недостаточности при COVID-19 рассказали в Сеченовском Университете

Согласно патогенезу, «цитокиновый шторм» является опосредованным последствием влияния коронавируса на иммунную систему человека. Шанс его возникновения может повыситься в случае тяжёлого течения заболевания и заражения побочными бактериальными инфекциями. А также другими факторами – средне-тяжёлым или тяжёлым течением заболевания, склонностью к тромбообразованию и быстрое прогрессирование болезни. Впоследствии он может привести к многочисленным осложнениям даже при успешном его погашении – для лёгких, сердца, сосудов и других органов.
«Краеугольным камнем в лечении коронавирусной инфекции является поддержание гипокоагуляции. Посредством прямого или опосредованного действия вируса выявляется склонность к тромбообразованию. Здесь в каждом учреждении необходимо использовать индивидуальный подход, руководствуясь рекомендациями, которые мы имеем на данный момент», – объяснил Борислав Силаев.
Он также напомнил, что необходимо проводить компьютерную томографию хотя бы раз в 7 суток, чтобы отследить динамику заболевания и потенциальные риски.
При лечении бактериального воспаления при коронавирусной инфекции важно знать о риске возникновения цитокинового шторма и своевременно проводить скрининг двух белков – прокольцитонина и C-реактивного белка. Диагностическими критериями возникновения цитокинового шторма являются нормальный или сниженный уровень прокальцитонина, фебрильная лихорадка, прогрессирующая полиорганная недостаточность, а также специфические показатели анализа крови.
Цитокиновый шторм – опасное явление, которое можно лечить как медикаментозно, так и экстрапорально. Но предпочтительнее не допускать его возникновения, и принимать меры для его предотвращения, подчеркнул эксперт.