Что находится в белковой головке бактериофага
Что в голове у бактериофага

Геном фага Т4 огромен, он содержит 168 903 пар нуклеотидов — всего в 30 раз меньше, чем геном его хозяина, кишечной палочки Escherichia coli. Для сравнения, длина генома папилломавируса человека — 8000 пар нуклеотидов. Что же кодирует такая длинная ДНК бактериофага и как она вообще умещается в головку вируса?
Фаг Т4 — один из самых сложно устроенных вирусов. Он несет в своей ДНК около 300 белок-кодирующих генов, причем из них только 69 необходимы ему для выживания в стандартных условиях лаборатории. Большинство белков фага Т4 не похожи на известные белки других организмов. Но есть и такие, чьи родственники найдены у прокариот и эукариот. Функции многих белков этого вируса до сих пор не установлены, одна только головка состоит по крайней мере из 12 типов белков. Кроме белков, ДНК бактериофага кодирует несколько транспортных РНК и коротких регуляторных РНК — свойство, обычное для самостоятельных организмов, но не распространенное среди вирусов.

Модель бактериофага Т4, разными цветами показаны белки. От головки вируса отходит длинная трубка — белковый чехол хвоста. Снизу к чехлу прикреплена базальная пластинка с шипами (фиолетовая), от которой отходят «ножки» — фибриллярные нити, с их помощью вирус удерживается на бактерии. Когда бактериофаг закрепляется на клеточной стенке жертвы, чехол сокращается, находящийся внутри стержень пробивает стенку и впрыскивает нуклеиновую кислоту из головки внутрь клетки бактерии. Изображение с сайта prophage.blogspot.com
В ходе инфекции бактериофаг Т4 полностью переключает работу клеточных систем хозяина на свои нужды. В этом паразиту помогают собственные ферменты для синтеза нуклеотидов, репликации (удвоения) и репарации (починки от повреждений) ДНК и множество других белков. Например, у Т4 есть белок, который попадает в бактерию вместе с ДНК фага и на ранних этапах инфекции модифицирует РНК-полимеразу (основной белок транскрипции — «переписывания» генетической информации с ДНК на РНК) бактерии так, что фермент охотнее взаимодействует с ДНК вируса, чем с ДНК клетки. Это способствует синтезу белков, необходимых фагу в начале инфекции. Позже другой белок модифицирует полимеразу так, что она начинает охотнее взаимодействовать с генами фага Т4, нужными на следующем этапе. И наконец, после очередной модификации, РНК-полимераза бактерии начинает взаимодействовать с так называемыми «поздними» генами Т4.
Другой интересный пример — белок, который встраивается во внутреннюю мембрану клетки-хозяина (у кишечной палочки, как у любой уважающей себя грамотрицательной бактерии, есть две клеточные мембраны) и не дает генетической информации других бактериофагов попасть внутрь. Есть у Т4 и белки, разрезающие ДНК бактерии-хозяина и проникших в нее других бактериофагов. С ДНК Т4 эти белки они не связываются, поскольку в ее состав вместо нуклеотида цитозина входит модифицированный гидроксиметилцитозин.
Отдельного внимания заслуживают белки, необходимые для синтеза новых вирионов (вирусных частиц) и для упаковки в них ДНК. Более 40% белков фага Т4 вовлечены в сборку вириона, состоящего из головки и сокращающегося хвоста с хвостовыми нитями для прикрепления к бактерии. Вирион устроен так сложно, что у Т4 есть специальные «белки строительных лесов», создающие каркас для сборки головки и удаляющиеся из нее при созревании.
Пока точно не известно, каким образом настолько огромная молекула ДНК укладывается в вирусной головке. Зато известно, что она затаскивается внутрь действием белкового «мотора», что сопряжено с гидролизом «энергетической молекулы» — АТФ. Весь геном Т4 проталкивается в головку за пять минут.
Современная модель упаковки ДНК в головку бактериофага Т4
Ученые уже пытаются «научить» Т4 упаковывать в свою головку чужеродные нуклеиновые кислоты или белки. Предполагают, что таким образом можно доставлять молекулярные грузы в конкретные эукариотические клетки.
О криоэлектронном микросопе см. также:
Нобелевская премия по химии — 2017, «Элементы», 12.10.2017.
О бактериофагах см. также:
Бактериофаги: 100 лет на службе человечеству, «Наука из первых рук» №4, 2016.
Пожиратели бактерий, «Популярная механика» №10, 2013.
Что находится в белковой головке бактериофага
ГОУ ВПО “Первый МГМУ им. И.М. Сеченова” Минздравсоцразвития РФ, Москва
Бактериофаги (от слов “бактерия” и греч. phagos – пожирающий; БФ), или фаги, – специфические вирусы бактерий, вызывающие их лизис (разрушение клеток) или изменяющие их свойства. Они впервые были обнаружены микробиологами Ф. Туортом (1915) в Великобритании и Ф. д’Эрелем (1917) во Франции. Однако изучить их морфологию удалось только после изобретения электронного микроскопа.
Биология бактериофагов
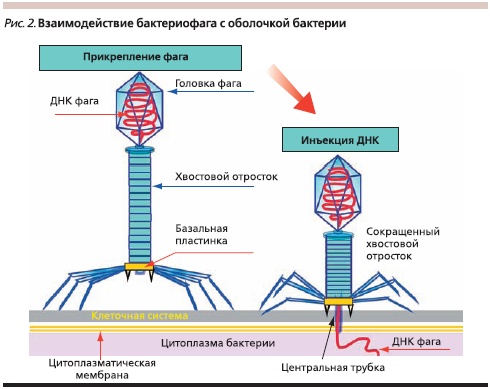
БФ состоят из белка – капсида, защищающего один тип нуклеиновой кислоты (ДНК или РНК, одно или двунитевые). Различают БФ с длинным отростком, имеющие сокращающийся или несокращающийся чехол, а также БФ с короткими отростками, аналогами отростков, без отростков и нитевидные (рис. 1, 2). Размер БФ колеблется от 20 до 800 нм (у нитевидных форм). БФ, имеющие форму сперматозоида, достигают до 200 нм длиной, состоят из хвостового отростка и головки икосаэдрического типа, содержащей нуклеиновую кислоту. Капсид головки и чехол хвостового отростка БФ состоят из полипептидных субъединиц, уложенных по икосаэдрическому (головка) или спиральному (отросток) типу симметрии. Хвостовой отросток имеет внутри полую трубку (стержень), через которую при инфицировании нуклеиновая кислота фага проходит из головки в бактерию. Чехол отростка заканчивается шестиугольной базальной пластинкой с шипами, от которых отходят фибриллы (нити). Базальная пластинка и хвостовые фибриллы участвуют в прикреплении БФ к бактериальной ячейке. Не все БФ имеют базальные пластинки и хвостовые фибриллы. В зависимости от жизненного цикла БФ могут быть вирулентными (литическими) или умеренными.
Вирулентные (литические) БФ для внедрения в бактерию адсорбируются на специфических рецепторах клетки, в т. ч. на липополисахариде, липопротеине, тейхоевых кислотах, протеинах, или даже на пилях. Специфичность рецепторов означает, что БФ может инфицировать только определенные бактерии. Попав в бактерию, БФ репродуцируется, формируя 200–500 фаговых частиц, и вызывает гибель бактерии. Это продуктивный (литический) тип взаимодействия. БФ с сокращающимся чехлом адсорбируются на клеточной стенке с помощью фибрилл хвостового отростка. Чехол хвостового отростка сокращается, и стержень с помощью ферментов (лизоцима) как бы просверливает оболочку клетки. Через канал трубки БФ нуклеиновая кислота инъецируется из головки в бактериальную клетку, а капсид БФ остается снаружи бактерии (рис. 2). Нуклеиновая кислота БФ направляет синтез его ферментов. При этом инактивируются ДНК и РНК хозяина. Нуклеиновая кислота БФ реплицируется и направляет синтез новых белков капсида. Происходят самосборка капсида вокруг фаговой нуклеиновой кислоты и формирование БФ, которые выходят из бактерии в результате ее лизиса, выталкивания или в некоторых случаях почкованием. Из бактерии высвобождается 200–1000 новых БФ, которые инфицируют другие бактериальные клетки.
Умеренные БФ взаимодействуют с бактериями по продуктивному или интегративному типу. Продуктивный тип умеренного фага, как и у вирулентных фагов, заканчивается лизисом бактерий. При интегративном типе ДНК умеренного фага встраивается в хромосому бактерии, реплицируется синхронно с бактериальным геномом, не вызывая ее лизиса (передается при делении бактерии). ДНК фага, встроенная в хромосому бактерии, называется профагом, а культура бактерий – лизогенной, сам процесс – лизогенией (от греч. lysis – разложение, genea – происхождение).
Хромосома умеренного фага лямбда, введенная в бактерию, вызывает либо лизис, либо лизогенизацию (проникшая в бактерию ДНК умеренного фага приобретает форму кольца и интегрирует в строго определенную область хромосомы). Ультрафиолетовое облучение индуцирует литический процесс с выходом фага. При лизогении фаги не образуются в результате “выключения” фаговых генов репрессором, кодируемым одним геном фага.
Профаги могут спонтанно или под действием индуцирующих агентов (ультрафиолетовые лучи, митомицин С и др.) дерепрессироваться, исключаться из хромосомы. Этот процесс заканчивается продукцией фагов (индукцией профага) и лизисом бактерий. Профаг придает бактерии новые свойства, что получило название фаговой конверсии (лат. conversio – превращение). Конвертироваться могут морфологические, культуральные, биохимические, антигенные и другие свойства бактерий. Например, наличие профага в холерном вибрионе обусловливает его способность продуцировать холерный экзотоксин.
БФ применяют для профилактики, лечения инфекций, а также для диагностики (например, для фаготипирования с целью выявления источника инфекции). Кроме того, БФ используют в генной инженерии в качестве векторов, переносящих участки ДНК; возможна также естественная передача генов между бактериями посредством трансдукции.
Фаготипирование – один из методов эпидемиологического маркирования. Применяется для выявления источника инфекции. Выделение бактерий одного фаговара от разных больных указывает на общий источник их заражения. При внутривидовой идентификации бактерий, т. е. при определении фаговара (фаготипа) бактерий с помощью фаготипирования, на чашку Петри с плотной питательной средой, засеянную чистой культурой возбудителя в виде “газона”, наносят капли различных диагностических типоспецифических фагов. Бактерии, чувствительные к фагу, лизируются (образуется стерильное пятно, “бляшка”, или т. н. негативная колония фага).
БФ – уникальное явление; они участвуют в разнообразных процессах:
Получение эффективных лечебно-профилактических БФ связано с тщательным и постоянным поиском штаммов с широким спектром (валентностью) действия на бактерии и высокой степенью их литической активности. Литическая активность и, следовательно, лечебная, а также профилактическая эффективность препаратов БФ зависят от видовой, инфравидовой принадлежности возбудителя, его рецепторных особенностей и факторов его микроокружения. Например, антитела и другие гуморальные белки могут заблокировать участки связывания бактерий с БФ, что исключает возможность парентерального введения последних. Кроме того, возможно быстрое формирование резистентности бактерий к применяемым БФ. Для получения лечебного эффекта при неблагоприятных бактериальных ассоциациях препараты БФ выпускают либо поливалентными, направленными против различных видов и сероваров одного возбудителя, либо комбинированными, содержащими БФ против различных видов возбудителя.
БФ не вызывают побочных реакций, не нарушают нормальную микрофлору. При дисбактериозе, нарушениях функций кишечника, обусловленных развитием местных воспалительных процессов, подавлении резидентной микрофлоры, происходит активация ряда условно-патогенных микроорганизмов и транзиторной микрофлоры. Эти обстоятельства поднимают значимость селективной деконтаминации, проводимой с помощью антибиотиков направленного действия и литических БФ.
БФ, обладая специфичностью действия против определенных возбудителей острых кишечных инфекций, могут также вносить вклад в развитие оральной толерантности. Известно, что организм человека проявляет пероральную (региональную) толерантность к собственной нормальной микрофлоре. Эта толерантность обусловлена блокадой активации сигнальных рецепторов (например, толл-подобных рецепторов – TLR и др.) к компонентам микрофлоры человека и активностью регуляторных T-лимфоцитов (Treg), которых в свою очередь активируют NKT-клетки (natural killer T cells). Компоненты (паттерны) БФ и разрушенных ими бактерий могут активировать определенные сигнальные рецепторы клеток организма, стимулирующие синтез антимикробных пептидов, подавляющих развитие наиболее агрессивных микробов (рис. 3). Срыв оральной толерантности влечет развитие различных нарушений, в т. ч. хронического гастрита, болезни Крона, неспецифического язвенного колита, некротизирующего энтероколита у детей, язвенной болезни желудка и двенадцатиперстной кишки.
Препараты БФ хранят при температуре 2–10 °С в сухом темном месте. БФ чувствительны к ультрафиолетовым лучам; даже их непродолжительное пребывание на свету приводит к утрате литической активности. Для защиты БФ от действия желудочного сока их выпускают в капсулах или таблетках, покрытых кислотоустойчивой оболочкой. Материалом защитного покрытия является нетоксичная целлюлоза, эстерифицированная уксусной и фталевой кислотами, образующая гладкую прозрачную пленку. Для детей из-за проблем проглатывания таблеток используют пектиновое покрытие. Пектин, обволакивая БФ, защищает их от разрушающего действия желудочного сока.
Нормализация микрофлоры, возможное участие БФ в поддержании колонизационной резистентности и оральной толерантности обеспечивают стабилизацию гуморального и клеточного звеньев иммунитета. Изредка применение БФ совпадает с ухудшением качества стула из-за массовой гибели чувствительных к нему бактерий. В этом случае для уменьшения интоксикации целесообразно назначать на ночь энтеросорбент – не ранее 3–4 часов после последнего приема БФ.
Препараты бактериофагов против возбудителей кишечных инфекций
Интести-бактериофаг жидкий содержит стерильные фильтраты фаголизатов шигелл (S. flexneri сероваров 1, 2, 3, 4, 6 и S. sonnei), сальмонелл (S. paratyphiA, S. paratyphiB, S. typhimurium, S. choleraesuis, S. infantis, S. oranienburg, S. enteritidis), энтеропатогенных кишечных палочек наиболее этиологически значимых сероваров (Escherichia coli О111, О55, О26, О125, О119, О128, О18, О44, О25, О20), протея (вульгарис и мирабилис), стафилококков, энтерококков и синегнойной палочки (Pseudomonas aeraginosa). Интести-бактериофаг (Bacteriophagum intestinalis fluidum) представляет собой прозрачную жидкость желтого цвета различной интенсивности.
Препарат предназначен для лечения и профилактики заболеваний желудочно-кишечного тракта, вызванных вышеуказанными бактериями, их сочетанием (в т. ч. бактериальной дизентерии, сальмонеллеза, брюшного тифа, паратифа, дисбактериоза, энтероколита, колита, диспепсии). Его назначают в остром периоде болезни: монотерапия при легких и стертых формах, при бактериовыделении; комбинированная терапия с другими антибактериальными средствами (при среднетяжелом течении) или иммуномодуляторами (при затянувшемся бактериовыделении). Залогом эффективности использования интести-бактериофага является определение фагочувствительности возбудителя и раннее применение препарата, который назначают перорально или ректально при помощи клизмы. Перорально интести-бактериофаг назначают 3–4 раза в сутки натощак за 1,0–1,5 часа до еды в течение 7–10 дней и в разовой дозе: детям до 6 месяцев – 5–10 мл, 6–12 месяцев – 10–15 мл, 1–3 года – 15–20 мл, старше 3 лет – 20 – 40 мл (см. таблицу). Для детей первых месяцев жизни назначенный препарат в первые двое суток разводят кипяченой водой в 2 раза. Если побочные осложнения отсутствуют (срыгивания, высыпания на коже), препарат назначают неразведенным. Перед приемом интести-бактериофага детям старше 3 лет и взрослым назначают раствор питьевой соды (0,5 чайной ложки на 0,5 стакана воды) или щелочную минеральную воду. В отсутствие колитического синдрома препарат назначают ректально 1 раз в день после опорожнения кишечника.
Бактериофаг дизентерийный поливалентный (в таблетках с кислотоустойчивым покрытием и в свечах) содержит стерильные фильтраты фаголизатов шигелл (S. flexneri и S. sonnei). Применяют с 6-месячного возраста для лечения и профилактики бактериальной дизентерии. Для лечения его применяют перорально 3 раза в сутки за час до еды в течение 5–7 дней и в разовой дозе: для детей от 6 месяцев до 3 лет – по 1 таблетке, 3–8 лет – по 1–2 таблетки, старше 8 лет – 2–3 таблетки. При слабовыраженном колитическом синдроме и в период реконвалесценции третий прием БФ внутрь можно заменить его ректальным применением: с 6 месяцев до 3 лет – 20–40 мл, с 3 до 8 лет – 40–60 мл, старше 8 лет – 60–80 мл.
С профилактической целью рекомендуют ежедневный прием препарата в зависимости от возраста: по 10–40 мл или 1–2 таблетки.
Бактериофаг сальмонеллезный групп A, B, C, D, E в таблетках с кислотоустойчивым покрытием, в свечах, жидкий содержит стерильные фильтраты фаголизатов сальмонелл (S. paratyphi A, S. paratyphi B, S. typhimurium, S. heidelberg, S. newport, S. choleraesuis, S. oranienburg, S. infantis, S. dublin, S. enteritidis, S. anatum, S. newlands). Для лечения его применяют перорально 3 раза в день за час до еды в течение 7–10 дней и в разовой дозе: для детей 6–12 месяцев – по 0,5 таблетки; 1–3 лет – по 0,5–1,0; 3–8 лет – по 1,0; старше 8 лет – по 2 таблетке. Третий пероральный прием можно заменить ректальным введением препарата. С профилактической целью БФ назначают детям по 1 таблетке и взрослым по 2 таблетке 2 раза в неделю.
Бактериофаг брюшнотифозный в таблетках с кислотоустойчивым покрытием содержит стерильный фильтрат фаголизата сальмонелл брюшного тифа (S. typhi). Препарат назначают для профилактики брюшного тифа внутрь за час до еды детям от 6 месяцев до 3 лет по 1 таблетке, а старше 3 лет и взрослым – по 2 таблетке 1 раз в 3 дня или каждый день до выздоровления.
Бактериофаг колипротейный жидкий содержит стерильные фильтраты фаголизатов энтеропатогенных (диареегенных) кишечных палочек (Escherichia coli наиболее распространенных серологических групп O20, O26, O33, O44, O55, O111, O119, O26, O124, O125, O127, O151), Proteusvulgarisи Proteusmirabilis. Препарат предназначен для лечения и профилактики заболеваний, вызванных вышеуказанными бактериями, а также дисбактериоза.
Сфера применения других препаратов бактериофагов многообразна; они используются как для местного применения (“раневые” бактериофаги), так и для приема перорально или ректально, в т. ч. в зависимости от формы выпуска:
В заключение следует отметить, что БФ и препараты БФ характеризуются многими положительными сторонами, они:
Информация об авторах:
Быков Анатолий Сергеевич – доктор медицинских наук, профессор кафедры микробиологии,вирусологии и иммунологии ГОУ ВПО “Первый МГМУ им. И.М. Сеченова” Минздравсоцразвития РФ.
Тел. 8 (495) 629-75-79, e-mail: bykov@imail.ru;
Быков Сергей Анатольевич – кандидат медицинских наук, ассистент кафедры клиническойиммунологии и аллергологии ГОУ ВПО “Первый МГМУ им. И.М. Сеченова” Минздравсоцразвития РФ.
Литература
1. Атлас по медицинской микробиологии, вирусологии и иммунологии / 2-е изд. Под ред. А.С. Быкова, А.А. Воробьева, В.В. Зверева. М., 2008. C. 272.
2. Дарбеева О.С., Жиленков Е.Л. Бактериофаги. Общая и санитарная микробиология с техникой микробиологических исследований: учебное пособие / Под ред. А.С. Лабинской, Л.П. Блинковой, А.С. Ещиной. М., 2004. C. 576.
3. Урсова Н.И., Минухина А.М. Бактериофаги. Клинико-иммунологическая эффективность иммунобиологических препаратов / Под. ред. М.П. Костинова, Н.В. Медуницина. М., 2008. C. 256.
Что такое бактериофаги простыми словами
В 1928 году британский бактериолог Александр Флеминг вернулся из отпуска в Шотландии в свою лабораторию в Лондоне и обнаружил, как в одной из чашек Петри бурно разрослась колония плесневых грибов (Penicillium notatum). С выделением пенициллина началась эра антибиотиков.
С тех пор антибиотики спасли миллионы жизней по всей планете. Флеминг также обнаружил, что бактерии обладали устойчивостью к антибиотикам, если действовали малым количеством пенициллина, либо если антибиотик употреблялся слишком короткое время.
Алмрот Райт предсказал устойчивость к антибиотикам еще до того, когда это было обнаружено экспериментально. Бактериальная резистентность — явление естественное по своей природе, а потому неизбежное.
Вот уже более десятка лет Всемирная организация здравоохранения, Центр по контролю заболеваний в США, многие крупные эксперты в России открыто признают, что мы вступили в так называемую пост антибиотиковую эру.
В 2016 году в США зафиксирован случай заражения человека одной из разновидностей энтеробактерий. Штамп оказался устойчивым к воздействию тетрациклина, колистина, ко всем до единого из 26 видов антибиотиков, представленных на рынке. Женщину так и не удалось спасти.
Ученые по всему миру продолжают изучать явление резистентности в надежде минимизировать угрозы. Однако одной из самых подходящих альтернатив можно назвать препараты (комбинированные или моно) на основе бактериофагов.
Бактериофаги являются важнейшим компонентом нашей продукции и помогают при профилактике бактериальных заболеваний и борьбе с ними. Название звучит непривычно и немного непонятно. На самом деле, с бактериофагами люди знакомы уже более ста лет.
Бактериофаг в переводе с греческого означает «пожиратель бактерий». Не самое доброе «существо», но в действительности никто никого не пожирает. Бактериофаги — это природные агенты, которые естественным образом ограничивают размножение бактерий. Они способны избирательно устранять только те бактерии, которым они соответствуют, при этом не повреждая нормофлору или человеческие клетки.
Они являются самым распространенным биологическим объектом на Земле.
Бактериальные вирусы были открыты дважды: в 1915 году Фредериком Уильямом Туортом и в 1917 году Феликсом Д’Эреллем, который и предложил термин «бактериофаг».
Второе открытие было сделано во время исследования вспышки дизентерии среди французских солдат во время Первой мировой войны. При изучении лизиса (разрушения клетки под действием собственных или чужеродных ферментов) бактериальных культур.
Ученый обратил внимание, что какое-то существо, невидимое в обычный микроскоп, разрушает выращенные им культуры бактерий. Микробиологу удалось настроить его размножение: бактерии, зараженные им, погибали, а количество агента увеличивалось.
В 1919 году ученый успешно вылечил бактериофагами первых пациентов. Он описал случай успешного лечения дизентерии с использованием фагов, доказав, что они обеспечивают выздоровление больного организма. Были проведены и первые опыты по применению фагов при раневых инфекциях, холере, тифе и даже бубонной чуме. Успех выглядел вполне убедительно.
После открытия бактериофаги начали использовать для борьбы с бактериальными патогенами. Однако в Западной Европе и США от такой терапии вскоре отказались из-за сомнительных результатов. Это было неудивительно, принимая во внимание тогдашний уровень понимания биологии бактериофагов и отсутствие стандартизации. А открытие в 1928 году пенициллина и последовавшая за этим событием «эра антибиотиков» надолго отодвинули интерес к профилактическому и медицинскому использованию бактериофагов.
Хотя в государствах Восточной Европы, таких как СССР, применение бактериофагов в терапии продолжилось, чему способствовало основание в 1934 году Института Бактериофага в Тбилиси Георгием Элиавой совместно с Феликсом Д’Эреллем.
В мире интерес к фаговой терапии возобновился только в 1980-е годы, когда эффективность лечения антибиотиками значительно снизилась, а бактерии стали более устойчивы к лекарствам. Сейчас исследования в этой области активно ведутся по всему миру.