Что можно узнать по диаграмме состояния сплавов
ОСНОВНЫЕ СВЕДЕНИЯ ИЗ ТЕОРИИ СПЛАВОВ
На этом сайте www.splavy-metallov.blogspot.com Вы узнаете: что называется сплавом, чем отличается сплав от чистого металла, как строится кривая охлаждения и что она характеризует, какую зависимость имеют свойства сплавов от их состава и строения.
среда, 23 мая 2012 г.
Свойства железа и его кривая охлаждения
50%, НВ 80. Химически чистое железо, без примесей, получить чрезвычайно трудно. Техническое железо всегда содержит ряд элементов, которые попадают в него непроизвольно при производстве или вводятся специально для придания особых свойств.
В твердом состоянии железо может находиться в двух модификациях: Fea (объемно-центрированная кубическая решетка) и FeT (гранецентрированная кубическая решетка). Кристаллические решетки, приведенные на кривой охлаждения железа (рис. 28), характеризуют аллотропические превращения. Остановка при 1539 °С связана с первичной кристаллизацией железа. При этом образуется б-железо с кристаллической решеткой объемно-центрированного куба (высокотемпературную а-мо-дификацию обозначают буквой б) с периодом 0,293 нм. При 1392 °С решетка объемно-центрированного куба превращается в гранецентрированную решетку, период которой при 911°С равен 0,364 нм (образуется у-железо). В интервале 1392. 911 °С железо находится в аллотропической форме FeT. При температуре ЭП^С гранецентрированная решетка Fev превращается в объемно-центрированную решетку Fea с периодом 0,286 нм. Ниже этой температуры решетка железа объемно-центрированная.
Площадка на кривой охлаждения при 768 °С (точка Кюри) указывает не на перестройку решетки, а на возникновение магнитных свойств в железе: выше 768 °С железо немагнитно, ниже 768 °С магнитно. Изменение строения кристаллической решетки железа влечет за собой изменение некоторых его свойств (например, Fea почти не растворяет углерод, aFeT растворяет до 2,14 %). Аллотропические превращения всегда сопровождаются
56
Рис. 28. Кривая охлаждения железа
выделением теплоты при охлаждении и поглощением скрытой теплоты при нагревании.
Углерод в природе существует в двух модификациях — в виде графита и алмаза.
При нормальных условиях стабилен графит, алмаз представляет собой его ме-тастабильную модификацию.
Углерод в железоуглеродистых сплавах присутствует или в виде графита в структуре чугунов, или в виде химического соединения карбида железа F3C (цементит). Углерод является неметаллическим элементом прочностью ав = 20. 40 МПа.
Металлические сплавы и диаграммы состояния
Сплавами являются твёрдые вещества, получаемые сплавлением двух или более простых веществ, называемых компонентами. В металлическом сплаве основными компонентами являются металлы. Для металлического сплава меняя соотношение компонентов, можно получить бесчисленное множество вариантов сплава, и каждый вариант будет иметь свою структуру и свойства, температуру плавления, затвердения и т.д.
В технике большинство сплавов получают взаимным растворением их составляющих в жидком состоянии, т.е. доводят компоненты до плавления. Однако сплавы могут быть получены в твёрдом состоянии в процессе смешивания и спекания порошков компонентов под давлением при высоких температурах. Расплавленные компоненты при охлаждении и кристаллизации могут образовывать твердые металлические сплавы с различным строением: смеси, твердые растворы, химические соединения.
Наиболее часто встречающиеся сплавы – твёрдые растворы, в которых компоненты в твердом состоянии частично или полностью растворены друг в друге. Можно просто представить понятие твёрдого раствора можно, если, например, заморозить солёную воду. В этом случае лёд уже будет представлять собой твёрдый раствор соли в воде.
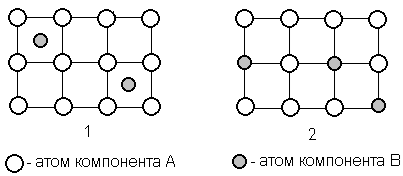
Растворение атомов одного из компонентов в кристаллической решётке другого компонента может идти по типу внедрения, когда атомы растворенного элемента располагаются между атомами растворителя (рисунок 1.1), и по типу замещения, когда атомы растворенного элемента замещают атомы растворителя (рисунок 1.2).
Рисунок 1 – Строение твёрдого раствора внедрения и замещения
При образовании твёрдого раствора внедрения его растворимость всегда ограниченная, что связано с ограниченными размерами межатомных промежутков в кристаллической решётке растворителя.
Чем больше концентрация твёрдого раствора, тем больше увеличены межатомные расстояния в решетке. Такие твёрдые растворы возникают при сплавлении металлов с неметаллами, имеющими малый атомный радиус – углеродом, азотом, бором, водородом. Примером твёрдых растворов внедрения, имеющих промышленное значение, являются твёрдые растворы углерода в ОЦК и ГЦК решётке железа – феррит и аустенит.
Информация о состоянии и структуре сплавов просто и сжато может быть представлена в виде диаграммы состояния – графического изображения состояния сплавов в зависимости от температуры и концентрации компонентов. Такие диаграммы также называют структурными с добавлением слова равновесные, что указывает на образование таких фаз и структур, которые соответствуют наименьшему значению свободной энергии системы.
На любой диаграмме состояния можно выделить следующие точки и линии:
Ликвидус – точка, отвечающая началу кристаллизации.
Линия ликвидус – геометрическое место точек ликвидус.
Солидус – точка, отвечающая концу кристаллизации.
Линия солидус – геометрическое место точек солидус.
Фигуративная точка– точка, взятая в пределах диаграммы состояния, которая показывает температуру сплава, его состояние, процентное соотношение компонентов.
Фигуративная линия – линия, проходящая через фигуративную точку параллельно оси температур.
Рассмотрим основные диаграммы состояния двойных сплавов.
Рисунок 2 – Диаграмма состояния I рода
Диаграмма состояния II рода характерна для сплавов с неограниченной растворимостью компонентов друг в друге, имеющих одинаковые типы кристаллических решеток. Диаграмма (рисунок 3) содержит область жидкой фазы (выше линии ликвидус АСВ), двухфазную область α + Ж, расположенную между линиями АСВ и АDВ, область твердой фазы α (ниже линии солидус АDВ). Фаза α представляет собой твердый раствор компонентов А и В, азерна этой фазы имеют общую кристаллическую решетку.
Рисунок 3 – Диаграмма состояния II рода
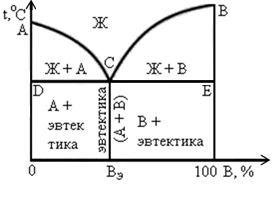
Диаграмма состояния III рода характерна для сплавов с ограниченной растворимостью компонентов друг в друге. На диаграмме (рисунок 4) линия АDВ является линией ликвидус, а линия АСDЕВ – линией солидус. Фаза α является твердым раствором компонента В в компоненте А, а фаза β – твердым раствором компонента А в компоненте В. Эвтектика для рассматриваемой диаграммы представляет собой смесь мелкозернистых фаз α и β. Эвтектика кристаллизуется при наименьшей для данной системы температуре, т.е. на линии СЕ.
Линия СF показывает предельную растворимость компонента В в компоненте А, а линия ЕК – предельную растворимость компонента А в компоненте В. Ниже линии СF из α-фазы начинают выделяться атомы компонента В, образуя вторичные кристаллы βIIβ-твер-дого раствора. Аналогично ниже линии ЕК из β-фазы выделяются атомы компонента А, образуя вторичные кристаллы αIIα-твердого раствора. Структура доэвтектических сплавов ниже линии СЕ состоит из первичных зерен α-фазы, эвтектики (α + β) и зерен вторичной βII-фазы. А структура заэвтектических сплавов состоит из первичных зерен β-фазы, эвтектики (α + β) и зерен вторичной αII-фазы.
Рисунок 4 – Диаграмма состояния III рода
Диаграмма состояния IV рода (рисунок 5) относится к сплавам, в которых сплавляемые компоненты образуют устойчивое химическое соединение АтВп. Поэтому в данном случае химическое соединение выступает в роли самостоятельного компонента, способного образовывать сплавы с каждым из исходных компонентов.
Химическое соединение АтВп образует с компонентами А и В сплавы, которые характерны для диаграммы состояния I рода.
Рисунок 5 – Диаграмма состояния IV рода
Рисунок 6 – Изменение твёрдости и электрического сопротивления в зависимости от рода диаграммы
Для сплавов и компонентов, образующих химическое соединение, максимальные значения твердости и электрического сопротивления наблюдаются при концентрации компонентов, соответствующих химическому соединению (рисунок 6,г).
Таким образом, если известны характер взаимодействия между компонентами и тип диаграммы состояния, то возможен выбор состава сплава, обеспечивающего заданные физико-химические свойства.
1. Что такое сплав? Что является компонентами для металлического сплава? Сколько компонентов должно присутствовать, чтобы вещество можно было назвать сплавом?
2. Способы получения сплава.
3. Типы растворения твёрдых растворов. Показать на рисунке. Какой тип растворения способствует увеличению межатомных расстояний.
4. Что такое диаграмма состояния?
5. Ликвидус как точка и как линия (определения).
6. Солидус как точка и как линия (определения).
7. Фигуративная точка, фигуративная линия (определения).
8. Диаграммы состояний I, II, III, IV рода. Для каких сплавов характерна каждая из диаграмм, особенности диаграмм. Уметь показать на каждой из диаграмм ключевые точки и линии (солидус, ликвидус и др.)
9. Диаграммы изменения твёрдости и электрического сопротивления. Уметь изобразить – как изменяются эти свойства для каждого рода диаграмм.
ДИАГРАММЫ СОСТОЯНИЯ СПЛАВОВ И ИХ ЗНАЧЕНИЕ
ПРИ КРИСТАЛЛИЗАЦИИ МЕТАЛЛА
СВАРНЫХ СОЕДИНЕНИЙ
В промышленности чаще всего применяют не чистые металлы, а сплавы двух или нескольких элементов на основе какого-либо одного металла. Так, стали – сплавы на основе железа – содержат углерод, марганец, кремний, а в специальных случаях – никель, хром, молибден и другие элементы. Содержание железа составляет обычно более 90 % и только у отдельных сталей со специальными свойствами – более 60 %.
Большое значение имеют сплавы на основе алюминия, содержащие магний, медь, цинк и другие элементы; сплавы на основе меди с добавлением цинка, олова, алюминия; сплавы на основе титана, содержащие железо, и др.
Путем термообработки можно в широких пределах изменять физические и механические свойства большей части промышленных сплавов. Возможность изменения свойств сплавов, их свариваемость, структура и свойства сварных соединений определяются природой сплавов, их строением, фазовым состоянием и составом, изменениями, происходящими при нагреве и охлаждении, как в процессе термообработки, так и в процессе сварки.
Как правило, элементы, образующие металлический сплав, в жидком состоянии полностью взаиморастворимы, т.е. образуют однородный материал с равномерно распределенными в объёме атомами элементов. Ряд металлов, не смешивающихся друг с другом даже в жидком состоянии, не могут образовывать сплавов, свариваемых методами сварки плавлением. При переходе жидкого однородного сплава в твердое состояние в нем могут происходить различные изменения, связанные с полиморфными превращениями основы сплава, с взаимодействием элементов, составляющих сплав.
Сплав двух или нескольких элементов после перехода из жидкого состояния в твердое может быть в виде твердых растворов, в виде механической смеси фаз и в виде химических соединений. Кроме того, могут существовать и промежуточные состояния, а также сочетания указанных состояний. Характер взаимодействия элементов, образующих сплав, имеет большое значение для сварки. Лучше всего должны свариваться элементы, дающие непрерывный ряд твердых растворов, хуже – дающие ограниченные твердые растворы, еще хуже – дающие химические соединения и невзаимодействующие.
То или иное состояние затвердевающего сплава зависит от взаимодействия между атомами составляющих его компонентов. Стремление к энергетически более устойчивому состоянию системы обусловливает форму взаимодействия. Твердый раствор имеет определенные отличия от металла растворителя и растворенного элемента.
Пример неограниченной взаимной растворимости в жидком и твердом состояниях двух металлов А и Б представлен на рис. 17. На диаграмме состояния линии, ограничивающие области существования различных фазовых систем, характеризуют условия (температуру, концентрацию) равновесия между фазами.
В твердом растворе переход от раствора Б в А к раствору А в Б происходит при постепенной замене в решетке А атомов А атомами Б без определенного порядка мест замещения.
Рисунок 17 – Диаграмма состояния сплавов металла А
с металлом Б при их неограниченной
растворимости в жидком и твердом состояниях
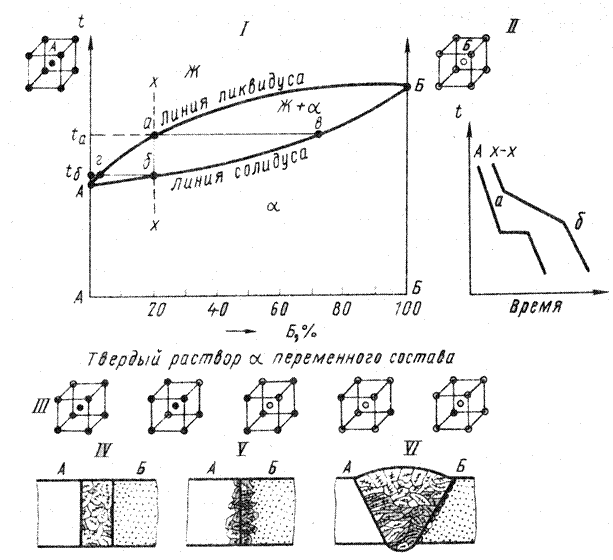
Такого рода взаимодействие возможно для металлов с аналогичными типами кристаллических решеток и атомами близких размеров. Металлы, дающие сплавы такого типа с неограниченной растворимостью, должны хорошо соединяться различными видами сварки. При сварке плавлением, будь то сварка без присадочного материала (рис. 17, IV) или дуговая сварка плавящимся электродом (рис. 17, VI), зоны плавления и смешивания свариваемых металлов А и Б в жидком состоянии представляют собой достаточно однородный раствор, может быть, с несколько большей концентрацией оплавляемого металла у кромки. После кристаллизации сварной шов представляет собой непрерывный ряд твердых растворов переменного состава. Различие в составе первых выпадающих кристаллов и последних кристаллизующихся порций металла, т.е. микрохимическая неоднородность, увеличивается с уменьшением разницы между температурами плавления свариваемых металлов и увеличением температурного интервала кристаллизации (расстояния между линиями ликвидуса и солидуса). Иным будет строение шва при сварке давлением (рис. 17, V).
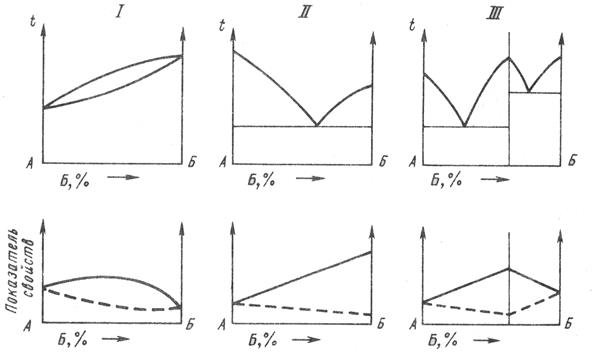
В сварных швах химическая неоднородность тем больше, чем больше размер сварочной ванны и чем меньше скорость кристаллизации. При сварке давлением в твердом состоянии (см. рис. 17, V) металлы, имеющие неограниченную взаимную растворимость, при наличии даже самых небольших элементов взаимодиффузии должны обеспечивать получение однородных твердых растворов в участках, примыкающих к сварному стыку. В таких соединениях металл должен быть однофазным, что обеспечивает высокие свойства, хотя в соответствии с правилом Н.С. Курнакова при непрерывном ряде твердых растворов свойства сплавов должны отличаться от свойств образующих их металлов (рис. 18). Для непрерывного ряда твердых растворов изменение свойств должно происходить плавно (рис. 18, I) по выпуклой или вогнутой кривой, без скачков. При образовании эвтектик – плавно по прямой (рис. 18, II). Это важно для сварных соединений, так как постепенное изменение свойств благоприятнее влияет на работоспособность сварного соединения, чем скачкообразное, имеющее место в случае образования в сплавах химического соединения (рис. 18, III).
Неблагоприятно для сварных соединений металлов с рассматриваемым типом диаграммы состояния отсутствие аллотропических превращений в твердом состоянии. Отсутствие вторичной перекристаллизации в твердом состоянии приводит к сохранению крупных кристаллитов, образующихся при первичной кристаллизации, в то время как перекристаллизация в связи с полиморфным превращением в твердом состоянии могла бы привести к измельчению зерна и улучшению свойств.
Рисунок 18 – Характер возможного изменения свойств сплавов
элементов с разными типами диаграммы состояния
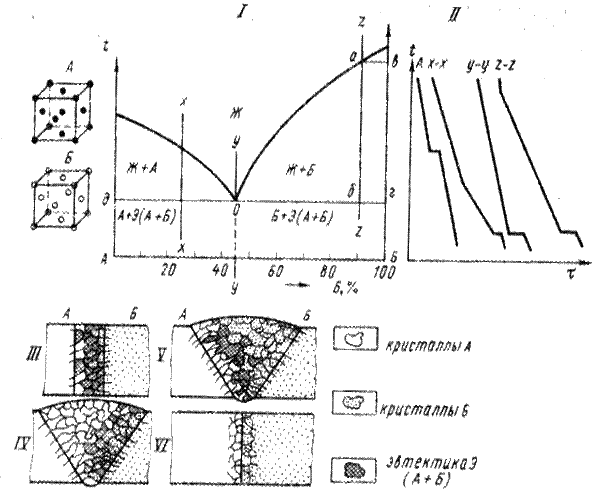
Большое практическое значение имеют сплавы элементов, образующих равновесные механические смеси – эвтектики при кристаллизации из жидкого состояния и эвтектоиды – при вторичной кристаллизации. При образовании таких смесей для формирования сварных соединений важно, образуют ли элементы (компоненты) смеси без ограниченных твердых растворов (рис. 19) или же имеют ограниченную взаимную растворимость в твердом состоянии (рис. 20). При отсутствии у компонентов ограниченной растворимости сварное соединение, полученное сваркой плавлением (рис. 19, III-V), имеет вполне равномерную микроструктуру с постепенным переходом от одного фазового состояния (кристаллы металла А) к другому (кристаллы металла Б).
В жидкой сварочной ванне находится равномерный твердый раствор компонентов А и Б, однако непрерывное контактирование жидкого раствора на одной кромке с компонентом А делает расплав вблизи этой кромки обогащенным компонентом А, а у другой кромки – компонентом Б.
I – диаграмма состояния; II – кривая охлаждения; III – кристаллическое строение сварного соединения при сварке плавлением без присадочного материала; IV – то же, с присадкой металла А; V – то же, с присадкой металла Б; VI – сварное соединение, полученное сваркой давлением
Рисунок 19 – Диаграмма состояния сплавов металлов А и Б, дающая
в твердом состоянии эвтектические смеси
Поэтому кристаллизация металла у кромок соответствует сечениям X—X у кромки А и Z—Z у кромки Б (см. рис. 19, I). При охлаждении сплава Z до температуры ликвидуса (рис. 16, II, точка а) начнется выпадение кристаллов Б, которое будет продолжаться до температуры солидуса, которой будет температура эвтектического превращения (точка г). При этой температуре остаток жидкого расплава превратится в равномерную механическую смесь кристаллов Б и А (эвтектику), имеющую состав, соответствующий проекции точки О на горизонтальную ось. Аналогично пройдет кристаллизация сплавов у кромки металла A с той лишь разницей, что первыми начнут выпадать кристаллы металла А.
Таким образом, при сварке плавлением микроструктура и фазовое состояние металла будут постепенно переходить от кристаллов одного металла с малым количеством эвтектики к кристаллам другого металла также с малым количеством эвтектики (см. рис. 19, V). Между этими зонами количество эвтектики будет постепенно увеличиваться, и где-то на промежуточных участках должна находиться чисто эвтектическая зона. Поскольку в участках сварного шва, примыкающих к кромкам каждого из свариваемых металлов, кристаллизуется металл с подавляющим количеством кристаллов данного свариваемого металла, обеспечиваются хорошие условия для сплавления основного металла и металла шва, а постепенное изменение структуры и фазового состояния в пределах металла шва обеспечивает плавный переход свойств одного металла к свойствам другого (см. рис. 19, II).
При данном типе диаграммы состояния свариваемых металлов хорошее сплавление металла шва с основными свариваемыми металлами обусловливается тем, что на кромках каждого металла из расплава надстраиваются зерна того же металла, т.е. имеет место полное соответствие атомно-кристаллического строения, а в связи с этим и создание надлежащей связи. Благоприятно и плавное изменение свойств в пределах сварного соединения. Образование химической неоднородности в таком сварном соединении неизбежно в связи с разной химической природой металлов А и Б. Градиент химической неоднородности (различие в составе соседних участков) тем больше, чем больше величина концентрационного интервала между эвтектической точкой О и чистыми металлами (см. рис. 19, отрезки Од и Ог).
При сварке давлением в твердом состоянии образование соединения связано с определенными ограничениями. Отсутствие жидкого раствора и кристаллизации с выделением на кромках однотипных кристаллов, отсутствие взаимной растворимости свариваемых металлов в твердом состоянии исключают протекание диффузионных процессов на границе раздела. Возможность получения сварного соединения в этом случае зависит от надлежащего контакта чистых свариваемых поверхностей, создания максимального количества активных центров и соответствия атомно-кристаллического строения.
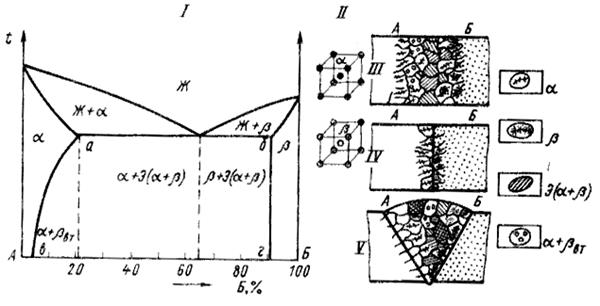
Для металлов, образующих эвтектические смеси, но имеющих взаимную ограниченную растворимость, механизм образования сварного соединения заметно изменяется (рис. 20). При сварке плавлением в сварочной ванне на кромках свариваемых металлов из жидкого расплава кристаллизуются не чистые металлы, а твердые растворы на основе соответствующих металлов. На кромке свариваемого металла А будут кристаллизоваться кристаллы твердого α-раствора (Б в А), а на кромках металла Б – кристаллы β-раствора (А в Б).
I – диаграмма состояния; II – элементарные ячейки α и β-растворов;
III – кристаллическое строение сварного соединения при сварке плавлением без присадки; IV – сварное соединение, получаемое сваркой давлением; V – то же, с присадкой металла Б; VI – то же, с присадкой металла А
Рисунок 20 – Диаграмма состояния сплавов металлов А и Б, дающих
в твердом состоянии эвтектические смеси и ограниченные
Эвтектическая смесь в такой системе состоит не из чистых металлов А и Б, а из граничных фаз α- и β-растворов. Для растворов типа α, где предельная растворимость элемента Б в элементе А изменяется с температурой, характерно появление в кристаллах α-частиц β-фазы, которая выделяется при охлаждении в интервале температур от максимальной растворимости Б в А до минимальной в виде избыточных вторичных кристаллов (βВТ).
Эти кристаллы βВТ мельче, чем первичные β-кристаллы, т.к. образуются при более низкой температуре. Поскольку укрупнение их может происходить только при длительном пребывании при повышенной температуре, когда они могут расти за счет диффузионного поступления к ним атомов образующих компонентов, их размер тем меньше, чем меньше время пребывания при повышенной температуре, т.е., чем больше скорость охлаждения. При очень большой скорости охлаждения можно переохладить до нормальной температуры твердый α-раствор с максимальной концентрацией растворимых атомов Б. Но такой перенасыщенный твердый раствор неустойчив и может разлагаться со временем с выделением очень мелких дисперсных частиц βВТ-фазы. При таком старении сплава выделяющиеся дисперсные частички вторичной фазы препятствуют движению дислокации, что может способствовать его упрочнению, а также повышению хрупкости.
Таким образом, при сварке плавлением на кромках свариваемых металлов А и Б кристаллизуются твердые α— и β-растворы. Атомное и кристаллическое соответствие твердых растворов свариваемым металлам создает хорошие условия для связи металла шва со свариваемым металлом.
Для металлов с рассматриваемым типом диаграммы состояния характерно также появление диффузионных зон на границе соединения. Образование диффузионных зон связано с тем, что в металл А в соответствии с наличием определенной растворимости проникает (диффундирует) некоторое количество атомов Б: либо из α-раствора при сварке плавлением, либо непосредственно из металла Б при сварке давлением в твердом состоянии.
Наличие зон взаимодиффузии улучшает связь в сварном соединении, так как при этом происходит более плавное изменение свойств.
Возможность даже ограниченной взаимодиффузии особенно важна при сварке давлением в твердом состоянии, когда она может стать дополнительным фактором улучшения свойств сварных соединений. Неблагоприятен в сварных соединениях рассмотренного типа эффект старения в отдельных участках как сварного шва, так и примыкающей к шву зоны, где могли образоваться кристаллы перенасыщенного твердого раствора.
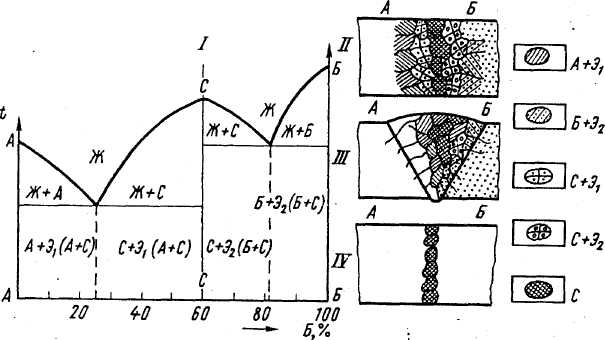
Элементы А и Б, которые при кристаллизации образуют химическое соединение АтБп, условно обозначенное как новое вещество C,дают диаграммы состояния типа представленной на рис. 21. Различие между указанными системами заключается в том, что в случае, представленном на рис. 21, новое химическое вещество С образует с металлами А и Б эвтектические смеси без какого-либо растворения одного из веществ в другом.
І — диаграмма состояния; ІІ — кристаллическое строение сварного
соединения при сварке плавлением без присадки; ІІІ — то же, с присадкой металла А; IV – сварное соединение, полученное сваркой давлением
Рисунок 21 – Диаграмма состояния сплавов металлов А и Б,
дающих в твердом состоянии химическое соединение АтБп – С и
эвтектические смеси без ограниченных твердых растворов
Химическое соединение, всегда состоящее из т атомов металла А и п атомов металла Б, с вполне определенными местами этих атомов в кристаллической решетке, имеет свой тип кристаллической решетки в отличие от упорядоченного твердого раствора с типом решетки элемента А или Б. Свойства их также различны.
Очень часто химические соединения двух мягких, пластинчатых и вязких металлов оказываются твердыми и хрупкими (например, соединения железа с алюминием). В связи с этим особенно важно учитывать возможность образования химических соединений в сварных соединениях.
Среди систем, дающих химические соединения, для сварки наиболее благоприятны системы с ограниченными твердыми растворами, как обеспечивающие получение на границе соединения переходных зон твердых растворов.