Что значит сильное основание в химии
Кислоты и основания
После прочтения статьи Вы сможете разделять вещества на соли, кислоты и основания. В статье описано, что такое pH раствора, какими общими свойствами обладают кислоты и основания.
В неорганической химии, как правило, под кислотой имеют ввиду кислоту Бренстеда-Лоури, то есть вещества, способные отдать протон. Если имеют ввиду определение кислоты по Льюису, то в тексте такую кислоту называют кислотой Льюиса. Данные правила справедливы для кислот и оснований.
Диссоциация
Свойства кислот и оснований
Основания, как правило, мыльные на ощупь, кислоты, в большинстве своём, имеют кислый вкус.
При реакции основания со многими катионами формируется осадок. При реакции кислоты с анионами, как правило, выделяется газ.
Сильные и слабые кислоты и основания
Сильные кислоты
Примеры сильных кислот: HCl, HBr, HF, HNO3, H2SO4, HClO4
Список сильных кислот
Слабые кислоты
Растворяются в воде только частично, например, HF:
Сильные основания полностью диссоциируют в воде:
К сильным основаниям относятся гидроксиды металлов первой (алкалины, щелочные металы) и второй (алкалинотеррены, щёлочноземельные металлы) группы.
Список сильных оснований
Слабые основания
Список слабых оснований
Реакции кислот и оснований
Сильная кислота и сильное основание
Такая реакция называется нейтрализацией: при количестве реагентов достаточном для полной диссоциации кислоты и основания, результирующий раствор будет нейтральным.
Слабое основание и слабая кислота
Сильное основание и слабая кислота
Основание полностью диссоциирует, кислота диссоциирует частично, результирующий раствор имеет слабые свойства основания:
Сильная кислота и слабое основание
Кислота полностью диссоциирует, основание диссоциирует не полностью:
Диссоциация воды
Способы определения pH
Инструментальный метод
Индикаторы
Вещество, которое изменяет цвет в некотором интервале значений pH в зависимости от кислотности раствора, используя несколько индикаторов можно добиться достаточно точного результата.
Все катионы кроме металлов первой и второй группы имеют кислотные свойства.
Буфферный раствор
Растворы, которые сохраняют уровень pH при добавлении небольшого количества сильной кислоты или сильного основания, в основном состоят из:
Для подготовки буфферного раствора определённой кислотности необходимо смешать слабую кислоту или основание с соответствующей солью, при этом необходимо учесть:
10 Самых сильных оснований когда-либо синтезированных
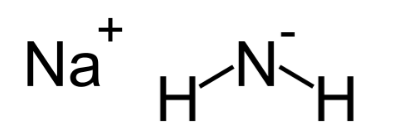
Основание, в химии, относится к любому веществу, которое высвобождает гидроксидные ионы (OH − ) при растворении в воде или водном растворе. Многие основания, однако, не легко переносят гидроксидные ионы, но они также производят высокие уровни OH − при обработке водой. Этот тип реакции можно наблюдать, когда аммиак обрабатывают водой с получением аммония и гидроксида.
Основания также имеют отличительные физические характеристики; например, они горьки на вкус (кислоты кислы) и дают скользкое ощущение при прикосновении. Основы необходимы и являются жизненно важным компонентом в конкретных отраслях промышленности. Они использованы для того чтобы сделать бумагу, мыло и синтетическую вискозу, порошок отбеливания, антацид. Хотя они обычно рассматриваются как химическая противоположность кислот, есть несколько известных кислот, которые могут вести себя так же, как основания при определенных обстоятельствах.
Cверхоснование
Термин «сверхоснование» не нов и использовался более полутора столетий. Поскольку сверхоснование подвержены бурной реакции, при контакте с водой или углекислым газом для проведения химических реакций требуется специальный растворитель. Сверхоснование могут быть классифицированы на три типа; органические, неорганические и металлоорганические. Ниже приведен список 10 сильнейших баз на Земле.
10. Гидроксид лития
Химическая формула: LiOH
Большое количество LiOH используется для производства литиевого мыла. Другое важное использование гидроксида лития делается в вентиляционных системах подводных лодок и космических аппаратов для устранения углекислого газа путем создания воды и карбоната лития.
Он также используется в качестве средства борьбы с коррозией в ядерных реакторах (реактор с водой под давлением) и в качестве электролита батареи.
9. Гидроксид натрия
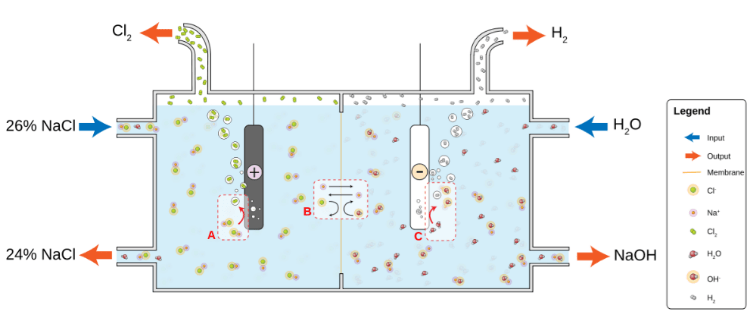
Рабочая модель процесса Хлоралкалия или электролиза Хлоралкалия
Химическая формула: NaOH
Гидроксид натрия широко используется для химической варки целлюлозы в бумажной промышленности. Его другие применения включают в себя производство мыла и моющих средств, обработку сырой пищи, производство цемента и водоочистные сооружения для нейтрализации значений pH воды. Он также время от времени используется в нефтяной промышленности для нейтрализации кислот и повышения уровня щелочности определенного раствора.
В древние времена NaOH получали обработкой гидроксида кальция карбонатом натрия. К 19 веку его заменил процесс Сольвея, который использовался для производства карбоната натрия, дешевой альтернативы NaOH. Сегодня большая часть промышленного гидроксида натрия создается с помощью процесса хлоралкалия.
8. Гидроксид калия
Химическая формула: KOH
Многие из вас могут распознать гидроксид калия как едкий калий, твердое белое вещество, известное своей высококоррозионной природой. Подобно гидроксиду натрия, KOH является бесцветным (коммерчески доступно в белом цвете) и прочным квинтэссенцией.
В то время как гидроксид калия и гидроксид натрия могут использоваться как взаимозаменяемые вещества для различных целей, в большинстве отраслей промышленности используется NaOH, так как он дешевле двух. В любом случае он используется для производства биодизеля, мыла и в качестве электролита в некоторых батареях.
Чистый гидроксид калия получают взаимодействием гидроксида натрия с деградированным или нечистым калием. Химическое соединение потенциально опасно и вызывает ожоги кожи при концентрации более 2%. Все, что от 0,5% до 2%, может вызвать сильное раздражение.
7. Бис(триметилсилил) амид лития
Химическая Формула: C 6 H 18 LiNSi 2
Бис (триметилсилил) амид лития, или сокращенно LiHMDS, представляет собой ненуклеофильную супероснову, которая имеет важные применения в лабораториях. Как и другие реагенты на основе лития, он может образовывать циклические соединения с тримером, анионом, созданным комбинацией трех ионов одного и того же вещества. LiHMDS обычно получают взаимодействием бис (триметилсилил) амина с бутиллитием.
HN (SiMe3) 2 + C4H9Li → LiN (SiMe3) 2 + C4H10
6. Гидрид натрия
Химическая формула: NaH
Гидрид натрия принадлежит к особой группе гидридов, известных как солевые/ионные гидриды (состоящие из ионов Na+ и H-), которые, в отличие от аммиака и воды, существуют в солеобразной форме. В основном он используется в качестве основы органического синтеза, хотя известно также малое количество незначительных случаев использования NaH. Гидрид натрия образуется при реакции водорода с жидким натрием.
В редких случаях соединение может принимать форму «обратного гидрида натрия», где натрий и ионы водорода обмениваются зарядами (Na- и H+). Na- является щелочью, что делает это соединение более энергетическим, чем стандартный гидрид натрия (из-за увеличенного чистого смещения между двумя электронами).
5. Амид Натрия
Химическая формула: NaNH 2
Азид натрия, иногда известный как Амид натрия, является одним из самых сильных известных оснований в мире. Это важное, коммерчески доступное химическое соединение, которое обычно используется в органическом синтезе. NaNH 2 проводит электричество (в сплавленном состоянии), так как его электрические свойства проводимости почти аналогичны свойствам гидроксида натрия.
В то время как чистый гидроксид натрия обычно белый, большая часть коммерчески доступных NaNH 2 имеет серый цвет из-за наличия примесей в виде металлического железа. Обычно Амид натрия получают путем взаимодействия аммиачного газа с натрием.
Амид натрия является предпочтительным в некоторых типах синтеза из-за его функций в качестве нуклеофила. Это потенциально опасное химическое вещество, с которым следует обращаться с особой осторожностью. Он может энергично реагировать с водой, особенно когда присутствует в твердой форме.
4. Диизопропиламид лития
Химическая формула: C 6 H 14 LiN
Следующим в списке является диизопропиламид лития, еще одна ненуклеофильная сверхоснова, которая известна своей сильно коррозионной природой и растворимостью. В нормальных условиях соединение синтезируется путем обработки охлажденного раствора диизопропиламина (тетрагидрофурана) Бутиллитием. Излишне говорить, что диизопропиламид лития является коррозионным, а пирофорные, но коммерческие растворы гораздо безопаснее.
3. Бутиллитий
Химическая формула: C 4 H 9 Li
Н-Бутиллитий коммерчески важное свероснова, главным образом используемое как катализатор для полимерности для того чтобы произвести синтетический каучук. Он также используется в фармацевтической промышленности. Хотя бутиллитий в основном бесцветный, он может претерпевать незначительные изменения цвета либо при контакте с алканами, либо при старении.
Помимо сверхосновы, Н-Бутиллитий является мощным восстановителем, а также нуклеофилом (химическое вещество, которое жертвует электронную пару, образуя связь). Бутиллитий обычно получают взаимодействием лития с 1-бромбутаном или 1-хлорбутаном.
Бутиллитий нестабилен и может активно реагировать с водой и углекислым газом, но его можно безопасно хранить под инертным газом.
2. Анион окиси лития
Анион монооксида лития когда-то был самой сильной основой в мире до того, как был свергнут с престола в 2008 году. Как и другие сверхосновы, монооксид лития готовят в апротонном растворителе и также известен своей чрезвычайно агрессивной природой.
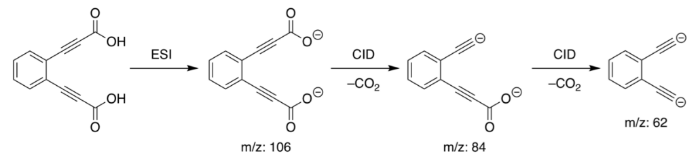
Синтез аниона моноксида лития является сложной процедурой, и ее сложно проводить контролируемым образом. Обычно небольшое количество оксалата лития (Li 2 C 2 O 4 ) используется в качестве предшественника, который проходит процесс ионизации электрораспылением. Полученное соединение оксалат-анион лития (LiC 2 O 4 ) выделяют и затем обрабатывают с индуцированной столкновением диссоциацией дважды.
В результате получаем анион оксида лития (LiO-) и молекулу диоксида углерода. Использование аниона оксида лития неизвестно.
1. Орто-diethynylbenzene дианион
Химическая формула: [C 6 H 4 (C2) 2 ] 2–
E pa: 1843 кДж / моль
Орто-diethynylbenzene дианион является, пожалуй, самым сильным сверхоснованием, известным нам. Он был первоначально синтезирован/открыт группой исследователей в Австралии с использованием масс-спектрометрии.
Кроме того, орто-diethynylbenzene имеет два изомера (с одинаковой молекулярной формулой, но различной химической структурой); Мета-диэтинилбензол дианион и пара-диэтинилбензол дианион, второе и третье сильнейшее основание, когда-либо синтезированное. Оба изомера, включая орто-diethynylbenzene, не имеют известного применения и существуют в газообразном состоянии.
Основания. Химические свойства и способы получения
Перед изучением этого раздела рекомендую прочитать следующую статью:
Получение оснований
1. Взаимодействие основных оксидов с водой. При этом с водой реагируют в обычных условиях только те оксиды, которым соответствует растворимое основание (щелочь). Т.е. таким способом можно получить только щёлочи:
основный оксид + вода = основание
Na2O + H2O → 2NaOH
При этом оксид меди (II) с водой не реагирует:
CuO + H2O ≠
2. Взаимодействие металлов с водой. При этом с водой реагируют в обычных условиях только щелочные металлы (литий, натрий, калий. рубидий, цезий) , кальций, стронций и барий. При этом протекает окислительно-восстановительная реакция, окислителем выступает водород, восстановителем является металл.
металл + вода = щёлочь + водород
2K 0 + 2 H2 + O → 2 K + OH + H2 0
2NaCl + 2H2O → 2NaOH + H2↑ + Cl2↑
4. Основания образуются при взаимодействии других щелочей с солями. При этом взаимодействуют только растворимые вещества, а в продуктах должна образоваться нерастворимая соль, либо нерастворимое основание:
щелочь + соль1 = соль2↓ + щелочь
щелочь + соль1 = соль2↓ + щелочь
Например: карбонат калия реагирует в растворе с гидроксидом кальция:
Например: хлорид меди (II) взаимодействет в растворе с гидроксидом натрия. При этом выпадает голубой осадок гидроксида меди (II):
CuCl2 + 2NaOH → Cu(OH)2↓ + 2NaCl
Химические свойства нерастворимых оснований
1. Нерастворимые основания взаимодействуют с сильными кислотами и их оксидами (и некоторыми средними кислотами). При этом образуются соль и вода.
нерастворимое основание + кислота = соль + вода
нерастворимое основание + кислотный оксид = соль + вода
При этом гидроксид меди (II) не взаимодействует с кислотным оксидом слабой угольной кислоты – углекислым газом:
2. Нерастворимые основания разлагаются при нагревании на оксид и воду.
3. Нерастворимые основания не взаимодействуют с амфотерными оксидами и гидроксидами.
нерастворимое оснвоание + амфотерный оксид ≠
нерастворимое основание + амфотерный гидроксид ≠
4. Некоторые нерастворимые основания могут выступать в качестве восстановителей. Восстановителями являются основания, образованные металлами с минимальной или промежуточной степенью окисления, которые могут повысить свою степень окисления (гидроксид железа (II), гидроксид хрома (II) и др.).
Химические свойства щелочей
щёлочь(избыток)+ кислота = средняя соль + вода
щёлочь + многоосновная кислота(избыток) = кислая соль + вода
При этом дигидрофосфаты образуются в избытке кислоты, либо при мольном соотношении (соотношении количеств веществ) реагентов 1:1.
При мольном соотношении количества щелочи и кислоты 2:1 образуются гидрофосфаты:
В избытке щелочи, либо при мольном соотношении количества щелочи и кислоты 3:1 образуется фосфат щелочного металла.
щёлочь (расплав) + амфотерный оксид = средняя соль + вода
щёлочь (расплав) + амфотерный гидроксид = средняя соль + вода
щёлочь (раствор) + амфотерный оксид = комплексная соль
щёлочь (раствор) + амфотерный гидроксид = комплексная соль
А в растворе образуется комплексная соль:
Обратите внимание, как составляется формула комплексной соли: сначала мы выбираем центральный атом (к ак правило, это металл из амфотерного гидроксида). Затем дописываем к нему лиганды — в нашем случае это гидроксид-ионы. Число лигандов, как правило, в 2 раза больше, чем степень окисления центрального атома. Но комплекс алюминия — исключение, у него число лигандов чаще всего равно 4. Заключаем полученный фрагмент в квадртаные скобки — это комплексный ион. Определяем его заряд и снаружи дописываем нужное количество катионов или анионов.
3. Щёлочи взаимодействуют с кислотными оксидами. При этом возможно образование кислой или средней соли, в зависимости от мольного соотношения щёлочи и кислотного оксида. В избытке щёлочи образуется средняя соль, а в избытке кислотного оксида образуется кислая соль:
щёлочь(избыток) + кислотный оксид = средняя соль + вода
щёлочь + кислотный оксид(избыток) = кислая соль
А при взаимодействии избытка углекислого газа с гидроксидом натрия образуется только гидрокарбонат натрия:
2NaOH + CO2 = NaHCO3
щёлочь + растворимая соль = соль + соответствующий гидроксид
Щёлочи взаимодействуют с растворами солей металлов, которым соответствуют нерастворимые или неустойчивые гидроксиды.
Cu 2+ SO4 2- + 2Na + OH — = Cu 2+ (OH)2 — ↓ + Na2 + SO4 2-
Также щёлочи взаимодействуют с растворами солей аммония.
Таким образом, получаем 2 схемы взаимодействия солей металлов, которым соответствуют амфотерные гидроксиды, с щелочами:
соль амф.металла(избыток) + щёлочь = амфотерный гидроксид↓ + соль
соль амф.металла + щёлочь(избыток) = комплексная соль + соль
5. Щёлочи взаимодействуют с кислыми солями. При этом образуются средние соли, либо менее кислые соли.
кислая соль + щёлочь = средняя соль + вода
Свойства кислых солей очень удобно определять, разбивая мысленно кислую соль на 2 вещества — кислоту и соль. Например, гидрокарбонта натрия NaHCO3 мы разбиваем на уольную кислоту H2CO3 и карбонат натрия Na2CO3. Свойства гидрокарбоната в значительной степени определяются свойствами угольной кислоты и свойствами карбоната натрия.
6. Щёлочи взаимодействуют с металлами в растворе и расплаве. При этом протекает окислительно-восстановительная реакция, в растворе образуется комплексная соль и водород, в расплаве — средняя соль и водород.
! Обратите внимание! С щелочами в растворе реагируют только те металлы, у которых оксид с минимальной положительной степенью окисления металла амфотерный!
2Al + 2NaOH + 6 H2 + O = 2Na[ Al +3 (OH)4] + 3 H2 0
7. Щёлочи взаимодействуют с неметалами. При этом протекают окислительно-восстановительные реакции. Как правило, неметаллы диспропорционируют в щелочах. Не реагируют с щелочами кислород, водород, азот, углерод и инертные газы (гелий, неон, аргон и др.):
NaOH +О2 ≠
NaOH +N2 ≠
NaOH +C ≠
Сера, хлор, бром, йод, фосфор и другие неметаллы диспропорционируют в щелочах (т.е. самоокисляются-самовосстанавливаются).
2NaOH +Cl2 0 = NaCl — + NaOCl + + H2O
6NaOH +Cl2 0 = 5NaCl — + NaCl +5 O3 + 3H2O
Кремний окисляется щелочами до степени окисления +4.
2NaOH + Si 0 + H2 + O= Na2Si +4 O3 + 2H2 0
Фтор окисляет щёлочи:
Более подробно про эти реакции можно прочитать в статье Окислительно-восстановительные реакции.
8. Щёлочи не разлагаются при нагревании.
Исключение — гидроксид лития:
2LiOH = Li2O + H2O
Основание (химия)
Основа́ния — класс химических соединений.
В статье смысл термина «основание» раскрывается в первом, наиболее широко используемом значении — осно́вные гидрокси́ды.
Содержание
Получение
Классификация
Основания классифицируются по ряду признаков.
Деление на растворимые и нерастворимые основания практически полностью совпадает с делением на сильные и слабые основания, или гидроксиды металлов и переходных элементов
Если в соединении есть оксидные и гидроксидные анионы одновременно, то в названиях используются числовые приставки:
Для соединений, содержащих группу O(OH), используют традиционные названия с приставкой мета-:
Для оксидов, гидратированных неопределённым числом молекул воды, например Tl2O3•n H2O, недопустимо писать формулы типа Tl(OH)3. Называть такие соединениями гидроксидами также не рекомендуется. Примеры названий:
Особо следует именовать соединение NH3•H2O, которое раньше записывали как NH4OH и которое в водных растворах проявляет свойства основания. Это и подобные соединения следует именовать как гидрат:
Химические свойства
См. также
Литература
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Hg2 2+ | Pb 2+ | Sn 2+ | Cu + | Cu 2+ | |
| OH − | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F − | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р |
| Br − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I − | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S 2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | — | Н | Н | Н | Н |
| SO3 2− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO4 2− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3 − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | Р |
| NO2 − | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO4 3− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO3 2− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | — | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN − | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO3 2− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
Полезное
Смотреть что такое «Основание (химия)» в других словарях:
Основание однородное — – естественное основание, сложенное горной породой одного вида. [Терминологический словарь по строительству на 12 языках (ВНИИИС Госстроя СССР)] Рубрика термина: Горные породы Рубрики энциклопедии: Абразивное оборудование, Абразивы,… … Энциклопедия терминов, определений и пояснений строительных материалов
Основание — – поверхность, на которую наклеивают стеновое покрытие, например стена или потолок. [ГОСТ Р 52805 2007] Рубрика термина: Обои Рубрики энциклопедии: Абразивное оборудование, Абразивы, Автодороги, Автотехника … Энциклопедия терминов, определений и пояснений строительных материалов
ХИМИЯ АНАЛИТИЧЕСКАЯ — наука о методах определения химического состава веществ. Химический анализ буквально пронизывает всю нашу жизнь. Его методами проводят скрупулезную проверку лекарственных препаратов. В сельском хозяйстве с его помощью определяют кислотность почв… … Энциклопедия Кольера
Основание Харькова — Харько, Харьков (Харитон) мифический персонаж казак Харько, Харьков Имя при рождении: вероятно, Харитон … Википедия
Неорганическая химия — Неорганическая химия раздел химии, связанный с изучением строения, реакционной способности и свойств всех химических элементов и их неорганических соединений. Это область охватывает все химические соединения, за исключением органических… … Википедия
Россия. Русская наука: Химия — Изучение химии в России формально ведет свое начало с учреждения в 1725 г. в СПб. Академии наук. В 1727 г. в качестве натуралиста и химика был приглашен сын тюбингенского аптекаря Иоганн Георг Гмелин, проведший почти все время своего пребывания в … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Органическая химия — В Викисловаре есть статья «органическая химия» Органическая химия раздел химии, изучающий со … Википедия
Аналитическая химия — Содержание … Википедия
Российский научный центр «Прикладная химия» — (ФГУП РНЦ «Прикладная химия») … Википедия
ФИЗИЧЕСКАЯ ХИМИЯ — ФИЗИЧЕСКАЯ ХИМИЯ, «наука, объясняющая на основании положений и опытов физическую причину того, что происходит через хим. операции в сложных телах». Это определение, к рое ей дал первый физико химик М. В. Ломоносов в курсе, прочитанном … Большая медицинская энциклопедия