Что значит экспрессия клеток опухоли
Диагностика экспрессии PD-L1
Что представляет собой лиганд программируемой клеточной гибели PD-L1?
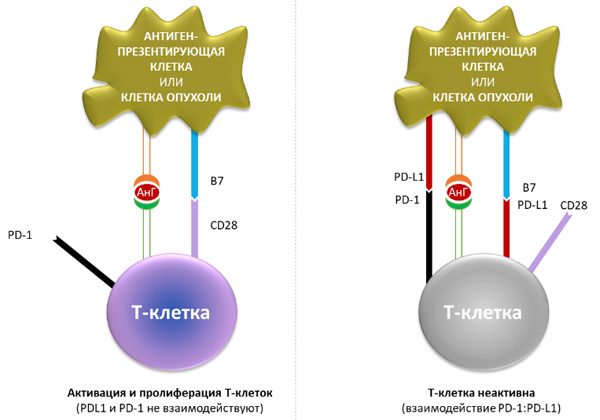
PD-L1 – лиганд рецептора программируемой клеточной гибели 1 (PD-1). Это трансмембранный белок с молекулярной массой 40 кДа, экспрессируемый на T- и B-лимфоцитах, NK-клетках, дендритных клетках, макрофагах, мезенхимальных стволовых клетках. PD-L1 способен связываться не только с рецептором PD-1, но и обладает сродством к CD80 (B 7.1) – белку, находящемуся на поверхности дендритных клеток, активированных B-клеток и моноцитов, который стимулирует активацию и выживаемость Т-лимфоцитов путем взаимодействия с CD28 на их поверхности. Лиганд PD-L1 способен угнетать этот процесс путем конкурентного связывания с CD80. На рисунке 1 представлены межклеточные взаимодействия (активирующие и ингибирующие сигналы) между Т-лимфоцитом и антигенпрезентирующей клеткой.
Рисунок 1. PD-1/PD-L1 сигнальный каскад в межклеточном взаимодействии иммунокомпетентных клеток. При связывании лиганда PD-L1 (лиганд рецептора программируемой клеточной смерти 1, также называемого PD-1) с рецепторами PD-1 и B7.1, находящимися на Т-лимфоцитах, происходит угнетение цитотоксической активности Т-лимфоцитов.
Роль PD-L1 в патогенезе злокачественных образований
Воздействие на сигнальный путь иммунной контрольной точки PD-1:PD-L1 лежит в основе иммунной терапии рака легкого, молочной железы, уротелиального рака и других злокачественных новообразований. Воздействие направлено на рецептор PD-1 и его лиганды PD-L1 и PD-L2. Наиболее важная роль в ускользании опухоли от иммунного ответа отводится взаимодействию рецептора PD-1 и лиганда PD-L1.
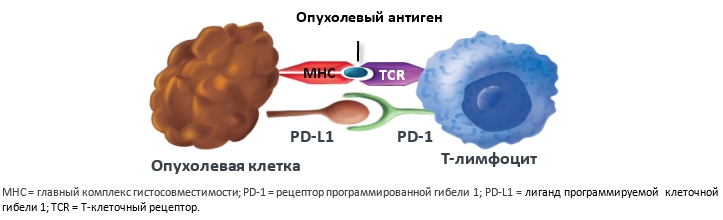
Длительная антигенная стимуляция, часто наблюдаемая при опухолевых заболеваниях, приводит к устойчивой экспрессии рецептора PD-1 на T-лимфоцитах и повышению экспрессии лигандов PD-L1 на опухолевых и иммунных клетках. Таким образом, опухоль вырабатывает механизм ускользания от иммунного ответа посредством гиперэкспрессии лиганда PD-L1, который, связываясь с рецептором PD-1 на T-лимфоцитах, нарушает их цитотоксическую активность (рис.2).
Рисунок 2. Сигнальный путь PD-1:PD-L1, инактивирующий действие Т-лимфоцитов.
Что нужно учитывать при выборе теста для оценки PD-L1 экспрессии?
Тест для определения экспрессии PD-L1 позволяет выделить группу пациентов с наибольшей вероятностью ответа на терапию ингибиторами иммунных контрольных точек. Важно учитывать, что для различных иммунных препаратов и показаний существуют отличия в методике проведения PD-L1 тестирования:
Вывод – перед проведением PD-L1 исследования необходимо удостовериться, что выбран правильный тест, на правильной культуре клеток и корректно интерпретировать полученные результаты.
Каким пациентам необходимо определение уровня PD-L1 экспрессии?
Анализ экспрессии PD-L1 в зависимости от планируемой к назначению терапии может быть рекомендован к назначению пациентам с:
НМРЛ: методы определения экспрессии PD-L1
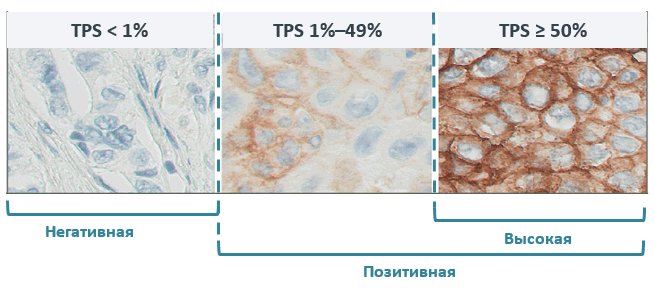
Экспрессия PD-L1 определяется методом иммуногистохимии. Оценка осуществляется путем подсчета соотношения опухолевых клеток с позитивным окрашиванием мембраны к общему количеству опухолевых клеток (TPS – tumor proportion score), результат выражается в процентах от 0 до 100.
В России зарегистрированы три диагностических набора для определения экспрессии PD-L1: производства Roche Diagnostics – PD-L1 sp142 и sp263, производства Dako – PD-L1 22C3. Тестирование проводится на платформах Ventana и Dako Autostainer Link 48 соответственно.
Экспрессия PD-L1 на опухолевых клетках
По уровню экспрессии PD-L1 выделяют следующие группы: отрицательная и позитивная экспрессия, в зависимости от количества окрашенных клеток.
Для тестирования может быть использован операционный или биопсийный материал первичной или метастатической опухоли, фиксированный в формалине и залитый в парафин. Обязательным требованием является наличие в исследуемом образце не менее 100 живых опухолевых клеток.
Определение уровня экспрессии PD-L1 и персонализированный подход к выбору терапии, основанный на результатах иммуногистохимического тестирования, позволяет сделать лечение пациентов с немелкоклеточным раком легкого более эффективным и безопасным в 1 линии терапии.
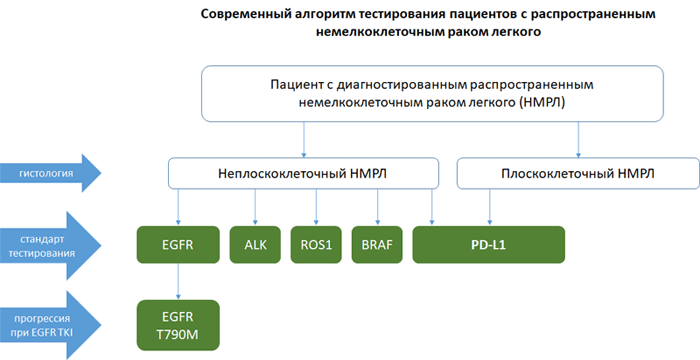
Алгоритм тестирования при распространенном НМРЛ
УРОТЕЛИАЛЬНЫЙ РАК: методы определения экспрессии PD-L1
Стандартом терапии 1 линии пациентов с раком уротелия продолжают быть химиотерапевтические режимы на основе цисплатина [4]. Однако по данным литературы до 50% больных не подходят для назначения данной терапии [5]. Ситуация с лечением изменилась с появлением иммунотерапевтических анти-PD-L1 препаратов [7]. Сейчас для назначения иммунотерапии в первой линии распространенного уротелиального рака пациентам, которые не могут перенести ципсплатин, рекомендовано проведение PD-L1 диагностики. Для остальных групп пациентов диагностика PD-L1 не требуется (при невозможности проведения любой платиносодержащей химиотерапии и у пациентов с прогрессированием заболевания в ходе или после окончания любой платиносодержащей химиотерапии или в течение 12 месяцев после неоадъювантной или адъювантной химиотерапии).
Какой метод используется для определения экспрессии PD-L1 у пациентов с уротелиальным раком?
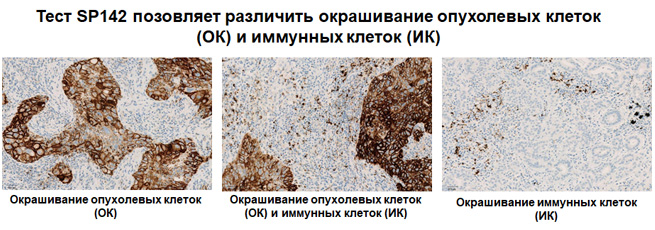
Экспрессия PD-L1 определяется методом иммуногистохимии. Для этих целей используется диагностический набор Ventana PD-L1 (SP142) Assay (Ventana Medical Systems, Inc.). Для тестирования используется ткань опухоли, фиксированная в формалине и залитая в парафиновый блок. PD-L1 статус у пациентов с уротелиальной карциномой определяется как часть площади опухоли, занятая PD-L1 экспрессирующими иммунными клетками, инфильтрирующими опухоль, любой интенсивности окрашивания.
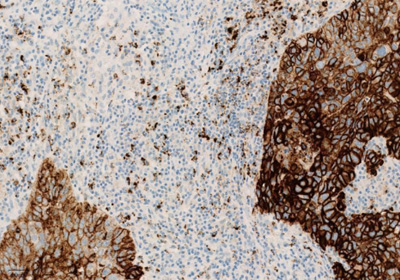
Рисунок 3. Окрашивание опухолевых и иммунокомпетентных клеток, инфильтрирующих опухоль, с помощью ИГХ-анализа VENTANA PD-L1 (SP142).
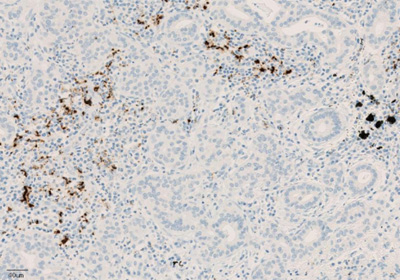
Рисунок 4. Окрашивание иммунокомпетентных клеток, инфильтрирующих опухоль, с помощью ИГХ-анализа VENTANA PD-L1 (SP142).
Определение уровня экспрессии PD-L1 иммуногистохимическим методом позволяет выделить группу пациентов для назначения анти-PD-L1 терапии.
Какой уровень PD-L1 экспрессии является основанием для назначения иммуннотерапии при уротелиальном раке?
Наличие у пациентов экспрессии PD-L1 ≥5% на иммунокомпетентных клетках, инфильтрирующих ткань уротелиальной карциномы, по данным клинических исследований ассоциирована с увеличением частоты объективного ответа на иммунную терапию.
ТНРМЖ: методы определения экспрессии PD-L1
Тройной негативный рак молочной железы – самая агрессивная форма среди рака молочной железы [4]. Традиционно применяемая химиотерапия не позволяла достичь значимого увеличения продолжительности жизни свыше медианы в 18 месяцев. Появление анти-PD-L1 терапии, с одной стороны, позволило преодолеть медиану общей выживаемости в 2 года, а с другой стороны – для назначения терапии необходимо выделить группу PD-L1 позитивных пациентов. В отличие от уротелиального рака, назначение анти-PD-L1 терапии обязательно требует тестирования пациенток с тройным негативным раком молочной железы.
Какой метод используется для определения экспрессии PD-L1 у пациентов с ТНРМЖ?
При определении статуса PD-L1 для решения вопроса об иммунотерапии важно выбрать оптимальный метод. Тест VENTANA PD-L1 (SP142) позволяет идентифицировать пациентов с тройным негативным раком молочной железы (ТНРМЖ), которые могут получать анти-PD-L1 терпию.
Ткани пациентов с ТНРМЖ, окрашенные с использованием теста VENTANA PD-L1 (SP142), оценивают по окрашиванию инфильтрирующих опухоль иммунных клеток (IC). IC – это иммунные клетки, присутствующие в интратуморальной и прилегающей перитуморальной строме. В это понятие включены лимфоциты, макрофаги, дендритные клетки и полиморфноядерные лейкоциты. IC оценивают как долю области опухоли, которую занимают иммунные клетки с окрашиванием PD-L1 любой интенсивности.
Какой уровень PD-L1 экспрессии является основанием для назначения иммунной терапии при ТНРМЖ?
Наличие у пациентов экспрессии PD-L1 ≥1% на иммунокомпетентных клетках, инфильтрирующих ткань опухоли, по данным клинических исследований ассоциирована с увеличением общей выживаемости, выживаемости без прогрессирования и частоты объективного ответа на иммунную терапию.
О программе определения экспрессии PD-L1
Для того, чтобы отправить материал на диагностику, вы должны быть зарегистрированным пользователем. Если у вас уже есть логин и пароль, то повторная регистрация не требуется.
Если вы новый пользователь, пожалуйста, пройдите процедуру регистрации.
Что значит экспрессия клеток опухоли
ИГХ, иммуногистохимическое исследование ткани, исследование образца опухолевой ткани, исследование ткани опухоли.
Какой биоматериал можно использовать для исследования?
Локализация б/м: образец ткани (биоптат) опухолевого образования стенки матки.
Общая информация об исследовании
Миома матки является самым распространенным доброкачественным новообразованием органов женской репродуктивной системы и выявляется у 25-30 % женщин.
Самая высокая заболеваемость и большинство показаний к оперативному лечению (быстрый рост, большие размеры узла, подозрение на малигнизацию лейомиомы) приходятся на перименопаузальный возрастной период, являющийся наиболее критическим по подобным рискам в жизни женщины. Возникающие болезни адаптации и компенсации, эндокринные, метаболические и иммунологические расстройства предрасполагают к манифестации опухолевых заболеваний.
Существуют определенные трудности в тактике ведения данного контингента больных. Реальный прогресс в решении проблем морфологической диагностики опухолей достигнут с использованием иммуноцистохимических методик. Оценка пролиферативной активности опухоли стала возможной на основании анализа белков ядра, связанных с репликацией ДНК, выявленных при помощи антител к Ki-67. Полученные данные помогают определиться с методикой лечения и объемом оперативного вмешательства по поводу быстро растущей миомы. Прежде всего это касается решения вопроса о сохранении придатков матки.
Большое значение при выборе тактики лечения, прогнозе риска осложнений имеет установление гистологического типа лейомиомы матки. ВОЗ рекомендует выделять обычную, или простую, лейомиому и гистологические варианты лейомиомы (клеточная, митотически активная, эпителиоидная, миксоидная, атипическая лейомиома и липолейомиома и т. д.). В настоящее время описано три основные формы миомы матки: 1) простая лейомиома, развивающаяся по типу доброкачественной очаговой мышечной гиперплазии, 2) митозы отсутствуют вовсе либо 3) единичные. Данная методика позволяет помочь в диагностике и дифференцировании лейомиом.
Иммуногистохимия (ИГХ) – метод выявления точной локализации клеточного или тканевого компонента (антигена) с помощью иммунологических и гистохимических реакций; при этом иммунологический анализ срезов тканей или цитологического материала проводится в условиях сохранения морфологии клеток. В диагностической практике можно выделить несколько основных областей применения ИГХ: во-первых, при исследовании опухолей человека в целях определения гистогенеза недифференцированных опухолевых образований, отдаленных метастазов, для дифференцировки различных тканевых компонентов, составляющих комплексные опухоли; во-вторых, в целях прогностической оценки дальнейшего течения заболевания и, наконец, при назначении терапии.
В целях прогностической оценки заболевания, предсказания биологического поведения опухоли, появления метастазов, эффективности терапии проводят исследование пролиферативной активности (Ki-67), выраженности ангиогенеза, выявление рецепторов к стероидным гормонам, изучение степени анаплазии клеток (мутантный белок гена p53).
Антиген Ki-67 является специфичным и оптимальным для широкого использования в патологоанатомической практике маркером пролиферации. Он впервые описан Gerdes и соавторами в 1983 г., состоит из двух полипептидных цепей с молекулярной массой 345 и 395 кДа. Это основная часть нуклеарного матрикса, в течение интерфазы ассоциированная с хромосомами фазы митоза. Ki-67−димерная молекула, имеющая тесную связь с 10-й хромосомой, конкретная роль этого протеина в процессе клеточного деления до сих пор точно не выяснена. Экспрессия Кi-67 позволяет выделить опухолевые клетки, находящиеся в активной фазе клеточного цикла, на всём его протяжении (G1-, S-, G2- и M-фазы). Кi-67 отсутствует только в G0-периоде. Активно пролиферирующие опухолевые клетки представляют собой «фракцию роста» новообразования. Антиген Ki-67, выявляемый соответствующими моноклональными антителами, представляет собой короткоживущий протеин, он разрушается в течение 1,5-2 часов. Поэтому антитела к Ki-67 выявляют только делящиеся клетки, так как Ki-67 не успевает накапливаться и не остается в покоящихся клетках. Пролиферативная активность является ведущим фактором как в механизме злокачественной трансформации клеток, так и в биологическом поведении уже возникших опухолей. Это наиболее важная характеристика фенотипа опухоли, в значительной степени определяющая скорость роста новообразования, риск метастазирования, потенциальный ответ на лечебные мероприятия и исход онкологического заболевания. Многие факторы, влияющие на течение и исход онкологических заболеваний, свое патогенетическое действие на опухоль опосредуют через изменение пролиферативной активности. Оценка пролиферативной активности опухолевых клеток необходимо не только для определения биологических характеристик опухолей, но и для селективного подхода к выбору терапии.
Индекс пролиферативной активности в различных опухолях имеет разные значения, являясь при этом независимым прогностическим признаком, определяющим клиническое течение и прогноз заболевания. При Ki-67 менее 15 % опухоль считается менее агрессивной, при показателе более 30 % опухоль считается высокоагрессивной. При высоком уровне (выраженном в %) Ki-67 опухоль с более высокой вероятностью ответит на химиотерапевтическое лечение. При низком его уровне опухоль при определённых условиях лучше отреагирует на гормонотерапию. Тест проводится на образце ткани, полученном из опухоли в результате биопсии или оперативным путем.
Дополнительно проводится комплексное определением пролиферативной активности гладкомышечных актинов – сократительных белков, являющихся главными компонентами системы микрофиламентов клетки. Выявлено шесть основных изоформ актина. Антитела к альфа-актину гладких мышц являются надежными маркерами для определения гладкомышечных опухолей. SMA и α-SMA также окрашивают клетки с частичной гладкомышечной дифференцировкой: перициты, миоэпителиальные клетки и миофибробласты. Определение перицитов вокруг сосудистых структур – признак доброкачественного сосудистого процесса, тогда как в большинстве злокачественных сосудистых новообразованиях число перицитарных клеток снижено. Высокая экспрессия гладкомышечного актина отмечается при непролиферативной и умеренной степени пролиферативной формы лейомиомы. В случае пролиферативной формы изменений выраженной степени экспрессия гладкомышечного актина слабее. Маркером, определяющим благоприятное течение заболевания, является высокая экспрессия гладкомышечного актина.
Комплексное гистологическое и иммуногистохимическое исследование с определением пролиферативной активности в растущих лейомиомах по экспрессии KI-67 и гладкомышечного актина представляет ценный современный метод диагностики, позволяющий определить степень пролиферативной активности и анаплазии опухолевых клеток, охарактеризовать прогноз и предложить адекватные методы лечения. Однако не следует и преувеличивать возможности данного метода при лечении конкретного пациента. Данный вид обследования является только дополнительной методикой исследования, и его результаты должны быть интерпретированы в контексте с другими данными обследования, включая клинические.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
При использовании данного метода визуализации антигенов должно получиться интенсивное четко выявляемое окрашивание тканевых антигенов в исследуемом образце и позитивном контроле. Окрашивание негативного контроля также необходимо принимать во внимание при оценке специфичного расположения исследуемых антигенов. Интерпретация полученных результатов ИГХ-реакции включает такие термины, как «выраженная позитивная реакция», «ложно-позитивная реакция», «негативная реакция», «ложно-негативное окрашивание».
Кто назначает исследование?
Экспрессия маркеров опухолевого роста
Экспрессия маркеров опухолевого роста: HER 2 neu, Ki 67, P 53, как фактор влияния на метастазирование рака молочной железы в легкие
В.Н. Плохов, И.И. Андреяшкина*
Кафедра онкологии с курсом онкологии ВолгГМУ, Дорожная клиническая больница на ст. Саратов II ОАО «РЖД»*
В работе представлен анализ данных литературы и результатов собственных наблюдений авторов относительно выявления закономерностей экспрессии маркеров опухолевого роста HER 2 neu, Ki 67, P 53 при метастазировании рака молочной железы в легкие. Рассмотрено влияние гиперэкспрессии HER 2 neu на клинические варианты метастазирования рака молочной железы в легкие. Оценены изменения иммуногистохимических маркеров на фоне проведения полихимиотерапии.
Ключевые слова: рак молочной железы, метастазы в легкие, иммуногистохимические маркеры.
Expression of tumors growth markers her 2 neu, ki 67, p 53 as afactor affecting mammary cancer metastasizing into lungs
V.N. Plohov, I.I. Andreiashkina
The paper presents an analysis of literature data and results of authors own observations on the identification of patterns of expression of markers of tumor growth: HER 2 neu, Ki 67, P 53, with metastatic breast cancer in the lungs. The influence of overexpression of HER 2 neu in clinical variants of metastatic breast cancer in the lungs. Evaluate the changes of immunohistochemical markers on the background of the chemotherapy.
Key words: breast cancer, lung metastases, immunohistochemical markers.
При метастазировании рака молочной железы в легкие большое значение имеет учет факторов, предсказывающих эффект от лечения и прогноз течения заболевания [3, 6]. Для определения прогноза и выбора терапии при метастазах рака молочной железы в легкие важное значение имеют ряд молекулярных маркеров. Во многих исследованиях получены доказательства большого прогностического значения таких иммуногистохимических маркеров, как эпидермальный фактор роста HER 2 neu, тканевые маркеры пролиферации и апоптоза при раке молочной железы. Иммуногистохимическое исследование позволяет оценивать данные показатели в связи с клеточным циклом опухоли [2, 5, 8].
Знание иммуногистохимических маркеров как эпидермальный фактор роста HER 2 neu, тканевые маркеры пролиферации и апоптоза позволяют разработать оптимальную модель для оценки риска метастазирования рака молочной железы в легкие у отдельного больного и выбора метода лечения [1, 4, 7, 9].
В изученной нами литературе практически отсутствуют систематизированные сведения о значении таких иммуногистохимических маркеров, как эпидермальный фактор роста HER 2 neu, тканевые маркеры пролиферации и апоптоза в построении оптимальной модели для оценки риска метастазирования рака молочной железы в легкие у отдельного больного и выбора метода лечения.
Установление закономерностей экспрессии маркеров опухолевого роста HER 2 neu, Ki 67, P 53 при метастазировании рака молочной железы в легкие.
Проведена сравнительная оценка показателей иммуногистохимического статуса у больных раком молочной железы с метастазами в легкие, находившихся на лечении в клинике факультетской хирургии и онкологии ГОУ ВПО Саратовского ГМУ им. В. И. Разумовского Минздравсоцразвития России, НУЗ Дорожная клиническая больница на ст. Саратов II ОАО «РЖД» за период с 2008 по 2010 гг.
В группы наблюдения были включены 62 больных раком молочной железы с метастазами в легкие (средний возраст составил 57,6 лет). Исследование проводилось в три этапа исследования: I этап — исследование уровня HER 2 neu, Ki 67, P 53 у первичных больных (до выявления метастазов в легкие); II этап — исследование уровня HER 2 neu, Ki 67, P 53 в метастатическом лимфоузле у первичных больных (до выявления метастазов в легкие); III этап — исследование уровня HER 2 neu, Ki 67, P 53 метастатического узла в легких у больных раком молочной железы.
Определение HER 2 neu, Ki 67, P 53 проводилось авидин-биотиновым методом. Методика приготовления срезов из парафинового блока для иммуногистохимии практически не отличается от обычного их изготовления для гистологической окраски. Результаты иммуногистохимической реакции могут оцениваться полуколичественным способом. Следует отметить, что универсальной оценки иммуноокрашивания нет, в исследовании применялась качественная оценка реакции и выражалась как отрицательная (-), слабо положительная (+), умеренно положительная (++) и сильно положительная (+++) реакции.
Статистический анализ и графика выполнялись с помощью стандартного пакета прикладных программ «Statistica 6.0», «Excel 2000». При статистической обработке полученных результатов использовались: критерий Шапиро-Вилкс для оценки нормальности распределения, критерий Стьюдента для независимых переменных, критерий Манна-Уитни для оценки значимости различий между группами при отсутствии нормальности распределения признака, односторонний критерий Фишера для оценки значимости различий между группами по качественным признакам.
Результаты исследования и их обсуждение
Результаты исследований показали, что частота встречаемости опухолей с гиперэкспрессией HER 2 neu на I этапе исследования составила 58 %, тогда как опухоли с отрицательным HER 2 neu статусом отмечались в 14,5 % наблюдениях. Экспрессия HER 2 neu как фактор прогноза статистически коррелирует с экспрессией рецепторов эстрогенов (РЭ), рецепторов прогестерона (РП). При оценке гормонального статуса иммуногистохимическим методом положительная экспрессия рецепторов эстрогенов выявлена в 35 % наблюдениях, из них слабая отмечена в 57,2 % наблюдениях, умеренная в 28,6 % наблюдениях и выраженная — в 14,3 % наблюдениях. Экспрессия рецепторов прогестерона отмечена в 45 % наблюдениях, из них выраженная экспрессия выявлена в 22,2 % наблюдениях, умеренная — в 22,2 % наблюдений, слабая в 55,6 % наблюдений. Увеличение экспрессии HER 2 neu сопровождается уменьшением экспрессии РЭ в 75 % наблюдений и уменьшением экспрессии РП в 80 % наблюдений (p Заключение
Анализ приведенных выше данных относительно закономерностей экспрессии маркеров опухолевого роста HER 2 neu, Ki 67, P 53 при метастазировании рака молочной железы в легкие позволил сделать следующие выводы:
Определение экспрессии PR, ER, Ki67, HER-2 при раке молочной железы
Рак молочной железы – злокачественная опухоль железистой ткани молочной железы, является ведущей онкологической патологией у женщин. По данным Всемирной Организации Здравоохранения каждая восьмая женщина рискует заболеть этой патологией, независимо от возраста. Ежегодно в мире регистрируется от 800 тыс. – до 1 млн. новых случаев рака молочной железы (ВОЗ).
В настоящее время заболеваемость раком молочной железы возрастает в связи с проведением маммографического скрининга и общего старения населения (по данным European Society For Medical Oncology).
PR – рецептор к прогестерону.
ER – рецептор к эстрогену.
Ki67 – онкогенный белок.
HER-2 – Рецептор второго типа к человеческому эпидермальному фактору роста (human epidermal growth factor receptor 2).
Опухоли молочной железы являются гормонозависимыми опухолями. Эстроген и прогестерон оказывают стимулирующее действие на рост опухоли молочной железы. Белок Ki 67 является показателем пролиферативной активности опухолевых клеток. Повышенная экспрессия HER-2 характеризуется усилением пролиферации клеток, уменьшением количества рецепторов эстрогенов в опухоли, снижением эффективности химио- и гормонотерапии, таким образом, служит маркером неблагоприятного прогноза и повышенного риска рецидива заболевания.
На основании иммуногистохимического исследования (ИГХ) выделяют 4 подтипа рака молочной железы. Каждый подтип имеет свои особенности клинической картины, прогноз и тактику лечения.
Известно, что люминальные типы РМЖ имеют менее агрессивное течение и благоприятный прогноз по сравнению с HER-2 положительным и трижды негативным РМЖ. Особо обращает на себя внимание трижды негативный рак молочной железы (отрицательные РЭ, РП, HER2), который отличается агрессивным течением, ранним появлением метастазов и неблагоприятным прогнозом.
Молекулярно-биологические подтипы рака молочной железы
Определение в опухоли молочной железы экспрессии РЭ, РП, HER2 и Кi 67 является обязательным при диагностике РМЖ. Данное исследование включено в алгоритм диагностики и лечения рака молочной железы.
В заключении об исследовании должна содержаться информация не только о процентном содержании клеток, положительных по РЭ и РП, но и об интенсивности окрашивания. При сомнительном результате ИГХ исследования экспрессии HER2, рекомендуется проводить определение амплификации гена HER2 методом гибридизации in situ (FISH). (Согласно Практическим рекомендациям по лекарственному лечению инвазивного рака молочной железы, 2019 г.).
Для интерпретации результатов иммуногистохимического исследования рецепторного статуса опухоли молочной железы применяется шкала Allred, с помощью которой оценивается количество клеток, с рецепторами гормонов и интенсивность окрашивания при определении рецепторов. В данной шкале процент положительных клеток оценивается от 0 до 5 баллов, а интенсивность окрашивания от 0 до 3.
Показания к исследованию:
Определение экспрессии PR, ER, Ki67, HER-2 при раке молочной железы используется для выбора тактики назначения адъювантной терапии.
Адъювантная терапия – лекарственная терапия, которая назначается в дополнение к хирургическому и лучевому методам лечения и направлена на снижение риска рецидива болезни.
План адъювантной лекарственной терапии основывается на принадлежности опухоли к одному из молекулярно-биологических подтипов и стадии заболевания.