Что открывает реакция фоля
ЦВЕТНЫЕ И ИМЕННЫЕ КАЧЕСТВЕННЫЕ РЕАКЦИИ НА БЕЛКИ
История химии в школьном курсе
РЕАКЦИЯ ПИОТРОВСКОГО (БИУРЕТОВАЯ РЕАКЦИЯ)
В белках аминокислоты связаны друг с другом по типу полипептидов и дикетопиперазинов. Образование полипептидов из аминокислот происходит путем отщепления молекулы воды от аминогруппы одной молекулы аминокислоты и карбоксильной группы другой молекулы:
Образующаяся группа –С(О)–NН– называется пептидной группой, связь С–N, соединяющая остатки млекул аминокислот, – пептидной связью.
При взаимодействии дипептида с новой молекулой аминокислоты получается трипептид и т. д.
Дикетопиперазины образуются при взаимодействии двух молекул аминокислот с отщеплением двух молекул воды:
Дикетопиперазины были выделены из белков Н.Д.Зелинским и В.С.Садиковым в 1923 г.
Наличие в белке повторяющихся пептидных групп подтверждается тем, что белки дают фиолетовое окрашивание при действии небольшого количества раствора медного купороса в присутствии щелочи (биуретовая реакция).
Реакция идет по схеме:
Это реакция на цистеин и цистин. При щелочном гидролизе «слабосвязанная сера» в цистеине и цистине достаточно легко отщепляется, в результате чего образуется сероводород, который, реагируя со щелочью, дает сульфиды натрия или калия. При добавлении ацетата свинца(II) образуется осадок сульфида свинца(II) серо-черного цвета.
Описание опыта. В пробирку наливают 1 мл раствора цистина, прибавляют 0,5 мл 20%-го раствора гидроксида натрия. Смесь нагревают до кипения, а затем добавляют 0,5 мл раствора ацетата свинца(II). Наблюдается выпадение серо-черного осадка сульфида свинца(II):
Описание опыта. В пробирку наливают 5 капель 1%-го раствора глицина и прибавляют 1 каплю индикатора метилового красного. Раствор окрашивается в желтый цвет (нейтральная среда). К полученной смеси добавляют равный объем 40%-го раствора формальдегида (формалин). Появляется красное окрашивание (кислая среда):
Это реакция на аминокислоту глицин.
В таких солях ион меди координационными связями соединен с аминогруппами.
Описание опыта. В пробирку наливают 3 мл 3%-го раствора сульфата меди(II), добавляют несколько капель 10%-го раствора гидроксида натрия до образования голубого осадка. К полученному осадку гидроксида меди(II) приливают 0,5 мл концентрированного раствора глицина. При этом образуется темно-синий раствор глицината меди:
Описание опыта. В пробирку наливают 1 мл раствора тирозина и добавляют 0,5 мл концентрированной азотной кислоты. Смесь нагревают до появления желтой окраски. После охлаждения добавляют 1–2 мл 20%-го раствора гидроксида натрия до появления оранжевой окраски раствора:
Описание опыта. В пробирку наливают около
0,5 мл раствора уксуснокислого свинца и прибавляют раствор едкого кали до растворения образовавшегося осадка гидроксида свинца. В другую пробирку наливают
Триптофан, реагируя в кислой среде с альдегидами, образует окрашенные продукты конденсации. Например, с глиоксиловой кислотой (являющейся примесью к концентрированной уксусной кислоте) реакция протекает по уравнению:
По аналогичной схеме протекает и реакция триптофана с формальдегидом.
В ходе проведенного исследования мы выявили по литературным источникам имеющуюся информацию о цветных качественных реакциях на белковые аминокислоты; выполнили ряд перечисленных реакций и составили базу данных. Эта база может быть использована в школьной практике как в теоретическом плане, так и в практическом, т. к. мы приводим краткие, но подробные описания выполнения всех опытов.
Из предложенных 18 качественных реакций каждая практически осуществима в школьном курсе химии и имеет важное практическое значение. Сопровождение реакций химическими уравнениями конкретизирует и углубляет знания по биологической и органической химии, особенно знания учащихся специализированных биологических и химических классов.
Использованная литература
Ермаков А.Н., Арасимович В.В., Смирнова-Иконникова М.И., Мирри И.К. Методы биохимического исследования растений. М.,1952, 520 с.
Полянская А.С., Шевелева А.О. Методическая разработка по лабораторным работам: «Аминокислоты» и «Белки». Л., 1976, 37 с.
Пустовалова Л.М. Практикум по биохимии. 1999, 541 с.
Руководство к практическим занятиям по органической химии. Под ред. В.М.Родионова. М., 1954, 111 с.
Соловьев Н.А. Лабораторные работы по биологической химии. Методическая разработка. СПб., 1996, 70 с.
Филиппович Ю.Б., Егорова Т.А., Севастьянова Г.А. Практикум по общей биохимии. М., 1982, 311 с.
З.Саитов, С.В.Телешов, Б.Харитонцев,
секция «Юный химик» РХО им. Д.И.Менделеева (г. Тобольск)
Лабораторная работа №1
Лабораторная работа №1
ХИМИЯ ПРОСТЫХ БЕЛКОВ.
ЦВЕТНЫЕ РЕАКЦИИ НА БЕЛКИ И АМИНОКИСЛОТЫ
Белки представляют собой высокомолекулярные полимерные органические соединения, построенные из остатков различных α-аминокислот, соединенных ковалентной пептидной связью.
Присутствие белка в растворах можно обнаружить с помощью цветных реакций, обусловленных наличием в белке аминокислот, их специфических групп и пептидных связей. Существуют универсальные цветные реакции, т. е. на все белки (биуретовая и нингидриновая), и специфические, т. е. на определенные аминокислоты (ксантопротеиновая, Миллона, Фоля и др.).
На основании некоторых цветных реакций разработаны методы количественного определения белков и аминокислот, которые широко используются в биохимических лабораториях.
Цель: Ознакомиться с универсальными цветными реакциями на белки и специфическими реакциями на отдельные аминокислоты, содержащиеся в белковых растворах.
Работа 1. Биуретовая реакция на пептидную связь (Пиотровского)
Биуретовая реакция обусловлена наличием в белке пептидных связей, которые в щелочной среде образуют с сернокислой медью комплексы фиолетового цвета с красным или синим оттенком. Группа, образующая пептидную связь, в щелочной среде присутствует в своей таутомерной енольной форме:
При избытке щелочи происходит диссоциация ОН-группы, появляется отрицательный заряд, с помощью которого кислород взаимодействует с медью. Возникает солеобразная связь. Кроме того, медь образует дополнительные координационные связи с атомами азота, участвующими в пептидной связи, путем использования их электронных пар. Возникающий таким образом комплекс очень стабилен. Интенсивность окраски комплекса зависит от концентрации белка и количества медной соли в растворе.
Исследуемый материал: раствор яичного белка, раствор растительного белка, 1% раствор желатина.
Реактивы: 10% раствор NaOH, 1% раствор CuSO4.
Оборудование: пробирки, капельницы.
Ход работы. К 5 каплям водного раствора белка добавляют 5 капель 10% раствора NaOH и 2 капли 1% раствора CuSO4. Содержимое перемешивают. Оно приобретает сине-фиолетовый цвет. Нельзя добавлять избыток CuSO4, так как синий осадок маскирует характерное фиолетовое окрашивание биуретового комплекса.
Работа 2. Нингидриновая реакция на α-аминокислоты
Белки, полипептиды и свободные α-аминокислоты дают синее или фиолетовое окрашивание с нингидрином. При нагревании белка с водным раствором нингидрина аминокислоты окисляются и распадаются, образуя СО2, NH3 и соответствующий альдегид. Нингидрин, являясь сильным окислителем, вызывает окислительное дезаминирование α-аминокислоты, приводящее к образованию аммиака, двуокиси углерода, соответствующего альдегида и восстановленной формы нингидрина. Нингидрин восстанавливается и связывается со второй молекулой нингидрина посредством молекулы аммиака, образуя продукты конденсации, окрашенные в синий, фиолетовый, красный, а в случае пролина – в желтый цвет.
Цветные реакции на белки и аминокислоты
| Исследуемый материал | Окраска продукта | Реагирующая группа |
| Биуретовая реакция | ||
| Вода | ||
| Казеин | ||
| Яичный белок | ||
| Желатин | ||
| Аминокислота | ||
| Нингидриновая реакция | ||
| Вода | ||
| Казеин | ||
| Яичный белок | ||
| Желатин | ||
| Аминокислота | ||
| Ксантопротеиновая реакция | ||
| Казеин | ||
| Яичный белок | ||
| Желатин | ||
| Фенол | ||
| Реакция Фоля (на слабосвязанную серу) | ||
| Вода | ||
| Казеин | ||
| Яичный белок | ||
| Желатин |
НИНГИДРИНОВАЯ РЕАКЦИЯ. В этой реакции растворы белка, полипептидов, пептидов и свободных α-аминокислот при нагревании с нингидрином дают синее, сине-фиолетовое или розово-фиолетовое окрашивание. Окраска в этой реакции развивается за счет α-аминогруппы. Реакция протекает в две стадии.
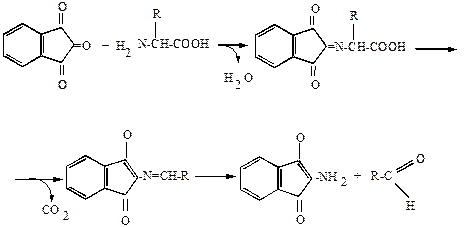 |
|
Нингидрин образует с аминокислотами соединения с двойной связью между углеродом и азотом, называемые иминами или основаниями Шиффа.
|
 |
|
Альдимин Промежуточный амин Альдегид
|
|
|
Эти соединения обладают высокой реакционной способностью. Дальнейшее превращение их приводит к промежуточному амину, который может реагировать со второй молекулой нингидрина, давая соединение окрашенное в сине-фиолетовый (пурпурный) цвет – сине-фиолетовый (пурпурный) Руэмана.
Очень легко реагируют с нингидрином a-аминокислоты. Наряду с ними сине-фиолетовый Руэмана образуют также белки, пептиды, первичные амины, аммиак и некоторые другие соединения. Вторичные амины, например пролин и оксипролин, дают желтую окраску.
Нингидриновую реакцию широко используют для обнаружения и количественного определения аминокислот.
ХОД РАБОТЫ. Берут пять пробирок, и вносят по 1 мл: в первую воды, во вторую – раствора казеина, в третью – раствора яичного белка, в четвертую – раствора желатины, в пятую – раствора аминокислоты (глицина). Затем в каждую пробирку добавляют по 10-12 капель раствора с массовой долей нингидрина в ацетоне или этаноле 1 %. Содержимое каждой пробирки перемешивают встряхиванием и ставят их в кипящую водяную баню на 3-5 мин. Записывают химизм реакции, схему постановки опыта, строение окрашенных соединений. Результаты вносят в табл. 1.
КСАНТОПРОТЕИНОВАЯ РЕАКЦИЯ. Эта реакция указывает на наличие в белках остатков ароматических аминокислот – тирозина, фенилаланина, триптофана. Основана на нитровании бензольного кольца радикалов этих аминокислот с образованием нитросоединений, окрашенных в желтый цвет (греческое «Ксантос» – желтый). На примере тирозина эту реакцию можно описать в виде следующих уравнений.
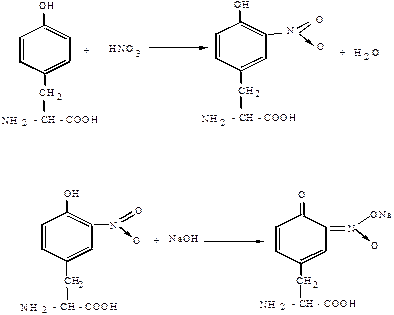 |
Тирозин Нитротирозин
|
Нитротирозин Натриевая соль нитротирозина
В щелочной среде нитропроизводные аминокислот образуют соли хиноидной структуры, окрашенные в оранжевый цвет.
Ксантопротеиновую реакцию дают бензол и его гомологи, фенол и другие ароматические соединения.
ХОД РАБОТЫ. Берут четыре пробирки и вносят по 1 мл: в первую раствора казеина, во вторую – раствора яичного белка, в третью – раствора желатины, в четвертую – раствора фенола. Во все пробирки добавляют по 10 капель концентрированной азотной кислоты. Содержимое перемешивают встряхиванием и пробирки помещают в кипящую водяную баню на 5-8 мин. Под действием кислоты появляется осадок белка, который при нагревании окрашивается в желтый цвет. После бани пробирки выдерживают при комнатной температуре 4-5 мин и записывают окраску содержимого. Затем в каждую пробирку прибавляют по 1 мл раствора с массовой долей гидроксида натрия 30 % (или другую щелочь). Содержимое пробирок перемешивают встряхиванием, окраску записывают. Работу оформляют в соответствии с табл.1.
РЕАКЦИЯ ФОЛЯ (на слабосвязанную серу). Этой реакцией открывают в белках радикалы цистеина содержащие как свободные –SH (тиоловые) радикальные группы, так и окисленные с образованием дисульфидных (-S-S-) связей цистина.
При нагревании белка, содержащегося в молекуле остатки цистеина и цистина, с концентрированным раствором щелочи и ацетатом (или другой растворимой солью) свинца (реактив Фоля) образуется бурое или черное окрашивание. Это объясняют тем, что под действием щелочи от радикалов цистеина отщепляется сера в виде иона со степенью окисления минус два, который, взаимодействуя с ионом свинца (II), дает бурый или черный нерастворимый осадок сульфида свинца. Белки, в составе которых нет цистина и цистеина, реакцию Фоля не дают. Химизм процесса можно описать следующими реакциями:
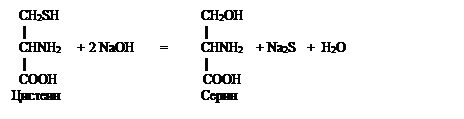 |
Ацетат свинца Ацетат натрия
При нагревании со щелочью часть белка подвергается гидролизу. Кроме того происходит отщепление части аминогрупп (реакция дезаминирования) в виде аммиака, который можно обнаружить по запаху и посредством смоченной водой красной лакмусовой бумажки, поднесенной к отверстию пробирки (не касаться стенок!).
ХОД РАБОТЫ. Берут четыре пробирки и вносят по 1 мл: в первую воды, во вторую – раствора казеина, в третью – раствора яичного белка, в четвертую – раствора желатины. В каждую пробирку добавляют по 1 мл раствора с массовой долей гидроксида натрия 30 % и по 6-8 капель раствора с массовой долей ацетата свинца 5 %, или можно приготовить реактив Фоля на всю подгруппу и добавить по 1 мл в каждую пробирку приготовленного раствора. Содержимое перемешивают встряхиванием, и пробирки помещают в кипящую водяную баню на 5-7 мин. Окраску содержимого пробирок записывают. Результаты оформляют в табл. 1.
РЕАКТИВЫ.Вода дистиллированная (в дальнейшем вода); растворы с массовыми долями: казеина 1 %, желатины 1 %, яичного белка 1 %, сульфата меди 1 %, гидроксида натря 10 и 30 %, глицина (или другой аминокислоты) 0,1 %, фенола 0,1 %, ацетата свинца 5 %, нингидрина в ацетоне или этаноле 1 %; концентрированная азотная кислота.
Реактив Фоля готовят в пробирке перед определением. В пробирку вносят 1 мл 5 % раствора ацетата свинца и небольшими порциями (по 1,5-2 мл) приливают 30 % раствор гидроксида натрия с интервалом 30 сек, каждый раз, перемешивая, до растворения молочно-белого хлопьевидного осадка появившегося после внесения первой порции гидроксида натрия.
1. Общая характеристика пептидов, полипептидов, белков и их строения.
2. Как соединяются аминокислоты в молекуле белка и за счет каких групп? Соедините Ала, Цис, Сер.
3. Перечислите цветные реакции на белки и аминокислоты.
4. Какая реакция открывает пептидные связи? Её химизм.
5. Что характеризуют цвет и интенсивность окраски при положительной биуретовой реакции?
6. Что открывает нингидриновая реакция? Её химизм.
7. Назовите аминокислоты имеющие в радикале бензольное кольцо. Какой реакцией можно обнаружить ароматические аминокислоты? Её химизм.
8. Назовите аминокислоты содержащие серу. Какую из них обнаруживает реакция Фоля? Химизм реакции.
9. Какую цветную реакцию используют для количественного определения белков в растворе и почему?
10. Какую цветную реакцию используют для количественного определения α-аминокислот и почему?
Реакция на слабосвязанную серу (реакция Фоля)
Лабораторная работа № 1
Качественные реакции на белки и аминокислоты
Реактивы, оборудование: 10% и 20% растворы гидроксида натрия, 1% раствор медного купороса, 0,5% водный раствор нингидрина, 1% раствор нингидрина в 95% растворе ацетона, конц. азотная и серная кислоты, реактив Миллона, реактив Фоля, 0,1% раствор фенола, ледяная уксусная кислота, 5% свежеприготовленный раствор нитропруссида натрия, 0,2% спиртовой раствор α-нафтола, раствор гипобромита натрия, крист. мочевина, 40% раствор мочевины, 0,01% раствор аргинина, 0,01% раствор тирозина, 0,005% раствор триптофана, раствор глиоксиловой кислоты, 1% раствор яичного белка, 1% раствор желатина, 10% раствор углекислого натрия, 1% раствор сульфаниловой кислоты в 5% растворе соляной кислоты (1:3), 5% раствор нитрита натрия; штативы с пробирками, держатели, спиртовки, стеклянные трубочки, пипетки.
Биуретовая реакция
Биурет – вещество, образующееся при нагревании мочевины и содержащее пептидные связи в молекулах. Если к раствору этого вещества добавить гидроксид натрия и несколько капель раствора медного купороса, то образуется продукт розового или сине-фиолетового цвета. Полученное окрашенное вещество называется биуретовым медным комплексом, а сама реакция получила название биуретовой.
О ООО
Мочевина биурет
Биуретовый медный комплекс
Биуретовую реакцию могут давать все вещества, которые содержат не менее двух пептидных связей. Раствор белка в щелочной среде при взаимодействии с ионами меди также приобретает сине-фиолетовый цвет, а продукты неполного гидролиза белков дают розовое окрашивание. И в этом случае происходит образование биуретового медного комплекса.
Интенсивность окраски биуретового комплекса зависит от концентрации белка и количества медной соли в растворе, поэтому биуретовую реакцию можно использовать для определения концентрации белка в растворе.
Опыт 1. К 1 мл 1% раствора яичного белка прибавляют 1 мл 10% раствора гидроксида натрия, 2-3 капли 1% раствора медного купороса и все перемешивают. Раствор приобретает фиолетовую окраску.
Опыт 2. Небольшое количество кристаллической мочевины поместить в пробирку, расплавить над спиртовкой и продолжать нагревать в течение 1-2 минут. Пробирку охладить, добавить 1-2 мл дист. воды для растворения образовавшегося вещества и проделать с ним биуретовую реакцию. Раствор должен приобрести розовую окраску.
Нингидриновая реакция
Аминодикетогидринден конденсируется еще с одной молекулой нингидрина. Образующееся соединение после енолизации переходит в окрашенную форму, получившую название «сине-фиолетовый комплекс Руэмана». Если реакция протекает в среде с органическими растворителями (спиртом или ацетоном), то продукт этой реакции содержит в своем составе радикал исходной аминокислоты, который и обуславливает различную окраску этого продукта: голубую, красную, синюю, фиолетовую, а в присутствии пролина – желтую.
Эта реакция с раствором нингидрина в ацетоне или спирте используется для идентификации аминокислот после хроматографии, для открытия отдельных аминокислот и для определения их количества.
Опыт 3. К 2 мл раствора белка добавляют несколько капель 0,5% водного раствора нингидрина и кипятят 1-2 мин. В пробирке появляется розово-фиолетовое окрашивание, а с течением времени раствор синеет.
Опыт 4. Аналогичную реакцию проделывают с раствором глицина и пролина, используя раствор нингидрина в ацетоне.
Ксантопротеиновая реакция
Этой реакцией можно доказать присутствие в белке ароматических аминокислот: триптофана, тирозина, фенилаланина. При добавлении к раствору белка концентрированной азотной кислоты появляется желтое окрашивание. Если к полученному раствору добавить щелочь, то окраска переходит в оранжевую.
Ксантопротеиновая реакция не является строго специфичной. Так как она обусловлена нитрованием ароматического ядра, то ее дают многие ароматические соединения, не являющиеся аминокислотами, например, фенол.
В щелочной среде нитропроизводные аминокислот образуют соли хиноидной структуры, окрашенные в оранжевый цвет.
Опыт 5. В одну пробирку наливают 2 мл раствора яичного белка, а в другую – 2 мл раствора желатина. В обе пробирки добавляют по 1 мл конц. азотной кислоты и нагревают. В первой пробирке образуется желтый осадок, а во второй – очень слабое окрашивание, так как желатин почти не содержит ароматических аминокислот. После охлаждения в каждую пробирку добавляют 20% раствор гидроксида натрия или концентрированный раствор аммиака до появления оранжевого окрашивания вследствие образования натриевой соли нитротирозина.
Реакция Миллона
Аминокислота тирозин, а также белки, содержащие в своем составе эту аминокислоту, взаимодействуют с реактивом Миллона, (смесь нитратов и нитритов оксида ртути (I) и (II) в концентрированной азотной кислоте). При кипячении образуется кроваво-красный осадок ртутной соли динитротирозина. Белки, которые не содержат тирозина, такие как желатин, протамины, реакцию Миллона не дают.
Опыт 6. Реакцию Миллона проделывают с тремя веществами: яичным белком, желатином и фенолом. В первую пробирку добавляют 2 мл 1% раствора яичного белка, во вторую – 2 мл 0,1% раствора фенола, в третью – 2 мл 1% раствора желатина. В каждую пробирку добавляют по 1 мл раствора Миллона и осторожно нагревают. В пробирке с яичным белком появляется кроваво-красное окрашивание, в пробирке с фенолом – красное, а в пробирке с желатином жидкость бесцветна или слегка желтеет.
Реакция на слабосвязанную серу (реакция Фоля)
У белков, содержащих цистеин, при нагревании в щелочной среде происходит гидролиз сульфгидрильных групп с образованием сульфида натрия. Сульфид натрия с плюмбитом свинца дает черный или бурый нерастворимый осадок сульфида свинца. Реакция протекает по уравнению:
В аминокислоте метионин сера связана прочно, поэтому метионин в отличие от цистеина этой реакции не дает.
Опыт 7. В пробирку налить 2 мл раствора белка и 2 мл реактива Фоля (к 5% водному раствору ацетата свинца добавляют 30% раствор гидроксида натрия до растворения образовавшегося осадка). Полученный раствор прокипятить, через 1 – 2 минуты появляется черный или бурый осадок сульфида свинца.
Дата добавления: 2018-05-13 ; просмотров: 2964 ; Мы поможем в написании вашей работы!
Презентация «Качественные реакции на белки. Биологическая роль белков в организме»
Описание презентации по отдельным слайдам:
Описание слайда:
Качественные реакции на белки
Биологическая роль белков в организме
Говырина А.Р.
учитель биологии
МБОУ «Школа №73»
Описание слайда:
Качественные реакции – это реакции, позволяющие определить наличие того или иного вещества (компонента) в среде.
Цветные реакции применяются для установления белковой природы веществ, идентификации белков и определение их аминокислотного состава в различных биологических жидкостях. В клинической лабораторной практике эти методы используются для определения количества белка в плазме крови, аминокислот в моче и крови, для выявления наследственных и приобретенных патологий обмена у новорожденных.
Описание слайда:
Определение
Пептиды и белки представляют собой высокомолекулярные органические соединения, построенные из остатков α- аминокислот, соединенных между собой пептидными связями.
Описание слайда:
Аминокислота триптофан в кислой среде, взаимодействуя с альдегидами кислот, образует продукты конденсации красно-фиолетового цвета.
Реактивы:
1) неразбавленные яичный белок,
2) концентрированная (ледяная) уксусная кислота;
3) концентрированная серная кислота.
Ход определения. К одной капле белка прибавляют 10 капель уксусной кислоты. Наклонив пробирку, осторожно по стенке добавляют по каплям 0,5 мл серной кислоты так, чтобы жидкости не смешивались. При стоянии пробирки на границе жидкостей появляется красно-фиолетовое кольцо.
Описание слайда:
При добавлении к раствору белка концентрированной азотной кислоты и нагревании появляется желтое окрашивание, переходящее в присутствии щелочи в оранжевое. Сущность реакции состоит в нитровании бензольного кольца циклических аминокислот азотной кислотой с образованием нитросоединений, выпадающих в осадок. Реакция выявляет наличие в белке циклических аминокислот.
Реактивы:
1) яичный белок, 1% раствор;
2) концентрированная азотная кислота;
3) NaOH,10% раствор.
Ход определения. К 5 каплям раствора яичного белка добавляют 3 капли азотной кислоты и (осторожно!) нагревают. Появляется осадок желтого цвета. После охлаждения добавляют (желательно на осадок) 10 капель NaOH, появляется оранжевое окрашивание.
Описание слайда:
Биуретовая реакция на пептидную связь
В основе ее лежит способность пептидных связей (-CO-NH-) образовывать с сульфатом меди в щелочной среде окрашенные комплексные соединения, интенсивность окраски которых зависит от длины полипептидной цепи. Раствор белка дает сине-фиолетовое окрашивание.
Реактивы:
1) яичный белок, 1% раствор (белок куриного яйца фильтруют через марлю и разводят дистиллированной водой 1:10);
2) NaOH, 10% раствор;
3) Cu(OH)2, 1% раствор.
Ход определения. В пробирку вносят 5 капель раствор яичного белка, 3 капли NaOH, 1 каплю Cu(OH)2, перемешивают. Содержимое пробирки приобретает сине-фиолетовое окрашивание.
Описание слайда:
Ход определения. В пробирку вносят 5 капель раствора яичного белка, затем 5 капель нингидрина, нагревают смесь до кипения. Появляется розово-фиолетовое окрашивание, переходящее с течением времени в сине-фиолетовое.
Описание слайда:
Ход определения. К 5 каплям раствора белка прибавляют 5 капель реактива Фоля и кипятят 2-3 мин. После отстаивания 1-2 мин. появляется черный или бурый осадок.
Описание слайда:
Белки в живом организме постоянно расщепляются на исходные аминокислоты (с непременным участием ферментов).
Одни аминокислоты переходят в другие, затем белки вновь синтезируются (также с участием ферментов), т.е. организм постоянно обновляется.
Некоторые белки (коллаген кожи, волос) не обновляются, организм непрерывно их теряет и взамен синтезирует новые.
Белки как источники питания выполняют две основные функции: они поставляют в организм строительный материал для синтеза новых белковых молекул и, кроме того, снабжают организм энергией (источники калорий).
Описание слайда:
Спасибо за внимание!
Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал.
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
Курс повышения квалификации
Педагогическая деятельность в контексте профессионального стандарта педагога и ФГОС
Курс повышения квалификации
Современные педтехнологии в деятельности учителя
Ищем педагогов в команду «Инфоурок»
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
также Вы можете выбрать тип материала:
Общая информация
Похожие материалы
«Изучение свойств карбоновых кислот на примере лимонной кислоты»
Урок химии с интеграцией самопознания в 9 классе. Лабораторная работа «Гидролиз солей»
Практическая работа «Урок химии в 9 классе по теме «Реакции ионного обмена». Проверочная работа. «Гарри Поттер в химической лаборатории»
Урок химии в 8 классе по теме «Движение электронов в атомах». Проверочная работа. Квест «В микромире атомов».
Урок химии в 7 классе.Проверочная работа по теме «Введение в химию.Чистые вещества и смеси». Квест «На шоколадной фабрике Вили Вонка»
Вероятность протекания химических реакций
Рабочая программа по учебному курсу «Вещества» (7 класс)
Презентация по химии на тему «Школьный эксперимент»
Не нашли то что искали?
Воспользуйтесь поиском по нашей базе из
5418860 материалов.
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Учителя о ЕГЭ: секреты успешной подготовки
Время чтения: 11 минут
Итоговое сочинение успешно написали более 97% выпускников школ
Время чтения: 2 минуты
Путин поручил не считать выплаты за классное руководство в средней зарплате
Время чтения: 1 минута
Учителя о ЕГЭ: секреты успешной подготовки
Время чтения: 11 минут
В Хабаровске родители смогут заходить в школы и детсады только по QR-коду
Время чтения: 1 минута
Дума проведет расследование отклонения закона о школьных онлайн-ресурсах
Время чтения: 2 минуты
В МГУ заработала университетская квантовая сеть
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.





















