Что нельзя при миастении
Еще раз о наболевшем… Препараты, противопоказанные при миастении
Всем известно понятие ятрогенных заболеваний. Но меньше всего мы подозреваем себя в качестве этиопатогенетического фактора. В каких случаях лечащий врач может стать причиной обострения?
В патогенезе миастении ведущую роль играют аутоиммунные механизмы, направленные против ацетилхолинового рецептора(АХР) поперечно-полосатых мышц (80–90 % случаев). При так называемой серонегативной форме миастении, когда нет антител к АХР, выявляются антитела к специфической мышечной тирозинкиназе (MuSK, в 40 % случаев) или к липопротеиновому рецептору низкой плотности (Lrp4, в 9 % случаев). Показано, что пусковым механизмом при миастении кроме аутоиммунных могут бытьи неиммунные факторы, которые посредством каскада патологических реакций запускают аутоиммунные процессы. Среди причин, запускающих миастенический процесс, описан целый ряд лекарственных препаратов, непосредственно или опосредованно отрицательно влияющих на нервно-мышечную передачу (НМП). Многие из этих препаратов обладают иммуномодулирующими и иммуногенным потенциалом. В литературе описаны случаи дебюта миастениии развития миастенических кризов (МК) после внутривенного введения йодсодержащих контрастных веществ и даже ботулинического токсина типа А. Транквилизаторы бензодиазепинового ряда вызывают центральный миорелаксирующий эффект, имея участки связывания на ГАМК-ергических рецепторах. Нейролептики могут изменять иммунный ответ, блокируя взаимодействие серотонина и дофамина с рецепторами. Кураре-подобные миорелаксанты (D-тубокурарин, ардуан) экранируют участки связывания ацетилхолина (АХ) на АХР. Схожим эффектомобладают такие антибиотики, как аминогликозиды, которые нарушают выделение медиатора АХ, блокируя потенциал-зависимые кальциевые каналы пресинаптической терминали аксона. Купренил (D-пеницилламин) стимулирует продукцию антител к АХР и приводит к развитию синдрома, клинически не отличимого от миастении. В последние годы получены новые доказательства регуляции иммунного ответа и клинического течения миастении метимазолому пациентов с сопутствующей гиперфункцией щитовидной железы. Препараты магния подавляют высвобождение АХ из терминалей аксонов; последствия их негативного действия на НМП ряд исследователей сопоставляют с эффектом кураре. Достоверность этих наблюдений проверена многочисленными экспериментамии многолетним клиническим опытом. Во всех доступных руководствах по миастении имеются разделы с перечнем препаратов, назначение которых категорически исключается при подозрении на наличие у пациента патологии НМП. Несмотря на это продолжают встречаться случаи развития ятрогенной миастении. Обескураживают сообщения и рекомендации о введении магнезии в период обострения миастении с целью коррекции гипомагниемии, что приводит к развитию МК. Самое удивительное, что развитие угрожающего жизни состояния не останавливает врача, который уверенно вводит магнезию повторно и, конечно, получает очередной МК.
Вся статья>>>
Миастения
Миастения – это патология, которая проявляется чрезмерной утомляемостью мускулатуры. В основе развития заболевания лежат аутоиммунные процессы, то есть выработка организмом антител против собственной ткани. Болезнь чаще всего возникает у молодых пациентов и без своевременной помощи врачей нередко приводит к глубокой инвалидизации и даже летальному исходу.
Общая информация
Любая мышца сокращается под влиянием нервного импульса. Он передается от нерва к мышечному волокну через специальное соединение, которое называется синапс. Во время прохождения импульса в нем выделяется большое количество ацетилхолина, который служит медиатором процесса. Повышение его концентрации приводит к возбуждению рецепторов мышцы и провоцируют сокращение волокна.
При миастении организм начинает активно вырабатывать антитела к рецепторам, реагирующим на повышение концентрации ацетилхолина. В результате они постепенно разрушаются, и качество реакции мышцы на возбуждение постоянно ухудшается. Чем интенсивнее работает мускулатура, тем заметнее снижается качество работы синапса. По мере прогрессирования патологического процесса разрушение захватывает все большее количество рецепторов, что может привести к полной потере способности к сокращению, т.е. параличу.
Причины возникновения
В настоящее время врачи и ученые не смогли найти точную причину развития миастении. Среди наиболее распространенных теорий, объясняющих биомеханизм развития заболевания, популярностью пользуется тимогенная. Считается, что антитела вырабатываются в тимусе (вилочковой железе). Она играет важную роль в формировании детского иммунитета, но по мере взросления подвергается обратному развитию вплоть до полной атрофии. У многих больных с миастенией обнаруживается увеличение вилочковой железы или опухоль в ее ткани, что говорит о высокой вероятности связи между этими патологиями.
Существует ряд факторов риска, которые повышают вероятность развития миастении:
Формы и симптомы
Врачи выделяют несколько форм миастении, которые отличаются друг от друга происхождением или особенностями течения. Причина и время появления специфического синдрома, характерного для нарушения нервно-мышечной проводимости, позволяют выделить две разновидности:
Среди практикующих врачей более востребована клиническая классификация миастении, которая позволяет выделить три основных формы.
Глазная миастения
Поражение захватывает мышцы, расположенные в непосредственной близости от глазного яблока. Они отвечают за процесс открытия и закрытия глаз, их повороты в ту или иную сторону, а также настройку на близкое и дальнее расстояние. В результате пациент жалуется на:
Все симптомы становятся особенно яркими к вечеру на фоне утомления мускулатуры, а утром проходят полностью или частично.
Бульбарная миастения
В первую очередь страдают мышцы, ротовой полости, глотки, гортани, а также мимическая мускулатура. В результате у пациента существенно нарушается дикция, речь становится неразборчивой, а голос – гнусавым и хриплым. Во время жевания и глотания быстро нарастает усталость, что делает прием пищи нелегкой задачей.
Если в патологический процесс вовлекается мимическая мускулатура, мимика становится бедной и неестественной. У пациента возникают затруднения при попытке улыбнуться или оскалить зубы.
Генерализованная миастения
Эта форма заболевания встречается наиболее часто и характеризуется последовательным поражением мускулатуры всего тела. Сначала пациент начинает быстро уставать при ходьбе, а затем затрудняются движения, связанные с подъемом рук. Способность к передвижению и самообслуживанию постепенно ухудшается, что в конечном итоге приводит к инвалидизации пациента.
Все виды миастении характеризуются нарастанием симптоматики к вечеру. Это связано с физической активностью пациента в дневные часы и постепенным утомлением мышц. Чем тяжелее заболевание, тем быстрее возникают затруднения движений.
Диагностика
Миастения относится к неврологическим заболеваниям, вот почему при появлении любых подозрительных симптомов необходимо обратиться к неврологу. Нередко специалисту достаточно взглянуть на мимику и походку пациента, чтобы заподозрить патологию. Затем проводится подробный опрос, в ходе которого уточняются:
Затем врач проводит подробный осмотр с оценкой мышечного тонуса и силы, чувствительности отдельных частей тела, выраженности рефлексов. Как правило, этого хватает для постановки предварительного диагноза, который затем подтверждается объективными исследованиями:
Диагностика дополняется стандартными тестами: общий анализ крови, общий анализ мочи, электрокардиография и т.п. При необходимости список исследований расширяется.
Лечение миастении
В настоящее время врачи не имеют возможности полностью остановить процесс разрушения ацетилхолиновых рецепторов и избавить человека от симптомов миастении. Основное лечение направлено на остановку патологического процесса и достижение ремиссии, а также снижение утомляемости мускулатуры.
Основу терапии составляют средства, тормозящие работу иммунной системы: гормоны (преднизолон), цитостатики (циклоспорин), а также иммуноглобулины. Специфические препараты прозерин и калимин тормозят разрушение ацетилхолина, что позволяет увеличить его концентрацию в нервно-мышечном синапсе и, соответственно, улучшить передачу нервного импульса. Для ускорения процесса возбуждения используют препараты калия.
Специфическое лечение миастении дополняется общими средствами, в частности, антиоксидантами, стабилизирующими работу нервной системы. В зависимости от ситуации также назначаются лекарства, устраняющие побочные эффекты основных медикаментов.
При выявлении в ходе диагностики опухоли вилочковой железы проводится ее хирургическое удаление, иногда в сочетании с лучевой терапией. Показаниями к операции выступает неуклонное прогрессирование заболевания и его генерализованная форма у пациентов младше 70 лет. При идеальном результате после удаления тимуса человек практически полностью отказывается от медикаментов, а симптомы контролируются диетой и образом жизни.
При запредельно высокой концентрации антител в крови может назначаться ее искусственная очистка: плазмаферез, криофероз, иммуносорбция. Во время ремиссии проводятся курсы физиопроцедур (электрофорез, электромиостимуляция), массаж, санаторно-курортное лечение.
Осложнения
Главная опасность миастении – это миастенический криз. Как правило, это осложнение провоцируется самим пациентом, например, при самовольной отмене или замене препаратов, изменении их дозировки. Вызвать криз также могут острые инфекции, запредельные физические или психические перегрузки. В результате утомляемость мышц повышается до такой степени, что пациент не может встать с постели, принимать пищу и даже говорить.
При крайне тяжелом течении миастенического криза страдает также дыхательная мускулатура, обеспечивающая движения грудной клетки. Это состояние может стать причиной летального исхода, вот почему пациент экстренно госпитализируется в реанимационное отделение. Врачи проводят мероприятия, направленные на снижение количества антител, при необходимости человека подключают к аппарату искусственного дыхания.
Первые признаки надвигающегося миастенического криза включают:
В случае появления подобных симптомов необходимо как можно быстрее обратиться за медицинской помощью.
Профилактика
Специфической профилактики возникновения заболевания не существуют. Основные профилактические меры рассчитаны, в первую очередь, на людей, у которых уже имеется миастения, и направлены на предотвращение ухудшения. Необходимо следовать следующим правилам:
Диета
Важным аспектом профилактики миастении является соблюдение диеты. Ежедневный рацион должен быть сбалансированным по основным нутриентам (белкам, жирам, углеводам) и обладать достаточным, но не чрезмерным калоражем. Если у человека имеется избыток массы тела, рекомендуется придерживаться дефицита калорий (не более 10-15% от ежедневной нормы). В меню должны присутствовать продукты с высоким содержанием калия (картофель, бананы и т.п.). По назначению врача допускается прием поливитаминных препаратов.
Лечение в клинике «Энергия здоровья»
Миастения – это тяжелое заболевание, но врачи клиники «Энергия здоровья» имеют огромный опыт работы с такими пациентами. Это позволяет нам добиваться значительного улучшения состояния и стойкой ремиссии. Вот основные преимущества лечения в нашем медицинском центре:
Преимущества клиники
«Энергия здоровья» – это современный многопрофильный медицинский центр, оборудованный в соответствии с самыми строгими стандартами. Мы делаем все, чтобы каждый пациент получил максимально полную и эффективную медицинскую помощь вне зависимости от диагноза. К Вашим услугам:
Совсем недавно диагноз миастения звучал как приговор. Человек был по умолчанию обречен на летальный исход от постепенной парализации дыхательной мускулатуры. Современные методы лечения, хотя и не дают возможности полностью избавиться от патологии, но позволяют добиться стойкой ремиссии на долгие годы. Если Вы сами или Ваш близкий человек стали замечать беспричинную слабость мышц, особенно заметную в вечерние часы, не тяните с обращением к неврологу. Врачи клиники «Энергия здоровья» ждут вас!
Миастения
Общая информация
Краткое описание
Миастения (болезнь Эрба – Гольдфлама – Жолли) – аутоиммунное нервно-мышечное заболевание, клинически характеризующееся патологической слабостью и утомляемостью произвольной мускулатуры, и связанное с повреждением ацетилхолиновых рецепторов постсинаптической мембраны поперечно-полосатых мышц специфическими комплементфиксирующими антителами. [Кузин М.И., Гехт Б.М.]
Соотношение кодов МКБ-10 и МКБ-9
| КодМКБ-10 | Код МКБ-9 | ||||||||||||||||||
| Код | Название | Код | Название | ||||||||||||||||
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортных или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с не высоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с не высоким риском систематической ошибки (+). Результаты, которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая фармацевтическая практика. |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Классификация [Б.М. Гехт 1965г]
По характеру течения:
• миастенические эпизоды (однократный или ремитирующее течение);
• миастенические состояния (т.е. стационарное течение);
• прогрессирующее течение;
• злокачественная форма.
По локализации
Локальные (ограниченные) процессы:
• глазные;
• бульбарные;
• лицевые;
• краниальные;
• туловищные.
Генерализованные процессы:
• генерализованные без бульбарных нарушений;
• генерализованные и генерализованные с нарушениями дыхания.
По степени тяжести двигательных расстройств:
• легкая;
• средней тяжести;
• тяжелая.
По степени компенсации двигательных нарушений на фоне АХЭР препаратов:
• полная;
• достаточная;
• недостаточная (плохая).
В зависимости от динамики клинической картины выделяют несколько форм миастении:
• миастенические эпизоды – представляющие из себя преходящие двигательные расстройства с полным восстановлением функции вне эпизода.
• миастеническое состояние – форма миастении, при которой клиника сохраняется на протяжении многих лет без изменений.
• прогрессирующая форма – форма миастении, при которой клинические проявления необратимо прогрессируют, без эпизодов восстановления сниженных двигательных функций.
• злокачественная форма – форма миастении, остро начинающаяся и неуклонно прогрессирующая весьма быстрыми темпами с неуклонным нарушением функций нервно-мышечного аппарата.
Классификации Американской Ассоциации неврологов, основанной на оценке тяжесть клинических проявлений миастении по пятибалльной шкале MGFA и распространенности патологического процесса:
Диагностика (амбулатория)
ДИАГНОСТИКА НА АМБУЛАТОРНОМ УРОВНЕ
Диагностические критерии
Жалобы:
• слабость, патологическая утомляемость мышц, которая возникает после физической нагрузки;
• патологическая слабость мышц конечностей, туловища, невозможность подняться по ступенькам городского транспорта;
• невозможность удержать голову, нижнюю челюсть;
• опущение век;
• двоение предметов;
• утомляемость жевательных мышц при пережевывании твердой пищи, разговоре;
• осиплость голоса, «носовой» оттенок голоса, его «затухание»;
• нечеткость речи, на затрудненное глотание.
NB! Предположение о миастении должно возникнуть в каждом случае глазодвигательных и бульбарных расстройств.
Анамнез:
• наличие в прошлом кратковременных эпизодов слабости и утомляемости, полностью/частично регрессировавших самопроизвольно/на фоне неспецифического лечения;
• семейный анамнез, наличие у родственников нервномышечных, аутоиммунных и онкологических заболеваний.
NB Наиболее высокая заболеваемость встречается в двух возрастных категориях: 20-40 лет (в этот период чаще болеют женщины) и 65-75 лет (в этот период женщины и мужчины поражаются одинаково часто). При расспросе больного нужно уточнить: Когда началось заболевание? – сколько времени назад (дни, недели, месяцы, годы). Нарастают ли слабость в ногах и руках к вечеру? Имеется ли двоение в глазах, нарушение глотания, изменения голоса? Если болезнь прогрессирует, то с чего она началась? Какими хроническими заболеваниями болеет и что постоянно принимает?
Физикальное обследование:
неврологический статус:
• нарушение зрения (двоение, слепота);
• нарушение речи и глотания (плохо говорит, не понимает обращенную речь); нарушение движений (в одной или нескольких конечностях с одной стороны, с двух сторон);
• нарушение болевой и температурной чувствительности (на лице, туловище, в одной или нескольких конечностях с одной стороны, с двух сторон);
• наличие координаторных расстройств (испытывает затруднения при ходьбе, выполнении мелких движений, пользовании предметами, чувствует сильное головокружение в покое или при движениях и др);
• мышечная слабость (при повторении стереотипных движений она резко усиливается и может достичь степени пареза/полного паралича), после отдыха объем движений увеличивется;
• характерна динамичность симптомов: интенсивность птоза может изменяться на протяжении суток в зависимости от физической нагрузки. Зрачковые реакции преимущественно живые, иногда встречается анизокория или истощение зрачковых реакций во время повторных обследований (например, усиление дисфагии во время еды/дисфонии во время разговора – так называемый феномен патологической мышечной утомляемости) и феномен генерализации мышечной слабости (например усиление птоза после нагрузки на мышцы руки);
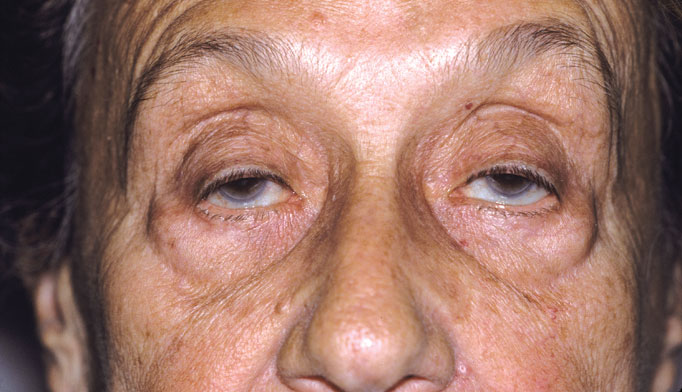
• при вовлечении в патологический процесс глазодвигательных, мимических и жевательных мышц при внешнем осмотре у пациента наблюдается характерное маскообразное лицо, с отсутствием морщин, бедной мимикой, с опущением век. Во время улыбки поднимается лишь верхняя губа, в то же время нижняя губа и углы рта остаются неподвижными. Чаще всего наблюдается слабость круговой мышцы рта, что приводит к невозможности произнести звук «Р», губные звуки «Б», «П».
• поражение бульбарной группы мышц вызывает нарушения функции мягкого неба и надгортанника. Из-за нарушения акта глотания могут развиваться аспирационная пневмония/алиментарное истощение.
• при наличии генерализированных форм миастении – наличие слабость дыхательных мышц и сердечной деятельности. Мышечная слабость, которая доходит иногда до состояния тетраплегии, сопровождается выраженными вегетативными нарушениями: тахикардией, вялым пульсом, мидриазом.
NB! В клинической практике для оценки степени выраженности двигательных расстройств используют шкалу силы мышц конечностей, предложенную А. Szobor (1976):
Фармакологические тесты:
Одним из наиболее значимых критериев диагностики миастении считают фармакологический тест с введением антихолинэстеразных препаратов.
Методика пробы с введением неостигмина метилсульфата: 0.05 % раствор неостигмина метилсульфат 1.5 мл вводят подкожно при весе больного 50-60 кг, при весе 60-80 кг доза препарата соответствует 2.0 мл и при весе 80-100 кг 2.5 мл соответственно. В детской практике вводится 1.0 мл препарата. Оценка проводится во временном интервале от 40 минут до 90 минут после введения препарата. В основе оценки теста лежит колебания выраженности клинических симптомов. Проба оценивается как позитивная при полной и неполной компенсации клинических симптомов, сомнительной – при частичной компенсации и негативной при отсутствии каких либо изменений. При возникновении мускариновых эффектов антихолинстеразных препаратов после оценки эффективности теста вводят 0.1 % раствор атропина 0.2-0.5 мл.
Лабораторные исследования:
• исследование сыворотки крови на уровень аутоантител к мышечному ацетилхолиновому рецептору – важное значение имеет динамика этого показателя для оценки эффективности патогенетической терапии;
• определение электролитов крови – снижение показателей калия крови;
• гормоны щитовидной железы: и тиреотоксикоз, и гипотиреоз могут усиливать слабость при миастении;
Инструментальные исследования
Электронейромиография (декремент тест):
• повторная ритмическая стимуляция нерва низкой (3 имп/с) и высокой (50 имп/с) частотой с использованием функциональных (постактивационные облегчение и истощение) и фармакологических (введение антихолинэстеразных препаратов) проб. При миастении ЭНМГ-исследование проводится именно на «клинически пораженной мышце».
• дополнительный метод диагностики – ЭНМГ с использованием концентрических игольчатых электродов (для выявления степени возможного вовлечения мышечного субстрата в патологический процесс, например, для выявления сопутствующего воспалительного процесса при полимиозите).
• электронейромиографическое исследование – для выявления нарушения нервно-мышечной передачи. В мышцах больных миастенией при стимуляции частотами 3 и 40 имп/с выявляется декремент амплитуды М-ответа в серии последовательных импульсов, который определяет степень нарушения нервно-мышечной передачи. Большое значение для диагностики имеет обратимость электрофизиологических феноменов на фоне АХЭП – нарастание амплитуды М-ответа и уменьшение декремента.
КТ/МРТ органов средостения: для исключения/подтверждения патологии вилочковой железы (тимома, гиперплазия вилочковой железы) с целью определения дальнейшей тактики лечения.
Сбор жалоб и анамнеза
Диагностический алгоритм:
Диагностика (скорая помощь)
ДИАГНОСТИКА НА ЭТАПЕ СКОРОЙ НЕОТЛОЖНОЙ ПОМОЩИ
Диагностические мероприятия:
· оценка общего состояния и жизненно важных функций пациента: сознания, дыхания, кровообращения (осмотр кожных покровов и видимых слизистых, измерение артериального давления, частоты пульса, частоты дыхания, температуры тела, и др.); визуальная оценка: положение больного, наличие асимметрии лица, птоза век.
· наличие очаговых неврологических симптомов: нарушение движений (в одной или нескольких конечностях с одной стороны, с двух сторон);
нарушение болевой и температурной чувствительности (на лице, туловище, в одной или нескольких конечностях с одной стороны, с двух сторон); наличие координаторных расстройств (испытывает затруднения при ходьбе, выполнении мелких движений, пользовании предметами, чувствует сильное головокружение в покое или при движениях и др.); нарушение зрения (двоение, слепота).
· установление или исключение критического состояния – миастенического криза.
NB! Каждый пациент с признаками миастении должен рассматриваться как пациент с потенциально возможной острой дыхательной недостаточностью. Обращают внимание на нарушения частоты, глубины и ритма дыхания, участие «вспомогательной» мускулатуры, обычно не участвующей в акте дыхания.
Поэтому в первую очередь оцениваются следующие признаки:
• одышка;
• ограниченная экскурсия грудной клетки и живота при вдохе;
• парадоксальное движение грудной клетки при дыхании;
• западание межреберных мышц на вдохе;
• попытка опираться руками при вдохе.
| Миастенический криз | Холинергический криз |
| Быстрое развитие (часы, минуты) | Медленное развитие (сутки и более) |
| Выраженная слабость произвольной мускулатуры с нарушением дыхания, сердечной деятельности, бульбарным синдромом, психомоторное возбуждение, нарушение сознания (сопор, кома) | |
| М-холинергические (вегетативные) симптомы | |
| · сухость слизистых | |
· густая слюна
· мидриаз
· тахикардия
· повышение АД
· задержка при мочеиспускании
· парез кишечника
· жидкая слюна
· миоз
· брадикардия
· снижение АД
· учащенное мочеиспускание, полиурия
· усиление перистальтики, диарея
тошнота, рвота, кишечная колика
· отсутствие фасцикуляций
· наличие фасцикуляторных подергиваний мышц, крампи, тремор конечностей и тела
Диагностика (стационар)
ДИАГНОСТИКА НА СТАЦИОНАРНОМ УРОВНЕ
Диагностические критерии на стационарном уровне:
Жалобы и анамнез: см. амбулаторный уровень.
NB! При сборе анамнеза обращается внимание на изменчивость симптомов в течение суток, связь их с нагрузкой, наличие частичных/полных ремиссий, обратимость симптомов на фоне приема АХЭ препаратов (на время их действия) и на фоне адекватной иммуносупрессивной терапии. Исключатся в анамнезе прием лекарственных препаратов, усиливающих мышечную слабость.
Физикальное обследование: см. амбулаторный уровень.
Инструментальные исследования:
· КТ/МРТ органов средостения – для определения тимомы или гиперплазии вилочковой железы.
· электронейромиография – для определения нарушения нейро-мышечной проводимости (снижение амплитуды М-ответа (больше чем на 10-15%) во время ритмической стимуляции нерва с частотой 2-3 Гц).
Перечень основных диагностических мероприятий:
· тесты на выявление патологической утомляемости;
· фармакологическая проба с неостигмина метилсульфатом/пиридостигмина бромидом;
· электронейромиография;
· исследование антител к ацетилхолиновым рецепторам;
· КТ/МРТ органов средостения.
Перечень дополнительных диагностических мероприятий:
· кровь на иммуноглобулины;
· УЗИ щитовидной железы;
· гормоны щитовидной железы;
· электролиты крови.
Дифференциальный диагноз
Лечение
Препараты (действующие вещества), применяющиеся при лечении
| Азатиоприн (Azathioprine) |
| Атропин (Atropine) |
| Галантамин (Galantamine) |
| Галоперидол (Haloperidol) |
| Декстроза (Dextrose) |
| Иммуноглобулин человеческий нормальный (Human normal immunoglobulin) |
| Калия хлорид (Potassium chloride) |
| Микофеноловая кислота (Микофенолата мофетил) (Mycophenolic acid (Mycophenolate mofetil)) |
| Неостигмина метилсульфат (Neostigmine methylsulfate) |
| Оротовая кислота (Orotic acid) |
| Пиридостигмина бромид (Pyridostigmine) |
| Преднизолон (Prednisolone) |
| Спиронолактон (Spironolactone) |
| Циклоспорин (Cyclosporine) |
| Циклофосфамид (Cyclophosphamide) |
Лечение (амбулатория)
ЛЕЧЕНИЕ НА АМБУЛАТОРНОМ УРОВНЕ
Тактика лечения:
Тактика лечения миастении определяются такими направлениями:
• компенсация нервно-мышечной передачи (препараты калия, систематический прием антихолинэстеразных препаратов);
• коррекция аутоиммунных нарушений (глюкокортикоидных препаратов, цитостатиков и плазмафереза);
• влияние на вилочковую железу.
Немедикаментозное лечение:
Режим:
• противопоказаны чрезмерные физические нагрузки, инсоляции.
Диета:
• диета богатая калием (печеный картофель, курага, бананы и др.).
Медикаментозное лечение:
В основу стратегии лекарственной терапии миастении положены следующие принципы:
• этапность лечебных мероприятий;
• сочетания компенсирующей, патогенетической и неспецифической терапии.
Учёт фазы течения заболевания (хроническая/острая (кризы)).
NB! Противопоказаны лекарственные препараты, содержащие магний/хинин; нельзя употреблять миорелаксанты, транквилизаторы, нейролептики, мочегонные препараты, аминогликозиды, фторхинолины, тетрациклин.
Первый этап
Компенсирующая терапия предполагает назначение следующих препаратов:
Антихолинэстеразные средства (отличаются они в основном длительностью действия).
| Препарат и его синонимы | Лекарственная форма | Начало дейтсвия, минуты | Продолжительность действия, часы |
| Неостигмина метилсульфат | Таблетки по 15мг, 0,05% раствор по 1мл (0,5мг) в ампулах | 20-40 | 2-4 |
| Пиридостигмина бромид | Таблетки по 60мг, 0, 5% раствор по 1мл (5мг) в ампулах | 60 | 4-6 |
| Галантамина гидрохлорид | Растворы 0,1%, 0,25%:, 0,5% по 1мл в ампулах | 60 | 8-12 |
Иньекционная форма неостигмина метилсульфат используется для оказания быстрого действия. Принцип дозирования – следующая доза принимается за 30 минут до окончания действия предыдущей. При переводе больных на парентеральное введение препаратов учитывается, что 1 таблетка пиридостигмина бромида (60 мг) равноценна 1 мл 0,05% раствора неостигмина метилсульфат. В некоторых ситуациях (mensis, инфекции, ремиссия) – чувствительность к АХЭ препаратам повышается. В этом случае доза препаратов уменьшается. Больных нужно обучать коррегировать дозу индивидуально в зависимости от течения болезни.
Относительные противопоказания к применению АХЭП:
• бронхиальная астма;
• тяжелый атеросклероз;
• ИБС, стенокардия;
• эпилепсия.
Второй этап
Лечение глюкокортикоидами назначается:
· при недостаточной эффективности препаратов, используемых на первом этапе;
· для создания своеобразного запаса прочности в компенсации миастенических расстройств перед подготовкой к операции (тимэктомии);
· больным миастенией с витальными нарушениями;
· при дебюте заболевания с бульбарных нарушений.
Применяемые чаще схемы – прием ГКС ежедневно или через день.
Дозу преднизолона (метилпреднизолона) подбирают индивидуально, ориентируясь на тяжесть состояния больного. В среднем она составляет 1 мг/кг/сут., но не менее 50 мг. Преднизолон 1 таблетка – 5 мг. При выраженном обострении назначают 60-150 мг/сутки утром ежедневно, через 5-7 дней (до терапевтического эффекта) переходят на схему через день. С больших доз следует уходить быстро. Эффект оценивают через 6-8 приёмов. В первые несколько дней некоторые пациенты могут отмечать эпизоды ухудшения состояния в виде нарастания мышечной слабости и утомляемости. Возможно, эти эпизоды связаны с прямым действием глюкокортикоидов на процессы освобождения синаптического медиатора и десенситизацией рецепторов. Это обстоятельство обусловливает необходимость временного уменьшения дозы антихолинэстеразных препаратов. По мере достижения эффекта и улучшения состояния больных дозу преднизолона постепенно уменьшают до поддерживающей. Длительно применяется поддерживающая доза через день 20-30 мг в сутки, возможно в течение нескольких месяцев или даже лет. При ухудшении состояния доза может быть увеличена. Используется так же ступенчатая схема приема ГКС. В разработанной схеме предлагается увеличение начальной дозы препарата до 25-30 мг в один прием утром. Каждый последующий прием гормонов увеличивается на 25-30 мг до достижения максимальной дозы 100 мг.
Третий этап
При недостаточной эффективности глюкокортикоидов/развитии выраженных побочных эффектов целесообразно назначение цитостатических препаратов.
• Азатиоприн можно использовать в качестве монотерапии/в сочетании с глюкокортикоидами, если они не оказывают достаточного эффекта/если из-за побочных эффектов необходимо снижение их дозы. Азатиоприн назначают перорально ежедневно по 50 мг/cyт с последующим увеличением дозы до 150-200 мг/cyт.
• Микофенолата мофетил назначают в дополнение к глюкокортикоидам в случаях, когда необходимо снижение их дозы. Микофенолата мофетил назначают перорально ежедневно по 2 г/cyт с последующей коррекцией дозы в зависимости от эффективности лечения.
• Циклоспорин успешно применяют при лечении тяжёлых форм миастении в случаях резистентности к другим препаратам. Препарат назначают перорально в дозе 3 мг/кг. При отсутствии токсических реакций дозу можно увеличить до 5 мг/кг 2 раза в день. После достижения стойкого терапевтического эффекта дозу циклоспорина можно снизить до минимальной поддерживающей.
• Циклофосфамид используют при отсутствии эффекта от других иммунодепрессантов как в виде монотерапии, так и в сочетании с азатиоприном. Препарат вводят внутримышечно ежедневно в дозе 200 мг/через день в дозе 400 мг. Терапию начинают в условиях стационара, и только убедившись в хорошей переносимости препарата, можно переводить больных на амбулаторное лечение.
NB! Следует отметить, что беременность не является противопоказанием к назначению основных препаратов лечения миастении. На время беременности желательно воздержаться от поддерживающей гормональной терапии, сеансов плазмафереза, использования больших доз калийсодержащих препаратов. Также следует строго придерживаться особых подходов терапии других заболеваний. Существует перечень препаратов, которые нельзя использовать при миастении.
Применение лекарств при миастении (по С. А. Мальбергу, 2001)
Алгоритм действий при неотложных ситуациях:
Кризы при миастении:
· миастенические
· холинергические
· смешанные.
Характеристика симптомов при миастеническом и холинергическом кризах
| Симптомы | При миастеническом кризе | При холинергическом кризе |
| Величина зрачков | широкие | узкие; парез аккомодации |
| Пульс | тахикардия | брадикардия |
| Артериальное давление | Нормально или нерезко снижено | быстро резко снижается |
| Мышечные фасцикуляции | не характерны | резко выражены |
| Боли в животе; бурная перистальтика кишечника; понос; рвота | не наблюдаются | резко выражены |
| Одышка, афония, невозможность отхаркивания содержимого ротоглотки | очень характерны | не характерны |
Алгоритм действий при миастеническом и/или холинергическом кризах
Другие виды лечения:
При хорошей эффективности препаратов первого этапа, но сохраняющихся лёгких бульбарных нарушениях на фоне отмены пиридостигмина бромида показано проведение тимэктомии.
Показания к тимэктомии у взрослых:
• опухоль вилочковой железы (тимома);
• вовлечение в процесс краниобульбарной мускулатуры;
• прогрессирующее течение миастении.
Показания к тимэктомии у детей:
• генерализованная форма миастении;
• прогрессирование заболевания при плохой лекарственной компенсации нарушенных функций.
Противопоказания к тимэктомии:
• тяжёлые соматические заболевания;
• острая фаза миастении (выраженные некомпенсированные бульбарные нарушения, а также нахождение больного в кризе);
• пациенты длительно страдающих миастенией при стабильном её течении, а также при локальной глазной форме миастении.
NB! Результатом операции могут стать полное клиническое выздоровление (эффект А), стойкая ремиссия при значительном уменьшении дозы антихолинэстеразных препаратов (эффект В), значительное улучшение состояния на фоне сохранения потребности в антихолинэстеразных препаратах (эффект С), отсутствие улучшения (эффект D).
Показания для консультации специалистов:
· консультация торакального хирурга – установление/исключения объемного образования средостения (тимома);
· консультация терапевта – установление/исключение терапевтического заболевания, онкопатологии внутренних органов (артериальная гипертензия, злокачественное новообразование, пневмония);
· консультация эндокринолога – установление/исключение заболевания щитовидной железы;
· консультация онколога – установления онкологического заболевания, проявлении паранеопластического синдрома.
· консультация офтальмолога – осмотр глазного дна для исключения патологии глаза, признаков внутричерепной гипертензии, застоя дисков зрительных нервов;
Профилактические мероприятия:
Первичная профилактика:
Постоянное лечение и регулярное посещение врача невролога является обязательным для больного миастенией, только так можно добиться улучшений и повысить качество жизни. Но также очень важно придерживаться следующих рекомендаций:
• нельзя загорать;
• нельзя заниматься тяжелым физическим трудом;
• избегать утомляемости и больше отдыхать;
• нельзя производить лечение самостоятельно или принимать лекарственные травы;
• нельзя употреблять лекарственные препараты, содержащие магний или хинин;
• нельзя употреблять миорелаксанты, транквилизаторы, нейролептики, мочегонные препараты, аминогликозиды, фторхинолины, тетрациклин.
Вторичная профилактика направлена на профилактику осложнений:
• тенденция к нарастанию веса требует систематического использования ограничения калорийности употребляемой пищи, в особенности углеводов;
• тенденция к снижению толерантности к углеводам и периодическое повышение сахара в крови, требует назначения препаратов, способствующих увеличению толерантности к углеводам, нормализации перекисного окисления липидов и сокращению переносимости к углеводным нагрузкам.
Мониторинг состояния пациента:
• оценка жизнеобеспечивающих функций – дыхания, гемодинамики;
• оценка неврологического статуса для выявления и мониторинга динамичности мышечной слабости и реакции на введение антихолинэстеразных препаратов (полная, неполная частичная компенсация, проба позитивная, сомнительная, негативная).
Индикаторы эффективности лечения:
• стойкая/частичная ремиссия на фоне приема медикаментозных средств/без них у больных миастенией.
Лечение (скорая помощь)
ЛЕЧЕНИЕ НА ЭТАПЕ СКОРОЙ НЕОТЛОЖНОЙ ПОМОЩИ
Медикаментозное лечение
Алгоритм экстренных мероприятий при любом варианте кризов:
· купирование нарушений дыхания: санация ротоглотки и трахеобронхиального дерева во избежание аспирационного трахеобронхита и пневмонии;
· интубация трахеи или перевод на ИВЛ — в зависимости от степени тяжести состояния больного.
· назначение антибактериальной терапии (класс цефалоспоринов) с учетом высокого риска возникновения аспирационной пневмонии.
· адекватное энтеральное или — при бульбарных нарушениях — парентеральное питание.
Алгоритм экстренных мероприятий при холинергическом кризе:
· немедленная отмена антихолинэстеразных препаратов.
· внутримышечное или подкожное – в зависимости от тяжести состояния больного – введение 0,5–1,0 мл 0,1% раствора атропина. Инъекции могут при необходимости повторяться с интервалом в 1–2 ч до появления сухости во рту.
Лечение (стационар)
ЛЕЧЕНИЕ НА СТАЦИОНАРНОМ УРОВНЕ
Тактика лечения:
На стационарном этапе в карте наблюдения за пациентом (история болезни) ежедневно отмечаются показатели гемодинамики (А/Д, пульс, ЧСС), оценивается дыхание и ЧДД, в неврологическом статусе определяется динамика синдрома патологической мышечной утомляемости, отмечается проводимая коррекция и переносимость медикаментозной терапии, уровень компенсации мышечной слабости после приема антихолинэстезаного препарата.
Немедикаментозное лечение:
Режим:
• противопоказаны чрезмерные физические нагрузки, инсоляции.
Диета:
• диета богатая калием (печеный картофель, курага, бананы и др.).
Искусственная вентиляция лёгких
В качестве первого мероприятия предполагает необходимость адекватного дыхания с помощью принудительной ИВЛ.
Показания к переводу на ИВЛ:
• нарушение ритма дыхания;
• цианоз;
• возбуждение;
• потеря сознания;
• участие вспомогательной мускулатуры;
• изменение величины зрачков отсутствие реакции на введение АХЭ препаратов.
Перевод пациента на самостоятельное дыхание после ИВЛ:
• отсутствия цианоза;
• тахипноэ;
• тахикардии;
• сохранности мышечного тонуса;
• достаточного дыхательного объёма (>300 мл), p.Oz более 80 мм рт.ст. при дыхании смесью с 50% кислорода;
• способности больного создать разрежение вдоха не менее 20 см вод.ст., полного восстановления сознания.
NB! В период проведения искусственной вентиляции полностью исключается введение антихолинэстеразных препаратов, проводится интенсивное лечение интеркуррентных заболеваний и патогенетическое лечение миастении.
NB! Введение АХЭП и использование ИВЛ одновременно недопустимо.
NB! Через 16-24 часа после начала ИВЛ, при условии ликвидации клинических черт холинергического или смешанного кризов, следует провести пробу с введением АХЭП (неостигмина метилсульфат) с учетом начала действия препарата и отключить от аппарата ИВЛ (не экстубируя!), затем оценить эффективность самостоятельного дыхания. Если в течение 1,5-2 часов больной самостоятельно дышит, процедуру повторить в течение суток 3-4 раза с АХЭП. В случае положительного результата больного экстубируют. Убедившись в возможности адекватного дыхания, перевести больного на прием пероральных антихолинэстеразных препаратов.
Если функция дыхания остается недостаточной и эффект от введения АХЭП непродолжительный, больного подключают к аппарату ИВЛ. До следующих суток неостигмина метилсульфат не вводить! Вышеуказанные действия повторить на следующие сутки. Если в течение 3-4 суток не наблюдается положительного эффекта (самостоятельное дыхание) больному необходимо наложить трахеостому для исключения пролежня трахеи. По мере восстановления жизненно важных функций дыхания и глотания больного отключают от аппарата ИВЛ и назначают прием АХЭП.
Медикаментозное лечение:
Лечение миастенических кризов должно быть направлено на компенсацию нарушений нервно-мышечной передачи и коррекцию иммунных расстройств.
Иммуноглобулины G:
• общепринятым режимом терапии считают короткие 5-дневные курсы внутривенного введения препарата Человеческий Ig в доза 400 мг/кг ежедневно. В среднем клинический эффект отмечается на 4 день терапии и продолжается в течение 50-100 дней.
Антихолинэстеразные препараты:
• чаще применяют парентеральное введение. Применение АХЭп в количестве диагностической пробы показаны при любой форме криза (наиболее эффективно их введение при миастеническом кризе). Неостигмина метилсульфат вводится п/к от 1,5 до 2,5 мл, для уменьшения нежелательных эффектов вводят атропин 0,2-0,5 мл 01% раствора. Результат оценивается как при неостигмина метилсульфатной пробе.
При назначении антихолинэстеразных препаратов должен соблюдаться определенный временной режим: применение каждой последующей дозы не чаще, чем через 3-4 часа для неостигмина метилсульфат и 5-6 часов для пиридостигмина бромида, в связи с опасностью возникновения холинергической интоксикации. В период максимальной выраженности клинических симптомов криза целесообразно парентеральное введение антихолинэстеразных препаратов. Препарат вводят под кожу, а при остановке дыхания внутривенно в дозе 20 мг при весе больного до 80 кг, в дозе 30 мг при весе более 80 кг. Для уменьшения нежелательных мускариновых эффектов антихолинэстеразных препаратов их вводят с атропином в виде 0,2 – 0,5 мл 0,1% раствора.
Своевременно и в правильной дозировке произведенное введение антихолинэстеразных препаратов, как правило, помогает восстановлению функции дыхания и бульбарной мускулатуры. По мере достижения стабильного клинического эффекта, восстановления жизненно важных функций дыхания и глотания, вместо парентерального введения назначается прием препаратов внутрь.
Для определения времени приема последующих доз пероральных препаратов следует ориентироваться на длительность и эффективность действия применяемой дозы. Вместе с тем необходимо помнить, что в различных состояниях длительность и эффективность действия каждого препарата может меняться.
Спиронолактон является антагонистом минералкортикоидного гормона альдостерона, необходимого для регуляции обмена электролитов в организме. Способность спиронолактона задерживать калий в клетках служит основанием для широкого его применения при лечении миастении. Препарат принимают внутрь в дозе 0,025 – 0,05 г 3-4 раза в день. Побочные явления: в отдельных случаях тошнота, головокружение, сонливость, кожные сыпи, обратимая форма гинекомастии.
Профилактика пневмонии (не применять аминогликозиды).
Проведение симптоматической терапии.
Специальный уход.
Некоторые лекарственные препараты могут сами по себе провоцировать обострение миастении (смотрите таблицу 2).
Перечень основных диагностических мероприятий:
— Определение электролитов крови
— Проведение неостигмина метилсульфатной пробы
— ЭНМГ
— КТ/МРТ органов средостения
— ЭКГ
Перечень дополнительных диагностических мероприятий:
— Определение гормонов щитовидной железы
— Определение уровня КФК
— МРТ головного мозга – для проведения дифференциального диагноза миастении с заболеваниями, при которых локализация патологического процесса определяется в стволе мозга: стволовым энцефалитом, опухолью ствола головного мозга, нарушением мозгового кровообращения в системе вертебрально-базилярных сосудов;
— УЗИ щитовидной железы – для исключения патологии щитовидной железы (обязательно надо проводить при подозрении на миастению. И тиреотоксикоз, и гипотиреоз могут усиливать слабость при миастении).
— КТ/МРТ органов грудной клетки, брюшной полости, органов малога таза.
— УЗИ органов брюшной полости, малого таза.
— глазное дно
Хирургическое вмешательство:
Тимэктомия:
Показанием к оперативному лечению:
• злокачественные формы;
• прогрессирующая форма;
• миастеническое состояние в зависимости от степени выраженности дефекта.
При локальных формах подходят избирательно.
Противопоказания к тимэктомии:
• тяжелые декомпенсированные соматические заболевания;
• старческий возраст.
До оперативного лечения обязательна предоперационная подготовка:
• общеукрепляющая терапия;
• проведение лечебного плазмафереза;
• при необходимости – курс глюкокортикостероидов.
Другие виды лечения:
Рентгеновское облучение вилочковой железы, когда противопоказана тимэктомия (как альтернатива тимэктомии).
Гамма-терапия на область тимуса. Данный метод применяют у пациентов, которым в силу тех/иных обстоятельств невозможно провести тимэктомию, а также как метод комплексной терапии после удалении тимомы (особенно в случаях инфильтрации опухоли в расположенные рядом органы). Суммарную дозу гамма-облучения подбирают индивидуально (в среднем 40-60 Грей).
Противопоказания гамма-терапии:
• дети пубертатного периода.
Методы экстракорпоральной иммунокоррекции (гемосорбция и плазмаферез – смотрите клинический протокол диагностики и лечения «Лечение кризов»). Можно использовать такие методы, как гемосорбция/энтеросорбция (угольные сорбенты СУМС 15-30 мг/кг веса 3 раза в сутки в течение 2-3 недель).
Проведение плазмафереза/плазмасорбции:
Основные показания для проведения плазмафереза:
· миастенический криз;
· острое течение миастении;
· начальная стадия стероидной терапии в связи с возможным обострением заболевания.
Обследование больного перед плазмаферезом включает:
· оценку состояния жизненно важных функций;
· полный клинический анализ крови (в том числе тромбоциты, гематокрит);
· определение группы крови и резус-фактора;
· серологические тесты на сифилис, ВИЧ, вирус гепатита В;
· определение концентрации общего белка, белковых фракций;
· определение основных показателей свёртываемости крови;
· клинический анализ мочи.
Как правило, плазмаферез проводится курсом на протяжении 1-2 недель с кратностью 2-5 операций. Прерывистый плазмаферез приводит к улучшению после проведения 3 – 4 сеансов.
Противопоказаний к применению плазмафереза нет.
Показания для консультации специалистов:
· консультация терапевта – при необходимости/в случае отсутствия специалиста на догоспитальном уровне – установление/исключение терапевтического заболевания (артериальная гипертензия, пневмония), коррекция показателей гемодинамики, электролитного баланса в ходе проводимой терапии;
· консультация эндокринолога – при необходимости/в случае отсутствия специалиста на догоспитальном уровне с целью коррекции терапии гормональных и электролитных нарушений;
· консультация торакального хирурга – при решении вопроса об оперативном лечении;
· консультация реаниматолога – для решения вопроса о переводе в отделение реанимации и интенсивной терапии.
Показания для перевода в отделение интенсивной терапии и реанимации:
· появление и нарастание симптомов миастенического криза;
· нестабильность гемодинамики;
· нарушение функции дыхания.
Индикаторы эффективности лечения:
· компенсация витальных нарушений;
· устранение метаболических нарушений, возникающих вследствие гипоксии и оксидантного стресса;
· снятие обострения миастенического процесса;
· полная или достаточная компенсации двигательных нарушений на фоне АХЭ препаратов.
Дальнейшее ведение.
· диспансерное наблюдение в поликлинике по месту жительства. Проведение первичной и вторичной профилактики при миастении (см.амбулаторный уровень).