Что называют бактерии паразиты
Бактерии-паразиты: виды, влияние на человека, пути заражения
Взрослый человек имеет до 4кг разных микроорганизмов, из них больше половины – микробы, приносящие пользу, населяют кишечный тракт, обеспечивают нормальное пищеварение. Еще килограмм бактерий распространён по всему организму.
Но проникнуть в системы органов и тканей способны и болезнетворные бактерии паразиты, вызывающие развитие тяжелых заболеваний.
Бактерии паразиты – это живые организмы, микроскопических размеров (от 0,1–30 мкм), которые проникая внутрь, поселяются в организме хозяина, питаются там, живут, размножаются. При этом оказывают негативное влияние на макроорганизм.
Влияние бактерий паразитов на человека
Вредоносные виды бактерий оказывают на человека разное влияние:
Виды бактерий паразитов
Бактерии паразиты делятся на облигатных и факультативных.
Облигатные виды ведут только паразитический способ жизни, им не свойственна свободноживущая фаза развития. Внутриклеточные микроорганизмы способны существовать только в клетках хозяина. После его гибели, умирают и сами (хламидии, риккетсии). Они развиваются в анаэробных условиях и не устойчивые во внешней среде. Поэтому передача возбудителя идет строго от одного организма к другому (трансмиссивно, трансплацентарно, через молоко матери).
Факультативные паразиты могут жить вне макроорганизма. Они способны сами продуцировать питательные вещества или при наступлении неблагоприятных условий замедлять метаболизм и временно прекращать жизнедеятельность. При случайном попадании в тело человека, начинают размножаться, вызывая повреждение органов и тканей.
Пути заражения организма
Заражение происходит тремя путями:
Питание бактерий паразитов
Есть виды с автотрофным и гетеротрофным типом питания. Автотрофы способны сами синтезировать необходимые питательные вещества. Гетеротрофы питаются уже готовыми продуктами и делятся на 3 подвида. Среди них не все паразитируют и приносят вред.
Сапрофиты получают органические соединения из отмерших растений и животных, за счет пищеварительных ферментов, которые они выделяют в перегнивающую массу.
Симбионты сожительствуют с другими организмами и в ходе эволюции стали приносить пользу высшим растениям. Это, к примеру, азотфиксирующие бактерии, которые селятся на корнях бобовых растений. Поглощают азот из почвы и воздушной среды, применяют его в процессе синтеза цитоплазмы, и обращают органические соединения N в минеральные, доступные для бобовых растений. За один вегетационный период азотфиксирующие бактерии способны скапливать около 100кг азота на гектар.
Паразиты выживают за счет организма хозяина, при этом наносят ощутимый вред. Приводят к развитию заболеваний, путем выделения токсических продуктов жизнедеятельности в кровь и разрушения тканей на клеточном уровне.

Среда обитания бактерий паразитов
Среда обитания бактерий паразитов весьма разнообразна:
Живые организмы для многих бактерий паразитов стали единственным способом выживания: обеспечивают питание, благоприятные условия для развития и размножения.
Значение бактерий паразитов в природе и жизни человека
Бактерии-паразиты выживают благодаря взаимодействию с живыми особями. Часть является причиной заболеваний животных и человека (чумы, туберкулеза, сепсиса, менингита, холеры и др.), другая часть — растений. Такие бактерии способны к спорообразованию и так длительный период времени (десятки лет) сохраняют жизнеспособность.
В России борьба с различными инфекционными заболеваниями: дифтерией, скарлатиной, туберкулезом и др. достаточно успешна. Для разных групп заболевания проводятся особые оздоровительные мероприятия.
Так в борьбе с дифтерией основную роль играют прививки, а при инфицировании туберкулезной палочкой — терапия специальными лекарственными средствами вместе с гигиеническим режимом и организацией специализированных отделений, госпиталей и санаториев. Препятствие к распространению кишечных инфекций (бактериальная дизентерия) заключается в лечении больных, борьбе с загрязнением окружающей среды возбудителями болезней.
При трансмиссивных инфекционных заболеваниях (эпидемический сыпной тиф и др.) оздоровительные мероприятия направляются на выявление и лечение больных людей и животных, и уничтожение переносчиков.
Что такое микробы и чем они отличаются от паразитов? (2021-03-15 11:08:14)
Что такое микробы и чем они отличаются от паразитов?
Микробы (микроорганизмы) являются живыми организмами, которых невозможно увидеть невооруженным глазом. Паразиты — это организмы, которые живут за счёт их хозяина (паразитируют). Они могут быть как микроорганизмами, так и нет.
Бактерии — это микроорганизмы меньше 500 микрометров (1 микрометр = 1 миллионная часть метра) состоящие только из одной клетки с ядром (эукариоты). Бактерии присутствуют везде: в воздухе, в воде и в почве. Как правило, большинство из них являются безвредными для человека.
Бактериология — это наука, которая занимается изучением бактерий. Эта наука классифицирует бактерии в 3 главные категории:
— спирохеты (в форме спирали);
— палочки/бациллы (удлиненные как палочки);
— кокки (в форме сферы/шара).
В зависимости от способа взаимодействия с различными красителями, бактерии классифицируются на грамположительные и на грамотрицательные. От этой реакции зависит дальнейшее лечение.
Чаще бактерии развиваются во влажных и теплых условиях. Бактерии, которые нуждаются в кислороде для развития и размножения (аэробные бактерии), наблюдаются в основном ближе к поверхности тела, на коже, и на уровне дыхательной системы. Другие развиваются в бескислородной атмосфере (анаэробные бактерии), например на уровне кишечника или глубоких ран.
В благоприятных условиях (тепло и питательные вещества в достаточном количестве) бактерии размножаются через деление на 2 одинаковых клетках, через каждые 20 минут. Таким образом, через 6 часов, одна бактерия может дать начало около 250.000 новым бактериям.
Что такое паразиты?
Паразит — это живое существо, живущее за счёт другого организма, которого он паразитирует (использует для жизнедеятельности питательные вещества, кровь и ткани организма-хозяина).
Паразиты, которые вызывают болезни у человека, бывают двух типов:
— одноклеточные организмы (простейшие одноклеточные организмы);
— многоклеточные организмы.
Заражение паразитами происходит через зараженные продукты питания или при транзите кожи (во время укуса насекомого или во время купания).Паразиты часто встречаются в тропических областях (из-за тепла и влажности), а также в странах с проблемными санитарно-гигиеническими условиями.Заболевания, вызванные паразитами, лечатся противопаразитарными препаратами.
Паразитами называют любые организмы, которые живут за счёт хозяина, а вирусы – иждивенцы особо беспринципные и привередливые: в отличие от бактерий, им нужны не просто живые клетки, а строго определённого вида. Когда вирус попадает внутрь, он разделяется на белковую оболочку и нуклеиновую кислоту, после чего начинает управлять биосинтезом в оккупированной клетке и плодить себе подобных, распространяющихся по организму захватчиков – так и возникает болезнь.
При своевременной диагностике и вакцинации победить болезнь проще, но до того, как человечество узнало о существовании вирусов, они успели нанести немалый урон – и продолжают это делать.
Подробнее
Медицинский лекторий
Сахарный диабет и ожирение. Новый взгляд на проблему.
Вирус папилломы человека: профилактика, вакцинация, лечение.
Как правильно измерить температуру тела?
Лечение перекисью водорода по методике Неумывакина
«Самое интересное в жизни – это человек. А я везучая на людей». Интервью с директором благотворительного фонда «КИСЛОРОД» Майей Сониной
Диагностику заболеваний почек можно автоматизировать
Лишний вес у детей и подростков: 6 способов сохранить здоровье своего ребенка
Если в анализе крови очень много лимфоцитов
Симптомы, при которых мужчине следует сразу обращаться к доктору
Рацион долгожителей: простые правила средиземноморской диеты
Оксалаты и здоровье почек: темная сторона растительной пищи и что со всем этим делать
Почему колени чаще болят у женщин?
Названа неожиданная польза горьких огурцов
Врач назвала минерал, необходимый здоровью человека осенью
Миколог дал рекомендации по безопасному сбору грибов
Эксперты рассказали о способе справиться с хандрой после выходных
Почему возникает аносмия (потеря обоняния) и как ее лечить (в т.ч. после коронавируса)?
О каких проблемах со здоровьем можно узнать по внешним признакам?
Диетолог назвала самый полезный способ готовить яйца
Бактерии паразиты вызывающие заболевания у человека
Бактерии-паразиты — патогенные микроорганизмы, которые живут за счет питательных веществ других организмов. Один из примеров таких бактерий — болезнетворные паразиты. В организме человека обитает до 4 кг различных микробов, около 3 кг – это полезные микроорганизмы, живущие в кишечнике, способствуя нормальному процессу пищеварения.
Остальные около 1 кг обитают в различных системах и тканях. Но есть и вредоносные организмы, которые убивают человека. Бактерии-паразиты – это микроскопические организмы,которые живут и питаются внутри или на поверхности хозяина, способные вызывать тяжелейшие инфекционные заболевания несовместимые с жизнью! Размеры микробов малы от 0,1–30 мкм.
Отдел бактерии
Бактерии так малы, что их можно увидеть только при увеличении в 1000 и даже до 2000 раз. К тому же они и по форме, и по своему внешнему виду очень часто трудно различимы между собой.
Клетки бактерий имеют разную форму: одноклеточные шаровидные формы называют кокками, прямые палочковидные — бациллами, имеющие форму запятой — вибрионами, спирально изогнутые — спириллами.
Если бактерии располагаются по одной, их называют монококки (от греч. «монос» — один и «коккус» — шарик), по две — диплококки (от греч. «диплос» — двойной и «коккус»), тетракокки (от греч. «тетра» — четыре и «коккус»); они могут иметь вид грозди — стафилококки (от греч. «стафилс» — виноградная гроздь и «коккус»), могут быть закручены — спирохеты (от лат. «спиpa» и греч. «хета» — щетинка).
Среди бактерий есть подвижные и неподвижные формы. Подвижные передвигаются при помощи жгутиков, которых иногда бывает несколько. Есть и колониальные формы.
У бактерий есть споры, но они предназначены не для размножения, а для перенесения неблагоприятных условий, так как они защищены толстыми оболочками. Они называются цистами.
Бактерии паразиты. Споры выдерживают длительное высушивание, нагревание свыше 100″С и охлаждение почти до абсолютного нуля. В обычном состоянии бактерии неустойчивы к внешним воздействиям и могут быстро погибать при высушивании, при нагревании до 65-80°С и под действием солнечного света или дезинфицирующих веществ.
Средой обитания бактерий может быть воздух, они поднимаются в верхние слои биосферы (часть оболочки Земли, населенной живыми организмами) до 30 км. Через воздух распространяются возбудители ангины, скарлатины, туберкулеза.
В почве больше всего бактерий сосредоточено в окультуренном черноземе: в 1 га почвы — 2,5-3 млрд бактерий. Здесь они играют большую роль в почвообразовании (азотобактерии, нитрифицирующие и гнилостные бактерии).
В воде: в поверхностных слоях воды открытых водоемов, особенно в черте города. Служат источником инфекционных болезней (дизентерия, холера, бруцеллез).
В живых организмах: бактерии и бывают болезнетворные (которые вызывают различные заболевания) и симбиотические, живущие в органах пищеварения животного и человека и помогающие им расщеплять и усваивать пишу.
На теле человека, его одежде могут быть разнообразные бактерии. Много их бывает в ротовой полости, на открытых участках кожи и других частях тела.
Бактерии паразиты. Питаются бактерии, всасывая питательные вещества всей поверхностью клетки. По способу питания они могут быть: сапрофиты и паразиты. Сапрофиты питаются органическими веществами умерших животных и растений.
Так, роль бактерий молочнокислого брожения положительная в том, что они способствуют: 1) приготовлению молочнокислых продуктов питания (творога, простокваши, сметаны, кефира, масла); 2) силосованию кормов; 3) закваске и засолке капусты, огурцов, помидоров. Отрицательная — порча продуктов.
Бактерии уксуснокислого брожения способствуют окислению спирта в уксусную кислоту, которая используется при мариновании и консервировании плодов и овощей. Отрицательная роль — порча продуктов.
Среда обитания бактерий паразитов
Среда обитания бактерий паразитов весьма разнообразна:
Живые организмы для многих бактерий паразитов стали единственным способом выживания: обеспечивают питание, благоприятные условия для развития и размножения.
Значение бактерий паразитов в природе и жизни человека
Бактерии-паразиты выживают благодаря взаимодействию с живыми особями. Часть является причиной заболеваний животных и человека (чумы, туберкулеза, сепсиса, менингита, холеры и др.), другая часть — растений. Такие бактерии способны к спорообразованию и так длительный период времени (десятки лет) сохраняют жизнеспособность.
В России борьба с различными инфекционными заболеваниями: дифтерией, скарлатиной, туберкулезом и др. достаточно успешна. Для разных групп заболевания проводятся особые оздоровительные мероприятия.
Так в борьбе с дифтерией основную роль играют прививки, а при инфицировании туберкулезной палочкой — терапия специальными лекарственными средствами вместе с гигиеническим режимом и организацией специализированных отделений, госпиталей и санаториев. Препятствие к распространению кишечных инфекций (бактериальная дизентерия) заключается в лечении больных, борьбе с загрязнением окружающей среды возбудителями болезней.
При трансмиссивных инфекционных заболеваниях (эпидемический сыпной тиф и др.) оздоровительные мероприятия направляются на выявление и лечение больных людей и животных, и уничтожение переносчиков.
Будьте осторожны
По статистике более 1 миллиарда человек заражено паразитами. Вы даже можете не подозревать, что стали жертвой паразитов.
Определить наличие паразитов в организме легко по одному симптому — неприятному запаху изо рта. Спросите близких, пахнет ли у вас изо рта утром (до того, как почистите зубы). Если да, то с вероятностью 99% вы заражены паразитами.
Заражение паразитами приводит к неврозам, быстрой утомляемости, резкими перепадами настроениями, в дальнейшим начинаются и более серьезные заболевания.
У мужчин паразиты вызывают: простатит, импотенцию, аденому, цистит, песок, камни в почках и мочевом пузыре.
У женщин: боли и воспаление яичников. Развиваются фиброма, миома, фиброзно-кистозная мастопатия, воспаление надпочечников, мочевого пузыря и почек. А так же сердечные и раковые заболевания.
Сразу хотим предупредить, что не нужно бежать в аптеку и скупать дорогущие лекарства, которые, по словам фармацевтов, вытравят всех паразитов. Большинство лекарств крайне неэффективны, кроме того они наносят огромный вред организму.
Это одноклеточные организмы. Они лишены ядер (прокариоты). Генетический материал представлен кольцевой молекулой ДНК, свободно плавающей во внутренней жидкости. Типичные для ядерных клеток элементы отсутствуют, их роль выполняют более простые органеллы.
Питание, поглощение жидкости происходит через мембрану клетки. Снаружи от нее располагается оболочка, которую называют клеточной стенкой. Она защищает микроорганизм от воздействия внешней среды.
Эти микроорганизмы относятся к гетеротрофам – они не синтезируют самостоятельно органические соединения и нуждаются в поступлении их извне.
Выделяют облигатных и факультативных паразитов человека:
Как происходит заражение бактериями
Выделяют три основных пути распространения паразита:
Примеры бактерий паразитов человека
Микробы-патогены питаются за счет людей, приводя к развитию различных заболеваний.
Bacillus anthracis — возбудитель сибирской язвы – микроорганизм, живущий на коже и слизистых дыхательных путей человека. Этот паразит может длительное время никак себя не проявлять. Заболевание начинается на фоне снижения иммунитета, в виде гнойников на коже, остеомиелита, сепсиса, поражения сердца, легких, оболочек мозга. Источником паразита становится или сам заболевший, или носитель.
Существование микроорганизмов вне хозяина
Многие типы бактерий могут вызывать заболевания различной степени тяжести у растений, животных и человека. При этом существует особый тип микроорганизмов – внутриклеточные паразиты, которые не могут существовать вне другого организма. Со смертью хозяина погибают сами. Другие могут не только существовать без хозяина, но и в процессе жизнедеятельности менять их. Поэтому патогенные микроорганизмы подразделяют на:
Облигатные паразиты получили такое название, потому что существуют только внутри клетки. К этой группе инфекций относятся риккетсии, вирусы, некоторые простейшие. Внутриклеточные паразиты зависят от другого организма и не могут существовать без него.
Факультативные паразиты могут существовать вне хозяина. В отличие от внутриклеточных они могут сами синтезировать органические вещества или же впадать в анабиоз. В это время у них прекращается вся жизнедеятельность, они капсулируются – покрываются специальной оболочкой. Попадая в организм хозяина, они начинают активно размножаться.
Важно знать! Внутриклеточные паразиты, такие как вирусы и риккетсии, встраиваются в клетку хозяина. В результате она начинает вырабатывать только те вещества, которые необходимы для роста и размножения микроорганизмов.
Пожиратели бактерий: убийцы в роли спасителей
Пожиратели бактерий: убийцы в роли спасителей
«Враг моего врага — мой друг» — это утверждение как нельзя лучше выражает главную причину интереса человека к вирусам бактерий. Фото фагов: Claudius Schulze.
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Сегодня в связи с нарастающей проблемой антибиотикорезистентности ученые всего мира ведут поиски новых антибиотиков и способов борьбы с инфекционными заболеваниями. И всё больше ученые оглядываются на естественный, но почти забытый метод — фаготерапию. Бактериофаги — природные враги бактерий, существовавшие задолго до появления человека. Почему же мы не используем их вместо антибиотиков, которые привели к такой глобальной проблеме, как резистентность бактерий, ну или хотя бы в дополнение к ним? Что это за диковинные создания и могут ли они быть полезны человеку? Безопасны ли они? В этом обзоре мы попытались собрать воедино имеющиеся данные о бактериофагах и показать вам, насколько красив и многообразен их невидимый мир.
«Био/мол/текст»-2016
Эта работа опубликована в номинации «Своя работа» конкурса «био/мол/текст»-2016.
Спонсор номинации — Future Biotech, проект, объединяющий профессионалов и энтузиастов в области биологии и биотехнологий.
Генеральным спонсором конкурса, согласно нашему краудфандингу, стал предприниматель Константин Синюшин, за что ему огромный человеческий респект!
Спонсором приза зрительских симпатий выступила фирма «Атлас».
Спонсор публикации этой статьи — Виктор Татарский.
ХХ столетие называют веком атома, нейлона и антибиотиков. С началом массового применения пенициллина в 1943 году медики всего мира получили мощнейший механизм для защиты организма от атак, казалось бы, всех болезнетворных бактерий. И ученые, подхватив знамя антибиотикотерапии, ринулись на поиски и разработку новых антибактериальных средств. Но если мирный атом и синтетические материалы с лихвой оправдали возложенные на них ожидания, то надежды на всемогущество антибиотиков, увы, постепенно тают: резистентность бактерий к ним становится всё шире. 16 сентября 2000 года на Всемирном дне резистентности в Торонто была принята Декларация по борьбе с бактериальной резистентностью [1], а годом позже ВОЗ опубликовала Глобальную стратегию по сдерживанию устойчивости к противомикробным препаратам, в тексте которой есть такие строки: «Без согласованных действий всех стран многие великие открытия, сделанные учеными-медиками за последние 50 лет, могут утратить свое значение из-за распространения антибиотикорезистентности» [2]. Означает ли это, что мы в скором времени вновь окажемся бессильны перед бактериями? Существуют ли альтернативные подходы к борьбе с инфекционными заболеваниями? К счастью, да. Один из них — применение бактериофагов, самых многочисленных, древних и распространенных на нашей планете вирусов [3], существующих на Земле свыше 3 млрд лет и неоправданно заброшенных исследователями в 1960–1970-е годы на фоне успехов антибиотикотерапии.
Открытие
Несомненно, многие бактериологи наблюдали и описывали проявления действия фага на бактериальные культуры. В 1896 году английский бактериолог Э. Ханкин, исследуя антибактериальное действие воды индийских рек, пришел к выводу о существовании агента, проходящего через бактериальные фильтры и вызывающего лизис холерных вибрионов. По некоторым данным, российский микробиолог Н.Ф. Гамалея в 1897 году наблюдал лизис бацилл сибирской язвы. Однако первая научная публикация о фагах — статья 1915 года английского микробиолога Ф. Туорта, в которой он описал инфекционное поражение стафилококков, значительно изменявшее морфологию колоний. Инфекционный агент свободно проходил через бактериальные фильтры, и его можно было переносить из одной колонии в другую. Туорт выдвинул несколько гипотез, объясняющих это явление, в частности — гипотезу о фильтрующемся вирусе, подобном вирусам растений и животных. Однако его работа не привлекла внимания ученых, а Туорт забросил ее из-за службы в армии: началась Первая мировая.
В 1917 году канадский бактериолог Ф. Д’Эрелль независимо от Туорта сообщил об открытии вируса, «пожирающего» бактерий, — бактериофага [4]. Микробиологи того времени считали, что чума свиней вызывается совместным действием микроба и вируса. Д’Эрелль предположил, что схожая этиология и у дизентерии. С помощью свечей Шамберлана он отфильтровал фекалии больных дизентерией и добавил их в пробирки с культурами шигелл, намереваясь ввести смесь бактерий и предполагаемого вируса экспериментальным животным. Однако на следующие сутки он обнаружил, что бульон, в котором росли шигеллы, стал прозрачным, что свидетельствовало о гибели бактерий. Профильтровав бульон из этих пробирок, он снова заразил полученными фильтратами культуры шигелл. И вновь на следующие сутки он обнаружил, что бульон стал прозрачным. Полученное «литическое начало» можно было бесконечно пассировать от одной культуры к другой, что привело Д’Эрелля к мысли о существовании вируса, разрушающего бактерии. В дальнейшем он обнаружил фаги стафилококка, холерного вибриона и сальмонеллы. Учитывая эффективность фагов против патогенных микроорганизмов и их широкое распространение в природе, Д’Эрелль предположил, что они играют определенную роль в развитии иммунитета к инфекционным заболеваниям и выздоровлении.
В 1920–1940-е годы было проведено множество исследований по клиническому применению бактериофагов, однако стабильных результатов получено не было, и на Западе бактериофаги стали в основном объектом изучения биологов. В 1931 году Совет фармации и химии Американской медицинской ассоциации опубликовал обзор 150 работ по фаготерапии, в котором M. Итон и С. Бэйн-Джонс [5] утверждали, что природа фага неживая; возможно, это фермент, и ошибочно связывать воздействие фага на бактерии или его терапевтический эффект с его жизнедеятельностью. Такие выводы способствовали существенному сокращению капиталовложений в исследования по медицинскому применению фагов на Западе.
В СССР в ранние годы бактериофагам уделяли достаточно внимания. В 1923 грузинский микробиолог Г.Г. Элиава, ученик Д’Эрелля, основал в Тбилиси Институт бактериофагов, ставший впоследствии Всесоюзным центром фаготерапии, коллекция которого на сегодняшний день составляет около 3000 фаговых штаммов. Однако успешное применение антибиотиков в 1960–1970-е годы практически похоронило идеи фаготерапии. Так, например, в Большой советской энциклопедии указано: «Антибиотики и другие химиотерапевтические средства оказались эффективнее фагов, в связи с чем их применение с лечебной целью сузилось».
Происхождение
Вопросом о природе бактериофага задавался еще Туорт в своей первой статье. Д’Эрелль в своем фундаментальном труде выдвинул несколько теорий (гипотез) происхождения фагов, из которых две сохранили значение до настоящего времени: «теория вируса» и «регрессивная теория».
В рамках вирусной теории бактериофаги, подобно вирусам растений и животных, рассматриваются как прямые потомки неких очень примитивных форм, существовавших еще до появления клеток, и представляют собой автономные агенты, являющиеся облигатными паразитами бактерий. Этой теории придерживался Д’Эрелль в самом начале своих исследований, и ее принимало как нечто само собой разумеющееся большинство вирусологов. Но эта концепция, по сути, мало что дает, так как в применении к вирусам такие термины, как автономность и паразитизм, трудно поддаются определению, а сама гипотеза сложно доказуема, поскольку нет ископаемых останков вирусов, а их родственные связи можно изучать только методами молекулярной филогенетики [6].
Согласно регрессивной теории, фаги постепенно развивались из более сложных форм жизни путем утраты всей протоплазмы, ненужной для присущего бактериофагу способа существования. Эта гипотеза лучше вписывается в современную биологию, так как промежуточные стадии процесса дегенерации довольно легко себе представить, а постепенную утрату бактериями способности к синтезу можно изучать экспериментально.
Вполне возможно, что бактериофаги произошли из примитивного полового аппарата бактерий, первоначально развившегося для передачи генетического материала от одной бактериальной клетки к другой. Это могло бы объяснить, почему некоторые фаги и в настоящее время способны выполнять эту функцию путем лизогенной конверсии. Теория предполагает, что генетический материал фагов — это редуцированный и модифицированный нуклеоид бактерий, сохранивший гомологию с «прародителем» и потому способный с ним рекомбинировать или даже частично замещать его. Это могло бы объяснить свойства умеренных фагов, способных встраиваться в определенные локусы ДНК клетки-хозяина, становясь частью бактериального наследственного аппарата. В процессе эволюции умеренные фаги могли путем дальнейших мутаций, влияющих на спектр литического действия [7], необратимо превращаться в вирулентные, поражающие хозяев, с которыми они не имели генетического родства. Согласно этой теории, различные штаммы фагов филогенетически не связаны друг с другом, и определенный фаг даже может быть филогенетически ближе клетке-хозяину, нежели другим фагам. Отсюда следует, что если данная теория верна, то между бактериофагами и вирусами животных и растений нет никакого родства, а фенотипическое сходство — чисто внешнее, обусловленное сходной экологией.
Тем не менее биоинформатические подходы — сравнения огромных массивов геномов и фолдингов белков, а особенно «архитектуры» фаговых частиц — всё же позволяют находить у бактериофагов, фагов архей и вирусов в целом филогенетически общие признаки [3], [8].
Строение и классификация
На протяжении почти 70 лет бактериофаги, как и другие вирусы, были для биологов такими же невидимыми, как атомы для физиков, в силу их субмикроскопических размеров. И только в 1942 году, с помощью недавно изобретенного (М. Кнолль, Э. Руска, 1931 г.) электронного микроскопа, будущий нобелевский лауреат С. Лурия (Колумбийский университет) и Т. Андерсон (RCA-лаборатория, Камден, Нью-Джерси) получили первые фотографии бактериофага Т2, или «анти-коли РС», как его называли Лурия и Андерсон (рис. 1).
Рисунок 1. Изображения бактериофага Т2, полученные С. Лурия и Т. Андерсоном с помощью просвечивающего электронного микроскопа: а — первая в мире фотография бактериофага (2 марта 1942 г.); б — бактериофаг Т2 в культуре Escherichia coli (2 марта 1942 г.); в — Т2 «крупным планом» (29 марта 1962 г.).
[42] (фото а и б)
Рисунок 2. Микрофотография фага Т2, полученная с помощью сканирующего электронного микроскопа.
Фаги весьма разнообразны по морфологии — в отличие от вирусов животных и растений. Все известные в настоящее время вирусы эукариот имеют либо форму многогранника (икосаэдра), либо спиралевидный тип симметрии. Что же касается фагов, то среди них тоже встречаются формы со спиралевидным или кубическим типами симметрии, но подавляющее число изученных к настоящему времени фагов сочетает в одной частице оба типа: кубический — у головки, а спиралевидный — у отростка (рис. 2). Столь своеобразное строение фагов, отличающее их от других вирусов, объясняется наличием у бактерий ригидной клеточной стенки, которая исключает возможность проникновения вирионов в клетку путем пиноцитоза или виропексиса. Такая структурная особенность бактерий способствовала формированию у фагов других способов инфицирования, что и нашло отражение в их облике.
Именно морфология легла в основу современной классификации бактериофагов. Казалось бы, целесообразнее разделять фаги по принципу их связи с определенным видом микроорганизма, который они поражают, — что и легло в основу первых классификаций. Но этот принцип не обеспечивает необходимой точности, так как один штамм фага может поражать разные микроорганизмы, то есть иметь широкий литический спектр. И наоборот, один вид бактерий может поражаться несколькими фагами, различающимися между собой по целому ряду свойств, в том числе морфологически, тогда как фаги, активные в отношении разных видов и даже родов микроорганизмов, могут быть морфологически тождественны.
Были попытки классифицировать фаги и по сумме признаков (антигенных, физиологических, биохимических, физико-химических, морфологии негативных колоний, спектру литического действия и т. п.).
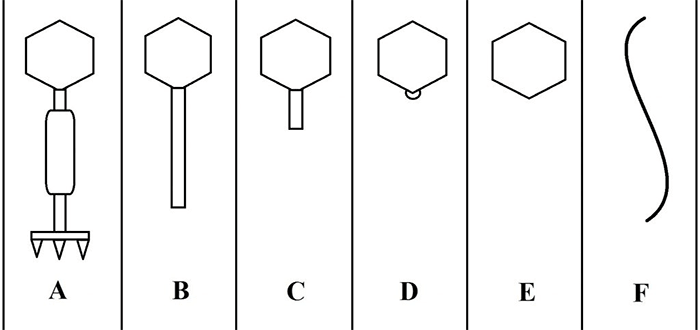
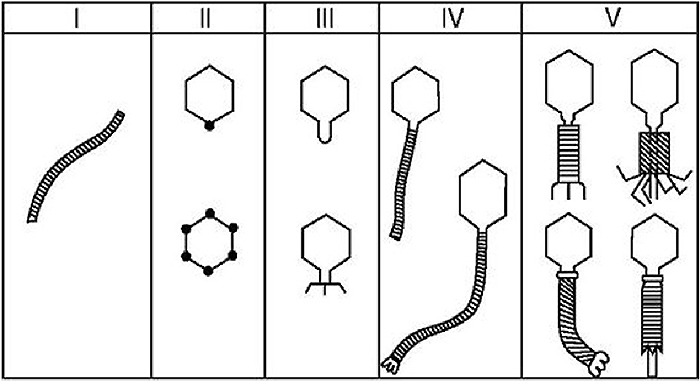
С развитием электронной микроскопии появилась возможность классифицировать фаги по морфологии. Дэвид Бредли в 1967 году предложил разделить фаги на шесть морфологических групп: с A по F (табл. 1, рис. 3). Вторая используемая классификация, предложенная А.С. Тихоненко в 1968, объединяет фаги групп D и E в одну (табл. 1, рис. 4). Микрофотографии фагов, относящихся к разным морфогруппам, представлены на рисунках 5 и 6.
| Группа по Бредли | Группа по Тихоненко | Морфология | Тип нуклеиновой кислоты |
|---|---|---|---|
| A | V | С сокращающимся отростком | Двухцепочечная ДНК |
| B | IV | С длинным несокращающимся отростком | Двухцепочечная ДНК |
| C | III | С коротким несокращающимся отростком | Двухцепочечная ДНК |
| D | II | Без отростка, с капсомерами | Одноцепочечная ДНК |
| E | II | Без отростка и капсомеров | Одноцепочечная РНК |
| F | I | Нитевидные | Одноцепочечная ДНК |
Рисунок 3. Схематическое изображение фаговых морфогрупп по Бредли (1967).
рисунок автора статьи
Рисунок 4. Схематическое изображение фаговых морфогрупп по Тихоненко (1968)
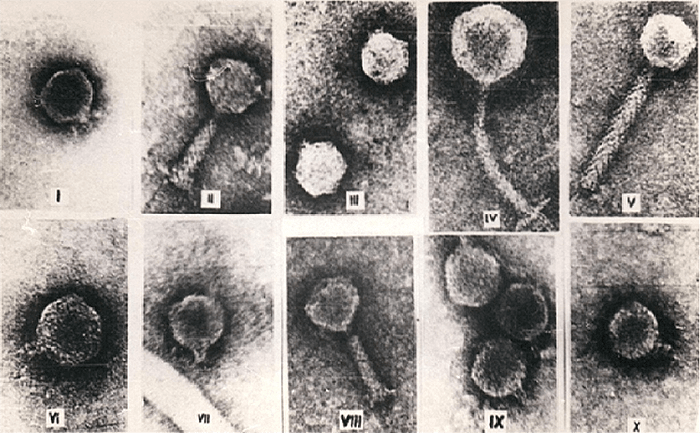
Рисунок 5. Различные морфоварианты бактериофагов.
микрофотографии автора статьи
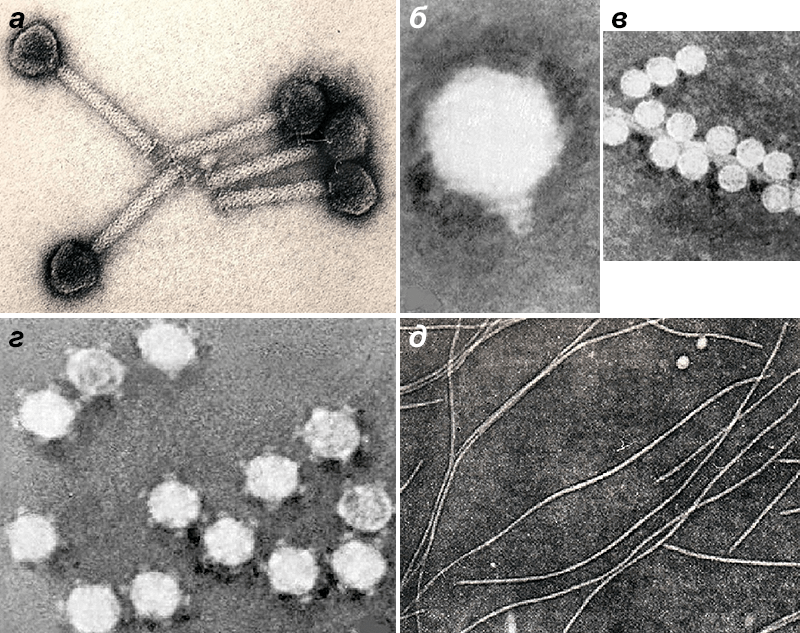
Рисунок 6. Микрофотографии бактериофагов из разных морфогрупп: а — фаг 1997 Yersinia enterocolitica с длинным несокращающимся чехлом; б — фаг Т3 с коротким отростком; в — фаг МS2 без отростка; г — фаг Х174 без отростка, с капсомерами; д — нитчатый фаг Fd.
микрофотографии автора статьи
Рисунок 7. Схема строения вириона фага семейства Myoviridae
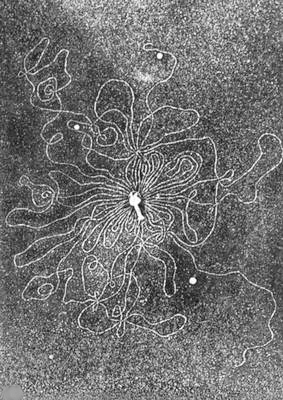
Большинство фагов состоит из головки диаметром 45–140 нм и отростка («хвоста») толщиной 10–40 нм и длиной 100–200 нм (рис. 7). Так выглядят представители порядка Caudovirales («хвостатых фагов»), и именно их образ обычно извлекается из памяти при упоминании термина «бактериофаг». Содержимое головки состоит преимущественно из плотно упакованной молекулы ДНК или (реже) РНК, длина которой во много раз превышает размеры головки и достигает 60–70 мкм (рис. 8), и иногда небольшого количества белка — например, ферментов, которые осуществляют первичную транскрипцию генетического материала фага или способствуют ей. Капсид представляет собой белковую или (не у Caudovirales) липопротеиновую оболочку, собранную из множества копий одного или двух белков. Капсид может быть икосаэдрическим, сферическим, лимоновидным или плеоморфным [9], и именно он, по сути, определяет размер фагового генома.
Рисунок 8. Микрофотография бактериофага с высвободившейся нитью ДНК.
Отросток представляет собой белковую трубку, окруженную у ряда бактериофагов (семейства Myoviridae, типовой представитель которого — фаг Т4) чехлом, состоящим из сократительных белков, подобных мышечным, благодаря чему он способен сокращаться, обнажая часть стержня. С головкой отросток стыкуется с помощью белкового кольца — «портала» («воротничка»). На противоположном конце, в основании, отросток содержит лизоцим (как домен белка, пронзающего клеточную стенку), служащий для точечного растворения пептидогликана. Возможно и нахождение в основании отростка АТФазы, обеспечивающей энергией инъекции нуклеиновой кислоты в бактерию [10]. Там же у фагов такого типа имеется гексагональная базальная пластинка с несколькими шиповидными выростами и тонкими длинными нитями, с помощью которых фаг распознает рецепторы «своих» бактерий и прикрепляется к ним.
Нитевидные фаги имеют размеры 8×800 нм и лишены выраженных «органов».
Бактериофаги довольно устойчивы к воздействию различных химических и физических факторов. Они выдерживают колебания рН в пределах 5,0–8,0; большинство резистентно к действию холодных водных растворов глицерина и этанола, а также цианидов, фторидов, динитрофенола, хлороформа, тимола и фенола. Бактериофаги хорошо сохраняются в лиофилизированном состоянии, но разрушаются при кипячении, УФ-облучении, действии некоторых химических дезинфектантов (в частности, кислот и формалина). Фаги хорошо сохраняются при низких температурах (до −200 °С в глицерине), но быстро инактивируются при 65–70 °С [10].
Взаимодействие с бактериями
Фаги — облигатные внутриклеточные паразиты, так как у них нет механизмов для выработки энергии и рибосом для синтеза белка. Размножение фага происходит только внутри бактерии-хозяина и посредством ее синтетической машинерии. Важным свойством бактериофагов является их специфичность: фаги могут поражать определенный вид бактерий (моновалентные фаги) или же только избранные штаммы/варианты внутри вида (типовые фаги, например, фаги V. cholerae classica и El Tor), но некоторые не столь разборчивы и поражают бактерий разных видов и даже родов (поливалентные фаги) [11]. Тем не менее очень сложно судить о специфичности фагов в природных условиях, поскольку там действуют многочисленные методологические ограничения и популяционные закономерности, и порой один и тот же фаг можно принять как за «генералиста», так и за «специалиста» [12].
По характеру действия на бактерии различают вирулентные и умеренные фаги.
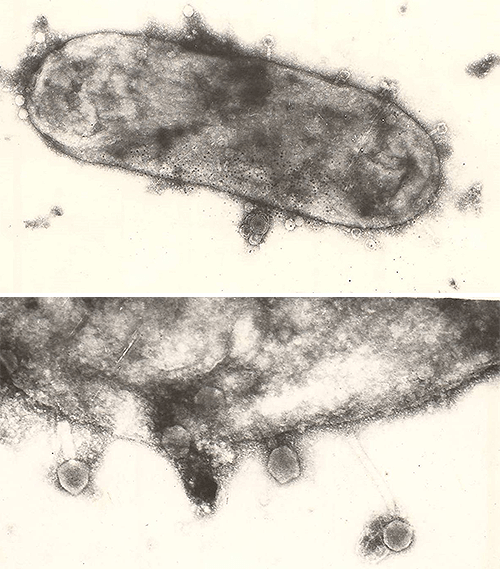
Рисунок 9. Адсорбция фага PIcmlclr 100ts на поверхности Yersinia pestis.
микрофотографии автора статьи
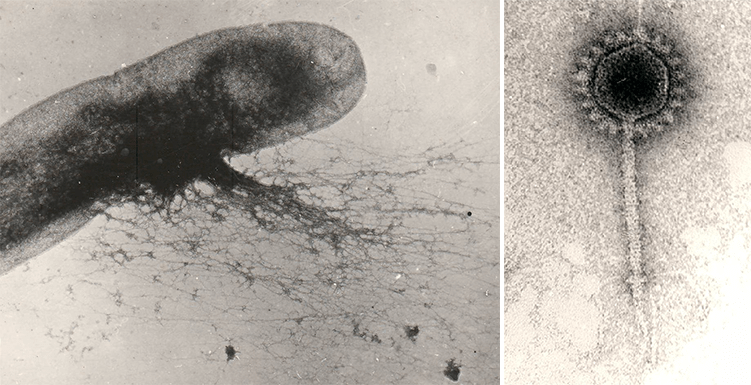
Рисунок 10. Лизис E. coli и выход фаговых частиц. Справа — зрелая форма бактериофага.
микрофотографии автора статьи
Но некоторые фаги способны покидать клетку без лишнего шума. Так делает, например, фаг L2, паразитирующий в бактериях рода Acholeplasma, лишенных клеточной стенки (их знаменитые родственники — микоплазмы). Вначале он проходит все стадии, соответствующие определению «литический цикл» — но за исключением собственно лизиса хозяина: вирионы как бы отпочковываются от бактерии, захватывая небольшие участки ее мембраны, которые становятся оболочкой фага. После такого деликатного литического цикла L2 может приступить к лизогенизации [20].
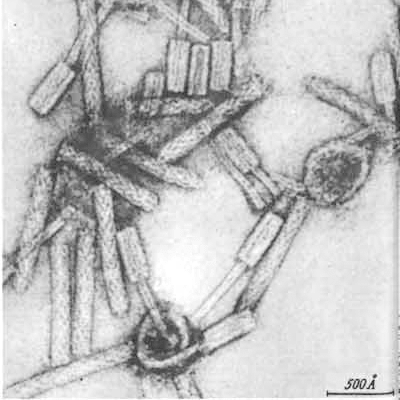
Рисунок 11. Дефектные фаги — пиоцины (бактериоцины Pseudomonas aeruginosa). Многие бактерии (особенно γ-протеобактерии) экспонируют на своей поверхности тейлоцины (tailocins) — «перевернутых безголовых фагов». Эти фаговые хвосты незаменимы в конкурентной борьбе бактерий с близкими родственниками (такие структуры называют бактериоцинами), а иногда служат для поражения эукариотических клеток (PLTS, фагоподобные структуры для транслокации белков). Гены тейлоцинов бактерии заимствовали у различных профагов семейств Myoviridae и Podoviridae, причем ДНК одной бактерии может содержать несколько генетических кластеров разных тейлоцинов наряду с полноценными родственными либо неродственными профагами, кодирующими все «запчасти» вириона [43]. Размножаться «дефектные фаги» не могут из-за отсутствия головки с ДНК, однако множественные отростки на поверхности клетки-хозяина способны подобно шприцам с токсичным содержимым повреждать клетки жертв.
микрофотография автора статьи
Бактериальный иммунитет
Казалось бы: если бактериофаги атакуют любых бактерий и их численность настолько велика (фаги — самые многочисленные вирусные формы в биосфере Земли, их общее количество — 10 30 –10 32 фаговых частиц [21], что примерно равно количеству бактерий, 4–6×10 30 ), то почему они до сих пор не уничтожили всех бактерий? Ответ очевиден: в процессе эволюционного соразвития бактерии выработали своего рода иммунитет против фагов. Причем иммунитет многослойный. Во-первых, бактерия может быть изначально лишена рецепторов к тому или иному фагу или лишиться их посредством мутаций. Во-вторых, бактерия может быть иммунизирована уже «прописавшимися» в ней профагами, которые с помощью специфических репрессоров просто не дадут вновь прибывшим сородичам размножиться. В-третьих, бактерия (или ее мобильные генетические элементы) кодирует рестрикционно-модификационные системы, которые просто рубят на кусочки нуклеиновые кислоты, не содержащие особых метильных меток — подписей «я свой».
А в-четвертых. В 2005 году стало известно, что функциональной основой бактериального иммунитета является система CRISPR [22], двумя годами позже — что для ее работы критически важен белок Cas, а в 2012-м уже появилась возможность создания инженерных систем на основе CRISPR-Cas9 Streptococcus pyogenes [23]. Работа системы CRISPR-Cas основана на том, что небольшой фрагмент, вырезанный из проникшей в бактериальную клетку фаговой ДНК, вставляется в специальный участок (локус CRISPR) генома бактерии. Каждый локус CRISPR содержит множество таких вставок (спейсеров, разделенных особыми короткими нуклеотидными повторами), представляющих собой фрагменты ДНК встреченных когда-либо фагов и плазмид. На основе спейсеров синтезируются молекулы РНК, комплементарные соответствующему участку фагового (или плазмидного) генома. Эти РНК в комплексе с белками Cas затем опознают и обезвреживают мишень — чужеродную ДНК с комплементарной последовательностью нуклеотидов. Таким образом, если в клетку однажды проникла фаговая ДНК, но клетка выжила и встроила фрагмент чужеродного генома в свой нуклеоид, то последующие попытки таких же фагов эксплуатировать клетку или ее потомков будут неэффективны [24].
Впрочем, бактериофаги за счет случайных мутаций и отбора умеют обходить системы CRISPR-Cas. Чтобы конкретный спейсер потерял эффективность, достаточно даже незначительного изменения комплементарного ему фрагмента фагового генома. Поэтому фаги успешно и довольно быстро преодолевают приобретенный иммунитет бактерий за счет точечных мутаций. С другой стороны, системы CRISPR очень широко распространены у бактерий и, судя по всему, обеспечивают своим обладателям надежную защиту. Эффективность CRISPR обеспечивается тем, что даже две разные бактерии одного и того же штамма встраивают в свой геном разные спейсеры, соответствующие разным участкам генома фага. В результате популяция бактерий быстро приобретает генетическое разнообразие, что значительно повышает их шансы на выживание. Точечные мутации, «обезвреживающие» один спейсер, позволят фагам заразить только небольшую часть бактериальной популяции. К тому же, бактериофаг не может определить заранее, какие спейсеры имеются у конкретной клетки. Поэтому большинство фагов в полиморфной популяции бактерий погибает даже при высокой скорости появления точечных мутаций.
Такой феномен коллективного бактериального иммунитета был продемонстрирован на бактериях P. aeruginosa и фагах DMS3vir [28]. Для начала ученые убедились, что система CRISPR действительно защищает бактерий от данной разновидности фагов, а культуры бактерий с отключенной CRISPR-системой активно этим фагом поражаются, хотя и выработали иную форму защиты: у них распространились мутации, меняющие рецептор, к которому прикрепляется фаг. Такой способ защиты оказался менее эффективным, так как по истечении 30 суток эксперимента бактериофаги всё еще находились в популяции. Чтобы доказать, что разнообразие спейсеров системы CRISPR-Cas — основа эффективности коллективной иммунной защиты, ученые сравнили устойчивость к фагам у бактериальных популяций с разным уровнем разнообразия спейсеров. Оказалось, что фаги в монокультурах бактерий уже в первые сутки приобретали мутации, нейтрализующие соответствующие спейсеры. У фагов же в популяциях, составленных из нескольких клонов бактерий с различными спейсерами, устойчивость формировалась лишь в немногих случаях. В популяциях, сформированных из 24–48 клонов, фаги не смогли преодолеть защиту CRISPR-Cas.
Отсюда следует, что в монокультуре единичная мутация фаговой ДНК, обеспечивающая защиту от конкретного спейсера, позволяет фагу заразить любую бактерию, а в полиморфной культуре из 48 клонов точно такая же мутация обеспечивает успех с вероятностью лишь 1/48. Даже при условии, что ДНК фага встроится в бактерию, защиту которой он преодолел, его потомки снова столкнутся с той же проблемой, и она будет усугубляться по мере снижения численности бактерий, чувствительных к этому фагу.
Таким образом, точечные мутации и отбор — недостаточно эффективная для вирусов эволюционная стратегия, что объясняет успешность систем CRISPR-Cas и их широкое распространение у бактерий. Но тогда почему бактериофаги до сих пор не «вымерли» — раз эта система так эффективна? Не так давно у них обнаружили особые гены, подавляющие работу CRISPR [29]. А что же могут противопоставить бактерии? Ответ, опять же, в разнообразии: существует много разных вариантов системы CRISPR, каждый из которых уязвим только для некоторых анти-CRISPR-генов и защищен от других. Содержать же в своем геноме множество подобных генов бактериофаги не могут, так как отбор у них ведется преимущественно в направлении компактизации генома — в угоду увеличению скорости размножения.
Такая антагонистическая коэволюция фагов и бактерий, протекающая параллельно на разных уровнях и в разных временных масштабах (формирование новых спейсеров бактериями — точечные мутации фагов, выработка новых генов анти-CRISPR — формирование новых вариантов системы CRISPR) позволяет соблюдать баланс в системе «бактериофаг — бактерия» на уровне одной популяции и биоценоза в целом [28], [30].
Получение бактериофагов
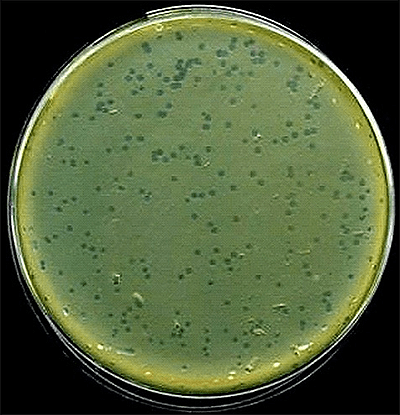
Рисунок 12. Фаговые бляшки (зоны лизиса на культуре E. coli).
Бактериофаги широко распространены в природе. Везде, где есть бактерии — есть фаги. Их можно выделить из открытых полостей организма человека и животных, водоемов, сточных вод, почвы, из соответствующих культур бактерий и т.д. Большое количество бактериофагов находится в выделениях больных людей и животных, особенно в период выздоровления от инфекционных заболеваний.
Таким образом, поиск и выделение новых фагов не представляет трудности. Для выделения бактериофага исследуемый материал (воду, испражнения, гной, почву и др.) засевают в жидкую питательную среду, инкубируют в термостате, и через сутки помутневшую жидкость пропускают через бумажный, а затем через бактериальный фильтры, асбестовые пластины, керамические свечи. Полученный фильтрат исследуют на наличие бактериофага путем совместного посева с подходящей микробной культурой на плотные или в жидкие питательные среды. Если бактериофаг выделился, то после 18-часовой инкубации на поверхности агара вырастает сплошной газон культуры с прозрачными бляшками — зонами лизиса (рис. 12). В бульоне бактериофаг обусловливает просветление среды.
Для выделения чистой культуры бактериофага материал из отдельной бляшки переносят бактериологической иглой в суспензию молодой микробной культуры.
Материал из вновь возникшего стерильного пятна засевают вместе с фагочувствительными микробами в жидкую питательную среду. После 6–18 часов инкубации среду фильтруют и получают чистую культуру бактериофага.
Для изготовления серийного препарата бактериофага применяют только апробированные штаммы и культуры микробов, обладающие типичными морфологическими, биохимическими и серологическими свойствами. Штаммы бактериофагов должны быть музейными и рабочими. Музейные производственные штаммы ежегодно обновляются путем выделения новых или пассажами имеющихся фаговых штаммов через организм больного, а также адаптацией к свежевыделенным, резистентным к данному бактериофагу культурам.
Промышленное получение бактериофага в настоящее время осуществляют в специальных аппаратах — реакторах емкостью 250–1000 л, с применением аэрации как фактора, стимулирующего развитие микроорганизмов. В реактор наливают жидкую питательную среду, которую стерилизуют при температуре 110 °С в течение 40 минут. После стерилизации среду охлаждают до 39 °С и засевают соответствующей микробной культурой и бактериофагом одновременно. Для засева используют 18-часовые агаровые культуры, которые прибавляют из расчета 50 млн микробных клеток на миллилитр среды. Бактериофаг добавляют в количестве не более 0,3 % по отношению к объему питательной среды. Среду с бактериальной культурой и фагом оставляют при температуре 37 °С на 6–18 часов. Фаги активно размножаются внутри бактериальных клеток и вызывают их лизис, что внешне проявляется полным просветлением среды. К полученному лизату добавляют в качестве консерванта хинозол (0,01 %) или фенол (0,25 %) и не позже чем через два часа после этого фильтруют содержимое реактора через бактериальные фильтры для удаления оставшихся микробных клеток.
Полученный препарат бактериофага должен иметь вид совершенно прозрачной жидкости желтого цвета. Он проходит контроль на стерильность, безвредность и литическую активность. Безвредность препарата проверяют путем введения животным. Например, брюшнотифозный и дизентерийный бактериофаги вводят подкожно трем мышам по 1 мл, либо внутривенно одному кролику 5 мл. За животными наблюдают в течение 3–4 суток. Литическую активность бактериофага определяют титрованием в жидкой питательной среде методом Аппельмана, на плотной питательной среде — методом Отто. За титр бактериофага при определении методом Аппельмана принимают то его наибольшее разведение, которое вызывает полный лизис тестовой культуры микроорганизмов.
После проведения контрольных исследований препарат разливают во флаконы нейтрального стекла. Помимо жидких препаратов бактериофага могут изготавливать и сухие. Для их получения фаголизат осаждают сернокислым аммонием, осадок отделяют от жидкой части, добавляют к нему стабилизатор (9 % глюконат кальция), смесь тщательно растирают и лиофилизируют [31].
Биологическое значение бактериофагов
Бактериофаги играют важную роль в круговороте углерода и энергии, контроле численности микробных популяций и эволюции бактерий. Бактериофаги, будучи подвижными генетическими элементами, служат мощным фактором изменчивости бактерий. Например, они осуществляют процесс трансдукции — перенос бактериальных генов из одной клетки в другую: вырезаясь из генома одной бактерии, они могут прихватывать с собой в капсид ее гены и, инфицируя другую клетку, передавать их новому хозяину. Есть все основания предполагать, что большинство бактерий содержит профаги. Многие культуры несут 2–4 и даже более умеренных фагов, то есть являются полилизогенными. Например, многие актиномицеты и клубеньковые бактерии содержат в геноме четырех и более профагов.
Способность фагов менять фенотип бактерий путем привнесения чужеродных (и фаговых в том числе) генов может быть одновременно залогом процветания для бактерий и источником больших проблем для человечества: так бактерии могут приобретать факторы вирулентности и устойчивости — к другим фагам, антибиотикам и прочим воздействиям (если фаг, например, награждает бактерию способностью формировать биопленки) [32]. В 1951 году была описана фаговая конверсия Corinebacterium diphtheriae: оказалось, что ген tox, кодирующий дифтерийный токсин, в геном нетоксигенных бактериальных штаммов привносится умеренным фагом β. В результате коринебактерия производит сильнейший токсин, инактивирующий в человеческих клетках один из компонентов трансляционного аппарата — EF-2 (эукариотический фактор элонгации 2). Подавление синтеза белка проявляется своеобразной дифтерийной симптоматикой. Аналогичные механизмы приобретения патогенных свойств позже выявили у холерных вибрионов, сальмонелл, клостридий и др.
Лабораторное и промышленное применение бактериофагов
Способность фагов к внесению в клетку определенного количества генетического материала, упакованного в капсид, широко эксплуатируется в генной инженерии: их часто используют в качестве векторов различного назначения. Например, для создания библиотек генов нередко конструируют векторы на основе бактериофага λ, содержащего двухцепочечную ДНК. Левое и правое плечи ДНК фага содержат гены, необходимые для литического цикла, а среднюю — несущественную для размножения — часть молекулы можно заменять крупным (примерно до 24 т.п.н.) фрагментом чужеродной ДНК, включая эукариотическую. Такую рекомбинантную ДНК упаковывают в вирионы и заражают ими подходящую культуру бактерий, которая затем многократно воспроизводит фаговую ДНК с интересующими человека фрагментами.
Из-за высокой специфичности многие фаги служат диагностическими инструментами для идентификации бактериальных культур в медицинской, ветеринарной, технической микробиологии и фитопатологии. Метод фаготипирования, основанный на исключительной специфичности определенных фаговых штаммов, позволил распределить на фаготипы ряд штаммов бактерий, неотличимых друг от друга по другим признакам. Фаготипирование с успехом применяют для идентификации типов кишечной палочки, сальмонелл (включая возбудителя брюшного тифа), стафилококков и др. Этот метод дает эпидемиологам возможность отследить цепочку случаев заболевания и определить источник инфекции.
Бактериофаги прекрасно подходят для быстрого обнаружения небольших количеств патогенных бактерий во внешней среде: появляются и множатся хозяева — нарастает титр специфического бактериофага. Определение колифагов стало одним из ключевых мероприятий в санитарном контроле вод, поскольку позволяет выявить фекальное загрязнение даже при малом количестве кишечной палочки, не определяемом бактериологическими методами.
Фаги применяются и в борьбе с бактериальными вредителями различных технических брожений, и в производстве ферментов с помощью бактериальных культур. В то же время, заражая промышленные культуры, бактериофаг вредит «полезным» производственным штаммам (вакцинным, продуцентам антибиотиков, возбудителям молочнокислого, ацетонобутилового и некоторых других брожений), чем вызывает серьезные нарушения технологического процесса.
Применение бактериофагов в медицине
Первый отчет об успешной фаготерапии был опубликован в 1921 году фламандцами Р. Бранохе и Ж. Майсином, которые использовали бактериофаг для лечения кожной стафилококковой инфекции [33].
Как уже было упомянуто, западная медицина c середины ХХ века практически отказалась от использования бактериофагов в терапевтических целях [5], однако в СССР фаги довольно широко применялись. Одним из самых, пожалуй, масштабных примеров практического применения фагов является использование комплексного препарата бактериофагов в Сталинграде во время Великой Отечественной войны. З.В. Ермольева во время работы в Ташкентском институте вакцин и сывороток разработала препарат, содержащий 19 видов бактериофагов, в том числе холерный, брюшнотифозный и дифтерийный. Во время Сталинградской битвы в связи с угрозой эпидемии холеры было налажено производство холерного фага в самом Сталинграде, и препарат ежедневно принимали около 50 тысяч человек [34].
После войны в СССР приступили к промышленному производству фаговых препаратов, которое действует и в настоящее время. В России производством бактериофагов занимаются в основном филиалы НПО «Микроген»: «Иммунопрепарат» (г. Уфа), «ИмБио» (г. Нижний Новгород), «Биомед» (г. Пермь).
На данный момент в РФ зарегистрировано и производится 13 фаговых препаратов (табл. 2).
| Препарат | Применение* | Состав |
|---|---|---|
| Секстафаг®, пиобактериофаг поливалентный жидкий | Для лечения и профилактики заболеваний, вызванных стафилококками, стрептококками, протеями, клебсиеллами, синегнойной и кишечной палочками | Стерильный фильтрат фаголизатов бактерий Staphylococcus, Streptococcus, Proteus (P. vulgaris, P. mirabilis), Pseudomonas aeruginosa, Klebsiella pneumoniae, энтеропатогенных Escherichia coli |
| Интести-бактериофаг | Для лечения и профилактики заболеваний, вызванных стафилококками, стрептококками, протеями, клебсиеллами, синегнойной и кишечной палочками | Смесь стерильных фильтратов фаголизатов Shigella flexneri (сероваров 1, 2, 3, 4, 6), Shigella sonnei, Salmonella enterica (сероваров Paratyphi A, Paratyphi B, Typhimurium, Infantis, Choleraesuis, Oranienburg, Enteritidis), энтеропатогенных Escherichia coli (серогрупп, наиболее значимых в этиологии кишечных инфекций), Proteus vulgaris, Proteus mirabilis, Enterococcus, Staphylococcus, Pseudomonas aeruginosa |
| Пиобактериофаг поливалентный очищенный | Для лечения и профилактики различных форм гнойно-воспалительных заболеваний и инфекций ЖКТ | Стерильный фильтрат фаголизатов Staphylococcus, Streptococcus, Proteus mirabilis, Proteus vulgaris, Escherichia coli, Pseudomonas aeruginosa, Klebsiella pneumoniae |
| Пиобактериофаг комплексный жидкий | Для лечения гнойно-воспалительных заболеваний, обработки операционных и свежеинфицированных ран | Смесь стерильных фильтратов фаголизатов Staphylococcus, Streptococcus, Enterococcus, Proteus (P. vulgaris, P. mirabilis), Pseudomonas aeruginosa, энтеропатогенных Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca |
| Бактериофаг стрептококковый | Для лечения и профилактики заболеваний, вызванных стрептококками | Стерильные фаголизаты Streptococcus spp. |
| Бактериофаг дизентерийный | Для лечения и профилактики дизентерии | Смесь стерильных фильтратов фаголизатов Shigella flexneri (сероваров 1, 2, 3, 4, 6) и Shigella sonnei |
| Бактериофаг стафилококковый | Для лечения и профилактики гнойно-воспалительных и кишечных заболеваний, вызванных стафилококками | Стерильные фаголизаты Staphylococcus spp. |
| Бактериофаг псевдомонас аеругиноза (синегнойный) | Для лечения и профилактики заболеваний, вызванных синегнойной палочкой | Стерильные фаголизаты Pseudomonas aeruginosa |
| Бактериофаг сальмонеллезный групп A,B,C,D,E | Для лечения заболеваний, вызванных сальмонеллами | Стерильный фильтрат фаголизатов наиболее распространенных сероваров Salmonella enterica (Paratyphi А и В, Typhimurium, Choleraesuis, Infantis, Oranienburg, Enteritidis) |
| Бактериофаг клебсиелл поливалентный очищенный | Для лечения и профилактики заболеваний, вызванных клебсиеллами | Стерильная смесь очищенных фильтратов фаголизатов Klebsiella (K. pneumoniae, K. ozaenae, K. rhinoscleromatis) |
| Бактериофаг коли | Для лечения и профилактики заболеваний, вызванных кишечной палочкой | Стерильный фильтрат фаголизатов патогенных штаммов Escherichia coli |
| Бактериофаг протейный жидкий | Для лечения и профилактики гнойно-воспалительных и кишечных заболеваний, вызванных протеями | Стерильный фильтрат фаголизатов Proteus vulgaris и Proteus mirabilis |
| Бактериофаг колипротейный | Для лечения и профилактики гнойно-воспалительных и кишечных заболеваний | Смесь стерильных фильтратов фаголизатов Proteus vulgaris, Proteus mirabilis и энтеропатогенных серогрупп Escherichia coli |
| * Производитель предупреждает, что препараты должны применяться после оценки чувствительности возбудителей болезни к фагам, что означает еще и необходимость идентификации бактерии-возбудителя. Кроме того, в случае тяжелых инфекций фаготерапия допустима только как часть комплексного лечения | ||
Отдельно стоит осветить вопрос применения фаготерапии в странах Запада. Как известно, после открытия антибиотиков работы, связанные с медицинским применением фагов, там были полностью свернуты. Однако в последние годы в связи с тревожной динамикой распространения внутрибольничных инфекций, резистентных к большинству известных антибиотиков, многие биотехнологические компании сделали резкий поворот к изучению возможности создания лекарств на основе бактериофагов. Однако, несмотря на существенные технологические преимущества, для создания эффективных препаратов необходима коллекция бактериофагов, действующих на клинически значимые штаммы возбудителей, и соответствующий опыт их клинического применения, чем эти компании пока не обладают.
С терапевтической целью бактериофаги применяют, например, в России, Грузии и Польше, причем самыми разными способами. Для коррекции кишечных дисбиозов жидкие препараты применяют внутрь или per rectum при помощи клизмы. Таблетированные формы принимают внутрь, возможно использование бактериофагов и в составе ректальных свечей. При кожных и раневых инфекциях их применяют в виде примочек на очаги поражения. При фарингитах, ларингитах и тонзиллитах препараты используют для орошения или полосканий, при отитах — закапывают в уши. Для лечения абсцессов в их полость вводят ватный шарик, пропитанный препаратом. Больным, страдающим хроническими остеомиелитами, препарат вводят непосредственно в пораженный участок кости. Также препараты можно вносить в брюшную, плевральную и суставные полости, а также применять в форме аэрозолей при поражениях легких. При инфекциях мочевыводящих путей бактериофаги вливают непосредственно в пораженный орган с помощью зонда. При гинекологических заболеваниях препарат вливают в матку либо применяют влагалищные тампоны, пропитанные фаговым раствором.
А еще их используют в методике под названием фаговый дисплей, которая, в частности, позволяет находить новые антитела для диагностики и терапии заболеваний: «Враг моего врага — мой друг. Как бактерии и вирусы помогают создавать антитела для лечения человека» [39]. — Ред.
Преимущества бактериофагов перед антибиотиками достаточно очевидны.
К сожалению, недостатков бактериофаги тоже не лишены.
Заключение
Прошло уже 100 лет с момента открытия бактериофагов. Неоправданно забытые на Западе и чудом сохранившиеся в России, они полвека пребывали в тени успеха антибиотиков. Но эпоха триумфа антибиотиков выявила и важнейшую проблему их активного применения — угрожающий рост резистентности к ним среди опасных патогенов, и многие ученые и врачи видят именно в фагах альтернативу антибиотикам. Если на сегодняшний день мы имеем штаммы бактерий, устойчивые даже к антимикробным препаратам «последней надежды», то фаги, благодаря описанным выше механизмам коэволюции с бактериями, никогда не утратят актуальности. За 100 лет они были детально изучены, признаны безопасными и стали незаменимым инструментом в генетике и биоинженерии, санитарной микробиологии и эпидемиологии, промышленности, медицине и даже в космической сфере (да-да, бактерии с профагом используют для оценки защиты обшивки космических кораблей от радиации). И как нельзя лучше характеризует значение фагов для человека древняя пословица: «Враг моего врага — мой друг».